Similar presentations:
Электрохимия
1.
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ УКРАИНЫЗапорожский государственный
медицинский университет
Кафедра физколоидной химии
Электрохимия
2.
ЭлектрохимияЭлектрохимия - это наука, которая
изучает процессы, либо протекающие с
возникновением электрического тока,
либо вызванные электрическим током.
3.
Гальванический элементНа поверхности раздела возникает разность потенциалов,
величина которой зависит от природы материала электрода,
температуры, концентрации раствора и других свойств
системы. Ее измеряют относительно электрода сравнения в
стандартных условиях.
Если замкнуть два разных по природе эл-да внешней и
внутренней цепью, получим машину способную производить
электрический ток - гальванический элемент, который состоит
из:
анода (процесс окисления)
катода (процесс восстановления)
Символическая запись:
А (-)Zn|Zn2+||Cu2+|Cu(+) К
4.
Механизм возникновения электродного потенциала иэлектродвижущей силы
Окунем любую металлическую пластинку в раствор собственных
ионов или в воду. Ионы металла в результате действия сильно
поляризованных молекул растворителя (воды), отрываясь от структурной
решетки металла, начинают переходить в толщу раствора, но не бесконечно,
потому что возникающее вследствие этого электростатическое притяжение
между ионами, перешедшие в раствор, и противоположно заряженным
пластинкой металла, препятствует дальнейшему прохождению этого процесса
и в системе наступает равновесие. Однако возникающая в результате этого
разность потенциалов между металлом и окружающей средой раствора
остается (ф). Так возникает электрохимический (электродный) потенциал.
Прыжки потенциалов на границе раздела проводников I i II рода
образуют двойной электрический слой. В приповерхностном слое образуется
плотный слой (до 10 см) и диффузный слой из разнородно заряженных ионов
раствора, размещенных на некотором расстоянии от поверхности электрода.
На ионы двойного электрического слоя одновременно действуют силы
притяжения и отталкивания, а также тепловое движение.
5.
Двойной электрический слойДвойной электрический слой (ДЭС) —
слой ионов, образующийся на поверхности
частиц в результате адсорбции ионов из
раствора,
диссоциации
поверхностного
соединения
или
ориентирования
полярных молекул на границе фаз. Ионы,
непосредственно
связанные
с
поверхностью
называются
потенциалоопределяющими.
Заряд
этого
слоя
компенсируется зарядом второго слоя ионов,
называемых противоионами.
6.
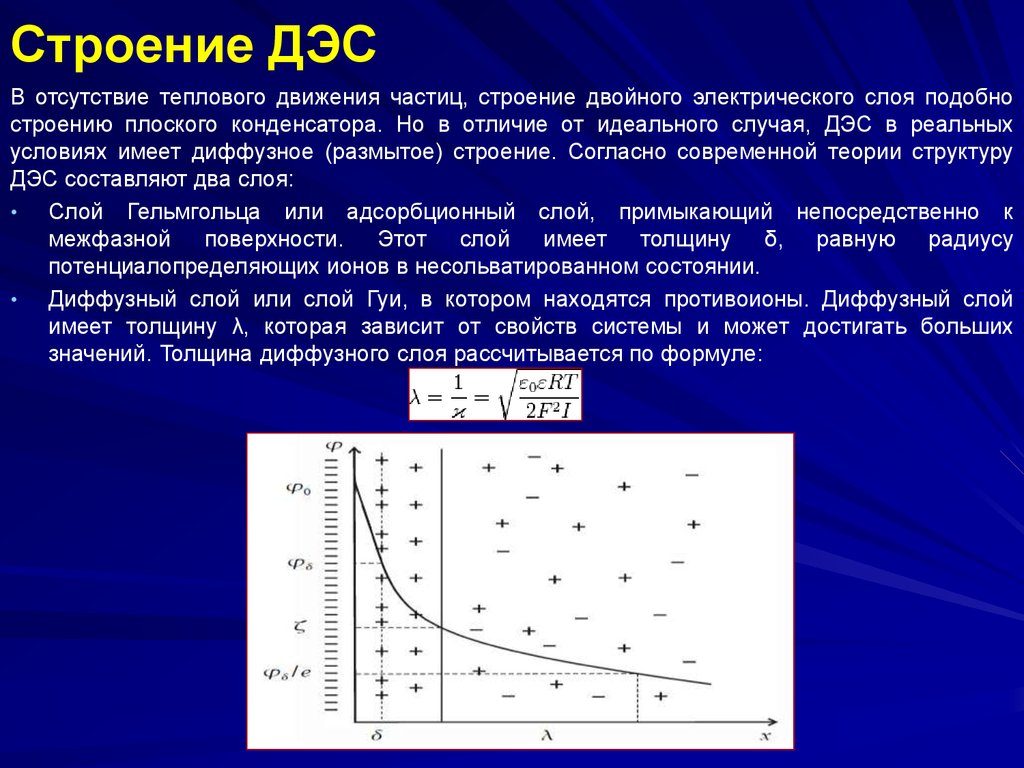
Строение ДЭСВ отсутствие теплового движения частиц, строение двойного электрического слоя подобно
строению плоского конденсатора. Но в отличие от идеального случая, ДЭС в реальных
условиях имеет диффузное (размытое) строение. Согласно современной теории структуру
ДЭС составляют два слоя:
Слой Гельмгольца или адсорбционный слой, примыкающий непосредственно к
межфазной поверхности. Этот слой имеет толщину δ, равную радиусу
потенциалопределяющих ионов в несольватированном состоянии.
Диффузный слой или слой Гуи, в котором находятся противоионы. Диффузный слой
имеет толщину λ, которая зависит от свойств системы и может достигать больших
значений. Толщина диффузного слоя рассчитывается по формуле:
7.
Уравнение НернстаПри изучении потенциалов различных электродных процессов
установлено, что их величины зависят от трех факторов:
1) от природы веществ - участников электродного процесса,
2) от соотношения между концентрациями этих веществ и
3) от температуры системы.
Эту зав-сть выражает
(В. Нернст, 1889 г.):
0 2 ,3
Ox
RT
lg
nF Re d
Стандартный электродный потенциал – это потенциал даного
электродного процесса при концентрациях (активностях) всех
участвующих в нем веществ, равных единице.
8.
Классификация электродовПо типу электродной реакции все электроды можно разделить на две группы (в
отдельную группу выделяются окислительно-восстановительные электроды
К электродам первого рода относятся электроды, состоящие из металлической
пластинки, погруженной в раствор соли того же металла. При обратимой работе элемента, в
который включен электрод, на металлической пластинке идет процесс перехода катионов из
металла в раствор либо из раствора в металл. Т.о., электроды первого рода обратимы по
катиону и их потенциал связан уравнением Нернста с концентрацией катиона (к электродам
первого рода относят также и водородный электрод).
Электродами второго рода являются электроды, в которых металл покрыт
малорастворимой солью этого металла и находится в растворе, содержащем другую
растворимую соль с тем же анионом. Электроды этого типа обратимы относительно аниона
9.
Измерение рНДля определения величины pH существуют два основных метода:
колориметрический и потенциометрический.
Колориметрический метод основан на изменении окраски
индикатора, добавленного к исследуемому раствору, в зависимости от
величины pH. Этот метод недостаточно точен, требует введения солевых
и температурных поправок, дает значительную погрешность при очень
малой минерализации исследуемой воды (менее 30 мг/л) и при
определении pH окрашенных и мутных вод. Метод нельзя применять для
вод, содержащих сильные окислители или восстановители. Используется
обычно в экспедиционных условиях и для ориентировочных
определений.
Потенциометрический метод намного точнее, лишен в значительной
мере всех перечисленных недостатков, но требует оборудования
лабораторий
специальными
приборами
pH-метрами.
Потенциометрический метод основан на измерении ЭДС электродной
системы, состоящей из индикаторного электрода и электрода сравнения.
Электрод сравнения иногда называют вспомогательным электродом.
10.
Электроды, используемые впотенциометрическом титровании
Стеклянный электрод до и после измерений калибруют по двум (или более)
буферным растворам с точно известными значениями рН. При этом значение рН
хотя бы одного из контрольных растворов должно лежать близко к области
измерения. Измерения проводят на приборе, который называется рН-метром.
Показания прибора должны быть устойчивыми все время проведения анализа, что
проверяется контрольными замерами по буферным растворам. Для обеспечения
стабильных показаний рН-метра необходимы стабилизация напряжения на входе в
прибор, а также заземление корпуса прибора и металлической оплетки
коаксиального кабеля стеклянного электрода.
После включения и предварительного прогрева прибора в течение 30 мин его
проверяют по встроенному стандартному элементу и цепь уравновешивают по
стеклянному и каломельному электродам, погруженным в рекомендованный в
инструкции к прибору буферный раствор с точно известным значением рН. Через
час показания прибора должны повториться без какой-либо дополнительной
подстройки с точностью, указанной в паспорте прибора (обычно 0,05-0,01 рН).
Толчок или вибрация могут нарушить настройку рН-метра. Поэтому прибор лучше
устанавливать на массивном столе на коврике из пористой резины.
11.
Электроды, используемые впотенциометрическом титровании
Хингидронный электрод, относящийся к классу окислительно-восстановительных электродов (см.
ниже), представляет собой платиновую проволоку, опущенную в сосуд с исследуемым раствором, в
который предварительно помещают избыточное количество хингидрона С6Н4О2·С6Н4(ОН)2 – соединения
хинона С6Н4О2 и гидрохинона С6Н4(ОН)2, способных к взаимопревращению в равновесном окислительновосстановительном процессе, в котором участвуют ионы водорода:
С6Н4О2 + 2Н+ + 2е- ––> С6Н4(ОН)2
Стеклянный электрод, являющийся наиболее распространенным индикаторным электродом,
относится к т.н. ионоселективным или мембранным электродам. В основе работы таких электродов лежат
ионообменные реакции, протекающие на границах мембран с растворами электролитов; ионоселективные
электроды могут быть обратимы как по катиону, так и по аниону.
Наиболее часто употребляется стеклянный электрод в виде трубки, оканчивающейся тонкостенным
стеклянным шариком. Шарик заполняется раствором НСl с определенной активностью ионов водорода; в
раствор погружен вспомогательный электрод (обычно хлорсеребряный).
12.
Электроды, используемые впотенциометрическом титровании
Водородный электрод
представляет собой платиновую пластинку, омываемую
газообразным водородом, погруженную в раствор, содержащий ионы водорода.
Адсорбируемый платиной водород находится в равновесии с газообразным водородом;
схематически электрод изображают следующим образом:
Рt, Н2 / Н+
Электрохимическое равновесие на электроде можно рассматривать в следующем виде:
2Н+ + 2е- ––> Н2
Потенциал водородного электрода зависит от активности ионов Н+ в растворе и давления
водорода; потенциал стандартного водородного электрода (с активностью ионов Н+ 1 моль/л
и давлением водорода 101.3 кПа) принят равным нулю.
13.
Электроды, используемые впотенциометрическом титровании
Каломельный электрод.
Работа с водородным электродом
довольно неудобна, поэтому в качестве электрода сравнения часто
используется более простой в обращении каломельный электрод,
величина электродного потенциала которого относительно стандартного
водородного электрода точно известна и зависит только от температуры.
Каломельный электрод состоит из ртутного электрода, помещенного в
раствор КСl определенной концентрации и насыщенный каломелью
Hg2Сl2:
Нg / Нg2Сl2, КСl
14.
Электроды, используемые впотенциометрическом титровании
Хлорсеребряный электрод.
В качестве электрода сравнения используют также
другой электрод второго рода – хлорсеребряный, представляющий собой серебряную
проволоку, покрытую хлоридом серебра и помещённую в раствор хлорида калия.
Хлорсеребряный электрод также обратим относительно анионов хлора:
Аg / АgСl, КСl
Чаще всего в качестве электрода сравнения используется насыщенный хлорсеребряный
электрод, потенциал которого зависит только от температуры. В отличие от каломельного, он
устойчив при повышенных температурах и применим как в водных, так и во многих неводных
средах.













 physics
physics chemistry
chemistry








