Similar presentations:
Азот
1.
2.
3.
Сабақтың мақсаты:Білімділігі: Периодтық жүйедегі
азоттың орнына байланысты
оны V топ элементі ретінде
сипаттау; оқушыларды оның
физикалық – химиялық
қасиеттерімен таныстыру.
Тәрбиелігі: Дәстүрлі емес оқыту
әдісін қолдана
отырып,оқушылардың химияға
танымдық қызығушылығын
арттыру.
Дамытушылығы:
Оқушыларды өзіндік жұмысқа
дағдыландыру және
сараптау,салыстыру
қабілеттерін дамыту.Өзін-өзі
бақылау мен талдауды іске
асыру.
4.
Сабақтың түрі:Жаңа білімді меңгерту
Сабақтың өту әдісі:
Сын тұрғысынан ойлауды
дамыту технологиясы.
5.
І-кезең: “Қызығушылықты ояту.”( Тақырыпқа танымдық қызығушылықты,
оқушының белсенділігін ояту.)
1.Танымдық сұрақтар.
2.”Кім білімпаз?”
ІІ-кезең: “Мағынаны ашу.”
(Жаңа ақпаратпен танысу.)
1. Азоттың табиғатта таралуы, алынуы,
физикалық – химиялық қасиеттері.
2. Азоттың қолданылуы, биологиялық рөлі.
ІІІ-кезең: «Ой толғау.»
(сабақты бекіту және қорытындылау.)
1. Семантикалық карта
2. Аудармашы
3. Сәйкестендіру тест
6.
І-кезең:Қызығушылықты ояту.”Танымдық сұрақтар.
1. Антониміне “көп” сөзінің тілсіз
жауды тіркесең, көз алдыңда
өзгеремін, қажетті тыңайтқышқа
айналамын.
2. Кремний оксидінің табиғатта
қандай түрлері кездеседі?
3. ҮА топшасының элементтерін
атаңдар.
7.
Next8.
Азот атомыныңэлектрондық
конфигурациясын
жаз.
Back
9.
Азот топшасынакіретін
элементтер
саны?
Back
10.
Азот қандай тотығудәрежелерін көрсетеді?
Back
11.
Құрамында азотболатын маңызды
қосылыстарды
атаңдар
Back
12.
Азоттың бес валенттіоксидіндегі көрсететін
тотығу дәрежесі?
Back
13.
Азот топшасыорналасқан
топ нөмірі.
Back
14.
Азоттың сутектіқосылысының
атауы?
Back
15.
Азот элементініңатомдық массасы
қанша?
Back
16.
17.
Ауада – 78,09%Адам ағзасында – 3,1 %
(ақуыз, дәрумен, гармон)
Өсімдіктер (ион түрінде)
Топырақта – 0,01 – 0,04 %
Азот - өмір элементі
18.
19.
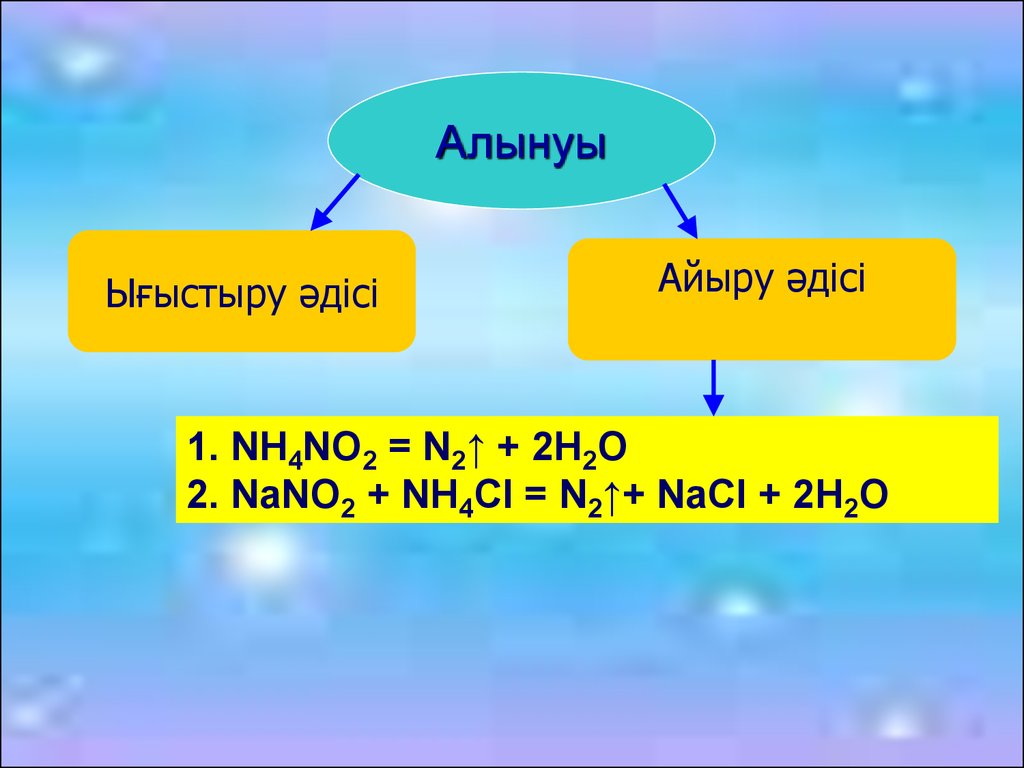
АлынуыЫғыстыру әдісі
Айыру әдісі
1. NH4NO2 = N2↑ + 2H2O
2. NaNO2 + NH4Cl = N2↑+ NaCl + 2H2O
20.
Инертті газg = 1,25 г/л(қ.ж)
tб = -2100С
tқ = -195,80С
Mr = 28
21.
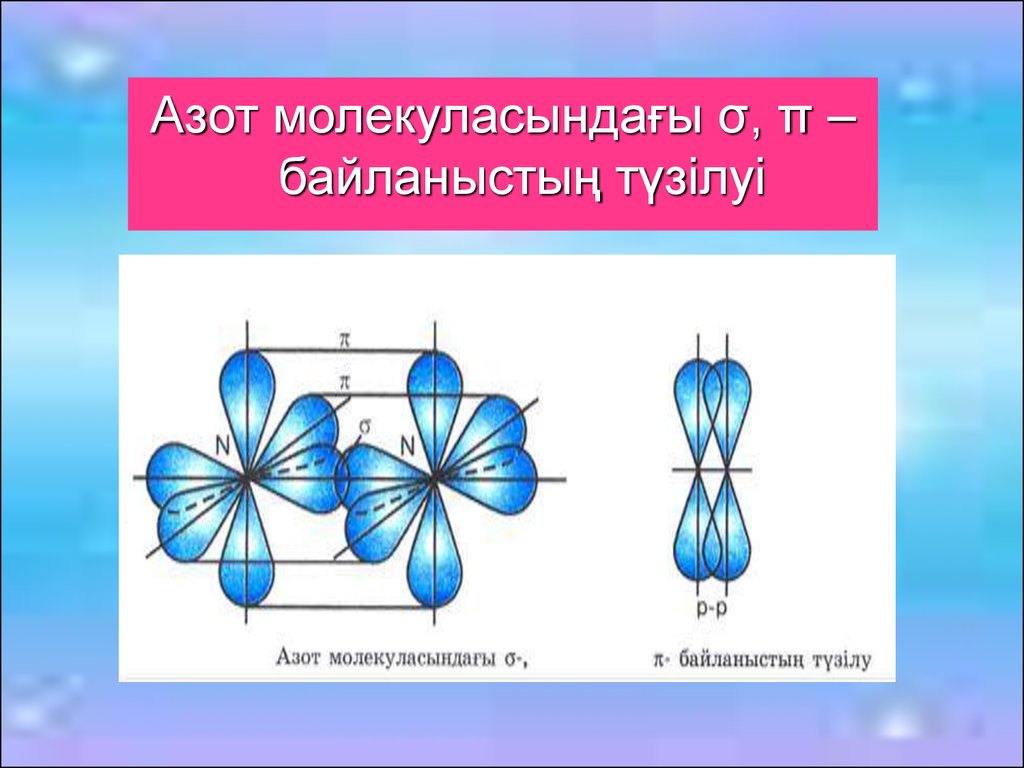
Азот молекуласындағы σ, π –байланыстың түзілуі
22.
6Li = 2Li3N2Al = 2AlN
N2 +
O2 = 2NO
3H2 =2NH3
23.
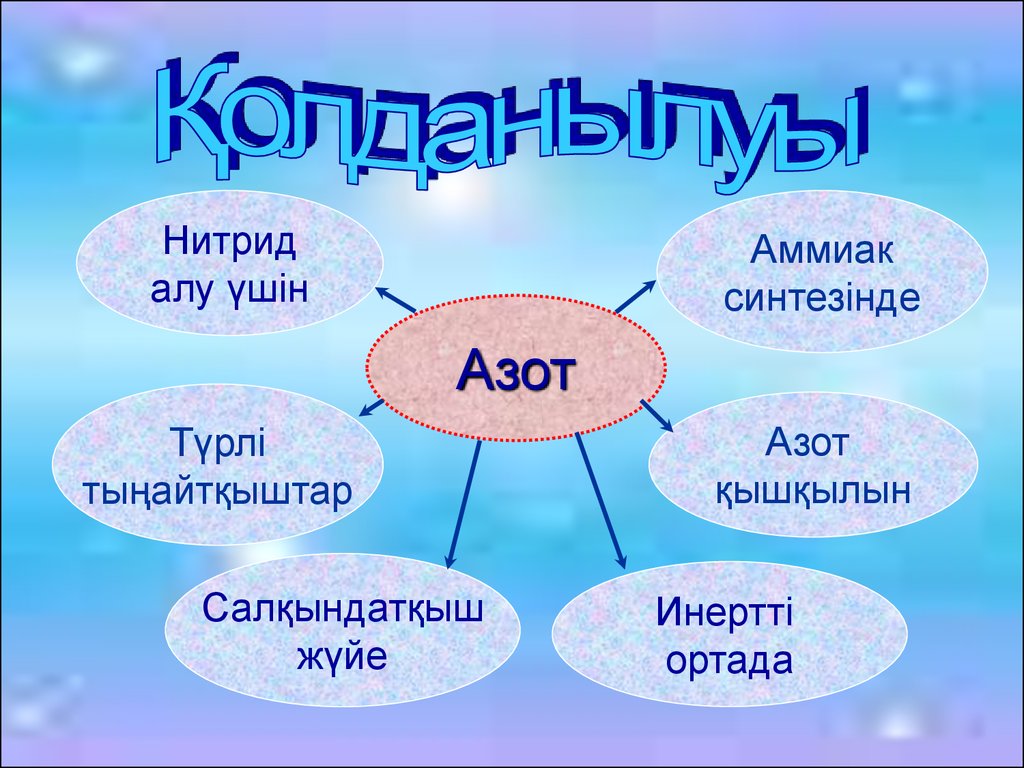
Нитридалу үшін
Аммиак
синтезінде
Азот
Түрлі
тыңайтқыштар
Салқындатқыш
жүйе
Азот
қышқылын
Инертті
ортада
24.
Азоттың табиғаттағы айналымы25.
26.
“Кім жылдам? ”1. Азоттың тотығу дәрежесі +5 болатын
қатарды көрсетіңіз:
NO2
KNO3
NO
HNO2
HNO3
KNO3
N2
NaNO3
NH4NO3
27.
1. Азоттың оксидтерін, тұздарынажыратыңдар:
Азот
Тұздары
Қышқылдары
Оксидтері
NH4Cl NO2 HNO3 NO NaNO3 NH4NO3 HNO2
28.
“Аудармашы”NaNO3KNO3Ca(NO3)2 –
NH4NO2 –
NH4Cl –
NH3 –
AlN -
29.
NФормуласы
Аттары
1.
NaHСO3
А) силан
2.
SiH4
Ә) литий нитриді
3.
Li3N
4.
HNO3
5.
Ca(NO3)2
Б) натрий
гидрокарбонаты
В) кальций
селитрасы
Г) азот қышқылы
30.
V. Сабақты бекіту:Кубизм әдісі
1. Азотқа қандай физикалық қасиет тән?
2. Азотты қайда қолданылады?
3. Азот табиғатта қайда кездеседі?
4. Зат мөлшері 0,5 моль аммиак алу үшін
аммоний хлориді мен кальций
гидроксидінің қандай массасы қажет?
5. Азотты қандай әдіс арқылы алады?
6. Мына айналударды жүзеге асырыңдар:
NH3 → NO → HNO3 → NH4NO3
31.
Үйге тапсырма:§8.9. №7




























 biology
biology physics
physics chemistry
chemistry








