Similar presentations:
Непредельные углеводороды - алкены
1. Непредельные углеводороды - Алкены
2. Домашнее здание
§4, тема «Алкены». Выучить конспектПисьменно написать все возможные
изомеры пентена.
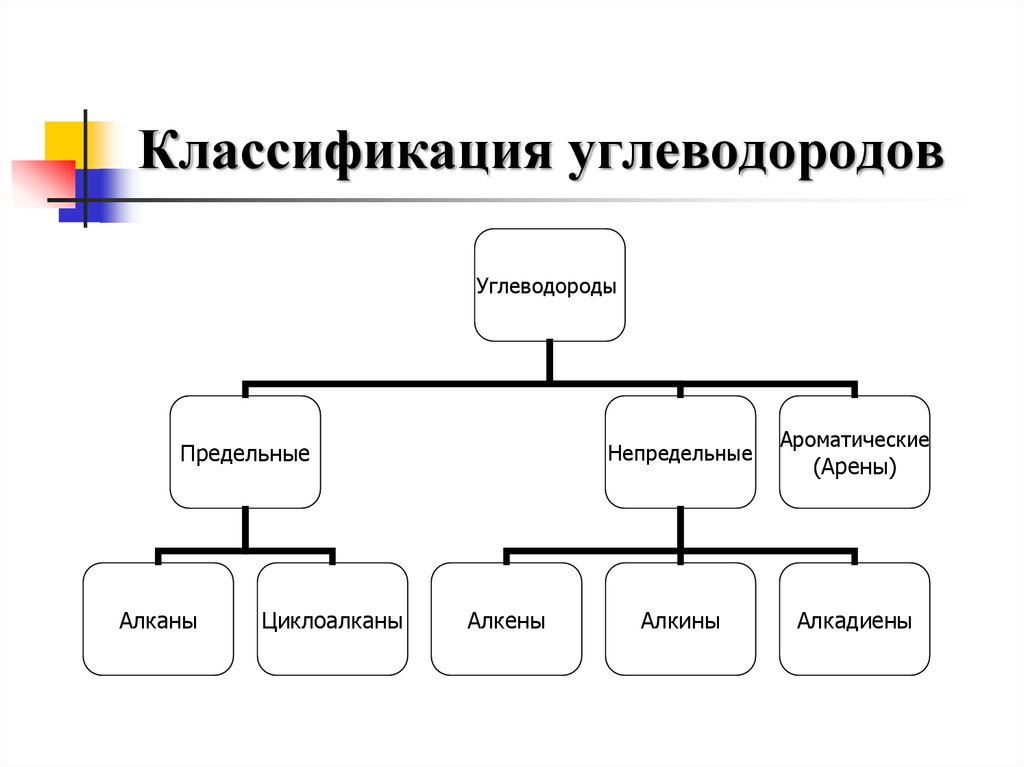
3. Классификация углеводородов
УглеводородыПредельные
Алканы
Циклоалканы
Непредельные
Алкены
Алкины
Ароматические
(Арены)
Алкадиены
4.
Общая формула: СnH2nАлкены – ациклические
углеводороды, в молекуле которых
кроме одинарных связей
содержится одна двойная связь
между атомами углерода.
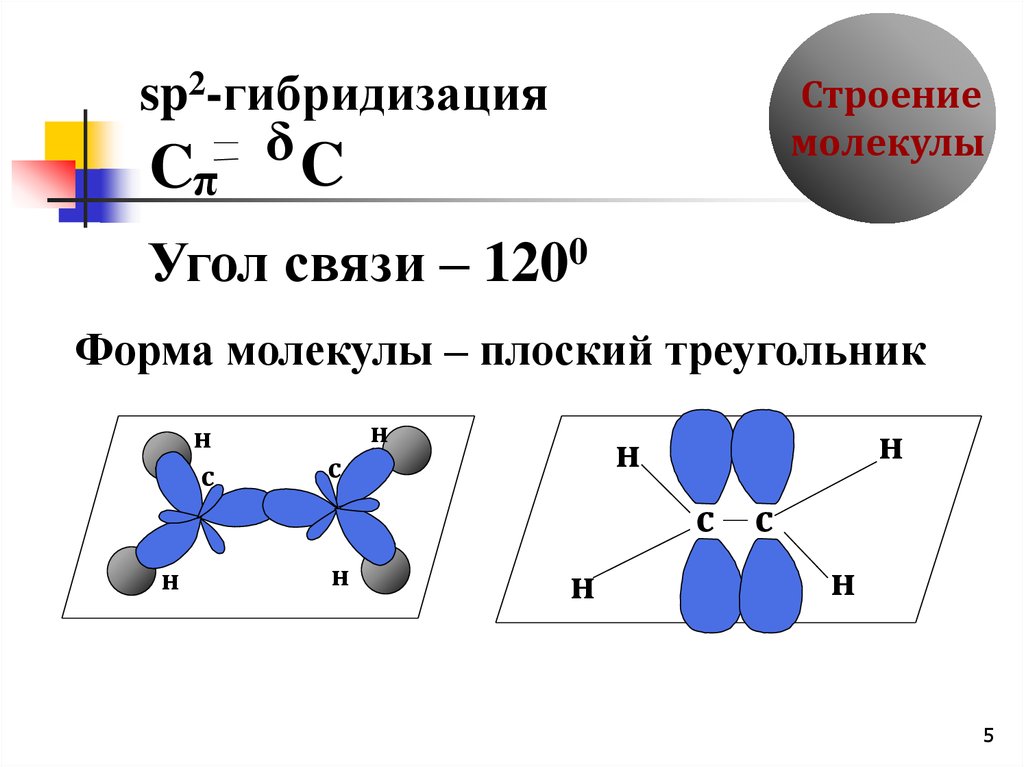
5.
Строениемолекулы
sp2-гибридизация
Cπ
δC
Угол связи – 1200
Форма молекулы – плоский треугольник
н
с
н
н
н
с
с
н
н
н
с
н
5
6.
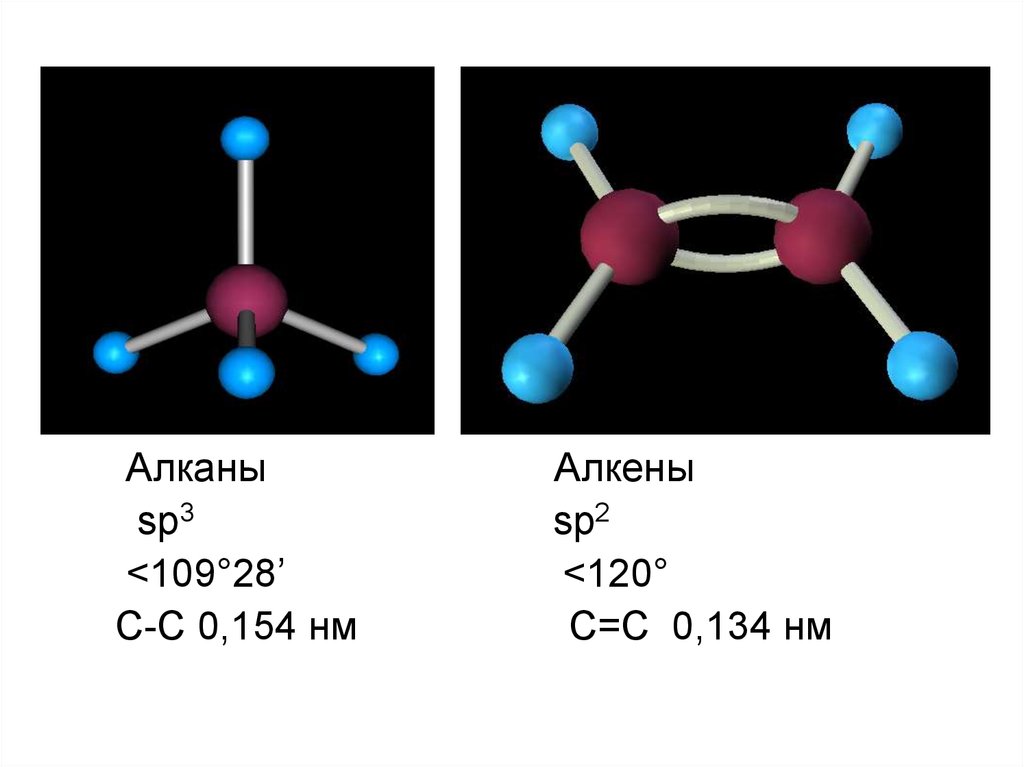
Алканыsp3
<109°28’
C-C 0,154 нм
Алкены
sp2
<120°
C=C 0,134 нм
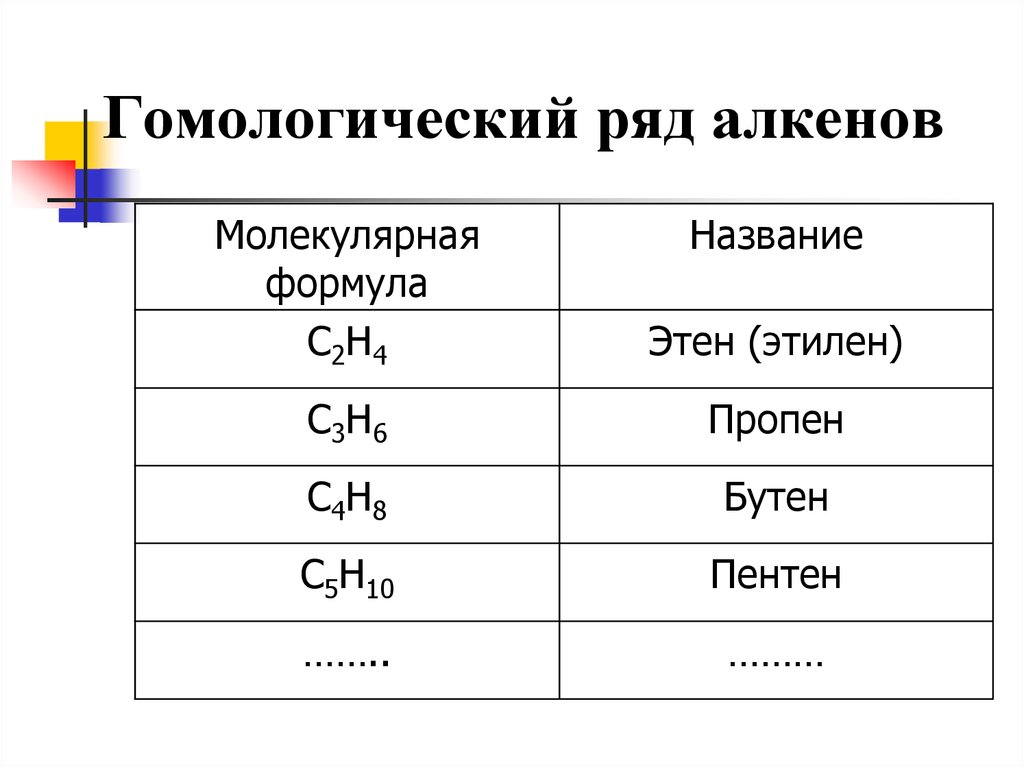
7. Гомологический ряд алкенов
Молекулярнаяформула
C2H4
Название
Этен (этилен)
C3H6
Пропен
C4H8
Бутен
C5H10
Пентен
……..
………
8. Правила номенклатуры алкенов
Выделяют в структурной формуле наиболее длинную цепь атомовуглерода, включающую двойную связь, и нумеруют их с того
конца, к которому ближе двойная связь.
В начале названия цифрой указывают положение замещающей
группы (радикала).
Если замещающих групп несколько, цифрами отмечают каждую
из них.
После названия замещающей группы (радикала) называют всю
неразветвлённую углеродную цепь.
В конце названия обозначают положение двойной связи номером
того атома углерода, от которого она начинается.
Пример:
1 2 3 4
СН3-С=СН-СН3
2-метилбутен-2
СН3
9. Виды изомерии алкенов
1. Изомерия углеродного скелетаСН2=СН-СН2-СН3 и
СН2=С-СН3
СН3
2. Изомерия положения кратной связи
СН2=СН-СН2-СН3 и СН3-СН=СН-СН3
10.
3. МежклассоваяСН2=СН-СН2-СН3
и
СН2
СН2
СН2
СН2
11.
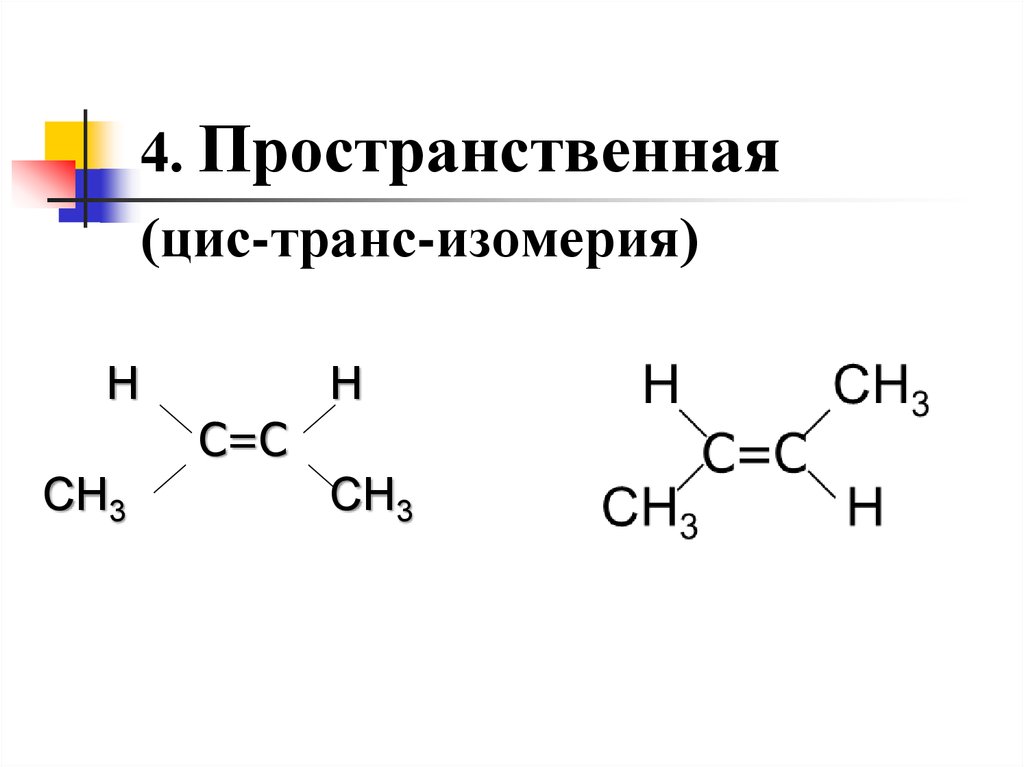
4. Пространственная(цис-транс-изомерия)
Н
Н
С=С
СН3
СН3
12. Вещества с общей формулой СnH2n относятся к классу
1.2.
3.
4.
алканов
алкинов
алкенов
аренов
13. Гомологом этилена является
1.2.
3.
4.
C6H6
CH3-CH=CH2
C2H4
CH3-CH2-CH3
14. π-связь имеется в молекуле
1.2.
3.
4.
пентана
циклопентана
2-метилпропана
пропена
15. Углеводород с формулой СН3-СН-СН=СН-СН3 называется
СН31.
2.
3.
4.
2-метилпентан
2-метилпентен-3
4-метилгексен-2
4-метилпентен-2
16. Изомерами являются
1.СН3-СН2-СН2СН3 и СН3-СН=СН-СН3
3.
СН3
СН2=С-СН2-СН3 и СН3-СН=С-СН3
СН3
СН3-СН2-СН3 и СН3-СН2-СН2-СН3
4.
СН2=СН-СН3 и СН3-СН2-СН3
2.
17. Получение алкенов
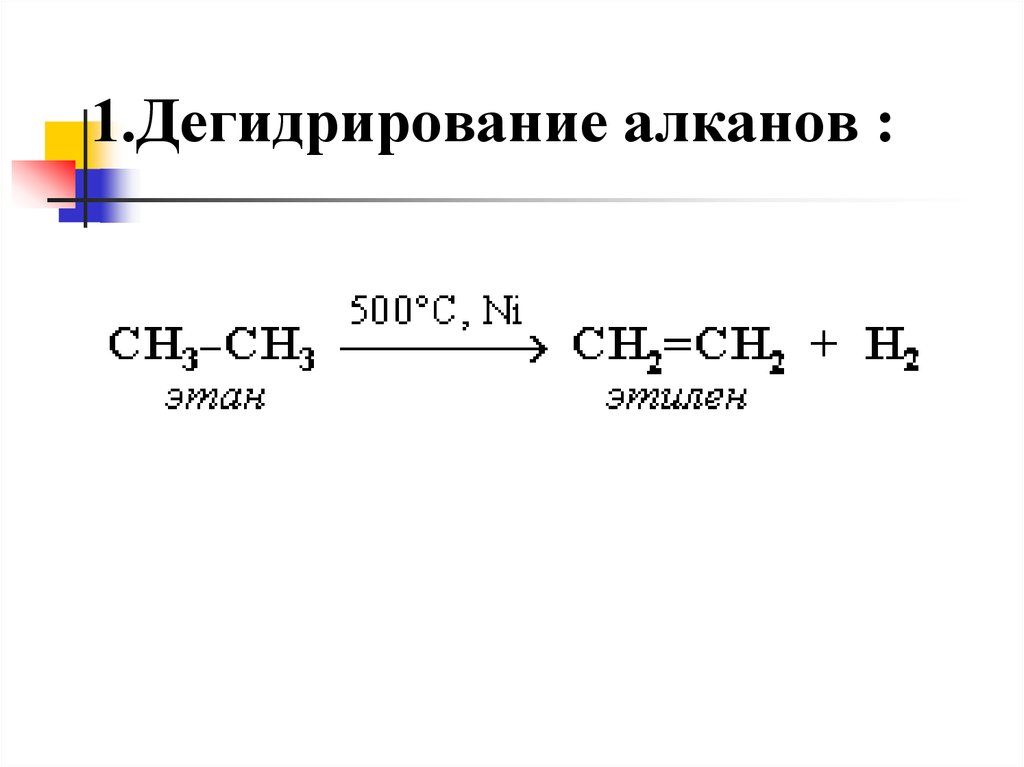
18. 1.Дегидрирование алканов :
19. 2.Крекинг алканов (под высокой температурой):
20. 2.Крекинг алканов (под высокой температурой):
C12H26Додекан
C6H14 + C6H12
гексан
гексен
С8Н18
С4Н10 + С4Н8
Октан
бутан
бутен
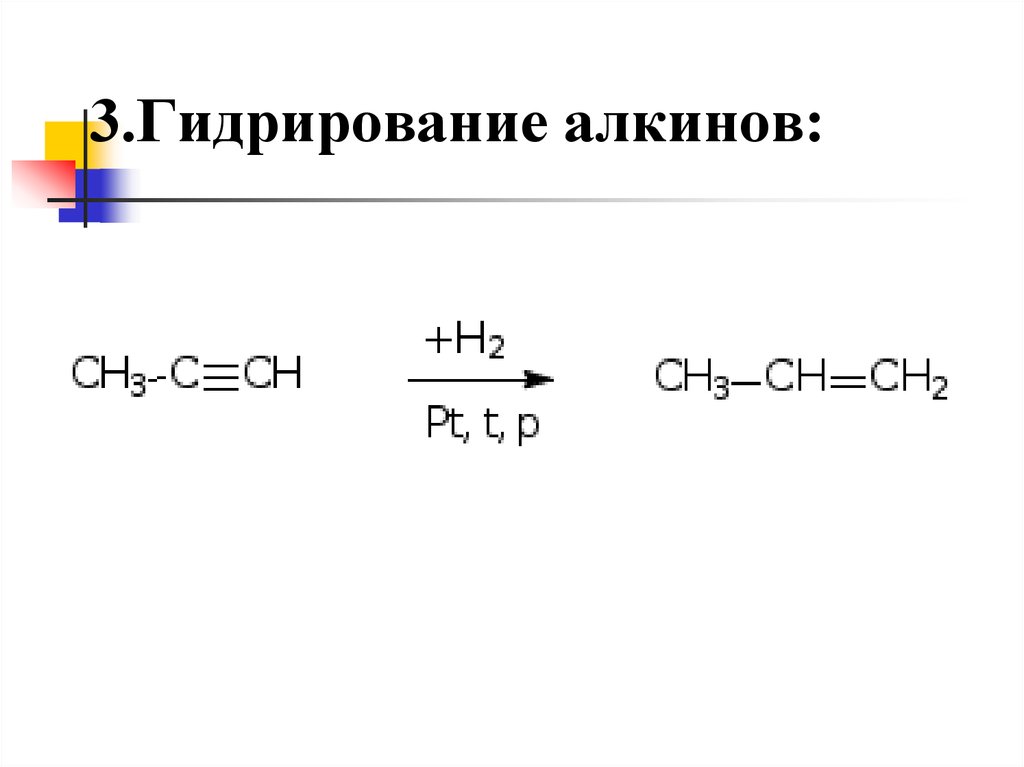
21. 3.Гидрирование алкинов:
22. 4.Дегидратация* спиртов (получение в лаборатории):
t>140°C, H2SO4(конц.)СН3-CH2-CH2-OH → СН3-CH=CH2 + H2O
*Правило А. М. Зайцева:
Отрыв атома водорода происходит от наименее
гидрогенизированного атома углерода.
23. 5.Дегидрогалогенирование* галогеналканов (по правилу Зайцева)
спиртовой раствор, tCH3-CH2-CH2-Cl +NaOH → CH3-CH=CH2+NaCl+H2O
C3H7Cl + NaOH = C3H6 + NaCl + H2O
24. 6.Дегалогенирование дигалогеналканов:
t, спирт. растворC2H4Cl2 + Zn → C2H4 + ZnCl2
25.
Спасибо за работуна уроке!


















 chemistry
chemistry








