Similar presentations:
Организация работы с наркотическими средствами, психотропными веществами, сильнодействующими, ядовитыми веществами
1.
ПЯТИГОРСКИЙ МЕДИКОФАРМАЦЕВТИЧЕСКИЙИНСТИТУТфилиал ГБОУ ВПО ВолгГМУ
Факультет последипломного
образования
Краткосрочное тематическое
усовершенствование (72 часа)
Очно-заочная форма обучения
2. Организация работы с наркотическими средствами, психотропными веществами, сильнодействующими, ядовитыми веществами и прекурсорами
Доцент БлиноваТатьяна Ивановна
3.
Незаконный оборот наркотиковв год составляет более 500 млрд.
долларов. Продажа наркотиков
обеспечивает 80% всех видов
прибыли от нелегального
бизнеса.
В Российской Федерации
наркоманов около 10 млн.
человек, из них 13% дети.
4.
• Прошло более 20 лет со дня принятияООН Конвенции о борьбе против
незаконного оборота наркотических
средств. Однако наркоугроза попрежнему является серьёзной
опасностью для любого государства,
независимо от его экономики и
географии. Смертельный бизнес
становится все изворотливей,
наркотиков все больше.
• За это время
в 2 раза возрос наркооборот,
в 2 раза - производство кокаина,
в 4 раза - опиатов,
в 7 раз - синтетических наркотиков.
5.
ОБРАЩЕНИЕ НАРКОТИЧЕСКИХ СРЕДСТВ,ПСИХОТРОПНЫХ, СИЛЬНОДЕЙСТВУЮЩИХ И
ЯДОВИТЫХ ВЕЩЕСТВ РЕГЛАМЕНТИРУЕТСЯ
НА МЕЖДУНАРОДНОМ УРОВНЕ
Единой конвенцией о наркотических средствах (Нью-Йорк,
30 марта 1961 г)
Конвенцией о психотропных веществах (Вена, 21 февраля
1971 г.)
Конвенции ООН (Вена, 1988 г.)
Политическими декларациях Генеральной Ассамблеи ООН и
МККН (Международный комитет по контролю наркотиков) ООН;
НА НАЦИОНАЛЬНОМ УРОВНЕ
Федеральным законом ФЗ- 3 «О наркотических
средствах и психотропных веществах»,
Указами Президента
Постановлениями Правительства РФ,
ведомственными приказами, в т. ч. МЗ РФ
6.
Необходимость контроля за оборотом НСи актуализация знаний нормативной базы
для медработников обусловлены :
• стремительным ростом больных
наркоманией,
• ростом онкологической
заболеваемости, требующей
паллиативной терапии;
• постоянными изменениями в
системе надзора и нормативноправовой базе обращения НС и ПВ
7. «Допуск лиц к работе с наркотическими средствами и психотропными веществами предусматривает ознакомление этих лиц с законодательством Р
«Допуск лиц к работе снаркотическими средствами и
психотропными веществами
предусматривает ознакомление этих
лиц с законодательством
Российской Федерации о
наркотических средствах и
психотропных веществах…»
Постановление Правительства
РФ от 06.08.1998 г. № 892
8. От лицензиата требуется «наличие в штате работников, имеющих среднее профессиональное, высшее профессиональное, дополнительное професси
От лицензиата требуется«наличие в штате работников, имеющих
среднее профессиональное, высшее
профессиональное, дополнительное
профессиональное образование и (или)
специальную подготовку в сфере оборота
НС, ПВ и их прекурсоров,
соответствующие требованиям и
характеру выполняемых работ»
Постановление Правительства
РФ от 22 декабря 2011 г. № 1085
9. Терминология в сфере обращения НС и ПВ Федеральный закон «О наркотических средствах и психотропных веществах» от 08.01.1998 г. № 3-ФЗ (в последн
Терминология в сфере обращения НС и ПВФедеральный закон «О наркотических средствах и
психотропных веществах» от 08.01.1998 г. № 3-ФЗ (в
последней ред. от 23.07. 2013)
наркотические средства
психотропные вещества
прекурсоры
аналоги НС и ПВ
препарат
оборот НС
незаконный оборот НС
производство НС и ПВ
переработка НС и ПВ
распределение НС и ПВ
ввоз (вывоз) НС
наркомания
больной наркоманией
незаконное потребление
НС
• государственные квоты
• профилактика наркомании
• антинаркотическая
пропаганда
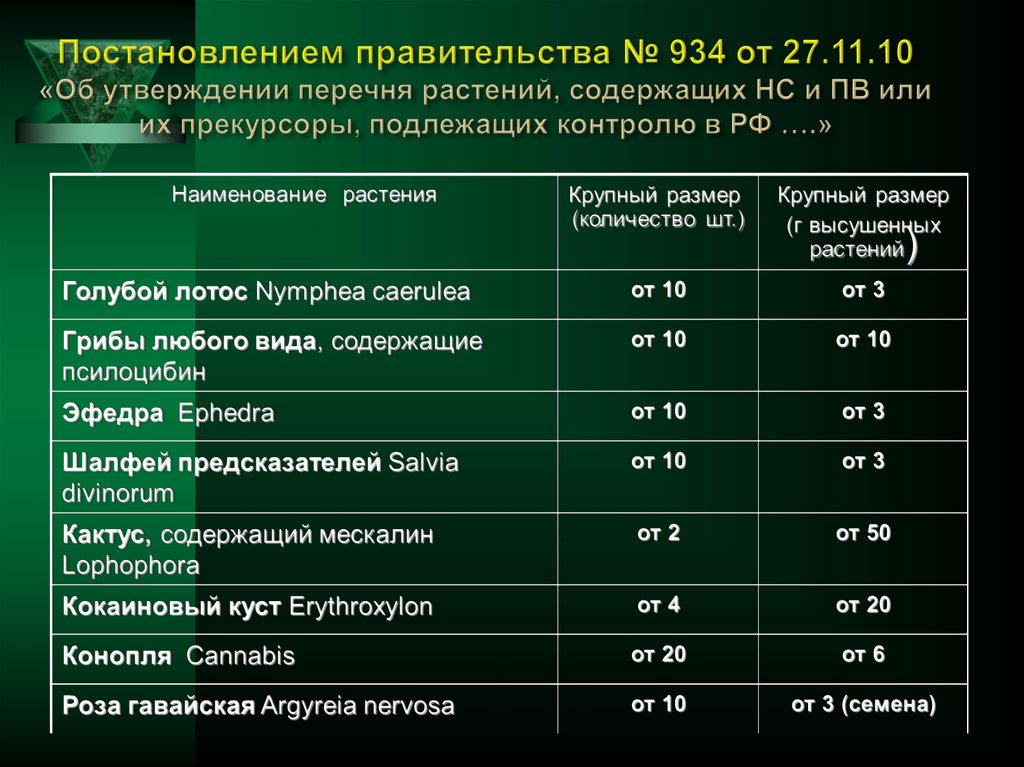
10. Перечни и списки НС, ПВ, их прекурсоров, СД и ЯВ, подлежащих контролю в РФ
11.
Списки НС, ПВ, их прекурсоров:• утверждены Постановлением Правительства РФ
от 30.06.1998 г. № 681
(в последней ред. от 09.09.2013. ПП № 788)
Список I
Список II
Список III
Список IV
Списки сильнодействующих и ядовитых
веществ:
• утверждены Постановлением Правительства РФ
от 29.12.2007 г. № 964 «Об утверждении списков
сильнодействующих и ядовитых веществ для целей ст. 234
УК РФ, …а также крупного размера…» (в ред. от 07.11.2013. )
12.
Постановление правительства РФ№ 681
13.
ИЗМЕНЕНИЯ в ПП № 681 внесены:Постановлениями правительства № 486 и № 990
(с 01.01.2011.)
Исключены из Перечня:
Остались в Перечне:
реазек (ремифентанил)
кодеин фосфат
кокаин г/х
морфина г/х
морфин сульфат
этилморфин г/х
свечи тилидина
кетамин г/х
пентобарбитал –
из Списка III
табл. барбамил +
бромизовал
Na оксибутират и соли
оксимасляной к-ты
фентанил
кодеин
кокаин
морфин
морфилонг
тилидин
кетамин
этаминал натрия (пентобарбитал) –
в Списке II
Барбамил
4-гидроксибутират Na и соли
оксимасляной к-ты
Гамма-оксимасляная к-та
14. ПОСТАНОВЛЕНИЕМ ПРАВИТЕЛЬСТВА от 03.06.10. N 398 – утвержден список прекурсоров: Табл.I Списка 4 (в конц. 10% и более) Ангидрид уксусной кислоты N-мети
ПОСТАНОВЛЕНИЕМ ПРАВИТЕЛЬСТВА от 03.06.10. N 398– утвержден список прекурсоров:
Табл.I Списка 4 (в конц. 10% и более)
Ангидрид уксусной кислоты
N-метилэфрин
Норпсевдоэфедрин, исключая катин
Псевдоэфедрин
Фенилпропаноламин (норэфедрин)
Эргометрин (эргоновин)
Эрготамин
Эфедрин
Табл. III Списка 4 (в конц. 45% и более)
Калия перманганат
ПОСТАНОВЛЕНИЕМ ПРАВИТЕЛЬСТВА от 13.06.13 г. N 496:
в Список II включен «КАРФЕНТАНИЛ» - капсулы
15.
16.
17.
ПОСТАНОВЛЕНИЕМ ПРАВИТЕЛЬСТВАот 4 февраля 2013 г. N 78:
переведены из сильнодействующих и ядовитых
веществ в перечень ПСИХОТРОПНЫХ
(Список III) следующие позиции:
Алпразолам
Мидазолам
Барбитал натрия
Нитразепам
Бромазепам
Оксазепам
Бротизолам
Темазепам
Диазепам
Тетразепам
Клоназепам
Фенобарбитал
Лоразепам
Флунитразепам
Медазепам
Флуразепам
Мезокарб
Хлордиазепоксид
Мепробамат
Эстазолам
18. Письмо МЗ РФ от 21.03.2013. № 25-4/10/2-1971
• включение в Списки III 20 указанных МНН исодержащих их ЛП с 08.08.13.;
• необходимость обеспечения условий хранения по ПП
№ 1148;
• оформить допуск лиц в соответствии с ПП № 392;
• завести Журналы учета операций в соответствии с ПП
№ 644;
• подать заявки в уполномоченную организацию_______
• *ПП от 01.03.13. № 170: «распределение ПВ
осуществляют ЮЛ независимо от формы соб-ности»
19.
СПИСКИ ПККН (протокол от 16.03.2006 г. № 1/102)Список I ПККН – сильнодействующие в-ва (126 позиций)
Список II ПККН – ядовитые в-ва (65 позиций)
Вступили в силу с 01.07.2006 г.
В соответствии с Постановлением № 964 и информационным
письмом МЗСР РФ № 4406-РХ от 24.06.2008 г.
«…ПККН утратил свое место в системе регулирования
правоотношений в сфере оборота сильнодействующих и
ядовитых веществ»
Списки, утвержденные Конвенцией ООН о психотропных
веществах 1971 г. и Конвенцией ООН о борьбе с незаконным оборотом
наркотических средств и психотропных веществ 1988 г.
(только эти СД и ЯВ подлежали хранению
по требованию приказа № 296н
- как НС и ПВ)
(в настоящее время все включены в
списки психотр. в-ств или прекурсоров )
20.
Списки А и Б – отменены приказом МЗСР РФ№ 380 от 24.05.2010.
Лекарственные в-ва, входящие в указанные
Списки, находятся на предметно-количественном
учете в аптеках и ЛПУ
Приказ МЗСР РФ от 14.12.2005 г. № 785 (в
ред. приказа от 12.02.2007 г. № 109)
- перечень
ЛС на ПКУ
262-ФЗ от 25.12.12. :
61-ФЗ дополнен Статьей 58.1 «ПКУ ЛС для
медицинского применения» - вступила в силу с апреля
2013 г.
21. ПРИКАЗ МЗ РФ от 17.07.2013. № 378н «Об утверждении правил регистрации операций, связанных с обращением ЛС для медицинского применения, включенны
ПРИКАЗ МЗ РФот 17.07.2013. № 378н
«Об утверждении правил регистрации
операций, связанных с обращением ЛС для
медицинского применения, включенных в
перечень ЛС для медицинского
применения, подлежащих ПКУ, в спец.
журналах учета операций, связанных с
обращением ЛС для медицинского
применения, и правил ведения и хранения
спец. журналов учета операций….»
22. ПРИКАЗ МЗ РФ от 17.07.2013. № 378н 1. Правила регистрации операций: - НС, ПВ и их прекурсоры по правилам, установленным ПП № 644 и ПП № 419; - остальные Л
ПРИКАЗ МЗ РФот 17.07.2013. № 378н
1. Правила регистрации операций:
- НС, ПВ и их прекурсоры по правилам,
установленным ПП № 644 и ПП № 419;
- остальные ЛС в спец. журналах учета:
приложение 1 форма для оптовых организаций,
приложение 2 форма для аптечных организаций,
приложение 3 форма для ЛПУ
Регистрация ведется по каждому наименованию и
дозировке в отдельном журнале или на
развернутом листе, лицом, уполномоченным
приказом руководителя
23. 2. Правила ведения и хранения спец. журналов: - на бумажном носителе, прошиваются, заверяются подписью и печатью руководителя; - заводятся на
2. Правила ведения и хранения спец.журналов:
- на бумажном носителе, прошиваются, заверяются
подписью и печатью руководителя;
- заводятся на календарный год;
- на электронных носителях ежемесячно распечатываются,
брошуруются, заверяются;
- записи ведутся уполномоченным лицом в конце рабочего
дня по приходным и расходным документам (хранятся
вместе с журналом);
- исправления заверяются только уполномоченным лицом;
- в последний день месяца уполномоченное ицо проводит
сверку и делает запись в журнале;
- журналы хранятся в сейфе, ключ у уполном. лица;
-заполненные журналы чдаются в архив.
СРОК ХРАНЕНИЯ НЕ УКАЗАН.
24. В журналы ПКУ вносятся все ЛС из ПП № 964 от 29.12.2007 г. ( в посл. ред. ПП № 999 от 07.11.2013. )
С 21.11.2013:• КЛОЗАПИН
• Азалептин
• Алемоксан
• Лепонекс
• Азалепрол
25.
Противоречия нормативно-правовых актов,утверждающих списки веществ с
ограниченным оборотом
•сибутрамин, даназол, 1-тестостерон есть в ПП № 964, но нет в
приказе МЗСР №785,
•эфедрин и его соли согласно ПП №964 – сильнодействующие в-ва,
по ПП №681 – прекурсоры,
•эргометрин, ангидрид уксусной кислоты, эрготамин по ПП
№964 – ядовитые в-ва, по ПП №681 – прекурсоры,
•клонидин (клофелин), золиксон (имован), золпидем (ивадал)
есть в ПП №964, но нет ни в перечне Конвенций ООН, ни в ПП №
681.
При контроле оборота должны применять максимальные
ограничения , предусмотренные любым из списков, в которые
данное вещество включено
26.
ПРИМЕР :Каковы правила хранения и отпуска препаратов,
содержащих сибутрамин (меридия, линдакса, редуксин)1.
аптеки, имеющие лицензию на фармдеятельность, имеют
право осуществлять оборот этих веществ (письмо МЗСР
РФ № 4406-РХ от 24.06.2008.),
2.
сибутрамин не включен в перечни Конвенции ООН (1971,
1988 г.г.), приказ № 785 о ПКУ, следовательно
препараты, содержащие сибутрамин не
подлежат ПКУ и на них не распространяются
специальные требования по хранению
основного запаса,
3.
Отпускается из аптек по рецепту, выписанному на бланке
107/У
27.
Лицензированиедеятельности,
связанной с оборотом
наркотических средств,
психотропных веществ
и их прекурсоров
28.
29.
30.
31.
32.
Процедура лицензирования описана введомственных актах:
В приказе МЗСР РФ от 29.03. 2012 г. "Об утверждении
Административного регламента Федеральной службы по
надзору в сфере здравоохранения и социального развития
по исполнению государственной услуги по
лицензированию деятельности по обороту наркотических
средств, психотропных веществ…..»
В приказе МЗСР РФ № 158 от 16.03. 2010 г. «Об
утверждении методических указаний по осуществлению
органами государственной власти субъектов РФ
переданных полномочий по лицензированию
деятельности, связанной с оборотом НС и ПВ» (приказ применяется в части, не противоречащей
99-ФЗ. Проект нового приказа от 23.01.13)
33.
Приказ МЗСР РФ № 158:1.Общие сведения, содержащие ссылки на нормативно-правовую
базу, полномочия лицензирующего органа, условия оплаты услуг.
2. Механизм предоставления лицензий, сроки исполнения,
требования к документам (в т.ч. в электронном виде),
3. Переоформление лицензий (продление)
4. Приостановление или прекращение действия лицензии.
5. Контроль за соблюдением лицензионных требований и условий
(порядок проведения проверок)
34.
Документы, необходимые для прохождениялицензирования оформляются в соответствии с
Приказом ФСКН РФ от 12.01.2012 г. № 9 (вместо пр. № 451)
«Об утверждении административного регламента федеральной
службы российской федерации по контролю за оборотом
наркотиков по предоставлению государственной услуги по
выдаче заключений о соответствии установленным требованиям
объектов и помещений, где осуществляется деятельность,
связанная с оборотом наркотических средств и психотропных
веществ… (срок выдачи 21 день)
Приказом ФСКН РФ от 29.12.2011 г. № 580 (вместо пр. №450)
«Об утверждении административного регламента федеральной
службы российской федерации по контролю за оборотом
наркотиков по предоставлению государственной услуги по
выдаче заключений об отсутствии у работников…» (срок
выдачи 34 дня)
35.
Контроль за соблюдениемлицензионных требований
Федеральный закон № 294-ФЗ от 26.12.2008г. (в ред. от
27.12.2009 г.) «О защите прав юридических лиц и
индивидуальных предпринимателей при осуществлении
государственного контроля (надзора) и муниципального
контроля»:
- утвержден порядок проведения плановых и внеплановых мероприятий по
контролю;
- узаконена недопустимость проводимых в отношении одного юр. лица
несколькими органами гос. контроля проверок исполнения одних и тех же
обязательных требований;
- утверждены права юр. лиц при проверках и порядок их защиты (глава 3);
- установлено, что плановые проверки проводятся 1 раз в 3 года, (для
сферы здравоохранения 2 и более раз в 3 года – ст.9)
36.
37.
Постановление Правительства РФ № 944 от 23.11.2009 г.«Об утверждении видов деятельности в сфере
здравоохранения и соц.развития, осуществляемых юр.
лицами и инд. предпринимателями, в отношении
которых плановые проверки проводятся с установленной
периодичностью»
Оказание амбул.-поликлин.
медицинской помощи
- проверки лицензир . органа
(Росздравнадзор) 1 р. в год;
Оказание стац. и сан-курорт.
медицинской помощи
- Росздравнадзор 1 раз
в 2 года;
Оказание скорой медицинской
помощи
Розничная торговля ЛС и
изготовление ЛС аптеками
- Росздравнадзор 1 раз
в 2 года;
- Росздравнадзор 1 раз в год
38.
Приказ Минэкономразвития № 141 от30.04.2009 г. «О реализации положений
ФЗ «О защите прав юридических лиц….»
Типовая форма акта проверки;
Типовая форма журнала проверок, проводимых
органами гос. контроля (надзора):
- прошнуровывается, пронумеровывается, ведется
лицензиатом;
- наименование граф;
- заполняется и подписывается лицом, проводившим
проверку;
39.
На основании приказа Минэкономразвития РФ от30.04.2009. № 141 издан приказ Росздравнадзора
от 01.03.2010. №1490-Пр/10 «Об использовании
форм актов проверки возможности выполнения
соискателями лицензии….»
Утверждены:
Акт проверки лицензионных требований и
условий при осуществлении
деятельности, связанной с оборотом НС
и ПВ.
Акты проверки медицинской,
фармацевтической деятельности,
производства лекарств и пр.
40.
Аксиома проверок1. Любая проверка должна проводиться на основании
приказа (распоряжения) руководителя проверяющего
органа или его заместителя
2. В приказе (распоряжении) указывается:
Номер и дата приказа
Наименование лицензирующего органа
Ф.И.О. и должность лиц, уполномоченных на проведение
проверки
Наименование проверяемого ЮЛ или Ф.И.О ИП,
Цели, задачи и предмет проверки
Правовые основания проведения проверки
Срок проверки: дата начала и окончания
3. Проверка должна проводиться в присутствии
руководителя проверяемой организации или лица его
замещающего, на основании доверенности или приказа
руководителя проверяемой организации
41.
Члены комиссии по проверке не вправе:проверять выполнение обязательных требований, не относящихся к их
компетенции ;
осуществлять плановые проверки в случае отсутствия должностных
лиц или работников проверяемых ЮЛ либо их представителей;
требовать представления документов, информации, образцов
продукции, если они не являются и не относятся к предмету
мероприятия по контролю, а также изымать оригиналы документов,
относящихся к предмету проверки;
требовать образцы ЛС для проведения их исследований, без
оформления акта об отборе образцов;
превышать установленные сроки проведения мероприятий по
контролю
( 294-ФЗ: не более 20 дней, приказ МЗСР РФ № 278н:
не более 30 дней)
42.
Предмет внепланового мероприятия прилицензионном контроле
Контроль исполнения ранее выданных предписаний
а также в случаях:
Получения информации от ЮЛ, ИП или органов государственной
власти:
о возникновении аварийных ситуаций;
о нарушениях технологических процессов;
о выходе из строя систем оборудования, которые могут
причинить вред жизни и здоровью людей и окружающей среде;
возникновение угрозы здоровью граждан, повреждения
имущества ЮЛ и ИП
Обращения граждан, ЮЛ и ИП о нарушении их прав
( анонимные обращения не могут служить основанием для
проверки)
43.
КоАП РФ: ст. 14.1. :Осуществление лицензируемой деятельности с грубым
нарушением лицензионных требований и условий влечет за
собой
ответственность, устанавливаемую решением суда:
- наложение административного штрафа на должностных
лиц – от 40 до 50 МРОТ; на юридических лиц - от 400 до 500
МРОТ;
- административное приостановление деятельности на срок
до 90 суток;
- при невозможности или нежелании устранения нарушений
в установленные сроки – аннулирование лицензии
КоАП РФ: ст.6.16. Нарушение правил оборота НС и ПВ:
- административный штраф от 200 до 400 тыс. рублей с
конфискацией НС (или без нее),
- административное приостановление деятельности на срок
до 90 суток
44.
Правила перевозкиНС и ПВ на
территориии РФ
45.
Правила перевозки НС и ПВ натерриториии РФ
ППРФ от 12.06.2008. № 449 (в ред. от 16.02.13.)
«О порядке перевозки НС и ПВ на территории РФ, а
также оформления необходимых для этого
документов»
Лицензия на осуществление охранной деятельности
(вневедомственная охрана или частная охранная
организация)
Приказ руководителя ЛПУ о назначении лиц,
ответственных за перевозку (при каждой перевозке)
46.
Товаро-транспортные накладные, счета,требования, пр.
Заверенные печатью ЮЛ копии лицензии
Копию приказа руководителя ЛПУ
Маршрут перевозки (по утвержденной ППРФ
форме)
Акт опечатывания (пломбирования) с
указанием номеров печатей и пломб (по
утвержденной ППРФ форме)
47.
Требования кперсоналу
48.
Требования к персоналу. Допуск к работе• Постановление Правительства РФ от 22.12.2011 г. № 1085 (в ред.
от 04.09.12.) «О лицензировании деятельности по обороту
наркотических средств, психотропных веществ и их прекурсоров,
культивированию наркосодержащих растений»
• Постановлением Правительства РФ от 06.08.1998 г. № 892
«Об утверждении Правил допуска лиц к работе с наркотическими
средствами и психотропными веществами»
В редакции
Постановления Правительства РФ от 22.12.2009 г. № 1065
- обязательность психиатрического освидетельствования,
-
получение допусков ФСКН только по запросу,
-
срок действия допуска ограничивается сроком действия трудового
договора со специалистом.
( вступило в силу с 22.07.2010)
• Приказ МЗСР РФ от 13.05.2005 г. № 330 «О перечне должностей
медицинских и фармацевтических работников и учреждений
(организаций) с правом отпуска наркотических средств и
психотропных веществ физическим лицам»
49.
Требования кхранению НС, ПВ и их
прекурсоров
50.
Требования к хранению НС, ПВ и ихпрекурсоров
Постановление правительства РФ N 1148 от
31.12.2009. «О порядке хранения НС и ПВ»
(в ред. от 16.02.2013.)
Хранение НС и ПВ осуществляется в изолированных
помещениях, специально оборудованных инженерными и
техническими средствами охраны, и в местах временного
хранения
Помещения подразделяются на 4 категории. В отношении
помещений каждой из категорий устанавливаются базовые
требования к их оборудованию инженерными и техническими
средствами охраны, а также к условиям хранения в них
наркотических средств и психотропных веществ.
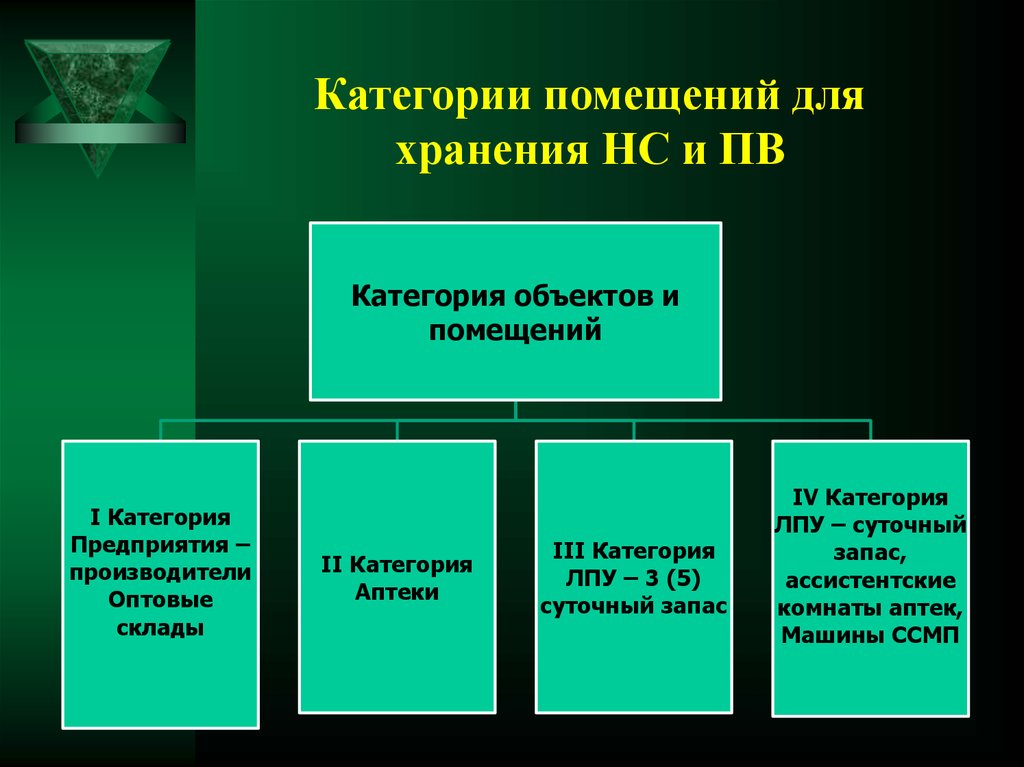
51.
Категории помещений дляхранения НС и ПВ
Категория объектов и
помещений
I Категория
Предприятия –
производители
Оптовые
склады
II Категория
Аптеки
III Категория
ЛПУ – 3 (5)
суточный запас
IV Категория
ЛПУ – суточный
запас,
ассистентские
комнаты аптек,
Машины ССМП
52.
Требования к технической укрепленности• Помещение, относящееся к 3-й категории,
оборудуется входной металлической дверью,
деревянной дверью, усиленной с 2 сторон листовым
железом, либо дверью из иного материала,
обладающей классом защиты от разрушающих
воздействий не ниже 3-го.
• Входная дверь имеет не менее 2 запирающих
устройств 3-го класса защиты от разрушающих
воздействий.
• Наркотические средства и психотропные вещества
хранятся в запирающихся насыпных или
прикрепленных к полу (стене) сейфах не ниже 3-го
класса устойчивости к взлому. Сейф массой менее
1000 килограммов прикрепляется к полу или стене
либо встраивается в стену с помощью анкерного
крепления.
53.
54.
*Укладка выездной бригады СМП всоответствии с приказом МЗСР РФ от
11.06.2010 г. № 445н (до 01.01.14.)
НС и ПВ для этих целей получает фельдшер центральной
заправки по требованию у главной мед. сестры СМП,
НС и ПВ комплектуются в отдельные заправочные блоки
и хранятся в сейфах,
отпуск заправочных блоков руководителю бригады СМП
осуществляется фельдшером центральной заправки.
_________________________________________________________
количество ампул в укладке (норматив запаса)
определить приказом гл. врача !
55. ТРЕБОВАНИЯ К ПОМЕЩЕНИЯМ
Постановление правительства РФ от 31.12.2009 г.№ 1148 «О порядке хранения НС и ПВ»
Приказ ФСКН РФ от 12.01.12.№ 9 «Об утвердлении
администратиыного регламента……по выдаче
заключений о соответствии установленным
требованиям объектов и помещений….»
Постановление правительства РФ от 18.08.10. №
640 «Об утверждении правил производства,
переработки, хранения, реализации, приобретения,
использования и уничтожения прекурсоров НС и
ПВ»
56. Постановление правительства РФ от 13.12.12. № 1303 – уточнение порядка хранения прекурсоров
• «Хранение прекурсоров осуществляетсяв металлическом шкафу (сейфе) или
изолированном помещении, которые
после окончания рабочего дня
запираются на ключ и опечатываются
(опломбировываются)»
Перманганат калия (табл. 3):
«исключение доступа посторонних лиц» (3-ФЗ).
Включен в перечень ПКУ (приказ № 785):
«хранить с метал. или деревянных шкафах,
опечат. в конце раб. дня» (приказ № 706н)
57.
Приказ МЗ РФ от 12.11.1997 г. № 330«О мерах по улучшению учета, хранения,
выписывания и использования наркотических
средств и психотропных веществ»
В редакции Приказа МЗСР РФ от 17.11.2010 № 1008н
«О признании утратившим силу некоторых приложений к
приказу № 330»:
- Приложение 1. Типовые требования по технической
укрепленности…
- Приложение 2. Форма спец. Рецептурного бланка
- Приложение 4. Правила хранения и учета НС и ПВ в аптеках
- Приложение 5. Правила хранения и учета НС и ПВ и спец.
рецептурных бланков в ЛПУ
- Приложение 7. Правила хранения и учета НС и ПВ на аптечных
складах (базах)
- Приложение 9. Правила хранения и учета НС и ПВ в НИИ….
58.
Учет НС и ПВ иотчетность
59.
Учет НС и ПВ и отчетность о деятельности,связанной с оборотом НС, ПВ и их
прекурсоров
Постановление Правительства РФ от 04.11.2006 г. № 644
«О порядке представления сведений о деятельности, связанной с
оборотом наркотических средств и психотропных веществ, и
регистрации операций, связанных с оборотом наркотических средств,
психотропных веществ» (и прекурсоров- слово отменено)»
Постановление Правительства РФ от 09.06.2010 г. № 419
«О предоставлении сведений о деятельности, связанной с оборотом
прекурсоров НС и ПВ и регистрации операций, связанных с их
оборотом»
1.
2.
Правила представления отчетов о деятельности
Порядок ведения и хранения специальных журналов
регистрации операций, связанных с оборотом НС, ПВ и их
прекурсоров
60.
Правила ведения и храненияспециальных журналов для НС и ПВ
(ПП № 644)
• Ведутся по утвержденной ППРФ форме
• На каждое наименование ведется отдельный журнал
(или отдельный развернутый лист)
• Назначаются лица, ответственные за ведение и
хранение журналов
• Вместе с журналом хранится папка с документами,
подтверждающими совершение операции
• Нумерация в пределах календарного года
• Ежемесячно вносятся итоги инвентаризации
• Хранятся в сейфе. Сданные в архив вместе с
документами хранятся 10 лет
61. Нормативы потребности и запасов
62.
Нормативы потребности• Приказ МЗ РФ от 12.11.1997 г. № 330 (в ред.
приказа МЗ РФ от 26.06.2008 г. № 296н) –
Приложение 3
• Письмо МЗСР РФ от 01.12.10. № 25-1/10/2-11295
«… Данные нормативы устарели и требуют
пересмотра…»
Нормативы запасов
Рассчитываются из выделенных квот (3- или 5дневный запас) или утверждается руководителем
ЛПУ.
Превышение норматива запасов – грубое
нарушение правил хранения!
63.
Хранение основного и 3-х дневногозапаса НС и ПВ
• Приказ МЗСР РФ № 397 от 16.05.2011. «Об
утверждении специальных требований к условиям
хранения НС и ПВ, зарегистрированных в качестве
ЛС для мед. применения в аптеках, ЛПУ…»:
ЛС для парентерального, внутреннего и наружного применения
хранятся раздельно;
на дверце сейфа – списки с В.с.д. и В.р.д.; в ЛПУ –
дополнительно списки противоядий;
хранение термолабильных ЛС в запирающихся холодильниках
или холодильниках, отделенных металлической решеткой с
замком;
в местах временного хранения в термоконтейнере, помещенном в
сейф, или в контейнере, помещенном в термоконтейнер;
подлежащие списанию и уничтожению – на отдельной полке или
отдельном отделении сейфа
64. Назначение, выписывание, формы рецептурных бланков
65.
Назначение, выписывание, формырецептурных бланков
ПРИКАЗ МЗ РФ от 20.12.12. № 1175н «Об утверждении
порядка назначения и выписывания ЛП, а также форм
рецептурных бланков на ЛП, порядка оформления
указанных бланков, их учета и хранения» (вступает в
силу с 01.07.13.)
Приказ МЗ РФ от 26.02.13. № 94н «О внесении
изменений в пр. № 110…..»
- отменены приложения 3-6, 11, 12, 13
-органиченно применимы прилож. 7-10, 14, 15
Приказ МЗ РФ от 01.08. 12. № 54н «Об утверждении
формы бланков рецептов, содержащих назначение
наркотических средств или психотропных веществ,
порядка их изготовления, распределения, регистрации,
учета и хранения, а также правил оформления» (с
01.07.13.)
66. Приказ 1175н утвердил порядок назначения и выписывания ЛП, в т.ч. НС и ПВ
• Приложение 1. Предельно допустимое количествоотдельных НС и ПВ для выписывания на 1 рецепт
• Приложение 2. Рекомендованное количество
отдельных ЛП для выписывания на 1 рецепт
(комбинированные ЛП, сод. кодеин, эфедрин,
теофедрин, псевдоэфедрин, фенилпропаноламин,
фенобарбитал, анаболические гормоны, др.)
Утвердил формы рецептурных бланков
107-1/у и 148-1/у (с 01.07.13.) ___________
* Письмо МЗ РФ от 04.07.13. № 25-4/10/2-4818 :
«полагаем возможным разрешить
использование старых бланков до 31.12.13»
67.
Отпуск комбинированных ЛП,содержащих малые количества
НС и ПВ
Постановление правительства РФ от 20.06.
2011 г. N 599 «О мерах контроля в отношении
препаратов, которые содержат малые
количества НС, ПВ и их прекурсоров,
включенных в перечень …» (отпуск
кодеинсодержащих препаратов по рецепту с
01.06.12.)
• Приказ МЗСР РФ № 157н от 16.03.10 « Об
утверждении предельно допустимого количества
НС, ПВ и их прекурсора, содержащегося в
препаратах»
68. Приказ МЗСР РФ № 562н от 17.05.2012. «Об утверждении порядка отпуска физическим лицам ЛП, содержащих иалые количества НС, ПВ, их прекурсоров и др.
Приказ МЗСР РФ № 562н от 17.05.2012. «Обутверждении порядка отпуска физическим лицам ЛП,
содержащих иалые количества НС, ПВ, их прекурсоров и
др. фармакологически активные вещества»
Отпуск по рецептам 107-1/у:
Комбинированные препараты, содержащие
эрготамин до 5 мг,
эфедрин до 100мг,
псевдоэфедрин до 30 мг
Отпуск по рецептам 148-1/у-88:
кодеин и его соли до 20 мг,
Псевдоэфедрин до 60 мг,
Эфедрин до 300 мг,
Фенилпропаноламин до 75 мг.
69. С 08.08.2013. 20 сильнодействующих ЛС стали ПСИХОТРОПНЫМИ Приказ МЗ РФ № 369н от 10.07.13 «О внесении изменений в некоторые приказы МЗ РФ»: (приказ № 157
С 08.08.2013. 20 сильнодействующих ЛС сталиПСИХОТРОПНЫМИ
Приказ МЗ РФ № 369н от 10.07.13 «О внесении
изменений в некоторые приказы МЗ РФ»:
(приказ № 157)
Фенобарбитал до 50 мг.,
Хлордиазепоксид (Элениум) до 20 мг
( приказ № 562н)
приведены возможные сочетания данных ЛВ
в ЛФ с дозировками
(корвалола и валокардина – НЕТ)
Положение приказа № 157
«Иные комбинированные лекарственные
препараты отпускаются из аптек, аптечных
пунктов и аптечных киосков БЕЗ РЕЦЕПТА» осталось действующим (не более 2-х упаковок)
70. Письмо МЗ РФ № 25-4/10/2-3714 от 28.05.13. (в связи с ПП № 78)
• «ЛС, подлежащие ПКУ (которыми являются СДВ,находящиеся под международным контролем), и ПВ
Списка III перечня выписываются на рецептурных
бланках 148-1/у-88»
• «В отношении комбинированных ЛП, содержащих
конвенционные СДВ, предполагается исключение
некоторых мер контроля путем отнесения их к
препаратам, содержащим малое количество НС, ПВ и
их прекурсоров.
71.
РАСПРЕДЕЛЕНИЕ НС И ПВ В АПТЕЧНЫЕ ИМЕДИЦИНСКИЕ ОРГАНИЗАЦИИ
Постановление Правительства РФ от 26.07.2010 г. № 558
«О порядке распределения, отпуска и реализации НС и ПВ»
Постановление Правительства РФ от 01.03.2013 № 170 (с 04.07.) –
уполномоч. организация любой формы собственности
Приказ Минпромторга РФ от 16.11. 2010г. № 1029
«Об утверждении форм документов, связанных с формированием
плана распределения НС и ПВ»
Распределение НС и ПВ осуществляется уполномоченным
государственным унитарным предприятием, государственным
учреждением или иными ЮЛ независимо от формы
собственности (ПП № 170 от 01.03.13) на основании заявок на
получение НС и ПВ.
В заявке указываются:
сведения о юридическом лице,
номер и срок действия лицензии на деятельность, связанную с оборотом
НС и ПВ,
наименование НС и ПВ, их форма выпуска и количество,
обоснование расчетов потребности в НС и ПВ.
72.
Упаковка имаркировка НС и
ПВ
73. Приказ МЗ РФ № 397 от 16.05.11. "Об утверждении специальных требований к условиям хранения наркотических средств и психотропных веществ…»
Приказ МЗ РФ № 397 от 16.05.11."Об утверждении специальных требований к
условиям хранения наркотических средств и
психотропных веществ…»
Внешняя упаковка НС и ПВ должна исключать возможность их
извлечения без нарушения целостности указанной упаковки
Внутренняя упаковка НС и ПВ , используемых в медицинских
целях, должна быть помечена двойной красной полосой
На экстемпоральных ЛФ: надпись черной краской «Яд»,
«Внутреннее»(наружное, др.), № аптеки, состав ЛС, дата
изготовления, № анализа, срок годности, подписи
В случаях несоответствия внешней и внутренней упаковок и
маркировки требованиям, предусмотренным пунктами 1-3
статьи 27, НС и ПВ уничтожаются в соответствии с
законодательством РФ (№ 3-ФЗ от 08.01.1998 г., Статья 27)
74. Порядок уничтожения НС и ПВ и их прекурсоров
75.
• Приказ МЗ РФ от 28.03.2003 г. № 127 «Обутверждении Инструкции по уничтожению
наркотических средств и психотропных веществ,
входящих в списки II и III Перечня НС, ПВи их
прекурсоров, подлежащих контролю в РФ,
дальнейшее использование которых в
медицинской практике признано
нецелесообразным»
• 305-ФЗ от 30.12.12. (вступил в силу с 10.04.13.) –
предоставлено право уничтожения НС, ПВ и их
прекурсоров МУПам
• Постановление правительства № 674 от 03.09.10.
Об утверждении правил уничтожения
недоброкачественных лекарственных средств,
фальсифицированных лекарственных средств и
контрафактных лекарственных средств
76.
Уничтожение осуществляют государственные унитарныепредприятия, государственные учреждения, МУПы и
МУЗы, входящие в муниципальную систему здравоохранения
в случаях:
истек срок годности;
НС или ПВ подвергалось химическому или
физическому воздействию;
неиспользованные НС, принятые от родственников
умерших больных;
трудно определить, является препарат НС или ПВ;
конфискованное из незаконного оборота
ПРОЕКТ ПРИКАЗА МЗ РФ от 31.01.13. « о внесении
изменений в приказ № 127…»:
«ЮЛ, имеющие лицензию на работу с НС без указания
вида работы (услуги) по уничтожению, заключают
договора…»
77.
СПИСАНИЕ НС, ПВ И ИХПРЕКУРСОРОВ
С ИСТЕКШИМ СРОКОМ ГОДНОСТИ
Факт обнаружения таких ЛП инвентаризационная
комиссия и материально-ответственное лицо
отражают в инвентаризационных описях
(Приказ Минфина РФ
от 13.06.1995 №49)
Письмо ФНС от 16.06.11. № ЕД-4-3/9486
«О порядке совершения операций с ЛС с истекшим
сроком годности»
78.
79.
Приказ МЗ РФ от 12.11.1997 г. № 330(в ред. приказа МЗ РФ от 26.06.2008 г. № 296н):
Приложение 6 – Положение о списании и
уничтожении наркотических средств и
психотропных веществ и специальных рецептов,
неиспользованных онкологическими больными
(форма журнала учета)
Приложение 10 – Акт на уничтожение
использованных ампул из-под наркотических
средств и психотропных веществ в учреждениях
здравоохранения
Сроки списания: на 30 число каждого месяца акт
списания,
до 5 числа – акт уничтожения
80.
ТДТС, содержащие НС81.
Благодарю за внимание.Желаю Вам здоровья и благополучия!















































































 medicine
medicine








