Similar presentations:
28. Кремний и его соединения. Силикатная промышленность
1.
Кремний и его соединения.Силикатная промышленность
2.
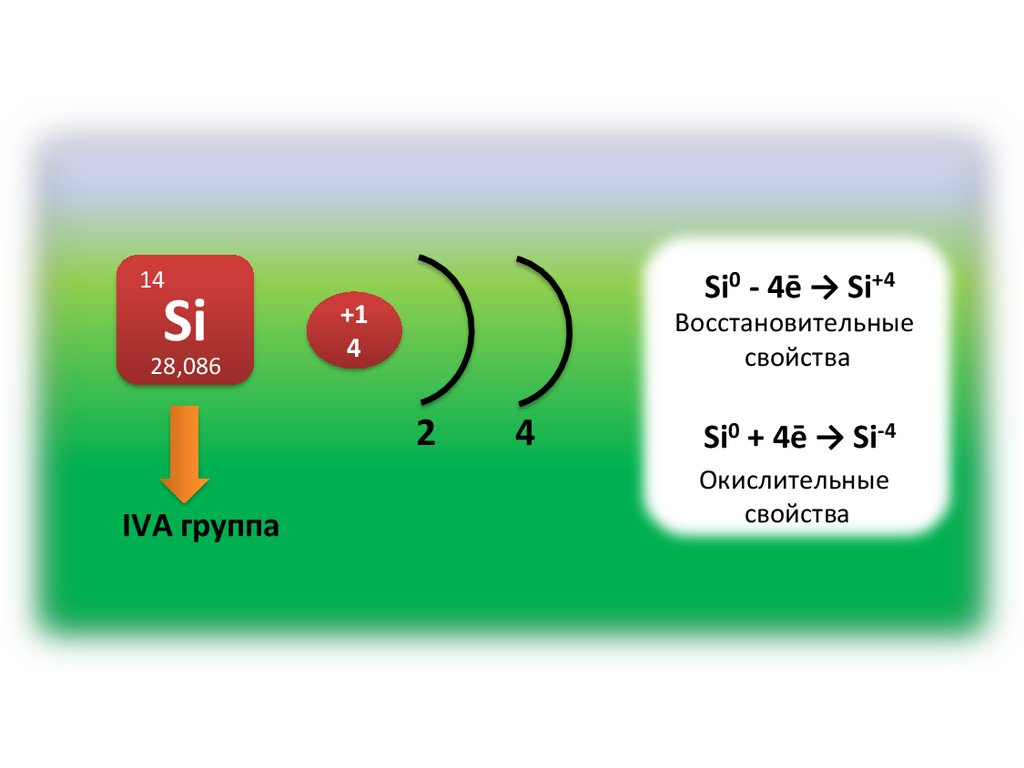
14Si
28,086
Si0 - 4ē → Si+4
+1
4
Восстановительные
свойства
2
IVA группа
4
Si0 + 4ē → Si-4
Окислительные
свойства
3.
Состав земнойкоры
О
7%
18%
26%
SiO2
оксид кремния (IV)
кремнезём
горный
хрусталь
топаз
аметист
опал
халцедон
агат
яшма
сердолик
49%
4.
Природные силикаты – сложные вещества.Алюмосиликаты – силикаты, в состав которых входит
алюминий.
каолинит
полевой шпат
Al2O3 · 2SiO2 · 2H2O
K2O · Al2O3 · 6SiO2
слюда
K2O · Al2O3 · 6SiO2 · 2H2O
5.
Асбест используется дляизготовления огнеупорных тканей.
6.
Из разновидностей минералов на основе оксида кремния (IV)первобытные люди изготавливали орудия труда.
7.
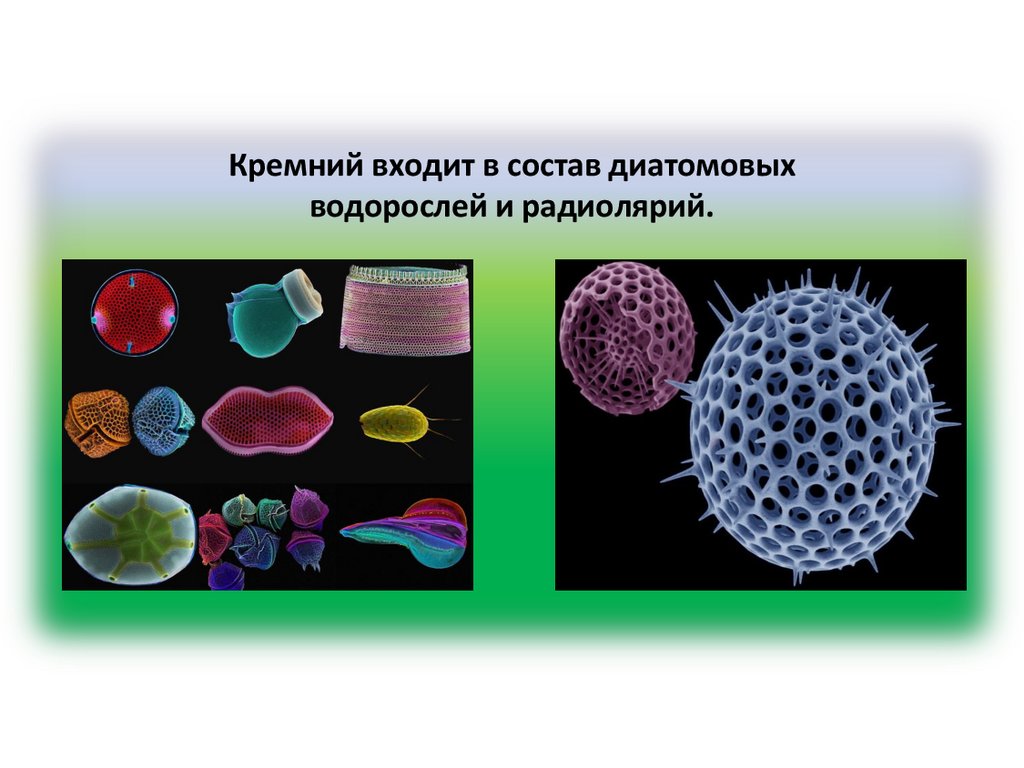
Оксид кремния (IV) у растений и животных8.
Кремний входит в состав диатомовыхводорослей и радиолярий.
9.
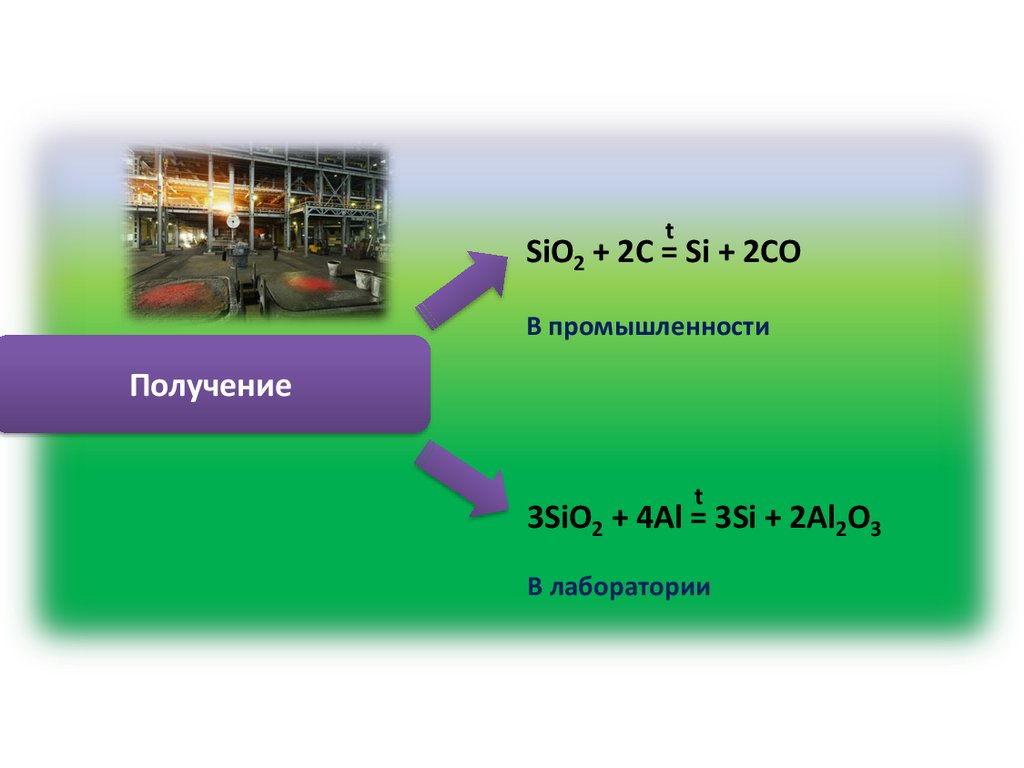
tSiO2 + 2C = Si + 2CO
В промышленности
Получение
t
3SiO2 + 4Al = 3Si + 2Al2O3
В лаборатории
10.
Аллотропные модификации кремнияАморфный кремний
Кристаллический
кремний
➢ Это бурый порошок.
➢ Твёрдое вещество тёмносерого цвета с
металлическим блеском.
➢ Он хрупок и тугоплавок.
11.
Кремний является полупроводником.С повышением температуры его
электропроводность увеличивается.
12.
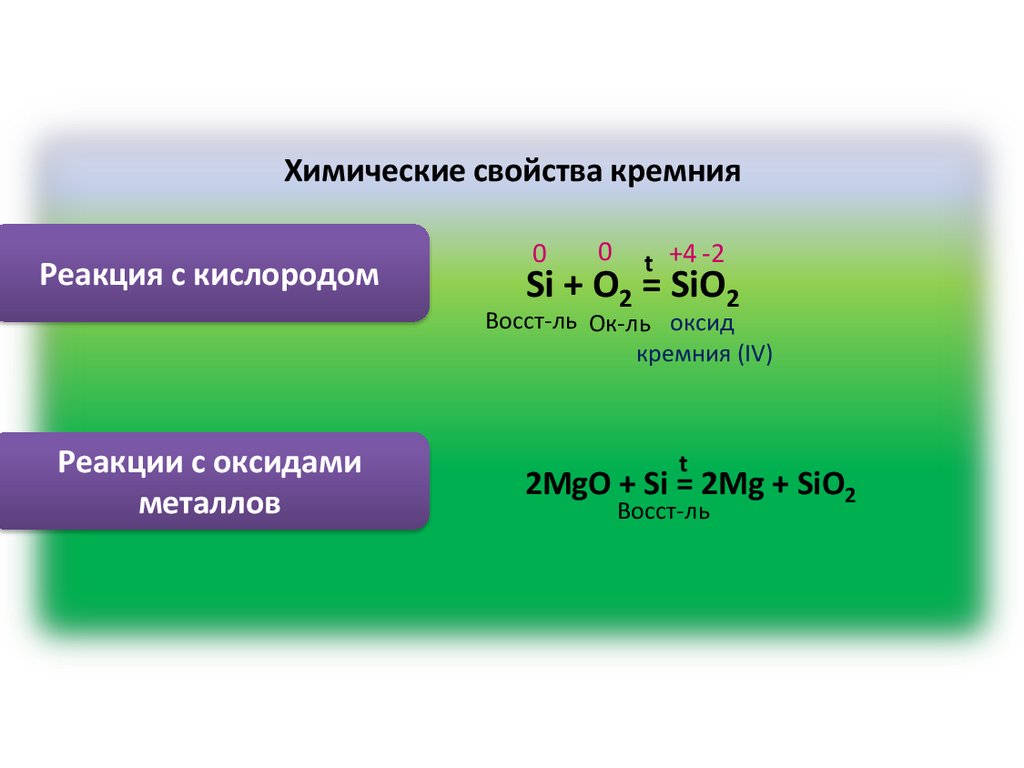
Химические свойства кремнияРеакция с кислородом
0
0
t +4 -2
Si + O2 = SiO2
Восст-ль Ок-ль оксид
кремния (IV)
Реакции с оксидами
металлов
t
2MgO + Si = 2Mg + SiO2
Восст-ль
13.
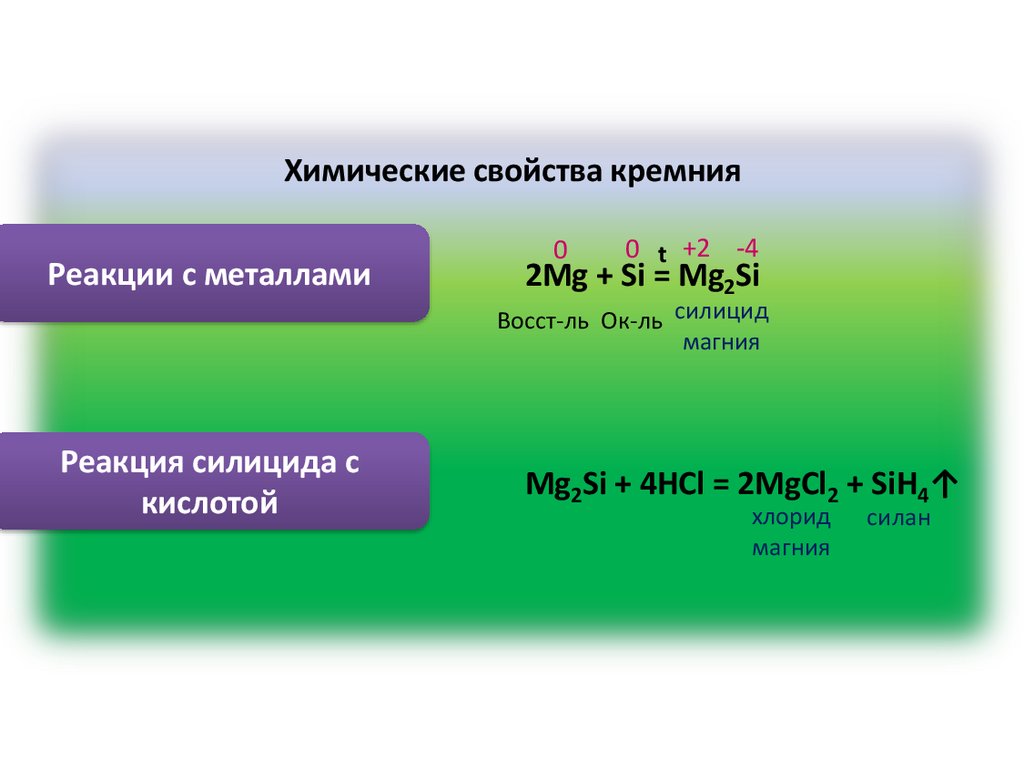
Химические свойства кремнияРеакции с металлами
0
0 t +2 -4
2Mg + Si = Mg2Si
Восст-ль Ок-ль силицид
магния
Реакция силицида с
кислотой
Mg2Si + 4HCl = 2MgCl2 + SiH4↑
хлорид
магния
силан
14.
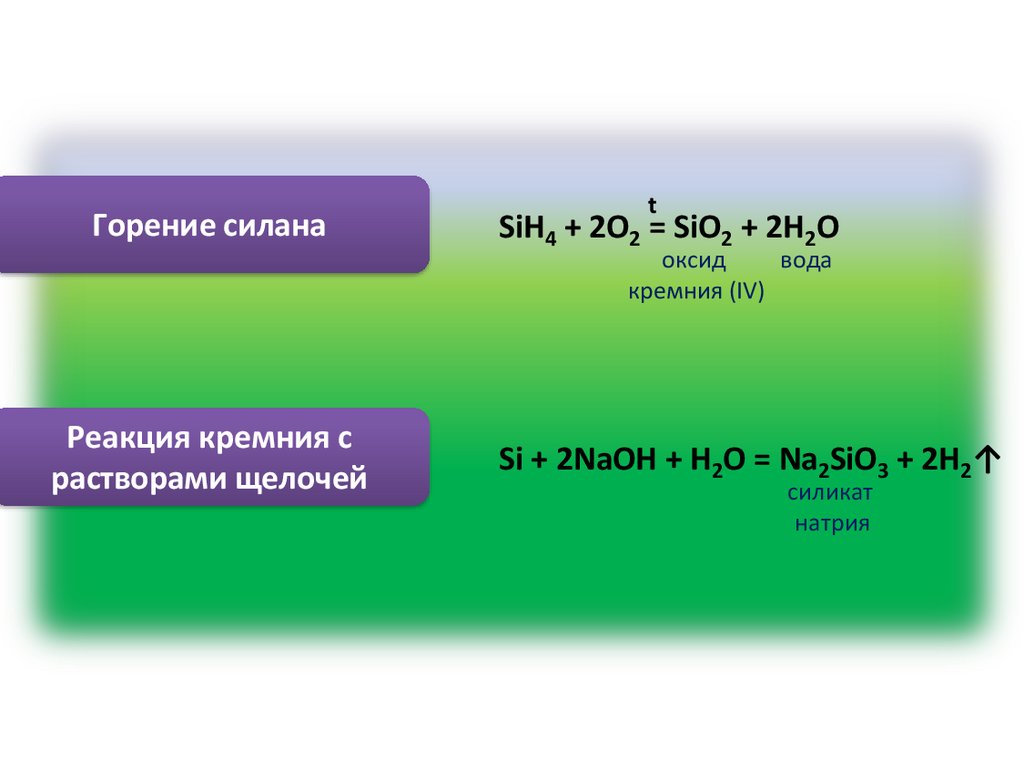
Горение силанаt
SiH4 + 2O2 = SiO2 + 2H2O
оксид
вода
кремния (IV)
Реакция кремния с
растворами щелочей
Si + 2NaOH + H2O = Na2SiO3 + 2H2↑
силикат
натрия
15.
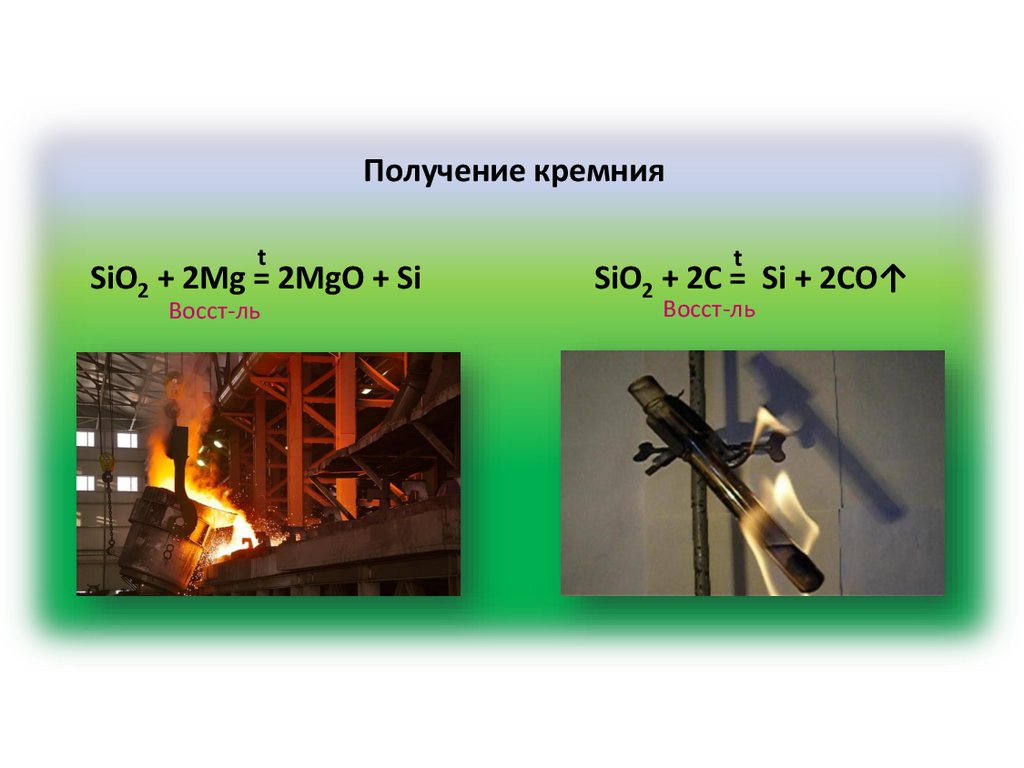
Получение кремнияt
SiO2 + 2Mg = 2MgO + Si
Восст-ль
t
SiO2 + 2С = Si + 2CO↑
Восст-ль
16.
Оксид кремния (IV), кремнезёмSiO2
➢ Это твёрдое, очень тугоплавкое вещество.
➢ Он нерастворим в воде.
➢ Имеет атомную кристаллическую решётку.
17.
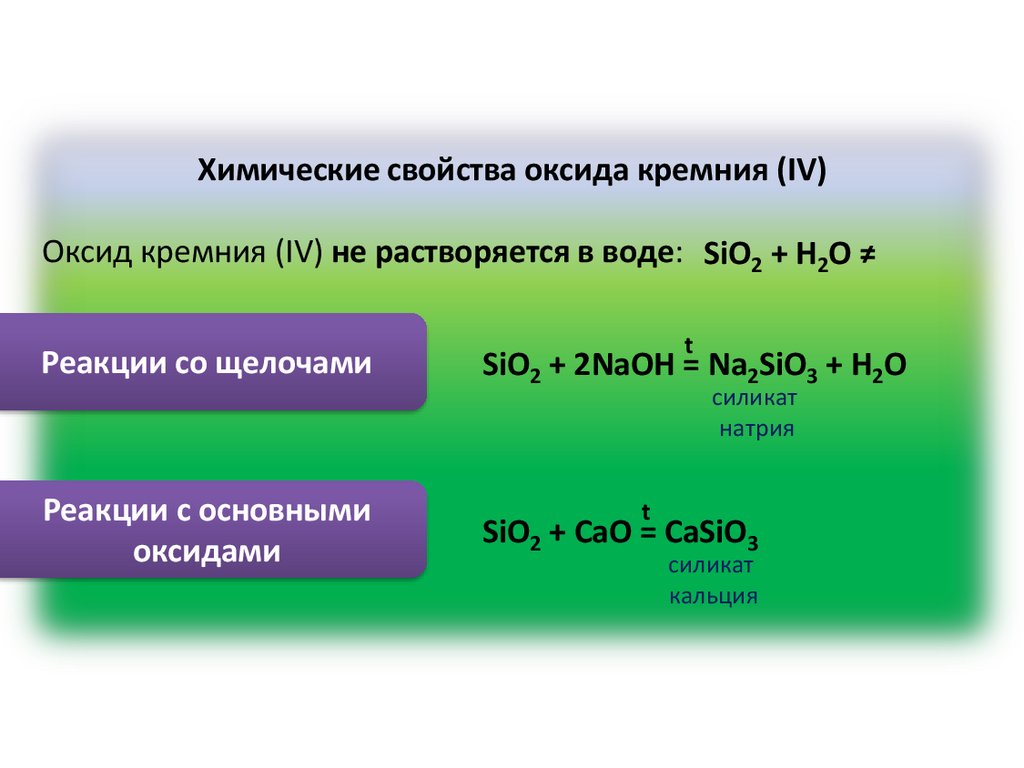
Химические свойства оксида кремния (IV)Оксид кремния (IV) не растворяется в воде: SiO2 + H2O ≠
Реакции со щелочами
t
SiO2 + 2NaOH = Na2SiO3 + H2O
силикат
натрия
Реакции с основными
оксидами
t
SiO2 + CaO = CaSiO3
силикат
кальция
18.
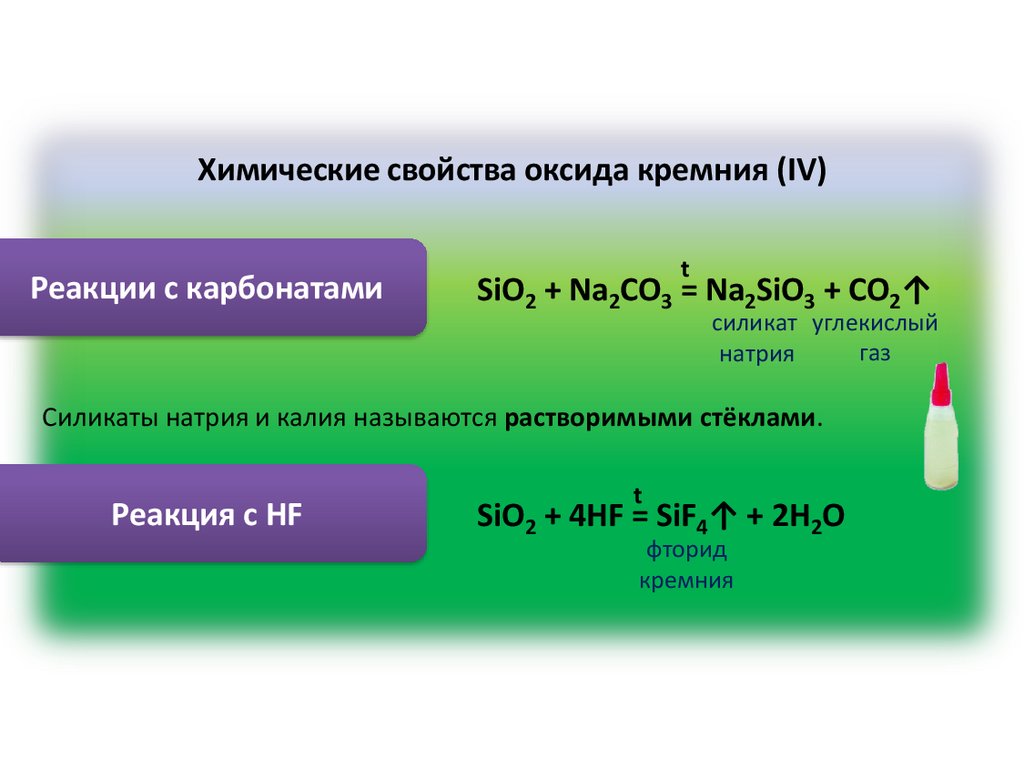
Химические свойства оксида кремния (IV)Реакции с карбонатами
t
SiO2 + Na2CO3 = Na2SiO3 + CO2↑
силикат углекислый
газ
натрия
Силикаты натрия и калия называются растворимыми стёклами.
Реакция с HF
t
SiO2 + 4HF = SiF4↑ + 2H2O
фторид
кремния
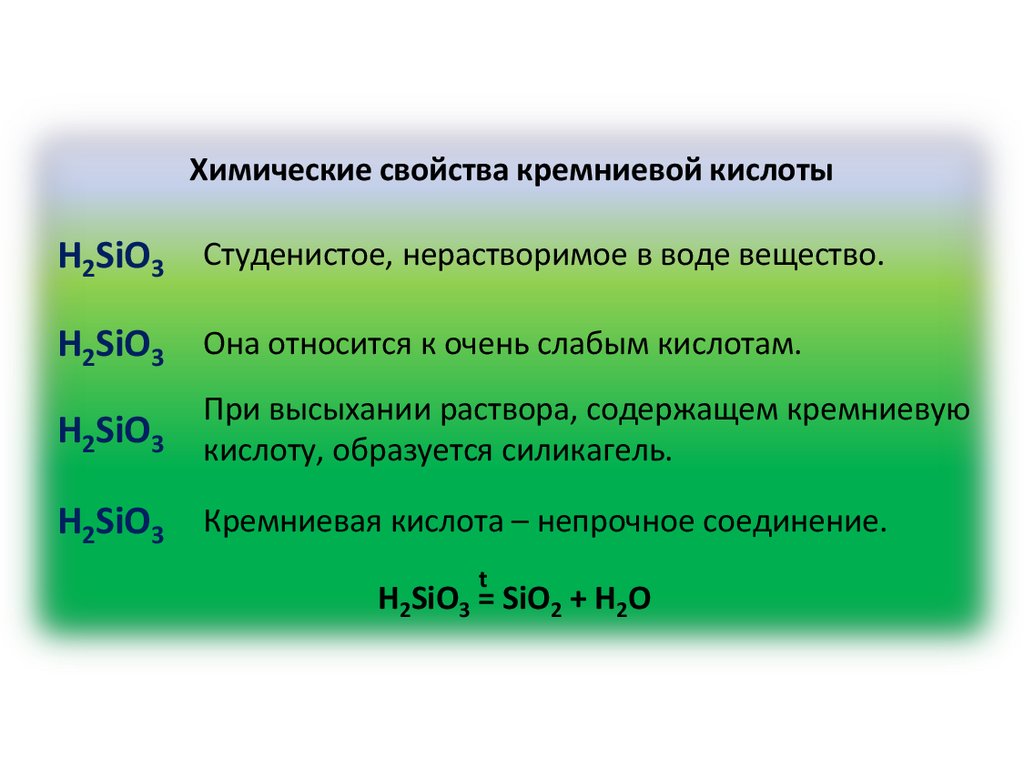
19.
Химические свойства кремниевой кислотыH2SiO3 Студенистое, нерастворимое в воде вещество.
H2SiO3 Она относится к очень слабым кислотам.
При высыхании раствора, содержащем кремниевую
H2SiO3 кислоту, образуется силикагель.
H2SiO3 Кремниевая кислота – непрочное соединение.
t
H2SiO3 = SiO2 + H2O
20.
Качественные реакции на силикат-ионNa2SiO3 + 2HCl = 2NaCl + H2SiO3↓
SiO32- + 2H+ = H2SiO3↓
Na2SiO3 + CO2 + H2O = Na2CO3 + H2SiO3↓
H2SiO3 + 2NaOH = Na2SiO3 + 2H2O
21.
Применение кремния и его соединений1
1 - получения полупроводниковых
материалов и кислотоупорных
сплавов
22.
Применение кремния и его соединений1
2
1 - получения полупроводниковых
материалов и кислотоупорных
сплавов
2 - карбид кремния используют для
затачивания резцов металлорежущих
станков и шлифовки драгоценных
камней
23.
Применение кремния и его соединений1
2
3
1 - получения полупроводниковых
материалов и кислотоупорных
сплавов
2 - карбид кремния используют для
затачивания резцов металлорежущих
станков и шлифовки драгоценных
камней
3 - из кварца изготавливают
кварцевую химическую
посуду
24.
Применение кремния и его соединений4
4 - «растворимые стёкла»
применяют как огнеупорное
средство для пропитки древесины и
тканей
25.
Применение кремния и его соединений4
5
4 - «растворимые стёкла»
применяют как огнеупорное
средство для пропитки древесины и
тканей
5 - асбест для изготовления
несгораемых и электроизоляционных
текстильных изделий
26.
Силикатное производствоСтекло
Керамические
изделия
Цемент
27.
Производство стеклаСода + известняк + песок = оконное стекло
Na2O · CaO · 6SiO2
28.
Оксид калияБогемское стекло
Оксид свинца (II)
Хрустальное
стекло
Оксид хрома (III)
Зелёное стекло
Оксид кобальта
Синее стекло
Оксид марганца (II)
Фиолетовое
стекло
Соли золота и селена
Рубиновое
стекло
29.
Закалка стеклаСтекло особого состава
нагревают до температуры
около 600 0С,
а затем резко охлаждают.
30.
Стекло человеку известно давно, уже3-4 тыс. лет назад производство стекла
было в Египте, Сирии, Финикии,
Причерноморье.
31.
Оконное стеклоБутылочное стекло
Ламповое стекло
Зеркальное стекло
Оптическое стекло
32.
Основным сырьём в производстве керамическихизделий является глина.
33.
При смешивании глины с водойобразуется тестообразная масса.
34.
Некоторые керамические изделияпокрывают глазурью.
35.
Цемент получают спеканием глиныи известняка.
36.
Если смешать порошок цемента сводой, то образуется так
называемый «цементный раствор».
37.
Если добавить к цементу песка илищебня, то получится бетон.
38.
Если ввести железный каркас, тогдаполучается железобетон.
39.
Кремний былполучен в
1824 году.
Латинское название силициум от
латинского силекс – «кремень».
Й. Я. Берцелиус
Получили
кремний,
но он был
очень
загрязнён
примесями.
Ж. Гей-Люссак
Л. Тенар
Русское название «кремний»
происходит от греческого кремнос –
«утёс, скала».
40.
Кремний – элемент IVA группы.В соединениях для него характерны степени окисления
+4 и -4.
В реакциях с кислородом и другими неметаллами
кремний проявляет восстановительные свойства, а в
реакциях с металлами – окислительные.
В природе кремний встречается в виде соединений.
Наиболее распространённое его соединение – оксид
кремния (IV) – кремнезём.
41.
Водородным соединением кремния является силан –SiH4.
Силан образуется при действии кислот или воды на
силициды.
Оксиду кремния (IV) соответствует кремниевая кислота.
Кремниевая кислота слабая двухосновная, студенистая и
нерастворимая в воде.
Качественной реакцией на силикат-ион является
действие сильных кислот на силикаты.
42.
Оксид кремния (IV) и силикаты находят широкоеприменение в промышленности.
К силикатной промышленности относят производство
стекла и цемента, керамических изделий и кирпича.






























 chemistry
chemistry








