Similar presentations:
https___school.mos.ru_ej_attachments_files_222_347_574_original_A0B5B0BA86B8B8D0D0D0D0D1D0D0D0D1%8F
1. Реакции замещения
02.02.2026Типы химических реакций
Учитель химии и биологии:
Бойко Эмиль Ричардович
2.
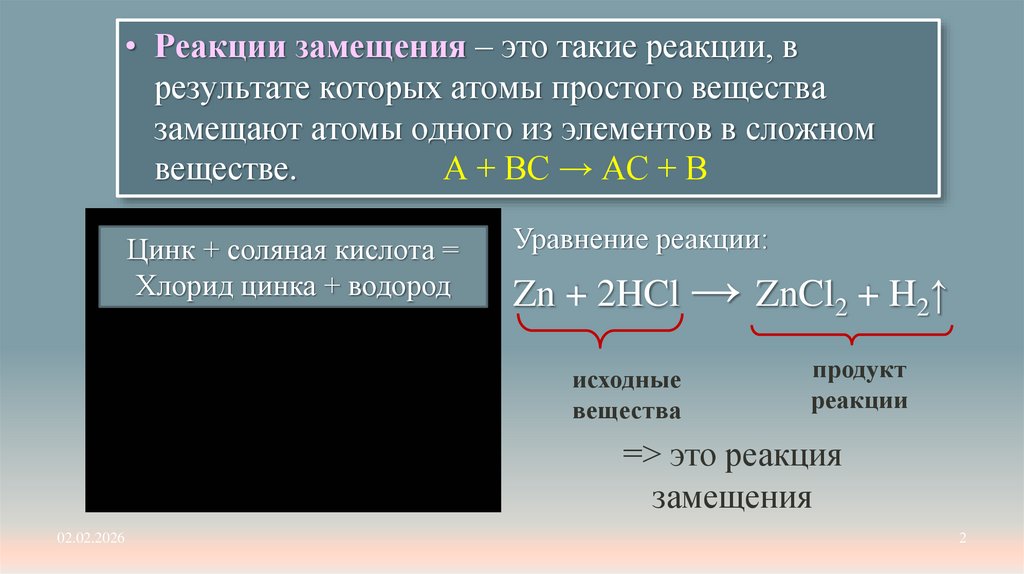
• Реакции замещения – это такие реакции, врезультате которых атомы простого вещества
замещают атомы одного из элементов в сложном
веществе.
A + BC → AC + B
Цинк + соляная кислота =
Хлорид цинка + водород
Уравнение реакции:
Zn + 2HCl → ZnCl2 + H2↑
исходные
вещества
продукт
реакции
=> это реакция
замещения
02.02.2026
2
3.
• Посмотрим видео-опыт «Реакция железа с раствором сульфата меди (II)».Железо + сульфат меди (II) =
сульфат железа (II) + медь
Уравнение реакции:
Fe + CuSO4 →
02.02.2026
FeSO4 + Cu↓
3
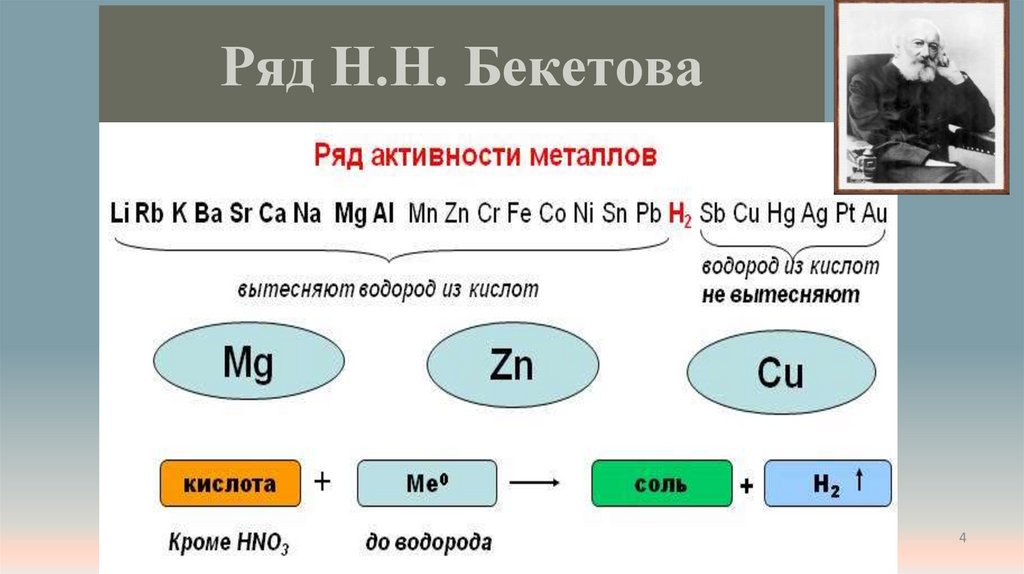
4. Ряд Н.Н. Бекетова
45.
Правила1. В реакциях между металлами и кислотами:
Металлы, стоящие в ряду напряжений до водорода вытесняют
водород из растворов кислот (исключение азотная кислота).
Mg + H2SO4 → MgSO4 + H2↑
02.02.2026
5
6.
Правила2. В реакциях между металлами и солями:
Каждый металл вытесняет из солей (в водных растворах) все те
металлы, которые стоят правее его в электрохимическом ряду.
Все соли и реагирующая и получающая в ходе реакции должны быть
растворимы в воде.
2AgNO3 +Mg →Mg(NO3)2 + 2Ag↓
6
7.
ЗАПОМНИ!!! ИСКЛЮЧЕНИЕ ИЗ ПРАВИЛА 1 И 2:Металлы, расположенные до Mg, в водных
растворах кислот и солей взаимодействуют сначала
с водой и вытесняют из неё водород,
2Na + 2H2O = 2NaOH + H2
А потом полученное основание реагирует или с
кислотой или с солью!!!
02.02.2026
7





 chemistry
chemistry








