Similar presentations:
6. Потомки светоносного элемента
1. Домашнее задание
• П. 19 читать• Стр.103 упр. 1,2
• Подберите коэффициенты методом электронного
баланса
P + Ag2O → P2O5 + Ag
А.Г.Волкова
1
2.
Потомки светоносного элементаУрок №6
А.Г.Волкова
2
3.
1. PH3 - фосфинФосфористый водород, фосфорный ангидрид.
Бесцветный, весьма ядовитый газ с неприятным запахом гнилой рыбы
(или чеснока).
кипит при -880С и плавится при -1330С. Хорошо растворим в воде, но химически с ней
не взаимодействует. В спирте и эфире растворяется плохо
.
Является очень сильным восстановителем. Газообразный фосфин восстанавливает
азотную, серную, сернистую кислоты, соли золота и другие соединения
.
Образуется при разложении содержащих фосфор органических
веществ – «болотный газ».
А.Г.Волкова
3
4.
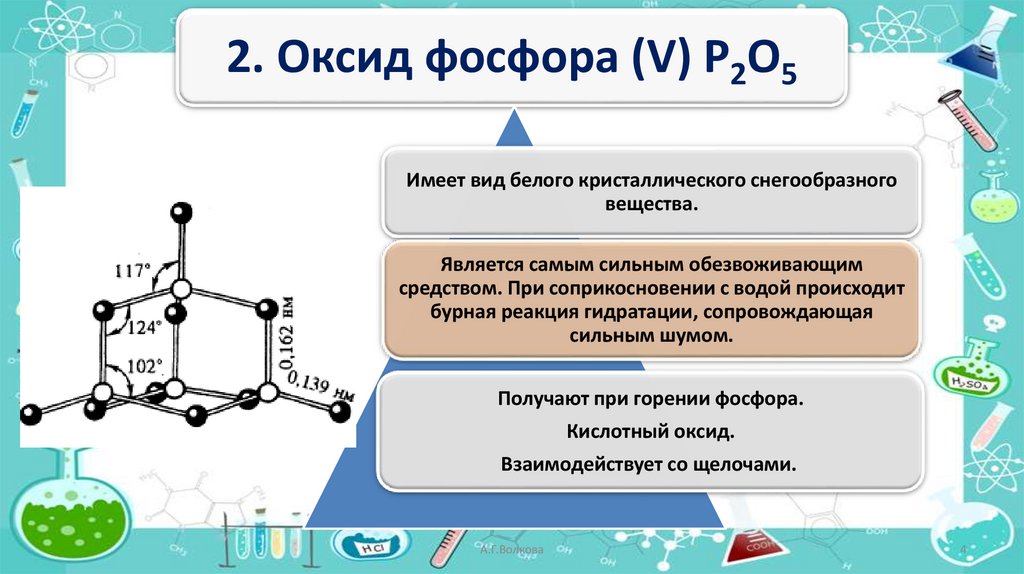
2. Оксид фосфора (V) P2O5Имеет вид белого кристаллического снегообразного
вещества.
Является самым сильным обезвоживающим
средством. При соприкосновении с водой происходит
бурная реакция гидратации, сопровождающая
сильным шумом.
Получают при горении фосфора.
Кислотный оксид.
Взаимодействует со щелочами.
А.Г.Волкова
4
5.
3. Фосфорные кислотыФосфорноватистая кислота H3PO2
Фосфористая кислота H3PO3
Фосфорноватая кислота H4P2O6
Ортофосфорная кислота H3PO4
НРO3 - метафосфорная кислота
H4P2О7- пирофосфорная кислота
Определите степени окисления
А.Г.Волкова
фосфора в кислотах
5
6.
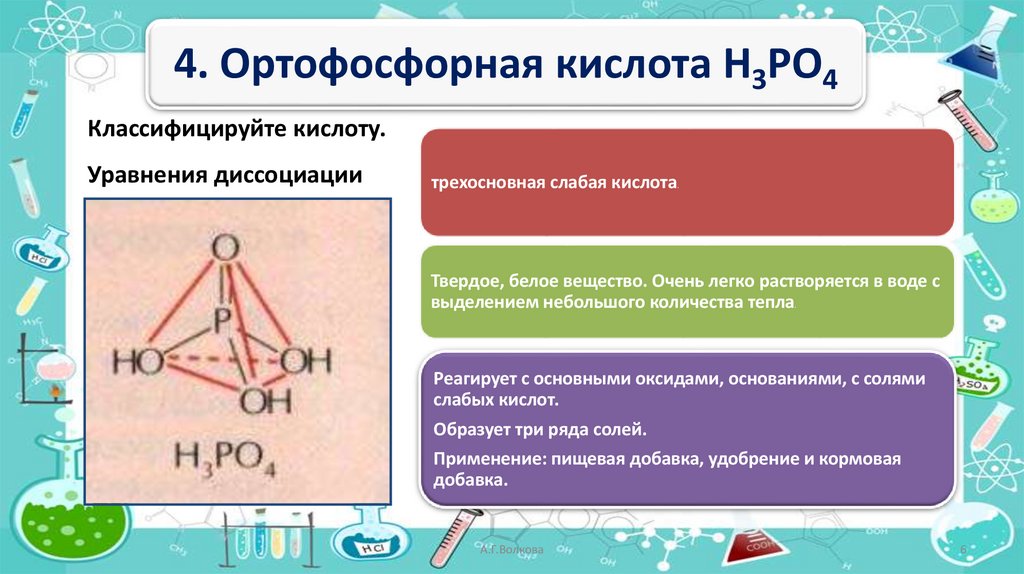
4. Ортофосфорная кислота H3PO4Классифицируйте кислоту.
Уравнения диссоциации
трехосновная слабая кислота
.
Твердое, белое вещество. Очень легко растворяется в воде с
выделением небольшого количества тепла
.
Реагирует с основными оксидами, основаниями, с солями
слабых кислот.
Образует три ряда солей.
Применение: пищевая добавка, удобрение и кормовая
добавка.
А.Г.Волкова
6
7.
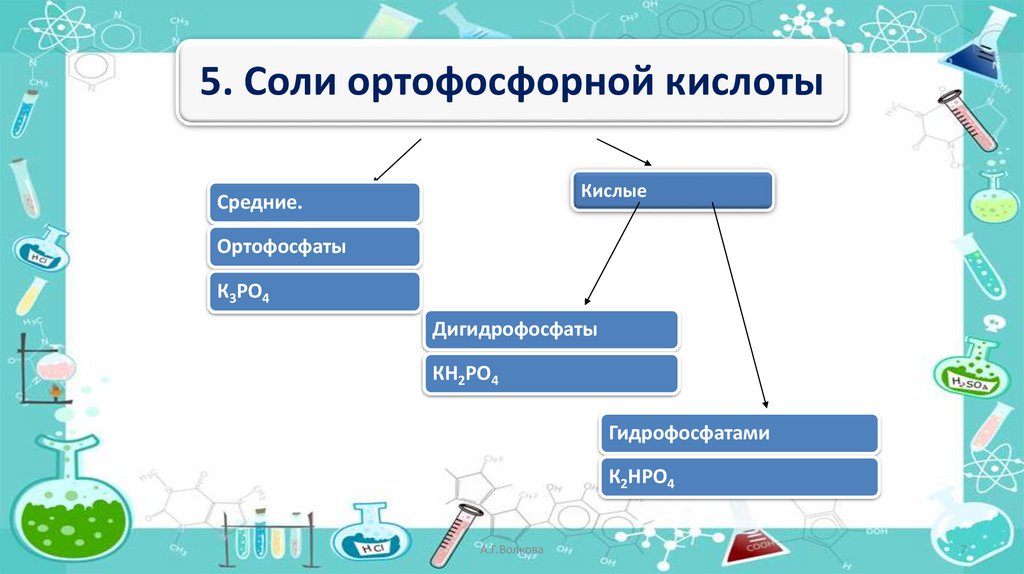
5. Соли ортофосфорной кислотыКислые
Средние.
Ортофосфаты
К3PO4
Дигидрофосфаты
КH2PO4
Гидрофосфатами
К2HPO4
А.Г.Волкова
7
8.
ФосфатыВ воде растворимы фосфаты и
гидрофосфаты щелочных металлов.
Фосфаты и гидрофосфаты остальных
металлов плохо растворимы.
Все дигидрофосфаты хорошо
растворимы в воде.
А.Г.Волкова
8
9.
6. Качественная реакцияна фосфат-ион
AgNO3 + Na3PO4 = ? + ?
А.Г.Волкова
9
10.
7. Применение.• Оксид фосфора (V) – осушитель
• Фосфорная кислота:
а) получения фосфорных удобрений
б) смягчения воды
в) огнестойкой пропитки
• Фосфаты - применяются в качестве удобрений.
• Лекарственные препараты, содержащие фосфор применяются
при заболеваниях мышц, нервной системы, при туберкулёзе,
упадке питания, малокровии и др.
• Стройматериалы
• Лаки и краски
• Зубные пасты
• Моющие средства…
А.Г.Волкова
10
11.
Домашнее задание• П.19
• Упр.4 стр.103
А.Г.Волкова
11
12.
ЗакреплениеКакова формула фосфина? Каковы его физические свойства?
Каков химический характер высшего оксида фосфора?
Назовите формулы главных фосфорных кислот.
Сколько видов солей может образовать ортофосфорная кислота?
Как называются эти соли? Приведите примеры формул и названий.
Как распознать соли фосфорной кислоты?
Где применяются ортофосфорная кислота и ее соли?
Какие вещества называются удобрениями?
Какие виды удобрений вам известны?
А.Г.Волкова
12









 chemistry
chemistry








