Similar presentations:
Образование_названий_химических_соединений
1. Образование названий химических соединений в рецептах
Выполнила преподавательГАПОУ НСО «Купинский медицинский
техникум» Саламахина В.Ю
2.
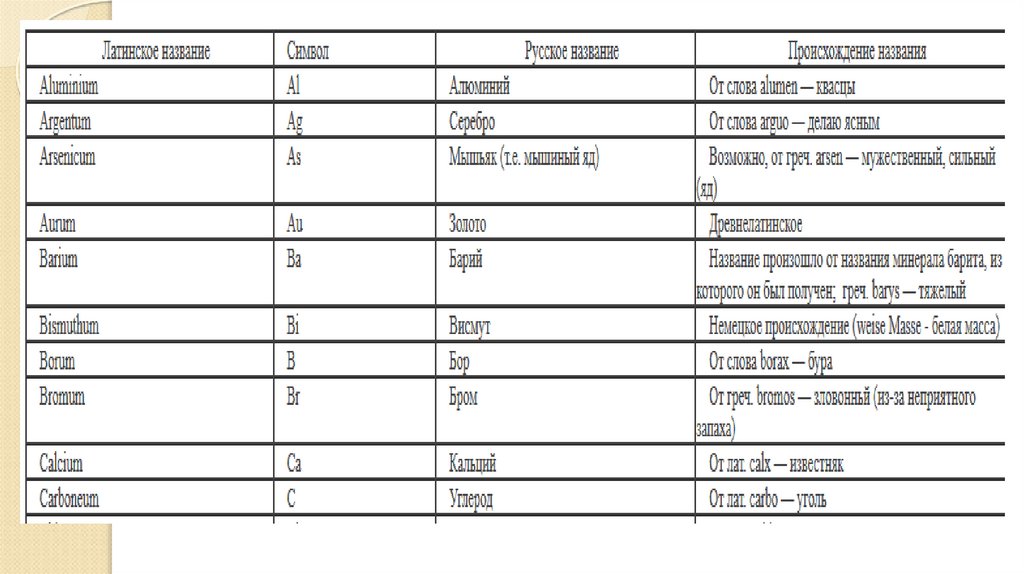
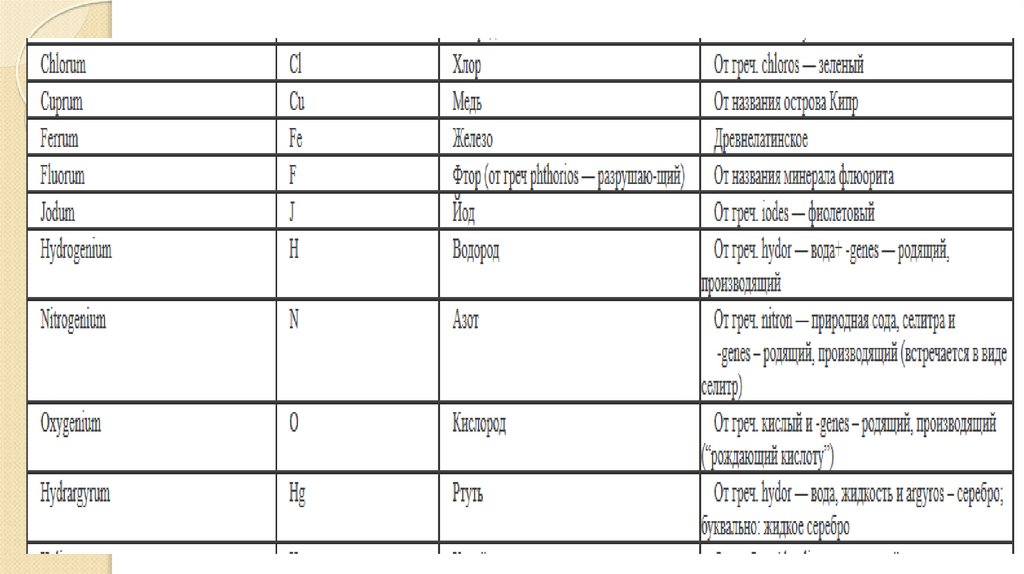
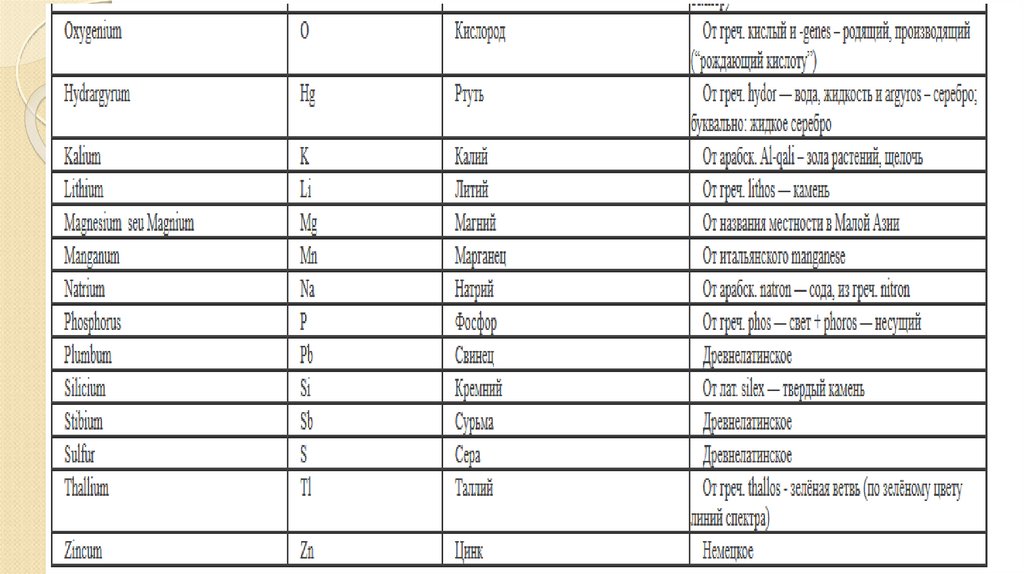
Все латинские названия химических элементов – существительныеср. р. II склонения, за исключением двух: Sulfur, -uris (n) (III
склонение) – сера, Phosphorus, -i (m) (м. р.) – фосфор. Химические
символы происходят от латинских названий элементов и отражают
их орфографические особенности: Са – Calcium, К – Kalium, P –
Phosphorus, Fe – Ferrum и др.
Некоторые
элементы в зарубежных изданиях имеют другие
латинские названия: Na – Sodium, Hg – Mercurium, К – Potassium и
др.
3.
4.
5.
6. Названия кислот
Латинские полусистематические и тривиальные названия кислот состоят изсуществительного acidum, -i (n) - "кислота" и согласованного с ним
прилагательного 1-й группы. К основе наименования кислотообразующего
элемента прибавляется суффикс -ic-um или -os-um.
Суффикс -iс- указывает на максимальную степень окисления и соответствует
в русских прилагательных суффиксам -н-(ая), -ев-(ая) или -ов-(ая), например:
1. аcidum sulfur-ic-um - сер-н-ая кислота;
2. аcidum barbitur-ic-um - барбитур-ов-ая кислота;
3. аcidum fol-ic-um - фоли-ев-ая кислота.
Суффикс
-os- указывает на низкую степень окисления и соответствует
русскому прилагательному с суффиксом -ист-(ая); например: аcidum sulfuros-um - серн-ист-ая кислота; аcidum nitr-os-um - азот-ист-ая кислота.
7. Название кислот
Прилагательныев наименованиях бескислородных кислот включают
приставку hydro-, основу названия кислотообразующего элемента и
суффикс -ic-um.
В русской номенклатуре лекарств этому соответствует прилагательное с
концовками -ис-товодородная (кислота), например:
Aс. hydro-brom-ic-um - бром-ис-товодородная кислота.
Acidum hydrochloricum – кислота хлористоводородная
8. Схема образования названия кислородсодержащих кислот
Основа названиякислотообразующего
элемента
суффикс
- ic –
-os -
окончание
- um
По такой же схеме образуются тривиальные названия органических кислот:
уксусная кислота – acidum acetĭcum
лимонная кислота – acidum citrĭcum
9. Схема образования названия кислот, не содержащих кислород
ПриставкаHydro -
Основа названия
кислотообразующ
его элемента
суффикс
- ic-
окончание
-um
В названия кислот, не содержащих кислород, прилагательные образуются с
помощью приставки hydro- и суффикса -ic+ окончание -um:
НСl — acidum hydrochloricum — хлористоводородная (соляная) кислота
HCN — acidum hydrocyanicum — цианистоводородная (синильная)
кислота
10. Название некоторых кислот
acĭdum-//-//-//-//-//-//-//-//-//-//-//-//-//-//-//-//-//-//-//-//-//-//-//-
acetĭcum
acetylsalicylĭcum
ascorbinĭcum
benzoĭcum
borĭcum
citrĭcum
carbolĭcum
carbonĭcum
formicĭcum
folĭcum
glutaminĭcum
lactĭcum
nicotinĭcum
salicylĭcum
tartarĭcum
arsenicĭcum
arsenicōsum
nitrĭcum
nitrōsum
sulfurĭcum
sulfurōsum
hydrochlorĭcum
hydrobromĭcum
hydroiodĭcum
— уксусная кислота
— ацетилсалициловая кислота
— аскорбиновая кислота
— бензойная кислота
— борная кислота
— лимонная кислота
— карболовая кислота
— угольная кислота
— муравьиная кислота
— фолиевая кислота
— глутаминовая кислота
— молочная кислота
— никотиновая кислота
— салициловая кислота
— винная или виннокаменная кислота
— мышьяковая кислота
— мышьяковистая кислота
— азотная кислота
— азотистая кислота
— серная кислота
— сернистая кислота
— хлористоводородная (соляная) кислота
— бромистоводородная кислота
— йодистоводородная кислота
11. Названия оксидов
Названия оксидов состоят из двух слов: первое - наименование элемента(катиона) в род. п. (несогласованное определение), второе - групповое
наименование оксида (анион) в им. пад. (склоняемое).
Названия
почти всех оксидов состоят из двух существительных. По
международному способу на первое место ставится наименование
химического элемента в родительном падеже (с прописной буквы), на
второе — групповое наименование оксида в именительном падеже (со
строчной буквы):
Например: СаО Calcii oxydum — оксид кальция
Zinci oxydum – оксид цинка
12. Название оксидов
Отрезок -оху- указывает на присутствие кислорода, а приставки уточняютструктуру соединения В русском наименовании используется и такой
порядок слов, как в международном (латинском).
оксид — oxydum, i n
пероксид — peroxydum, i n
гидроксид — hydroxydum, i n
Н2О2 Hydrogenii peroxydum — пероксид водорода
Al(OH)3 Aluminii hydroxydum — гидроксид алюминия
13. Название оксидов
Названия закисей состоят из двух слов.Первое — наименование элемента в именительном падеже, второе —
групповое название закисей — прилагательное oxydulatus, a, um
(закисный), которое стоит тоже в именительном падеже.
N2O Nitrogenium oxydulatum — закись азота
Ferrum oxydulatum – закись железа
Модель конструирования названий оксидов: Gen.sing. + Nom.sing.
(название химического oxydum элемента) hydroxydum, peroxydum
14. Названия солей
Названия солей состоят из двух имен существительных—наименований катиона и аниона. Наименование катиона,
представляющего название химического элемента, пишется с
прописной буквы, а наименование аниона — со строчной.
Согласно международному способу в латинской химической
номенклатуре: 1-м месте ставится в родительном падеже единстве
на 1-м месте наименование катиона (электроположительного
элемента),
на 2-м — наименование аниона (электроотрицательного элемента) в
именительном падеже единственного числа (в русской номенклатуре на
1-м месте ставится наименование аниона, а на 2-м – наименование
катиона).
Gen.sing. + Nom.sing.
15. Название солей
Вназваниях анионов солей очень важно знать значение суффиксов,
указывающих на высокую или низкую степень окисления в химическом
соединении, а также на бескислородный характер соединения.
Наименования анионов в солях кислородных кислот — это
существительные III склонения, которые относятся по исключению к
мужскому роду. Они образуются с помощью суффиксов:
-as (родит. падеж -atis) — для солей с большим содержанием кислорода (в
русском соответствует суффикс -ат): sulfas, sulfatis m — сульфат;
-is (родит. падеж -itis) — для солей с меньшим содержанием кислорода (в
русском соответствует суффикс -ит): nitris, nitritis m— нитрит.
Наименования анионов в солях бескислородных кислот — это
существительные II склонения среднего рода с суффиксом –id +
окончание -um (в русском соответствует суффикс -ид). Например:
chloridum — хлорид, bromidum — бромид.
16. Наиболее употребительные наименования анионов
acetas, atis m — ацетатarsenas, atis m — арсенат
arsenis, itis m — арсенит
benzoas, atis m — бензоат
bromidum, i n — бромид
carbonas, atis m — карбонат
citras, atis m — цитрат
chloridum, i n — хлорид
gluconas, atis m — глюконат
glycerophosphas, atis m —
глицерофосфат
hydrochloridum, i n — гидрохлорид
iodidum, i n — йодид
nitras, atis m — нитрат
nitris, itis m — нитрит
phosphas, atis m — фосфат
salicylas, atis m — салицилат
subacetas, atis m — основной ацетат
subcarbonas, atis m — основной
карбонат
subnitras, atis m — основной нитрат
sulfas, atis m — сульфат
tetraboras, atis m —
тетраборатhydrocarbonas, atis m —
гидрокарбонат
17. Названия солей
Наименования анионов солей бескислородных кислот с органическимиоснованиями имеют приставку hydro- и суффикс -id+ окончание -um:
hydro-brom-idum — гидробромид
hydro-iod-idum —гидройодид
hydro-chlor-idum — гидрохлорид, или хлороводород
Названия анионов основных солей образуются от названий средних солей
присоединением к основе аниона приставки sub-: Bismuthi subnitras –
основной нитрат висмута.
Названия анионов кислых солей образуются так же, как названия средних
солей, но с добавлением приставки hydro-: Natrii hydrocarbonas –
гидрокарбонат натрия.
18. Название солей
Названия анионов органических солей натрия и калия состоят издвух существительных II склонения среднего рода в именительном
падеже единственного числа, соединенных дефисом:
1) наименование основания,
2) наименование natrium или kalium.
Например:
Sulfacylum-natrium
сульфацил-натрий,
Веnzylpenicillinum-kalium - бензил-пенициллина калиевая соль.















 medicine
medicine