Similar presentations:
Лекція_№17_Метали_та_їх_сплави_ab572d6a_6958_44cc_ac6e_cfbb3d21c757 (1)
1. Застосування металів та їх сплавів
2.
Найпоширеніші метали та їхні сплавиМетали — речовини, що набули широкого застосування в
промисловості й техніці завдяки своїм унікальним
властивостям, зумовленим їхньою будовою.
Залежно від властивостей, деякі з них використовують менше,
а без деяких неможливий розвиток економіки країни.
3.
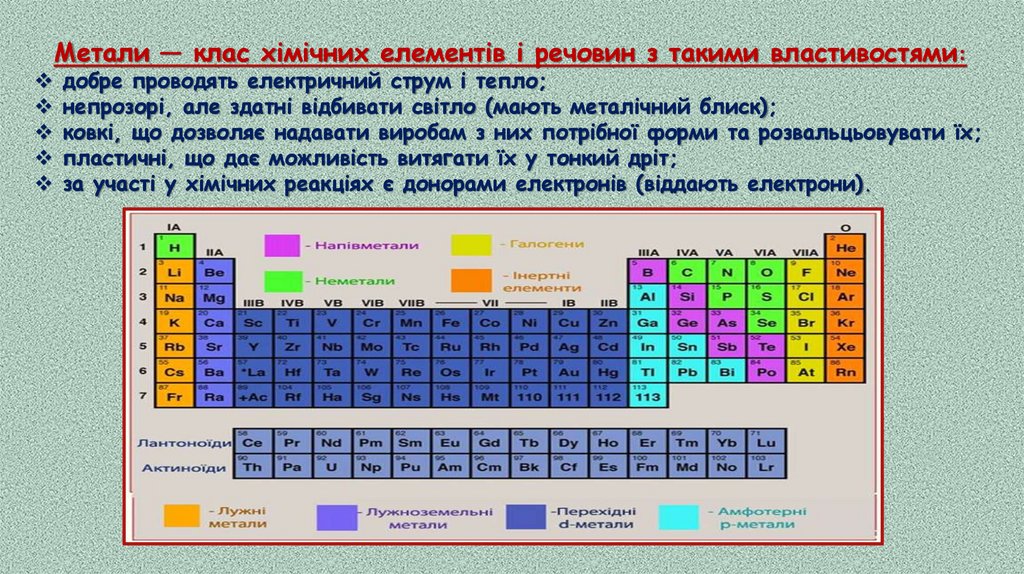
Метали — клас хімічних елементів і речовин з такими властивостями:добре проводять електричний струм і тепло;
непрозорі, але здатні відбивати світло (мають металічний блиск);
ковкі, що дозволяє надавати виробам з них потрібної форми та розвальцьовувати їх;
пластичні, що дає можливість витягати їх у тонкий дріт;
за участі у хімічних реакціях є донорами електронів (віддають електрони).
4.
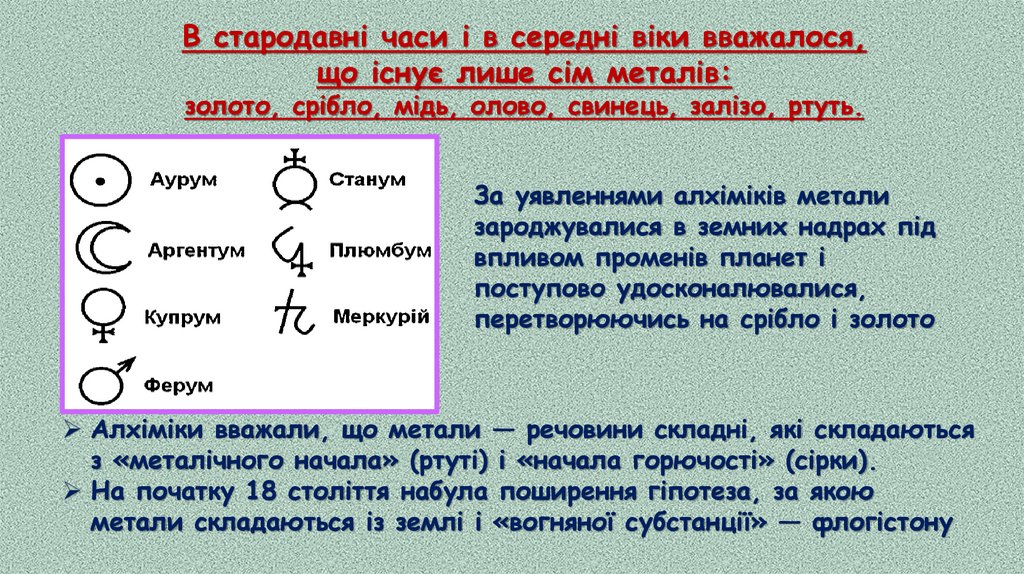
В стародавні часи і в середні віки вважалося,що існує лише сім металів:
золото, срібло, мідь, олово, свинець, залізо, ртуть.
За уявленнями алхіміків метали
зароджувалися в земних надрах під
впливом променів планет і
поступово удосконалювалися,
перетворюючись на срібло і золото
Алхіміки вважали, що метали — речовини складні, які складаються
з «металічного начала» (ртуті) і «начала горючості» (сірки).
На початку 18 століття набула поширення гіпотеза, за якою
метали складаються із землі і «вогняної субстанції» — флогістону
5.
Наприкінці 18 століття А. Л. Лавуазьєспростував гіпотезу флогістону і доказав, що
метали — прості речовини.
У 1789р. Лавуазьє у посібнику з хімії дав
список простих речовин, в який включив всі
відомі тоді 17 металів (Sb, Ag, As, Bi, Co, Cu,
Sn, Fe, Mn, Hg, Mo, Ni, Au, Pt, Pb, W, Zn).
У міру розвитку методів хімічного дослідження
число відомих металів зростало.
У першій половині 19 століття були відкриті
елементи-супутники платини — платиноїди,
отримано шляхом електролізу деякі лужні і
лужноземельні метали, відкриті невідомі
метали при хімічному аналізі мінералів.
6.
7.
Феномен відкриття металів мав визначальнийвплив на життя людського суспільства,
розмежувавши його розвиток на
„доісторичну” (кам’яна доба) та „історичну”
епохи.
Видобуток руд забезпечив людство
принципово новими матеріалами, які мали
невідомі раніше властивості (ковкість,
плавкість) та важливі переваги (здатність до
зміни форми, висока міцність,
експлуатаційна довговічність).
Це дозволило не тільки ефективно
вдосконалювати наявні знаряддя, але й
створювати їх численні нові типи, що
відкрило можливості для технічного
прогресу.
8.
Область застосування металіввизначається їх властивостями.
Властивості металів поділяють на:
механічні (ударна в'язкість, пружність,
пластичність, міцність і твердість металу);
технологічні (фізична і технологічна
зварюваність, зносостійкість, ковкість,
оброблюваність різанням, ливарні
властивості, здатність до паяння тощо);
фізичні (колір, питома маса, теплова і електрична провідність,
магнітні якості, температура плавлення, температурний
коефіцієнт лінійного розширення тощо);
хімічні (стійкість проти корозії, жароміцність, жаротривкість)
9.
Метали в природіБільша частина металів присутні в природі у
вигляді руд і з'єднань. Самим поширеним
металом в земній корі являється алюміній. За ним
слідує залізо, натрій, калій, магній і титан. Вміст
інших металів незначний.
Боксит
Гематит
Магнетит
10.
Лише деякі метали існують у вільному вигляді,утворюючи самородки.
Самородок
платини
Самородок
срібла
Самородок
золота
Ртуть
11.
Лужні метали натрій та калій, які добуваютьелектролізом розплавів солей, лугів або
оксидів цих металічних елементів,
незважаючи на їхню високу активність,
отримали промислове застосування в різних
галузях.
Металічні натрій та калій застосовують як
каталізатори під час синтезу органічних
сполук, зокрема синтетичного каучуку.
За допомогою натрію в металургійній
промисловості відновлюють кольорові
метали, наприклад титан. Рівняння реакції:
TiCl4 + 4Na = Ti + 4NaCl.
Крім того, натрій використовують у ядерних
реакторах як теплоносій.
12.
Літій застосовують у фотоелементахзавдяки здатності перетворюватися на
позитивно заряджені йони під час його
освітлення.
Кальцій, як і натрій, застосовують у
металургії для добування
важковідновлюваних металів, наприклад
хрому з його оксиду:
Cr2O3 + 3Ca = 2Cr + 3CaO.
Цей метал використовують для
виготовлення сплавів. На основі свинцю з
добавкою кальцію добувають сплав, яким
заливають підшипники залізничних вагонів.
13.
Легкі метали — алюміній, титан і магній —використовують як конструкційні матеріали в
авіації, космічній галузі, автомобілебудуванні.
Алюміній завдяки його властивостям:
легкості, пластичності, електро- й
теплопровідності та міцності, набув дуже
широкого застосування.
14.
Важкі метали— мідь, цинк, олово ісвинець — застосовують в
машинобудуванні, електротехніці,
енергетиці.
Рідкісні важкі метали — нікель,
кадмій, вольфрам, молібден,
манган, кобальт, ванадій, бісмут —
використовують як тугоплавкі
конструкційні матеріали, а також в
сплавах з чорними металами як
легуючі елементи.
15.
Дорогоцінні метали— золото, срібло і платина —використовують в ювелірній промисловості, електроніці,
електротехніці, хімічній промисловості
16.
Сплави — це системи, утворені з двох або більшекомпонентів (металів з металами або металів з
неметалами).
Основою для виготовлення сплавів є залізо й
алюміній, хром і мідь, магній та титан. З
неметалів — бор, кремній та вуглець.
Є також сплави - розчини, сплави- механічні
суміші й сплави, у яких речовини реагують одна
з одною з утворенням інтерметалідів.
Сплави- розчини утворюють подібні за
властивостями речовини.
Різні за хімічними властивостями метали
утворюють сплави- механічні суміші.
Сплави третього виду можуть не тільки
змішуватися, а й утворювати між собою та з
атомами неметалів різні сполуки
17.
Металевими сплавами називають речовини, якіскладаються не менше, як з двох компонентів і
одним з них обов’язково повинен бути метал.
Сплави металів відіграють велику роль, оскільки
зазвичай вони мають вищі функціональні
(механічні, електричні) і технологічні
властивості, ніж їхні складові - чисті метали.
Найчастіше застосовують сплави на основі заліза
(чавун, сталь) і сплави кольорових металів на
основі
міді (латунь, бронза),
алюмінію (силумін, дюралюміній),
свинцю, цинку, олова, нікелю.
Деякі сплави створюють на основі вольфраму,
титану, ванадію, молібдену й інших металів.
18.
Сплави виявляють загальні властивостіметалів:
металічний блиск, високі електропровідність і
теплопровідність.
Але деякі властивості сплавів відрізняються від
властивостей їхніх компонентів.
температура плавлення сплавів звичайно нижча від
температури плавлення металів, що входять до
їхнього складу.
так, натрій і калій при певному складі утворюють
сплав, який при звичайній температурі є рідиною,
хоча натрій плавиться при 97,5°С,
а калій — при
62,3°С.
19.
Твердість сплавів у більшості випадків вища від твердості окремихметалів, що їх утворюють.
Наприклад, добавка1% берилію до міді збільшує її твердість у 7 разів.
Ковкість і пластичність металів у сплавах звичайно знижується.
Тепло- і електропровідність металів у сплавах теж зменшується.
Механічна міцність сплавів, навпаки, у більшості випадків підвищується.
Хімічні властивості металів у сплавах теж змінюються.
Наприклад, при додаванні до звичайної сталі 15—20% силіцію
одержують кислотостійку сталь.
Металічні сплави мають надзвичайно велике значення.
Сучасна техніка вимагає сплави з найрізноманітнішими властивостями:
надтверді і м'які, тугоплавкі і легкоплавкі, стійкі до дії різних
газів, кислот, лугів, і т.д.
Відомо вже кілька тисяч різних сплавів з різноманітними властивостями.
Найбільш поширені сплави на основі заліза і алюмінію.
20.
Сплави на основі алюмініюЧистий алюміній не має високої міцності
та твердості, тому частіше використовують
його сплави. Для поліпшення механічних
властивостей алюмінію добувають його
сплави з міддю, магнієм і марганцем.
В промисловості використовують сплави
алюмінію на основі систем:
Al-Cu, Al-Si, Al-Mn, Al-Mg.
Легуючі добавки (мідь, кремній, магній,
цинк, манган) вводять в алюміній
головним чином з метою підвищення
його міцності.
Найпоширеніші сплави алюмінію — це
дюралюміни, силуміни й терміт.
21.
Дюралюміній (від фр. dur — твердий; aluminium — алюміній) —сплави, що містять у своєму складі мідь (1,4-13 %), магній (0,42,8 %), манган (0,2-1 %), цинк (5-7 %), залізо (0,8-1,8 %),
титан (0,02-0,35 %) і силіцій (0,5-6 %).
Дюралюміни завдяки особливим властивостям — міцності,
легкості, стійкості до корозії та теплопровідності — набули
широкого застосування в авіа-, корабле- й ракетобудуванні.
Перше застосування дюралюмінію — виготовлення
каркасу дирижаблів жорсткої конструкції, з 1911 року — більш
широке застосування. Склад сплаву і термообробка у
роки війни були засекречені.
Завдяки високій питомій міцності дюралюміній
починаючи з 1920-х років стає важливішим
конструкційним матеріалом у літакобудуванні.
Густина сплаву 2 500—2 800 кг/м³,
температура плавлення близько 650 °C.
22.
Силуміни –Сплави з високим вмістом силіцію.
Мають найкращі ливарні властивості.
Силуміни — сплави, які, крім алюмінію, мають
високий вміст силіцію (3-26 %). До їхнього складу
також входять магній (0,2-1,5 %), мідь (1-4 %), цинк
(2-4 %), хром (0,2-0,4 %), нікель (0,8-2 %), титан
(0,05-1,5 %).
Їх використовують у виробництві машин для
сільськогосподарських потреб, деталей багатьох
приладів, дисків коліс в авіа- й автомобілебудуванні.
Терміт — сплав алюмінію з ферум(ІІ, ІІІ) оксидом.
Під час використання виділяє багато тепла, тож його
застосовують для зварювання шин.
Головними перевагами всіх сплавів алюмінію є їх
мала густина (2,5…2,8 г/см³), висока міцність,
стійкість проти атмосферної корозії, порівняно мала
вартість та легкість отримання і обробки.
23.
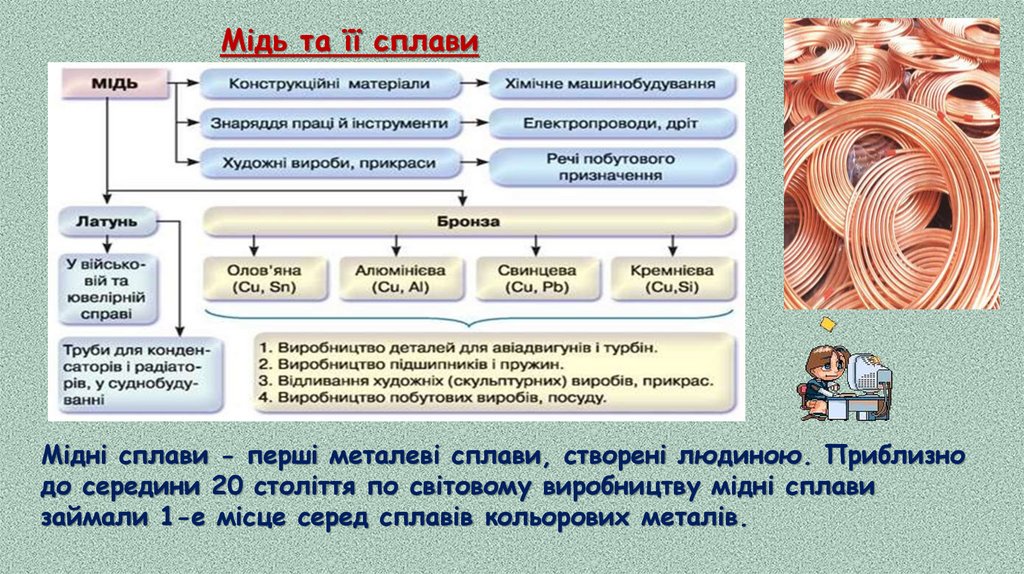
Мідь та її сплавиМідні сплави - перші металеві сплави, створені людиною. Приблизно
до середини 20 століття по світовому виробництву мідні сплави
займали 1-е місце серед сплавів кольорових металів.
24.
Бронза –сплав міді, звичайно з оловом як основним
легуючим елементом, але застосовуються і
сплави з алюмінієм, кремнієм, берилієм,
свинцем та іншими елементами, за винятком
цинку та нікелю.
Типова бронза має склад: 94.65% — мідь,
5% олово, 0.35% — фосфор. Фосфор надає
бронзі додаткової пружності, твердості, та
збільшує корозостійкості. Температура
плавлення бронзи перебуває в межах
990-1190 °С.
Латунь –
це подвійний або багатокомпонентний сплав на
основі міді, де основним легуючим елементом є
цинк, іноді з додаванням олова, нікелю, свинцю,
марганцю, заліза та інших елементів.
25.
Мельхіорє сплавом міді з нікелем, іноді з добавками заліза і марганцю.
Зазвичай до складу мельхіору входить 5-30% нікелю, ≤ 0,8% заліза
і ≤ 1% марганцю, хоча в окремих випадках він відрізняється від
накреслених рамок. Наприклад, при виготовленні резисторів
використовується сплав, який містить 55% міді і 45% нікелю.
Мельхіор має високу стійкість проти корозії як в повітрі, так і у воді,
добре обробляється, тому є гарним сплавом для карбування монет.
26.
Нікелеві сплавиЗдатність нікелю розчиняти в собі значну
кількість інших металів і зберігати при
цьому пластичність, призвела до створення
великої кількості нікелевих сплавів.
Корисні властивості нікелевих сплавів в
певній мірі обумовлені властивостями
самого нікелю, серед яких поряд із
здатністю утворювати тверді розчини з
багатьма металами виділяються
феромагнетизм, висока корозійна стійкість в
газових і рідких середовищах, відсутність
алотропічних перетворень.
27.
Чорні метали — залізо, манган, хром — є основними продуктамичорної металургії, а їх сплави використовують у всіх галузях
машинобудування.
28.
У техніці найбільшого застосування набулизалізо, алюміній, мідь, свинець, цинк,
олово, нікель. Вони ще мають назву
«технічні метали».
Залізні сплави - металеві системи, одним з компонентів яких (як
правило, переважаючим) служить залізо. Залізні сплави містять
зазвичай домішки (марганець, кремній, сірку, фосфор та ін).
Найважливішими залізними сплавами, найбільш часто використаними
в техніці, є залізовуглецевих сталі (сталь, чавун). До залізних сплавів
відносяться також спеціальні сплави на залізній основі (з високим
електричним опором, магнітні, жароміцні та ін), феросплави. На частку
залізних сплавів доводиться близько 95% всієї металевої продукції.
29.
СплавиВ сучасній техніці найбільше
застосовуються сплави заліза. Так,
наприклад, в машинобудуванні на їх
частку припадає 90% від всієї маси
металів. Важливими сплавами заліза
являються чавун і сталь.
Чавун – сплав заліза, який містить
більше 1,7% карбону, а також
кремній, манган, невелику кількість
сульфуру і фосфору.
Сталь – це сплав заліза, який
містить 0,1-2% карбону і невелику
кількість кремнію, мангану,
фосфору і сульфуру.
30.
Залізо та його сплавиЧисте залізо має обмежене використання. Здебільшого
застосовують сплави заліза — чавун і сталь.
Сировиною для виплавлення чавуну є залізні руди.
Чавун - сплав заліза з вуглецем з вмістом
більше 1,7%, та домішки мангану, сполук
Фосфору, Силіцію та Сульфуру. Вуглець в
чавуні може міститися у вигляді цементиту і
графіту.
В залежності від форми графіту та кількості
цементиту, виділяють: білий, сірий, ковкий і
високоміцні чавуни.
Властивості: чавун – це сіра речовина, тверда,
але важка і крихка, добре тримає тепло.
Застосування: більша частина чавуну слугує
сировиною для виплавлення сталі, а з решти
відливають металеві вироби різного призначення.
31.
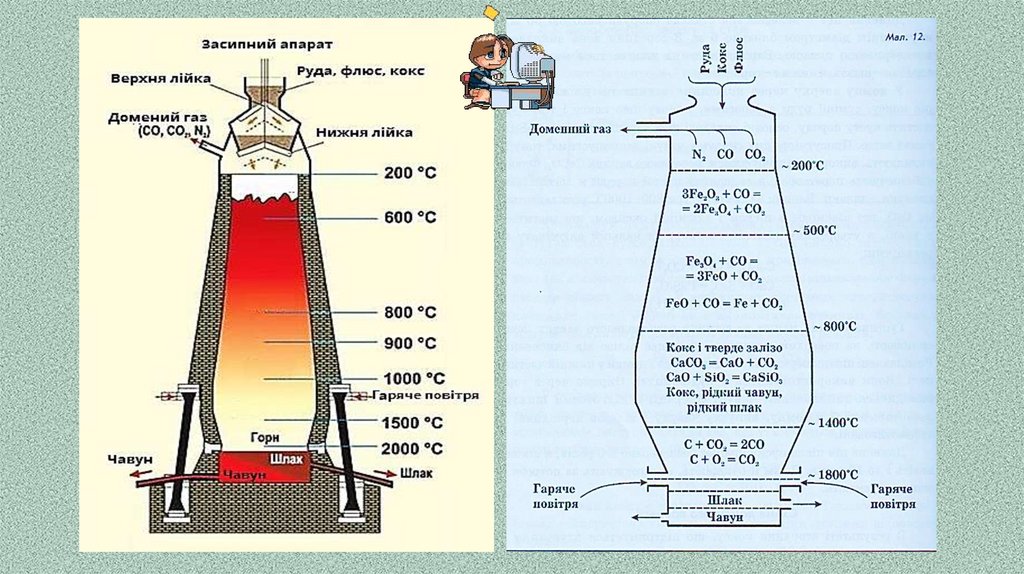
Добування чавуну базується на відновленні заліза ізоксидів Феруму та переводі пустої породи в шлак.
Головною технологією виробництва чавуну є виплавка в
доменних печах.
Чавун виплавляють у величезних доменних печах висотою до
30-45 м, а діаметром — до 12 м. Внутрішня частина домни
викладена вогнетривкою цеглою, а зовнішня облицьована
стальними листами.
Сировиною для виробництва чавуну в доменних печах є залізні
руди, паливо та флюси. Таку суміш сировинних матеріалів
називають шихтою.
Найважливіші залізні руди: магнетит Fе3О4, гематит Fe2О3,
пірит FеS2 , сидерит FеСО3.
У якості палива використовують кокс, який є продуктом
переробки кам’яного вугілля. Іноді замість коксу використовують
природний газ або мазут.
За допомогою флюсів тугоплавкі домішки та пусту породу
перетворюють на легкоплавкі сполуки, шлак. У якості флюсів
використовують вапняк СaCO3 і доломіт MgCO3.
32.
Доменна піч працює безупинно. Висока температура в печіпідтримується завдяки екзотермічним реакціям. Періодично у піч
додають нові порції шихти.
В одній доменній печі за добу можна зварити понад 2000 т чавуну.
Робота печі триває протягом кількох років, аж до капітального
ремонту.
По застосуванню чавун ділиться на три групи: ливарний,
спеціальний, передільний.
Із ливарного чавуну виливають найрізноманітніші вироби: деталі
складної конфігурації, скульптури, предмети декору.
Додавання магнію та інших металів значно поліпшує механічні
властивості чавуну, зменшує його крихкість.
Із передільного чавуну виплавляють сталь.
Доменний шлак використовують для виготовлення шлакобетону,
гравію, щебеню тощо.
33.
34.
Майже 10% чавуну використовується якметал у машинобудуванні,решту (майже
90%) переробляють на сталь.
Побічні продукти – шлаки –
використовують у виробництві цементу,
шлакоблоків;
35.
Сталь — сплав, у якому значно менший вмістКарбону (0,1-2 %) і домішок мангану, сполук
Силіцію, Фосфору та Сульфуру. Менший вміст
Карбону надає сталі більшої ковкості та
пластичності. Тому її можна штампувати,
прокатувати, кувати.
Для поліпшення цих якостей сталь загартовують,
тобто розжарену сталь швидко охолоджують.
Гартована сталь значно твердіша. Водночас сталь з
низьким вмістом Карбону загартовуванню не
піддають.
Для надання сталі певних якостей її легують, тобто
додають до неї інші метали. Легувальними
металами найчастіше є хром, вольфрам, нікель,
ванадій, манган, молібден, меншою мірою —
титан, кобальт, берилій. А з неметалів — силіцій.
36.
Сталі за хімічним складом:Вуглецеві
Леговані
37.
За механічними властивостями розрізняють сталі:Конструкційні – використовують для виготовлення деталей машин,
конструкцій і споруд. Можуть бути вуглецеві і леговані (найчастіше
хром, нікель, марганець – 1 – 1,5%).
Інструментальні – використовують для виробництва ріжучих та
вимірювальних інструментів. Це – леговані (хром, ванадій, вольфрам)
сталі.
Сталі з особливими властивостями – нержавіючі, жаростійкі,
жароміцні, магнітні та ін.
Нержавіючі – стійкі до корозії за нормальних умов (вода, кислоти).
Жаростійкиі – стійкі до корозії за високих температур.
Магнітні – виявляють феромагнітні властивості (леговані хромом і
вольфрамом).
Залежно від призначення металу розрізняють:
конструкційну сталь (матеріал для арматури, рейок, труб, листів,
будівельного і технічного обладнання , транспортних засобів)
інструментальну сталь (для різальних інструментів, пружин)
нержавіючу сталь (для труб і апаратів хімічної та харчової
промисловості).
Сталь і в майбутньому залишатиметься одним із найважливіших
матеріалів.
38.
Виробництво сталіСуть процесу переробляння чавуну на сталь полягає у зменшуванні
до потрібної концентрації вмісту вуглецю і шкідливих домішок —
фосфору і сірки, які роблять сталь крихкою і ламкою.
Залежно від способу окиснювання вуглецю є різні способи
переробляння чавуну на сталь:
конверторний, мартенівський і електротермічний.
До фінасової кризи в 2008 році Україна залишалася однією з
небагатьох країн, де широко використовули мартенівський спосіб
виплавляння сталі, що є досить енергозатратним та екологічно
шкідливим. Наразі більшість мартенівських печей в Україні виведено
з експлуатації, а ті що лишилися, невдовзі також будуть закриті.
Зараз в Україні, як і в усьому світі, переважну більшість сталевої
продукції виробляють конвертерним способом. Україна станом на
2008 р. займає п’яте місце у світі за обсягами експорту сталі,
76,46 % сталі, що її виробляють на світовому ринку, припадає на
десять провідних країн.
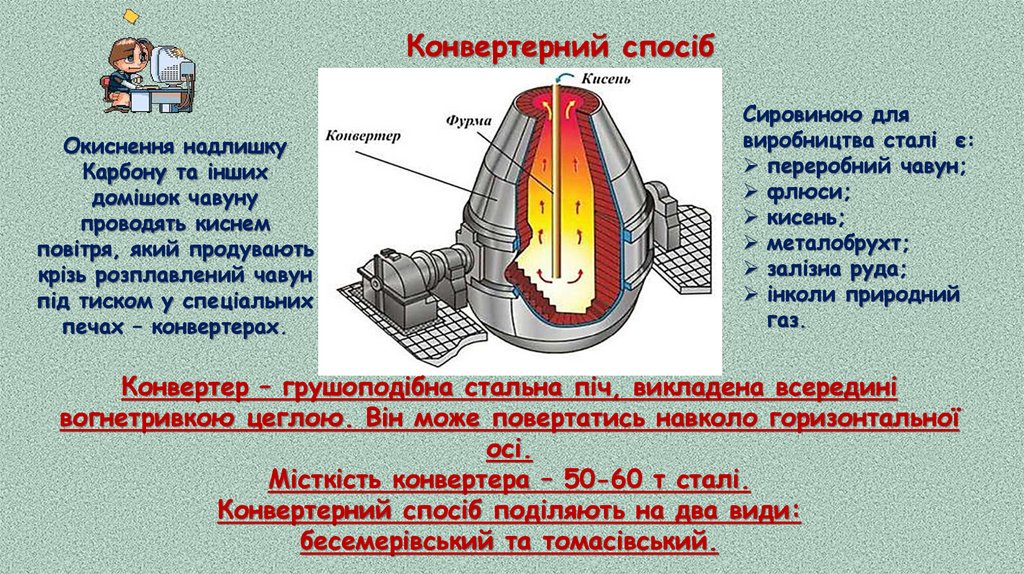
39.
Конвертерний спосібОкиснення надлишку
Карбону та інших
домішок чавуну
проводять киснем
повітря, який продувають
крізь розплавлений чавун
під тиском у спеціальних
печах – конвертерах.
Сировиною для
виробництва сталі є:
переробний чавун;
флюси;
кисень;
металобрухт;
залізна руда;
інколи природний
газ.
Конвертер – грушоподібна стальна піч, викладена всередині
вогнетривкою цеглою. Він може повертатись навколо горизонтальної
осі.
Місткість конвертера – 50-60 т сталі.
Конвертерний спосіб поділяють на два види:
бесемерівський та томасівський.
40.
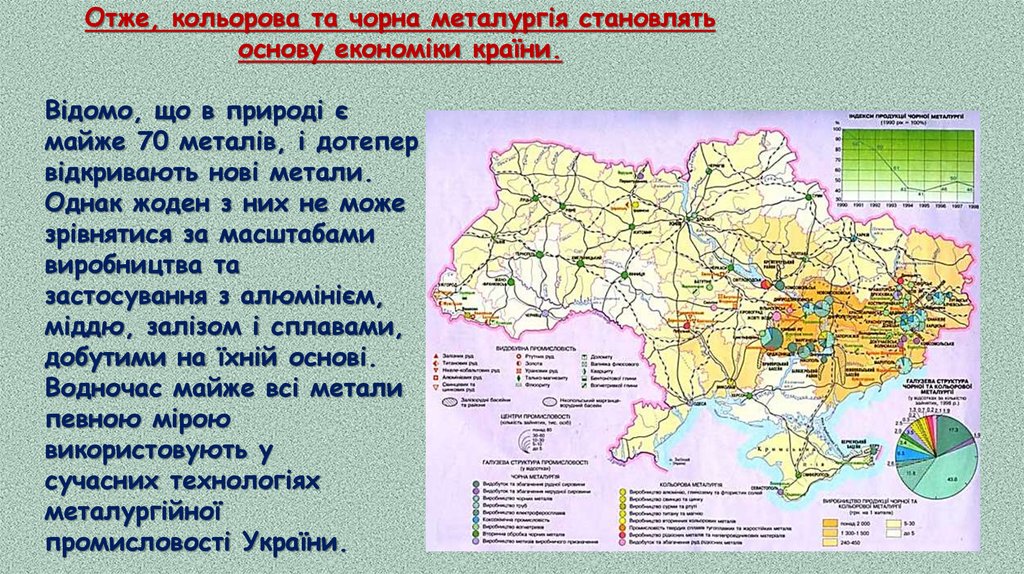
Отже, кольорова та чорна металургія становлятьоснову економіки країни.
Відомо, що в природі є
майже 70 металів, і дотепер
відкривають нові метали.
Однак жоден з них не може
зрівнятися за масштабами
виробництва та
застосування з алюмінієм,
міддю, залізом і сплавами,
добутими на їхній основі.
Водночас майже всі метали
певною мірою
використовують у
сучасних технологіях
металургійної
промисловості України.
41.
Чорна металургія УкраїниЧорна металургія України— дуже
матеріаломістка галузь, яка споживає
близько ЗО % палива, майже 20 %
електроенергії та води, які
використовуються в господарстві країни.
В Україні можна виділити три райони
чорної металургії:
Придніпров'я, Донбас і Приазов'я.
Однією з основних проблем чорної
металургії є вичерпаність багатьох
родовищ залізних руд. Кількість заліза
в руді зменшується.
42.
Екологія та металургія.За сучасних технологій виготовлення металів
не вдається уникнути забруднення
навколишнього середовища.
Як наслідок на територіях з розвиненою
чорною металургією підвищений уміст
шкідливих речовин у повітрі, воді, продукції
рослинництва й тваринництва.
Така несприятлива екологічна ситуація є
предметом уваги технологів, лікарів, екологів.
Під час металургійного виробництва й
переробки руд утворюються отруйні гази, які
потрапляють в атмосферу. Це відомі вам
сульфур(IV), нітроген(IV) і карбон(IV) оксиди,
що спричиняють випадання кислотних дощів;
карбон(ІІ) оксид отруює повітря.
43.
Крім газів, утворюється пил, який уловлюють за допомогоюспеціальних пристроїв і фільтрів. У чорній металургії
використовують велику кількість води для охолодження металів.
Вода забруднюється, а водоочисні споруди не завжди забезпечують
її повне очищення від шкідливих домішок. Унаслідок потрапляння
відпрацьованої води в природні водойми шкідливі речовини
забруднюють їх.
Усі ці забруднення негативно впливають на довкілля, а отже, і на
здоров'я людини, ріст і розвиток рослин і тварин.
44.
З метою забезпечення охорони навколишнього середовищапід час виробництва й використання металів наукові
дослідження проводяться в чотирьох напрямках.
Впровадження безвідходних
технологій і технологій комплексного
використання сировини.
При цьому забезпечується
збагачення руд, раціональна
повнота вилучення основних і
супутніх елементів,
утилізація відходів виробництв
без заподіяння шкоди навколишньому
середовищу.
Шлаки ― цінна сировина для
будівельної та дорожньобудівельної
галузей.
45.
Виробництво переводиться на замкненийцикл водокористування.
Річ у тім, що на металургійних комбінатах не
завжди водоочисні споруди забезпечують повне
очищення води від шкідливих домішок ,перш ніж
відпрацьована вода потрапить за межі заводу у
водойми.
Відповідальність місцевої влади та
керівництва підприємств за захист
навколишнього середовища.
Місцева влада, керівництво металургійних підприємств
повинні нести відповідальність за дотриманням
санітарних норм, за збереження та примноження зелених
насаджень, які відіграють важливу роль у поліпшенні
складу повітря, оздоровленні навколишнього середовища.
46.
Тому найважливішим завданням металургійноїпромисловості є впровадження безвідходних
технологій. Це дасть змогу багаторазово
використовувати відходи та здешевити виробництво
багатьох продуктів промисловості. Прикладом
безвідходної технології може бути використання
сульфур(IV) оксиду для виробництва сульфатної
кислоти.
Лікарі,фармацевти і дієтологи повинні
скеровувати свої дії на розроблення
належних раціонів харчування, засобів
профілактики та лікування професійних
захворювань тощо.
47.
Список необхідної літератури.Основна:
1. Попель П. П. Хімія: підруч. Для 11 кл. Закладів загальної середньої освіти
(рівень стандарту) П.П. Попель, Л. С. Крикля. — Київ: ВЦ «академія», 2018.
2. Чернобельська Г.М., Чертков И.Н. Хімія – М.: Медицина, 1993.
3. Сухан В.В., Табунська Т.В., Хімія (посібник для вступників до вузів) – К.: Либідь
1993.
4. Електронний підручник з хімії: https://sites.Google.Com/view/allhemi/
4.виконати тести за посиланням:
https://naurok.com.ua/test/start/2056836
https://naurok.com.ua/test/start/1357676
Додаткова:
1. Луцевич Д.Д., Березан О.В. Конспект – довідник з хімії.– К.: Вища школа 1997.
2. Ярошенко О.Г., Новицька В.І. Збірник задач і вправ з хімії. – К.: Станіца 1996.
3. Буринська Н.М. Основи загальної хімії. 11 клас. 1997.
48.
Відео за посиланнямhttps://www.google.com/search?sca_esv=b8098a47c6cf00ad&rlz=1C1N
DCM_ruUA1042UA1042&sxsrf=AE3TifM26cvvnAUzsWR8Oxth2HUlm_h
wKg:1762235409823&udm=7&fbs=AIIjpHy3vMFde4-As4rkZ3m7V6OfAwebRfpLMqO9KzeNsNGe0FFk144n84FQPpG5s2ziYxuPT
yc4jMzTPcQbTjMjsHBpq4o716z27qQrTD1l8wfi7IbQz0mI_Zn6cN3_PMA5JsuU8TYUTXq3SUR4c3DNnvAqWppQq7q
OE4P75xm4QODkmVPhiOs6dPDx1GS93JzXhY3QmjModejXTtnrmHRQJjAqpn_uBz24QgOeiFdFPJIj4TjL-ZWQZ3MXo2RKIFy03pEc7TCX7lgyMtKcEr6eIJDNg&q=%D0%BC%D0%B5%D1%
82%D0%BE%D0%B4%D0%B8+%D0%B4%D0%BE%D0%B1%D1%83%D0%B
2%D0%B0%D0%BD%D0%BD%D1%8F+%D0%BC%D0%B5%D1%82%D0%B
0%D0%BB%D1%96%D0%B2&sa=X&ved=2ahUKEwj_y_O85teQAxUFQvE
DHbk3CmQQtKgLegQIExAB&biw=1280&bih=559&dpr=1.5#fpstate=ive
&vld=cid:3bfa5b2a,vid:ZpXN8jDBnLU,st:0










































 industry
industry








