Similar presentations:
Тема 23. Аллотропные модификации серы. Нахождение (2)
1.
Аллотропные модификации серы.Нахождение серы и её соединений в
природе. Химические свойства серы
2.
Строение атома серы.3 период.
VI группа, главная подгруппа.
Заряд ядра +16.
Электронная формула 1s²2s²2p⁶3s²3p⁴.
Степени окисления: -2, +4, +6.
Валентность: II, IV, VI.
3.
Физические свойства серы.Твёрдое агрегатное состояние.
Жёлтого цвета.
Не растворима в воде.
Не смачивается водой.
Растворяется в органических
растворителях.
4.
Аллотропные модификации серы.Ромбическая сера.
S
S
S
S
S
S
S
S
Ромбическая сера (α– сера) - S₈ жёлтого цвета.
Температура плавления: 113°C.
Наиболее устойчивая
модификация.
5.
Аллотропные модификации серы.Моноклинная сера.
S
S
S
S
S
S
S
S
S
S
S
S
S
S
S
S
Моноклинная сера (β-сера) - S₈ тёмно-жёлтые иглы.
Температура плавления 119°C.
Устойчива при температуре выше
96°C.
При обычных условиях переходит
в ромбическую серу.
6.
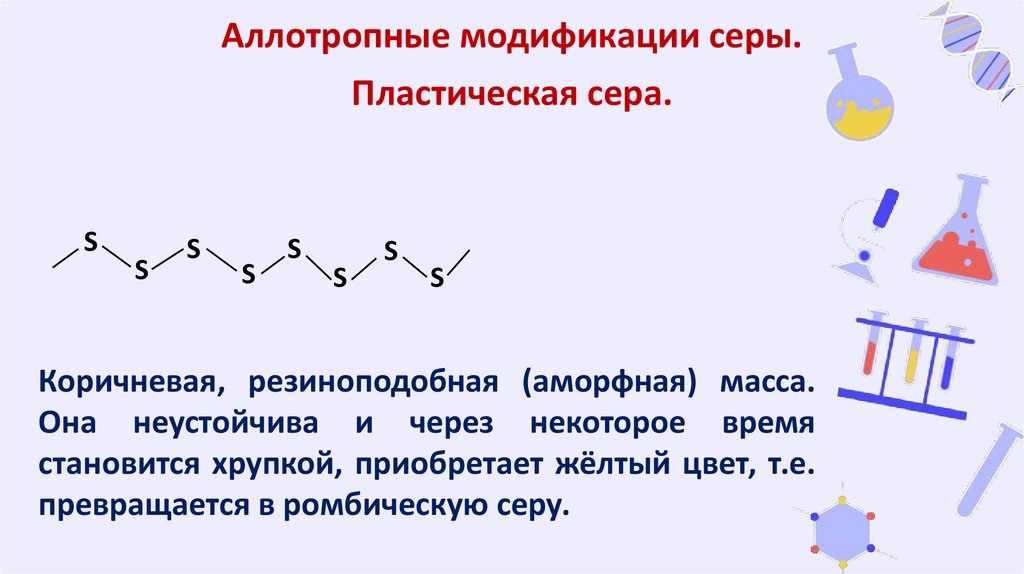
Аллотропные модификации серы.Пластическая сера.
S
S
S
S
S
S
S
S
Коричневая, резиноподобная (аморфная) масса.
Она неустойчива и через некоторое время
становится хрупкой, приобретает жёлтый цвет, т.е.
превращается в ромбическую серу.
7.
Химические свойства серы.Окислительные свойства
Восстановительные свойства
1. Сера взаимодействует почти со 1. Сера взаимодействует с
всеми металлами.
кислородом (горит):
Fe + S = FeS
S + O2 = SO2
2. Со щелочными металлами
2. Сера взаимодействует со
сера взаимодействует без
фтором:
нагревания.
S + 3F2 = SF6
2Na + S → Na2S
3. При повышенной температуре
сера взаимодействует с
водородом:
H2 + S = H2S
8.
Сера в природе.• Сульфидная
• Самородная
• Сульфатная
Сера в 3-х формах
9.
Разновидности серы в природе.- Пирит FeS2 (железный колчедан)
- Сфалерит ZnS (цинковая обманка)
- Галенит PbS (свинцовый блеск)
- Киноварь HgS (ртутная обманка)
- Халькопирит CuFeS2 (медный колчедан)
- Халькозин Cu2S (медный блеск)
- Антимонит Sb2S3 (сурьмяный блеск)
- Гипс CaSO4 · 2H2O (лёгкий шпат)
- Мирабилит Na2SO4 · 10H2O (глауберова соль)
- Барит BaSO4
Сульфидная
сера







 chemistry
chemistry








