Similar presentations:
Термодинамические процессы идеальных газов
1. Термодинамика и теплопередача
Термодинамические процессыидеальных газов
2. Изохорный процесс
dv 0V const
Закон Шарля или второй закон ГейЛюссака: р Т
2
р1
2
Т1
Р
const
Т
Теплота в изохорном процессе:
q u cv (Т 2 Т1 )
Qv U v M cv (t 2 t1 ) VH cv (t 2 t1 )
/
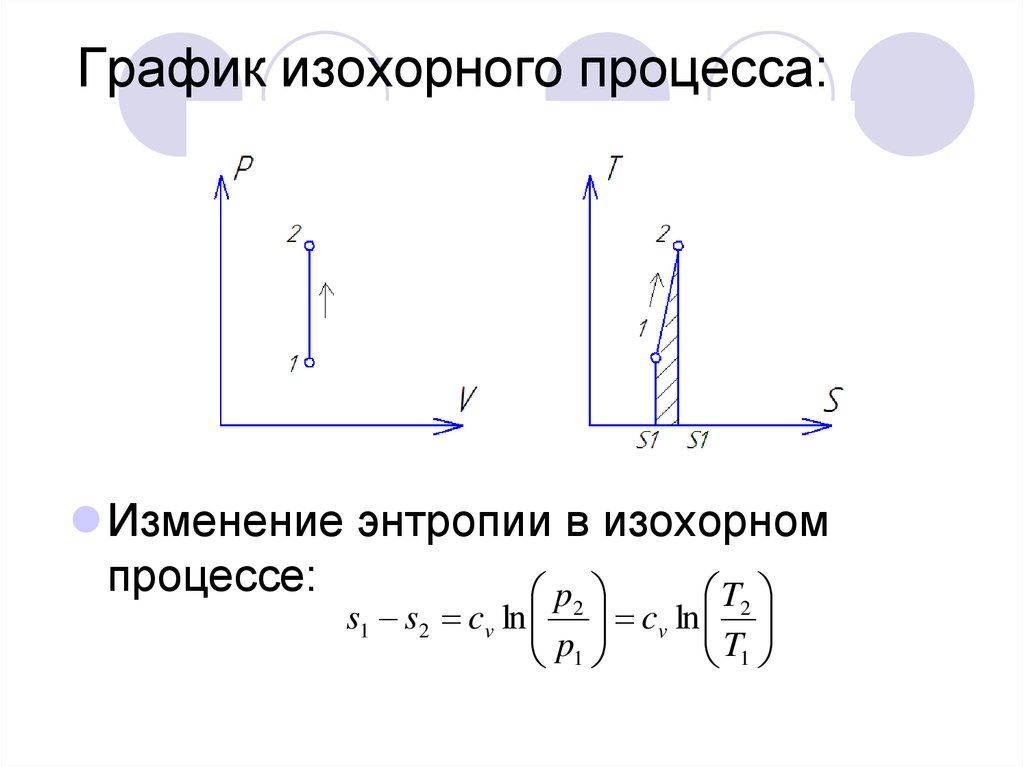
3. График изохорного процесса:
Изменение энтропии в изохорномпроцессе:
p
T
s1 s2 cv ln 2 cv ln 2
p1
T1
4. Изобарный процесс
dр 0Р const
Закон Гей-Люссака:
Работа расширения:
v 2 T2
v1 T1
5.
Теплота в изобарном процессе:График изобарного процесса:
Изменение энтропии:
T2
s2 s1 c p ln
T1
6. Изотермический процесс
dТ 0Т const
Уравнение изотермического процесса:
p2 v2
p1 v1
Работа 1 кг идеального газа:
7.
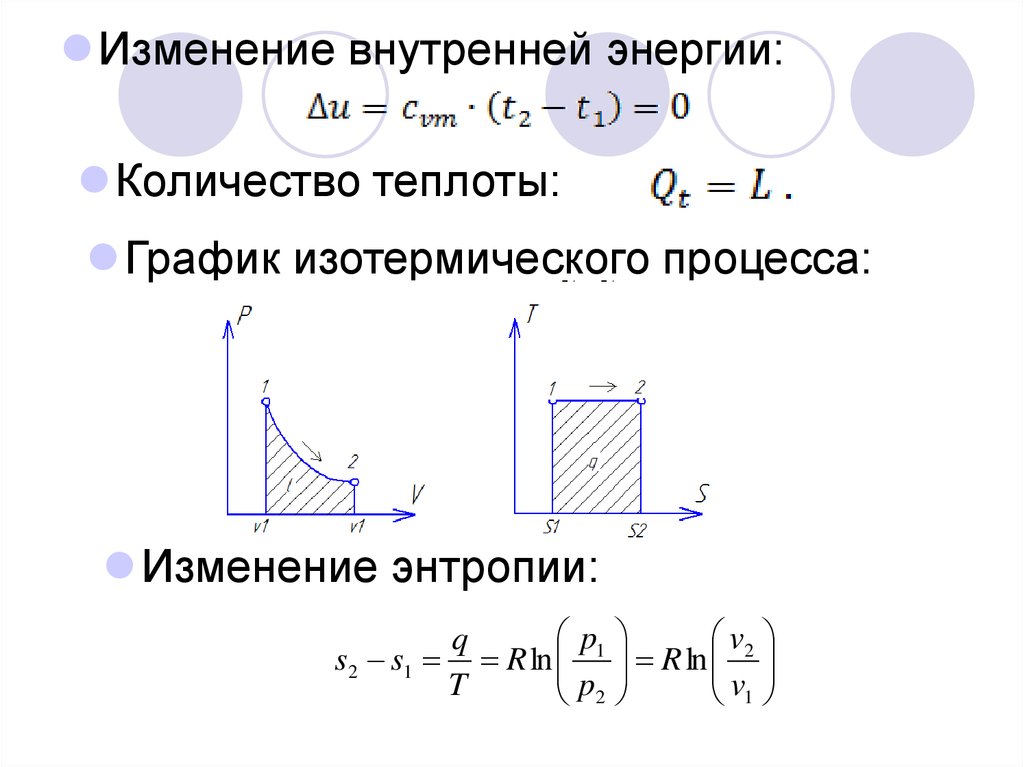
Изменение внутренней энергии:Количество теплоты:
График изотермического процесса:
Изменение энтропии:
p1
v2
q
s2 s1 R ln R ln
T
v1
p2
8. Адиабатный процесс
q 0q 0
S 0
S const
Уравнения адиабаты идеального газа:
рv p v
k
1 2
р v const
k
T2 V1
T1 V2
K 1
P
2
P1
k
2 2
K 1
K
Показатель адиабаты:
k c p / cv
9. Работа 1 кг идеального газа в адиабатном процессе:
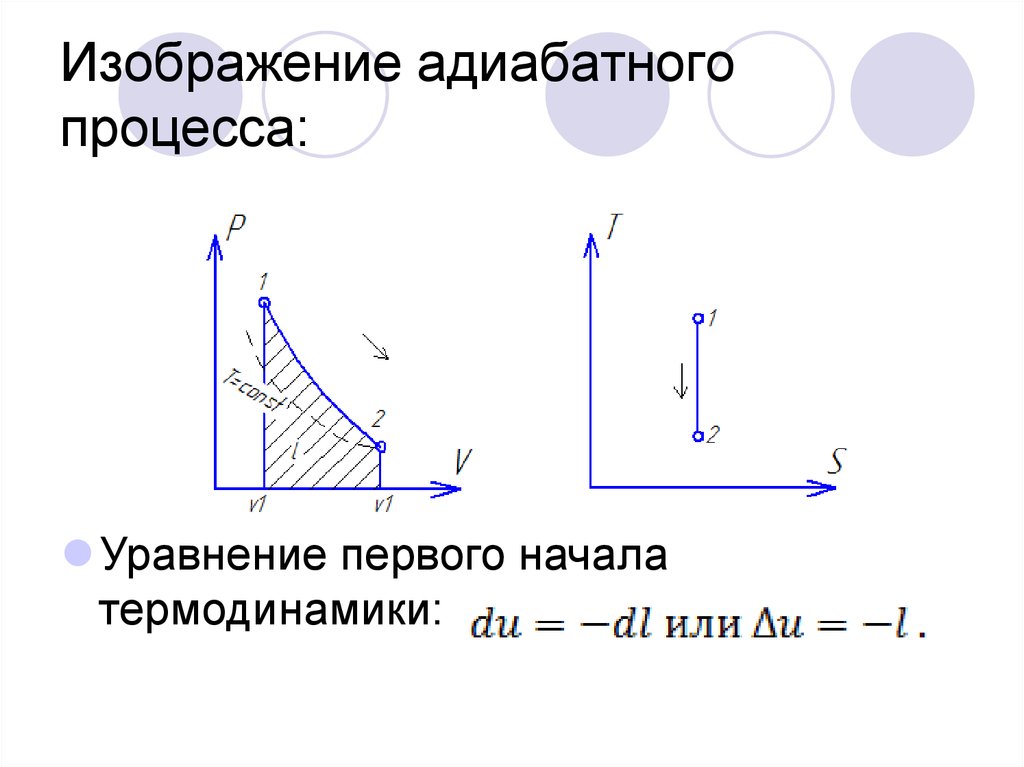
10. Изображение адиабатного процесса:
Уравнение первого началатермодинамики:
11. Политропный процесс
с constpv const
n
Уравнение политропного процесса:
Т 2 р2
Т 1 р1
n 1
n
Т 2 v1
Т 1 v2
n 1
p 2 v1
p1 v 2
n
Работа расширения:
l
R
T1 T 2
n 1
pv T
l 1 1 1 2
n 1 T1
l
1
p1v1 p2 v2
n 1
Количество теплоты в политропном
процессе:
n k
q cv
n 1
(T2 T1 ) c П T2 T1
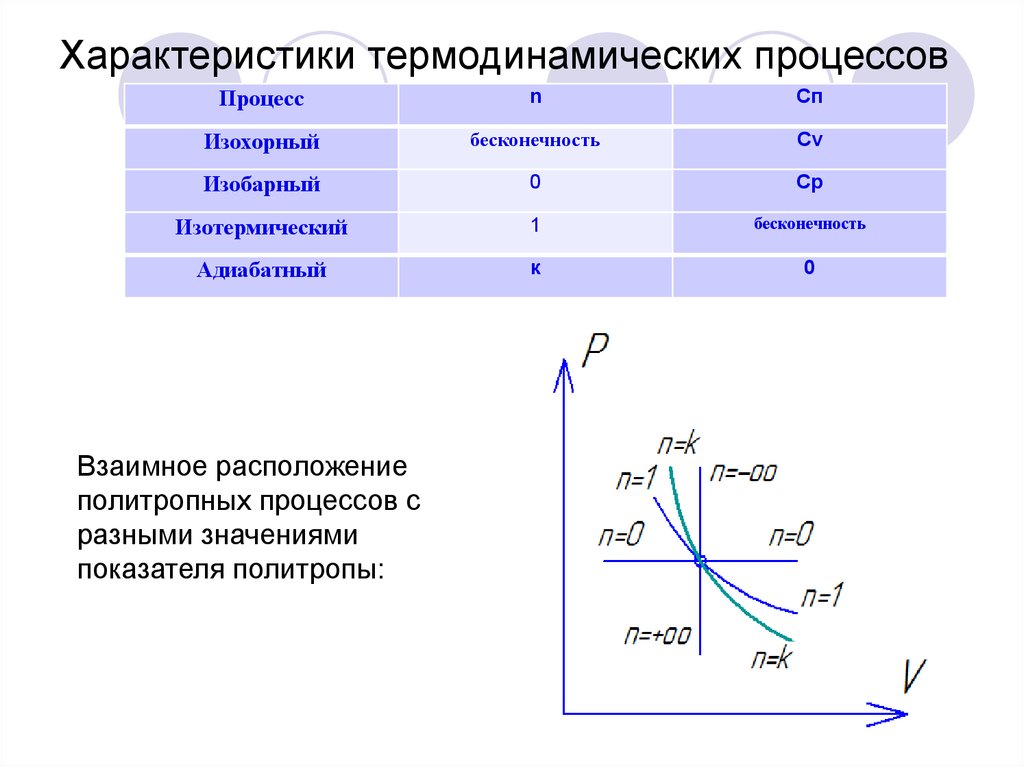
12. Характеристики термодинамических процессов
Процессn
Cп
Изохорный
бесконечность
Сv
Изобарный
0
Ср
Изотермический
1
бесконечность
Адиабатный
к
0
Взаимное расположение
политропных процессов с
разными значениями
показателя политропы:








 physics
physics








