Similar presentations:
Свойства газов и жидкостей
1.
Свойства газов и жидкостей1
2.
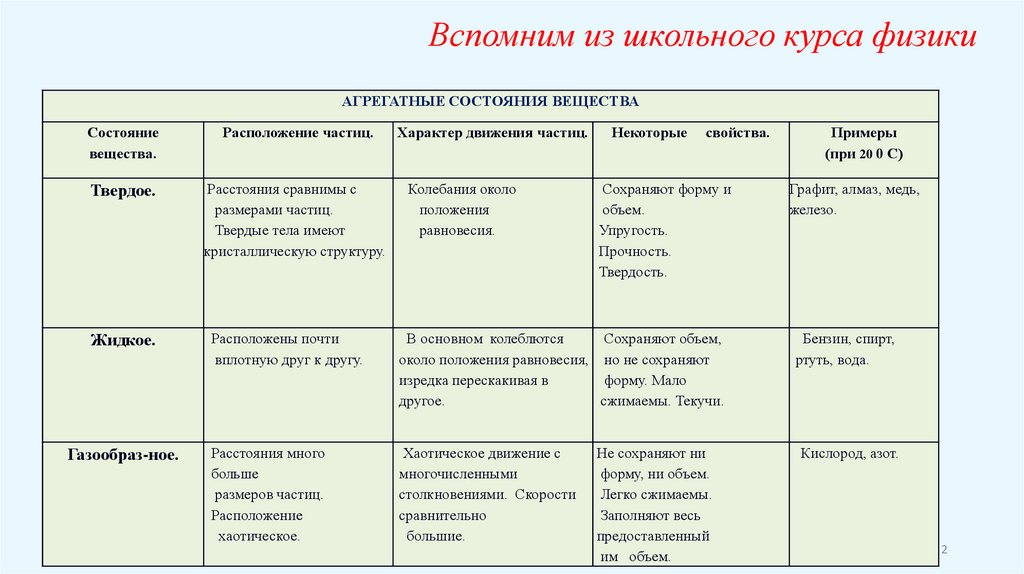
Вспомним из школьного курса физикиАГРЕГАТНЫЕ СОСТОЯНИЯ ВЕЩЕСТВА
Состояние
вещества.
Расположение частиц.
Твердое.
Расстояния сравнимы с
размерами частиц.
Твердые тела имеют
кристаллическую структуру.
Колебания около
положения
равновесия.
Жидкое.
Расположены почти
вплотную друг к другу.
В основном колеблются
Сохраняют объем,
около положения равновесия, но не сохраняют
изредка перескакивая в
форму. Мало
другое.
сжимаемы. Текучи.
Бензин, спирт,
ртуть, вода.
Расстояния много
больше
размеров частиц.
Расположение
хаотическое.
Хаотическое движение с
многочисленными
столкновениями. Скорости
сравнительно
большие.
Кислород, азот.
Газообраз-ное.
Характер движения частиц.
Некоторые
свойства.
Сохраняют форму и
объем.
Упругость.
Прочность.
Твердость.
Не сохраняют ни
форму, ни объем.
Легко сжимаемы.
Заполняют весь
предоставленный
им объем.
Примеры
(при 20 0 С)
Графит, алмаз, медь,
железо.
2
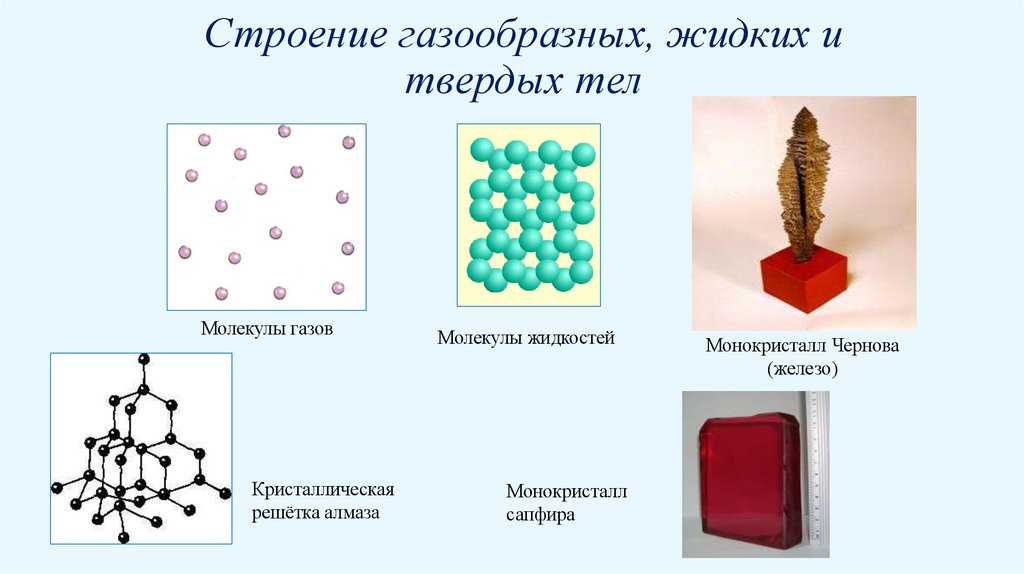
3. Строение газообразных, жидких и твердых тел
Молекулы газовКристаллическая
решётка алмаза
Молекулы жидкостей
Монокристалл
сапфира
Монокристалл Чернова
(железо)
4.
На поверхности земли мынаблюдаем H2O в трёх
агрегатных состояниях:
водяной пар,
лёд,
вода.
Водяной пар
Из всех разделов физики только
молекулярная
физика
даёт
возможность показать - почему
вещество может находиться в
газообразном,
жидком
и
твердом состояниях.
Лёд
Вода
5. Газообразное состояние
Они не сохраняют не формы, ни объема. Многочисленные ударымолекул о стенки сосуда создают давление газа.
В газах расстояние между атомами и молекулами в среднем во много раз
больше размеров самих молекул.
Газы легко сжимаемы, при этом уменьшается среднее расстояние между
молекулами, но молекулы не сдавливают друг друга.
Они могут неограниченно расширятся.
Газы не cохраняют ни формы, ни объема.
Многочисленные удары молекул о стенки сосуда создают давление газа.
5/40
6. Свойства газов
Объём и форму не сохраняют.Расстояние между молекулами большое, во много раз больше самих молекул .
Легко сжимаемы.
Молекулы газов совершают беспорядочное движение, поэтому заполняют собой
весь предоставленный им объём.
При повышении температуры расширяются. Если сосуд отсутствует, то
расширяются неограниченно.
При критически низких температурах превращаются в жидкости, твердые тела
6/40
7.
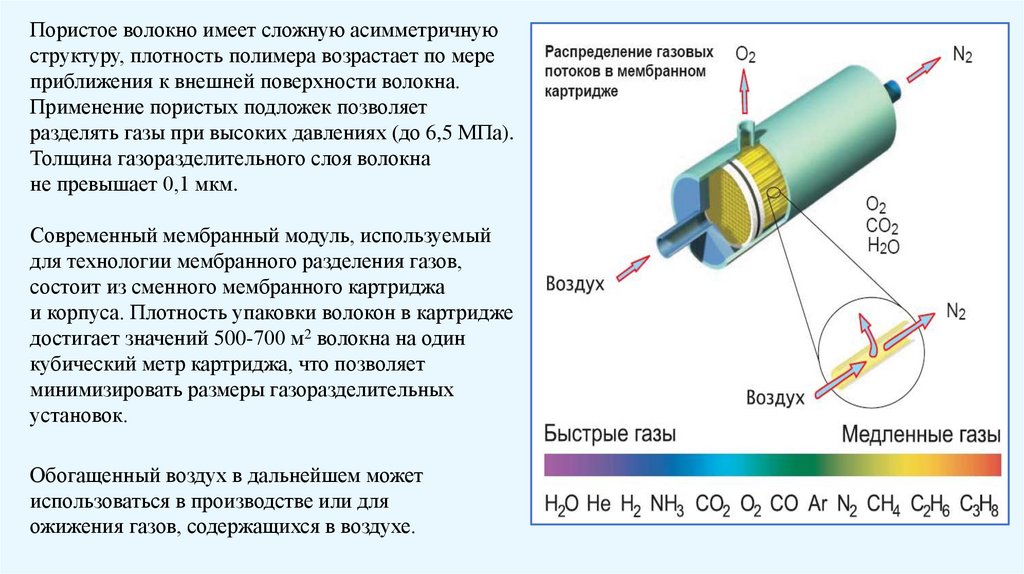
Пористое волокно имеет сложную асимметричнуюструктуру, плотность полимера возрастает по мере
приближения к внешней поверхности волокна.
Применение пористых подложек позволяет
разделять газы при высоких давлениях (до 6,5 MПа).
Толщина газоразделительного слоя волокна
не превышает 0,1 мкм.
Современный мембранный модуль, используемый
для технологии мембранного разделения газов,
состоит из сменного мембранного картриджа
и корпуса. Плотность упаковки волокон в картридже
достигает значений 500-700 м2 волокна на один
кубический метр картриджа, что позволяет
минимизировать размеры газоразделительных
установок.
Обогащенный воздух в дальнейшем может
использоваться в производстве или для
ожижения газов, содержащихся в воздухе.
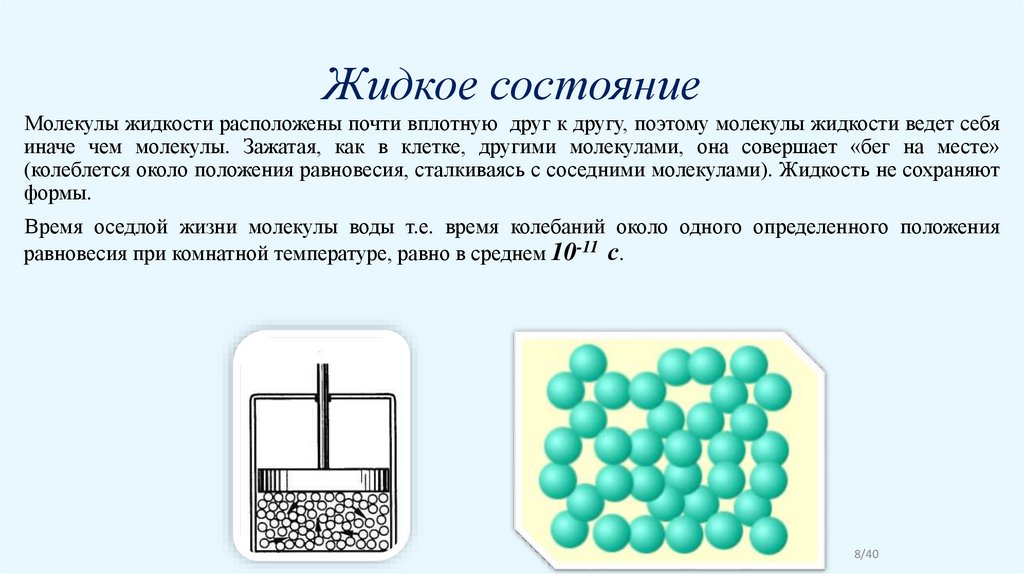
8. Жидкое состояние
Молекулы жидкости расположены почти вплотную друг к другу, поэтому молекулы жидкости ведет себяиначе чем молекулы. Зажатая, как в клетке, другими молекулами, она совершает «бег на месте»
(колеблется около положения равновесия, сталкиваясь с соседними молекулами). Жидкость не сохраняют
формы.
Время оседлой жизни молекулы воды т.е. время колебаний около одного определенного положения
равновесия при комнатной температуре, равно в среднем 10-11 с.
8/40
9. Вывод:
1.В зависимости от условий одно и то же вещество может находиться в различных
агрегатных состояниях.
Вещество может переходить из одного агрегатного состояния в другое.
2.
Переход из одного состояния вещества в другое называется фазовым переходом.
9
10.
Особенности свойств жидкостей11.
Почему монетка и водомерка не тонут?У жидкостей имеется свободная поверхность – граница раздела
жидкости и газа.
На молекулу на этой границе действуют разные силы,
равнодействующая направлена внутрь жидкости и перпендикулярно
поверхности. Поэтому молекулы «втягиваются» внутрь жидкости
11
12.
Способность жидкости сокращать свою поверхность называютповерхностным натяжением
Поверхностное натяжение - явление молекулярного давления на жидкость, вызванное,
притяжением молекул поверхностного слоя к молекулам внутри жидкости.
12
13. Энергия поверхностного слоя
Молекулы поверхностного слоя обладают избыточной по сравнению с молекуламивнутри жидкости потенциальной энергией, т.е. поверхностной энергией:
Еп= σ S;
σ - коэффициент поверхностного натяжения
Жидкость принимает такую форму при которой эта энергия будет иметь
минимальное значение, а ее площадь оказывается минимальной для данного
объема жидкости.
Коэффициент поверхностного натяжения σ – это физическая величина, равная
отношению силы, с которой поверхностный слой жидкости действует на
ограничивающий его контур к длине этого контура. Измеряется в Н/м
Fп.н.= σ L;
13
14. Жидкость в свободном состоянии принимает форму шара
1415.
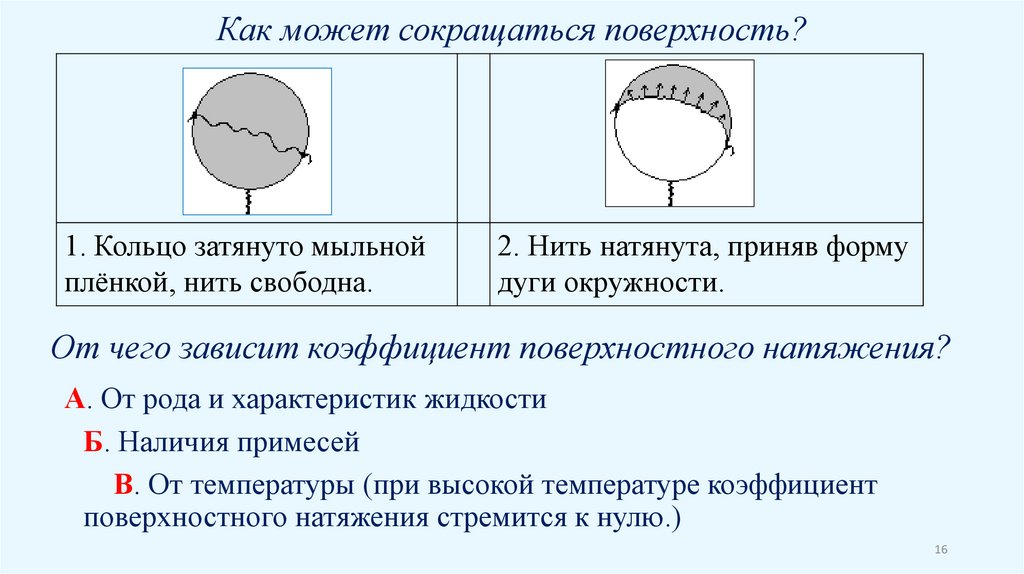
Как может сокращаться поверхность?1. Кольцо затянуто мыльной
плёнкой, нить свободна.
2. Нить натянута, приняв форму
дуги окружности.
От чего зависит коэффициент поверхностного натяжения?
А. От рода и характеристик жидкости
Б. Наличия примесей
В. От температуры (при высокой температуре коэффициент
поверхностного натяжения стремится к нулю.)
16
16. Как может сокращаться поверхность?
Сложные мыльные пузыриИз всего вышесказанного можно сделать вывод о
том, что жидкости стремятся образовать фигуры
с минимальной площадью поверхности при
максимальном объеме
17.
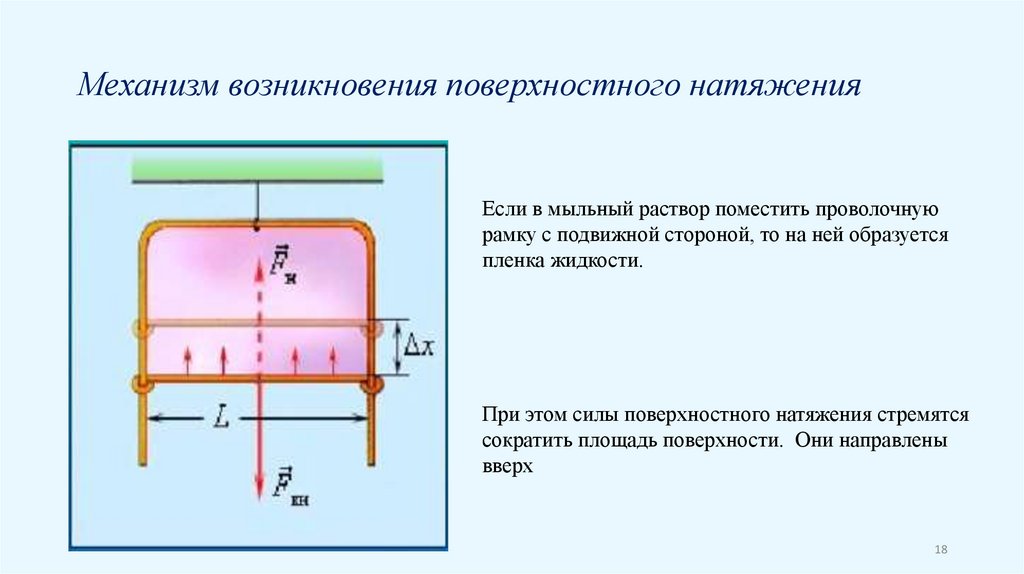
Механизм возникновения поверхностного натяженияЕсли в мыльный раствор поместить проволочную
рамку с подвижной стороной, то на ней образуется
пленка жидкости.
При этом силы поверхностного натяжения стремятся
сократить площадь поверхности. Они направлены
вверх
18
18. Механизм возникновения поверхностного натяжения
Молекулы жидкости притягиваются друг у кругу слабее, чем к молекулам твердого тела. Врезультате жидкость стремится прижаться к поверхности, расплывается по ней. Так ведет
себя ртуть на цинковой пластине, вода на чистом стекле или дереве.
В этом случае говорят, что жидкость смачивает поверхность.
19/40
19.
Молекулы жидкости притягиваются друг у кругу сильнее, чем к молекулам твердого тела.В результате силы притяжения между молекулами жидкости собирают её в капельку. Так ведет себя
ртуть на стекле, вода на парафине или "жирной" поверхности.
В этом случае говорят, что жидкость НЕ смачивает поверхность.
20
20.
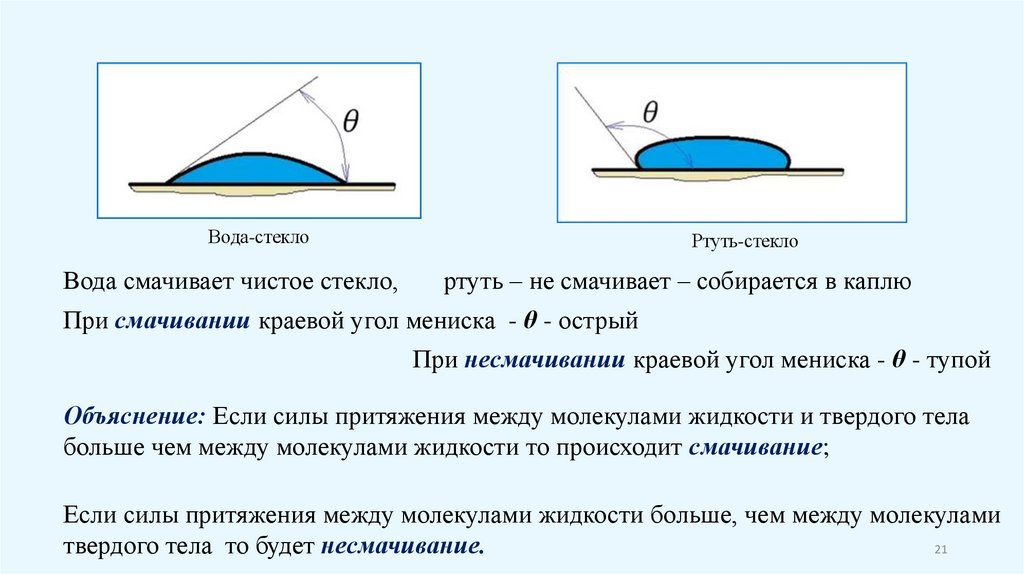
Вода-стеклоВода смачивает чистое стекло,
Ртуть-стекло
ртуть – не смачивает – собирается в каплю
При смачивании краевой угол мениска - θ - острый
При несмачивании краевой угол мениска - θ - тупой
Объяснение: Если силы притяжения между молекулами жидкости и твердого тела
больше чем между молекулами жидкости то происходит смачивание;
Если силы притяжения между молекулами жидкости больше, чем между молекулами
твердого тела то будет несмачивание.
21
21.
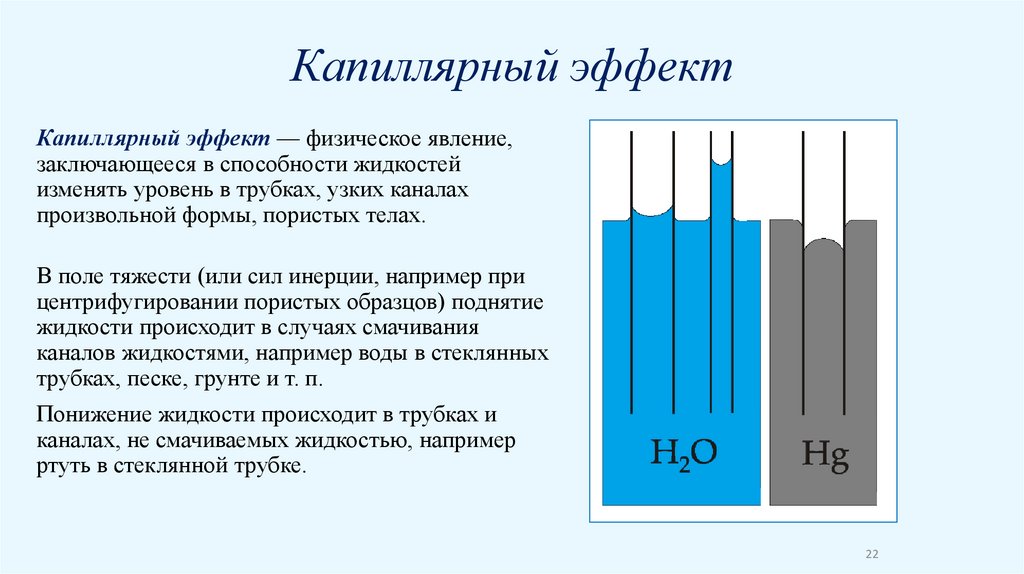
Капиллярный эффектКапиллярный эффект — физическое явление,
заключающееся в способности жидкостей
изменять уровень в трубках, узких каналах
произвольной формы, пористых телах.
В поле тяжести (или сил инерции, например при
центрифугировании пористых образцов) поднятие
жидкости происходит в случаях смачивания
каналов жидкостями, например воды в стеклянных
трубках, песке, грунте и т. п.
Понижение жидкости происходит в трубках и
каналах, не смачиваемых жидкостью, например
ртуть в стеклянной трубке.
22
22. Капиллярный эффект
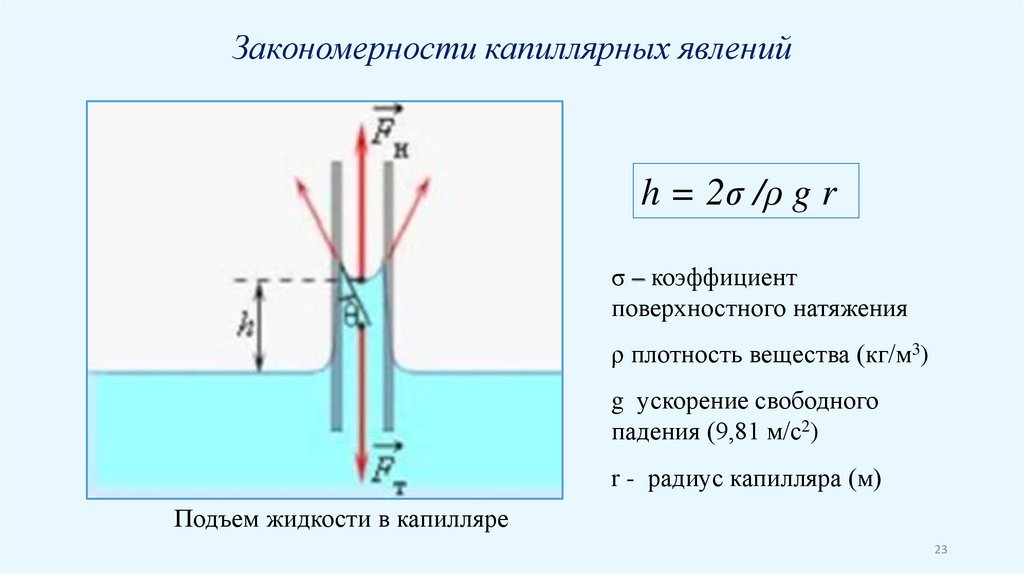
Закономерности капиллярных явленийh = 2σ /ρ g r
σ – коэффициент
поверхностного натяжения
ρ плотность вещества (кг/м3)
g ускорение свободного
падения (9,81 м/с2)
r - радиус капилляра (м)
Подъем жидкости в капилляре
23
23. Закономерности капиллярных явлений
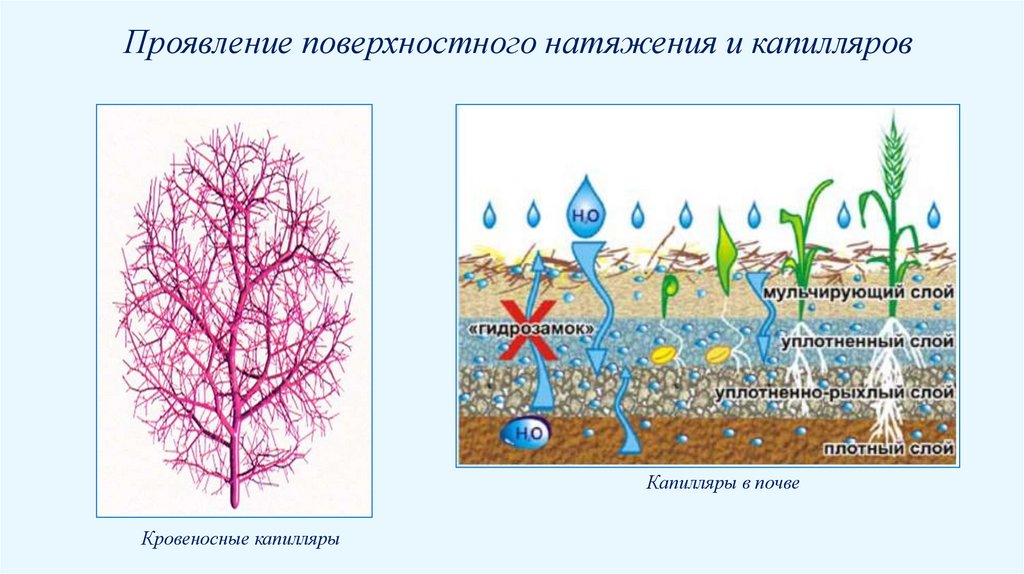
Проявление поверхностного натяжения и капилляровКапилляры в почве
Кровеносные капилляры
24. Проявление поверхностного натяжения и капилляров
Контроль качества сварных швов пенетрантамиСтрелками показаны микродефекты сварных швов
Пенетранты - вещества, обладающими малым поверхностным натяжением и высокой световой и цветовой
контрастностью, позволяющей легко их увидеть
25
25.
Применение в медицинеРаствор, под действием силы тяжести, поступает из флакона в полиэтиленовую
трубку, проходит воздушный клапан (каплеобразователь) с фильтром и опять же
через трубку попадает через иглу в вену.
Если бы не было воздушного клапана, в флаконе создалось бы отрицательное
давление и жидкость из него перестала бы выходить. После каплеобразователя
как правило находится регулирующее устройство, с помощью которого
регулируется скорость поступления раствора
Устройство медицинской капельницы
Капиллярный электрофорез, известный также как капиллярный
зональный электрофорез, используется для разделения ионов по
заряду. В случае обычного электрофореза заряженные молекулы
перемещаются в проводящей жидкости под действием электрического
поля. В 1960-х годах была предложена методика капиллярного
электрофореза для разделения молекул по заряду и размеру в
тонком капилляре, заполненном электролитом
Капиллярный электрофорез
26.
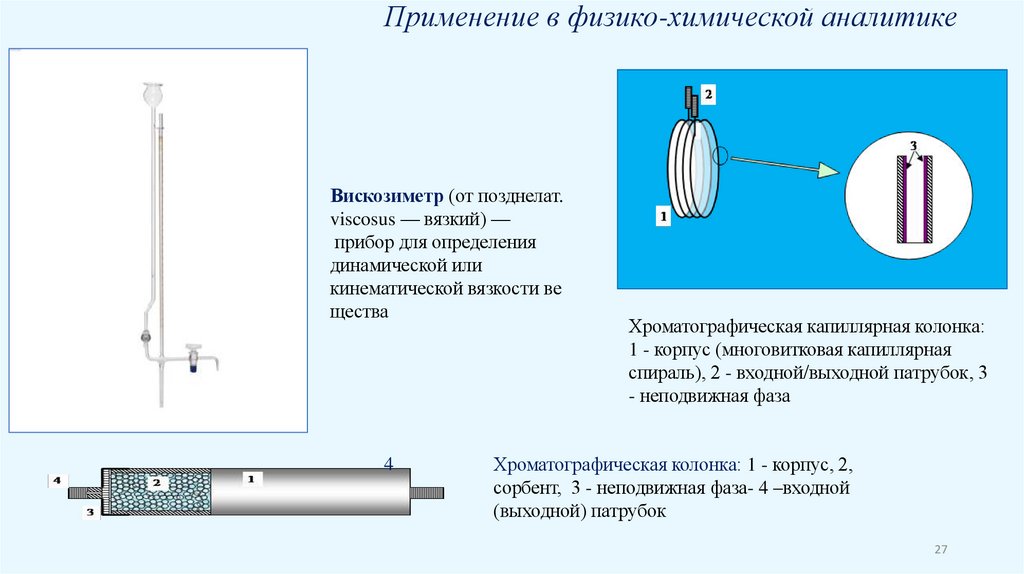
Применение в физико-химической аналитикеВискозиметр (от позднелат.
viscosus — вязкий) —
прибор для определения
динамической или
кинематической вязкости ве
щества
4
Хроматографическая капиллярная колонка:
1 - корпус (многовитковая капиллярная
спираль), 2 - входной/выходной патрубок, 3
- неподвижная фаза
Хроматографическая колонка: 1 - корпус, 2,
сорбент, 3 - неподвижная фаза- 4 –входной
(выходной) патрубок
27
27.
Примеры решения задач1. В капиллярной трубке радиусом 0,5 мм жидкость поднялась на высоту 11 мм. Оценить плотность
данной жидкости, если ее коэффициент поверхностного натяжения равен 22 мН/м.
Решение





















 physics
physics








