Similar presentations:
1_Общая характеристика неметаллов
1.
§11.Неметаллы: атомы ипростые вещества.
Кислород, озон, воздух.
2.
Цель урока:Формирование умений устанавливать связь между
строением атомов, строением кристаллической решетки и
физическими свойствами неметаллов. Ознакомление с
составом воздуха.
Проблемный вопрос урока:
Какие химические элементы относят к неметаллам? В чем
отличие строения атомов неметаллов от атомов металлов?
Можно ли выделить общие физические свойства неметаллов?
Какие простые веществанеметаллы входят в состав воздуха?
3.
4.
Э -2. НеметаллыСхема образования ковалентной химической связи в молекуле хлора:
Cl2
Cl
VII A группа
++17
2
•
•
•
•
•
•
Cl Cl
•
•
•
•
•
•
Cl + Cl → Cl Cl
•
8
7
5.
Э -1. Актуализаций знанийВещества с двойной связью
•
•
•
•
•
•
O+ O → O O
•
•
•
•
••
••
•
•
••
••
•
N + N = N N
•
Вещества с тройной связью
6.
вещества молекулярного строенияH2, O2, N2, Cl2, F2, Br2, I2, O3, P4,S8
вещества немолекулярного строения
C, B, Si, Se, Te
Вещества молекулярного строения имеют низкие температуры
плавления и кипения и находятся в стандартных условиях в твердом,
жидком или газообразном состоянии.
7.
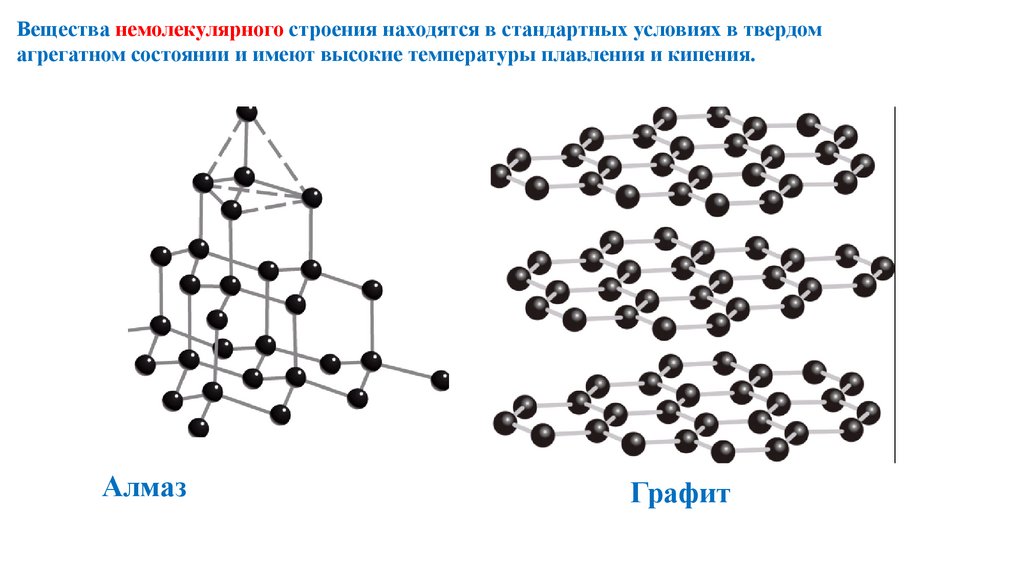
Вещества немолекулярного строения находятся в стандартных условиях в твердомагрегатном состоянии и имеют высокие температуры плавления и кипения.
Алмаз
Графит
8.
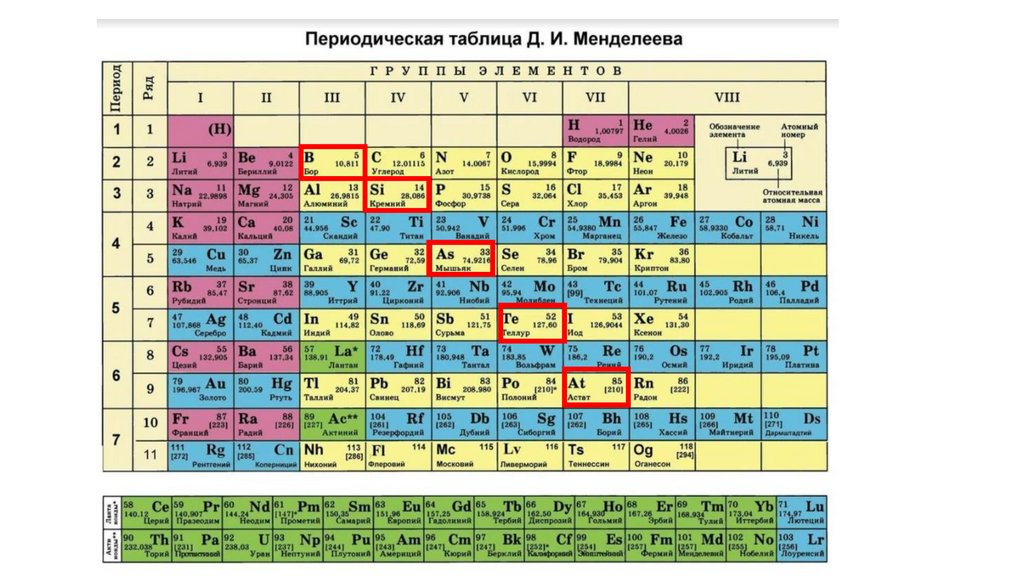
Э-1.Актуализация знаний об особенностях положения неметаллов в Периодической системеД. И. Менделеева.
Вспомните, что такое аллотропия и аллотропные видоизменения.
Приведите примеры известных вам аллотропных видоизменений металлов
и неметаллов. Объясните причины различия свойств аллотропных
видоизменений кислорода, фосфора и углерода.
Аллотропия-явление, при котором один химический элемент может
образовать несколько простых веществ.
9.
Аллотропныевидоизменения
кремния
10.
Кремний аморфныйКремний кристаллический
11.
Аллотропныевидоизменения
углерода
12.
13.
Фуллерен – это материальная частица с размеромоколо трети нанометра (трети миллионной доли
миллиметра). Фуллерены представляют собой
замкнутые молекулы углерода, в которых все атомы
расположены в вершинах правильных
шестиугольников или пятиугольников,
покрывающих поверхность сферы или сфероида.
14.
фу
л
л
е
р
е
н
15.
• Для измерения твердости алмазов и алмазныхпленок.
• Фуллерены также широко исследуются как
материалы для электроннооптической области
применения.
• Фуллерены и соединения на их основе также
являются
• перспективными материалами для создания
наноструктур.
16.
Так, фуллереновые плёнки могут бытьиспользованы для создания двумерных
фотонных кристаллов. Причем оптические
свойства фуллереновых пленок(оптика)
можно изменять за счет введения в них добавок
полупроводниковых материалов
17.
Углеродные нанотрубки — полые продолговатые цилиндрическиеструктуры диаметром порядка от единиц до десятков нанометров
(длина традиционных нанотрубок исчисляется микронами, хотя в
лабораториях уже получают структуры длиной порядка миллиметров
и даже сантиметров)
18.
• Особенностью углеродных нанотрубок является ихэлектропроводность, которая оказалась выше, чем у всех
известных проводников.
• Они также имеют прекрасную теплопроводность, стабильны
химически и, что самое интересное, могут приобретать
полупроводниковые свойства.
По электронным свойствам углеродные нанотрубки могут вести
себя как металлы, либо как полупроводники
19.
Как сообщает сайт Nano Technology World, новаятехнология позволит создавать очень тонкую
электронную бумагу. Благодаря высокой прочности
нанотрубок и чрезвычайно малой толщине
матрицы электродов
20.
• Кстати, углеродные нанотрубки не только имеютлучшую по сравнению с металлами проводимость,
но и могут играть роль полупроводников.
Таким образом, реальной видится возможность в
будущем полностью вытеснить кремний в
процессорах и других микросхемах и создавать
чипы, сделанные целиком из углеродных
нанотрубок.
21.
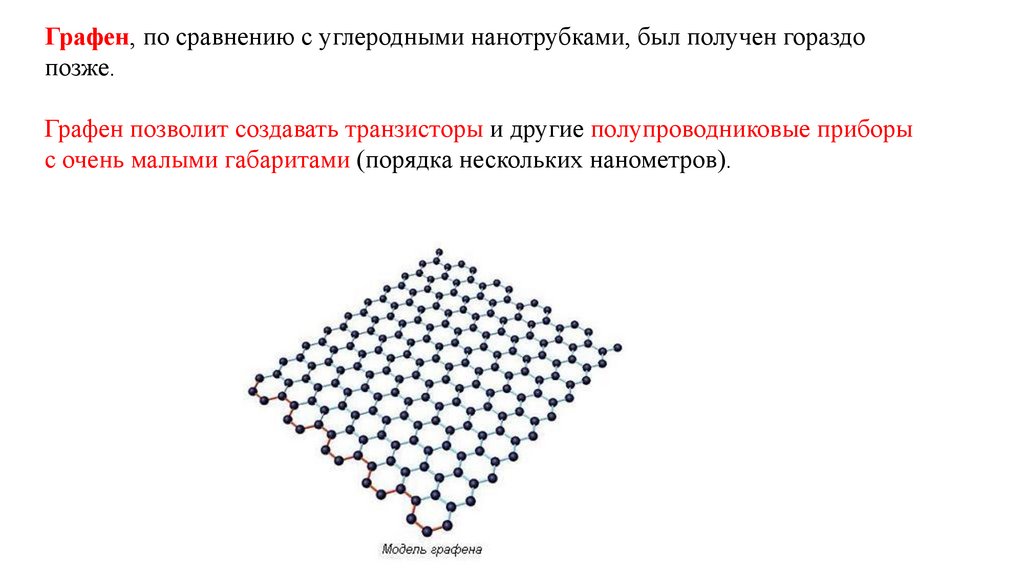
Графен, по сравнению с углеродными нанотрубками, был получен гораздопозже.
Графен позволит создавать транзисторы и другие полупроводниковые приборы
с очень малыми габаритами (порядка нескольких нанометров).
22.
23.
24.
25.
Э-1.Актуализация знаний об особенностях положения неметаллов в Периодической системеД. И. Менделеева.
1.Какие свойства проявляют неметаллы?
2. Как окислительные свойства элементов
изменяются по группе и по периоду?
26.
Э-2.Неметаллы.Неметаллы характеризуются большим многообразием
свойств. Неметаллы имеют различное агрегатное состояние
при обычных условиях:
Газы – Н2, О2, О3, N2, F2, Cl2.
Жидкости – Br2.
Твердые вещества – модификации серы, фосфора, углерода и т.д.
У неметаллов гораздо богаче спектр цветов: красный – у
фосфора, брома , желтый – у серы, желто-зеленый – у
хлора, фиолетовый – у паров йода и т.д.
Элементы – неметаллы способны к аллотропии.
Аллотропия может быть обусловлена разным составом
(нап. О2 и О3) и с разным строением кристаллов (нап.
графит, алмаз )
27.
Ряд электроотрицательностинеметаллов
B, H, As, I, Si, P, Se, C, S, Br, Cl, N, O, F
28.
29.
IV. Подведение итоговДомашнее задание: § 11, выполнить задания № 1—4 после
§ 11


























 chemistry
chemistry








