Similar presentations:
13. Секвенирование ДНК
1.
Секвенирование ДНК.Методы геномики,
транскриптомики,
протеомики
2.
История и значениесеквенирования ДНК и
омных методов
Первое секвенирование ДНК в 1977
году дало толчок к развитию
геномики. Современные технологии,
включая RNA-Seq и массспектрометрию, расширили изучение
генов и белков, укрепив основы
молекулярной биологии.
2
3.
Основные методы секвенирования ДНКМетод Сэнгера и секвенирование
следующего поколения
Метод Сэнгера обеспечивает точное чтение
коротких ДНК-фрагментов. NGS позволяет
параллельно секвенировать миллионы
фрагментов, быстро генерируя большие
объемы данных.
Технологии третьего поколения и процесс
анализа
Современные технологии позволяют считывать
длинные фрагменты ДНК в реальном времени.
Процесс включает несколько этапов: выделение
ДНК, подготовку библиотеки, непосредственное
чтение и последующую обработку данных с
помощью биоинформатического анализа.
3
4.
Сравнительная таблица методов секвенирования ДНКОсновные характеристики
методов: точность, длина
чтения, скорость, стоимость и
области применения.
Выбор метода зависит от целей
исследования и нужного
баланса точности, объема,
скорости и затрат.
4
5.
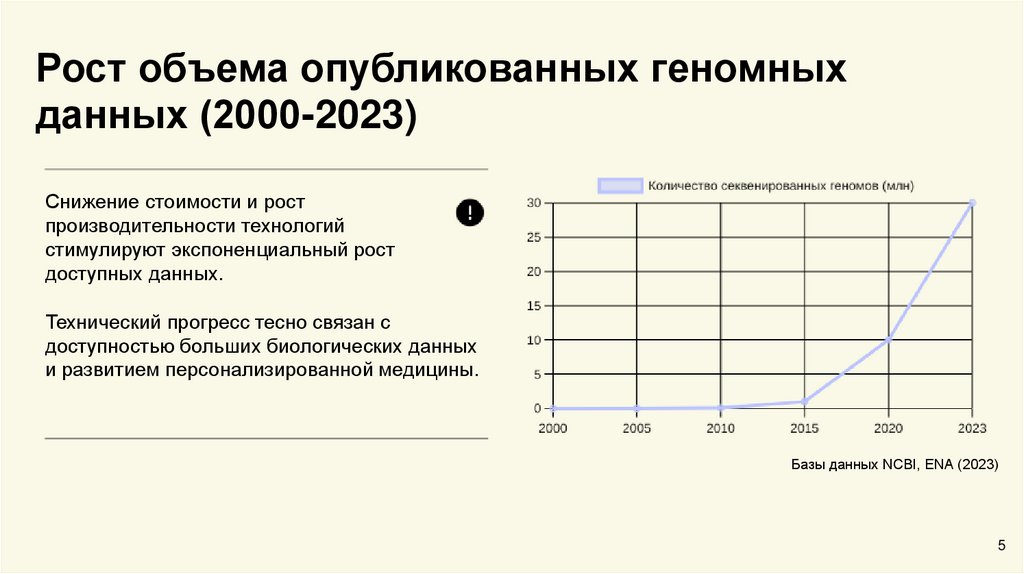
Рост объема опубликованных геномныхданных (2000-2023)
Снижение стоимости и рост
производительности технологий
стимулируют экспоненциальный рост
доступных данных.
Технический прогресс тесно связан с
доступностью больших биологических данных
и развитием персонализированной медицины.
Базы данных NCBI, ENA (2023)
5
6.
Основы транскриптомики: что и как изучаютТранскриптомика изучает весь набор
РНК клеток, отражающий активность
генов и их регуляцию в
разнообразных состояниях
организма.
Методы включают микрочипы и
секвенирование RNA-Seq, дающие
информацию о разнообразии и
количестве транскриптов на
клеточном уровне.
6
7.
Методы анализа транскриптомных данныхКачество данных проверяется и
очищается от ошибок. Затем
последовательности
выравниваются на референсный
геном для точного сопоставления.
Подсчитывается количество
транскриптов, выявляется
дифференциальная экспрессия с
помощью специализированных
программ, что позволяет изучать
генные изменения при различных
состояниях.
7
8.
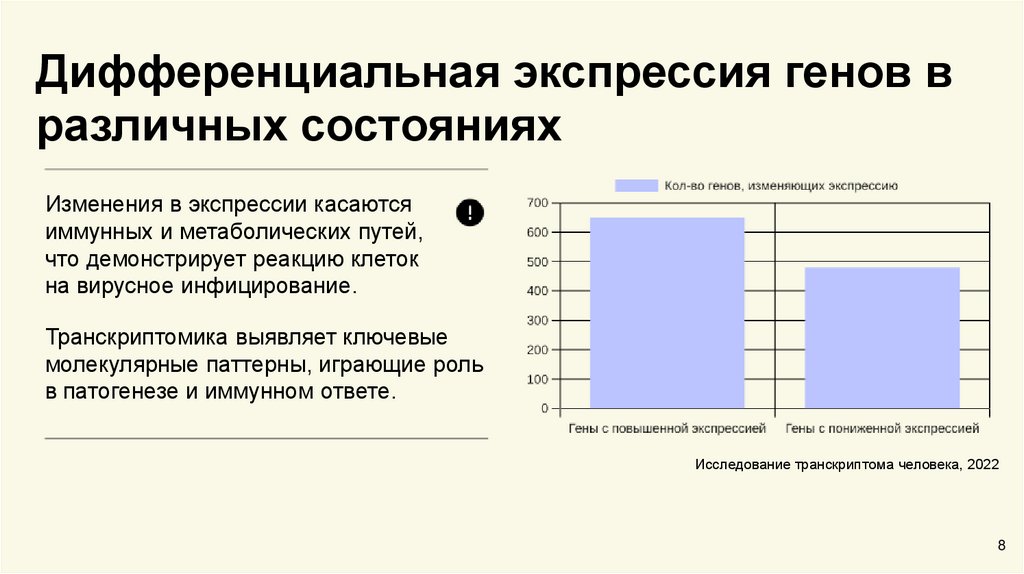
Дифференциальная экспрессия генов вразличных состояниях
Изменения в экспрессии касаются
иммунных и метаболических путей,
что демонстрирует реакцию клеток
на вирусное инфицирование.
Транскриптомика выявляет ключевые
молекулярные паттерны, играющие роль
в патогенезе и иммунном ответе.
Исследование транскриптома человека, 2022
8
9.
Протеомика: изучение белкового состава клеткиОсновы протеомных
исследований
Протеомика анализирует полный набор
белков, их модификации и
взаимодействия, что помогает понять
функциональное состояние клетки.
Методы и задачи протеомики
Применяются масс-спектрометрия,
гель-электрофорез и хроматография
для идентификации биомаркеров и
изучения сигнальных путей в
биологии и медицине.
9
10.
Технологии масс-спектрометрии в протеомикеМасс-спектрометрия с жидкостной
хроматографией (LC-MS/MS)
позволяет расщеплять белки на
пептиды и точно измерять их массу
для качественного и
количественного анализа.
Эта технология служит основой для
профильного исследования
белкового состава, что существенно
повышает понимание клеточных
процессов и биомаркеров
заболеваний.
10
11.
Сравнение характерных методов геномики,транскриптомики и протеомики
Таблица отражает основные
характеристики трёх ключевых омных
технологий: цели, применяемые
технологии, тип выходных данных и
практические области использования.
Каждая методика дополняет другие,
обеспечивая глубокое понимание
биологических процессов на разных
уровнях молекулярной организации.
11
12.
Доля генов, экспрессируемых в разных тканяхчеловека
Особенность мозга и печени —
высокая тканеспецифичность,
отражающая сложные функции и
дифференцированные
биологические процессы.
Различия в экспрессии генов показывают
уникальные биологические роли тканей,
что важно для разработки направленных
терапий.
12
13.
Применение секвенирования и омных методов всовременной медицине
Геномное секвенирование активно
применяется для точного выявления
генетических мутаций, обеспечивая
диагностику наследственных и
онкологических заболеваний. Оно
помогает персонализировать лечение
пациентов.
Транскриптомика и протеомика
способствуют отслеживанию
изменений в экспрессии генов и
белков, что расширяет возможности
для обнаружения новых
терапевтических мишеней и
биомаркеров заболеваний.
13
14.
Будущие направления развития омных технологийИнтеграция ИИ и машинного
обучения
Современные разработки сосредоточены на
применении методов искусственного
интеллекта для глубокого анализа
интегрированных данных генома,
транскриптома и протеома, раскрывая
сложную биологию.
Секвенирование одиночных клеток и
редактирование генома
Технологии одиночных клеток обеспечивают
анализ клеточной гетерогенности, а генное
редактирование с CRISPR создаёт потенциал
для точечных терапий с учётом омных
данных.
14
15.
Заключение: интеграциясеквенирования и омных
исследований в биомедицине
Омные технологии секвенирования обеспечивают
фундаментальные данные для понимания жизненных
процессов и болезней, продвигая эффективные
терапевтические стратегии и персонализированную
медицину.












 biology
biology








