Similar presentations:
Ерітінділер. Дәріс жоспары
1.
ЕРІТІНДІЛЕРКафедра: Молекулалық биология жалпы химия және биохимия курстарымен
medkrmu.kz
2. ДӘРІС ЖОСПАРЫ
ХИМИЯЕРІТІНДІЛЕР
ДӘРІС ЖОСПАРЫ
1) Химиялық эквивалент.
2)Ерітінді жөнінде жалпы түсінік. Ерітінді
түрлері.Ағза тіршілігіндегі ерітінділердің
маңызы.
3)Ерітінділердің концентрациясын өрнектеу
тәсілдері
4)Ерітінділердің коллигативтік қасиеттері
3.
4.
5.
6.
7.
8.
Физикалықтеориясы
XIX
ғасырдың
екінші
жартысында
қалыптасты.
Негізін
салушылар:
С. Арениус
пен Я. ВантГофф
Ерітінділер
жайлы
ілім
Химиялық
теориясы
Д.И
Менделеев
тұсында
қалыптасты.
Негізін
салушылар:
Д.И
Менделеев.
Үлес
қосқандар:
И.А Каблуков
және Н.С
Курнаков
9.
ХИМИЯЕРІТІНДІЛЕР
Ерітінді жөнінде жалпы түсінік. Ерітінді түрлері
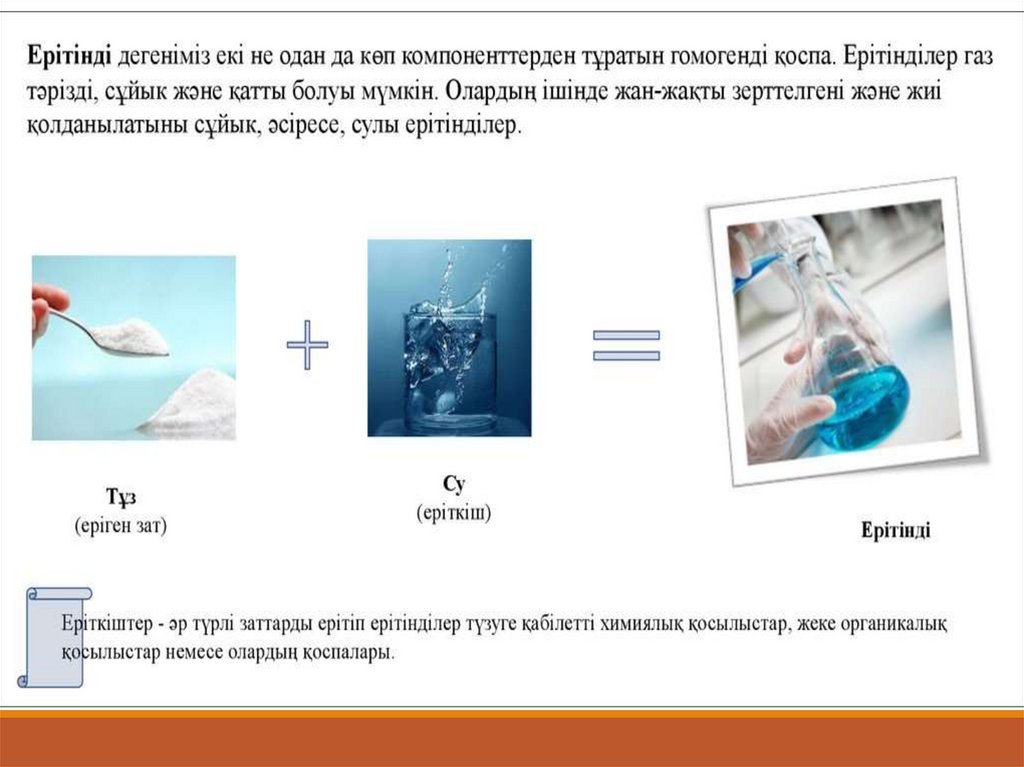
Ерітінділер— кем дегенде екі құрамдас бөліктерден тұратын құрамы
өзгермелі гомогенді (біртекті) жүйелер. Әрбір ерітінді еріген зат пен ерітіндіден
тұрады. Ерітінділер газ тәрізді, сұйық және қатты болуы мүмкін. Олардың ішінде жанжақты зерттелгені және жиі қолданылатыны сұйық, әсіресе, сулы ерітінділер.
Сондықтан тұрмыста ерітінділер деп, көбінесе, сұйық күйдегі молекуладисперстік жүйелерді айтады. Араласатын заттың және агрегаттық күйіне қарай
дисперсті жүйенің 9 түрі болады.
1) г-г мысалы: ауа;
2) с-г тұман (ауадағы тамшы)
3) қ-г
түтін
4) г-с
судағы ауа яғни газды су
5) с-с
судағы спирт ерітіндісі
6) қ-с
судағы тұз ерітіндісі
7) г-қ
катализатор, Pt, Pd сияқты металдардағы Н2
8) с-қ
ылғал болған қатты зат
9) қ-қ
құймалар
10.
11.
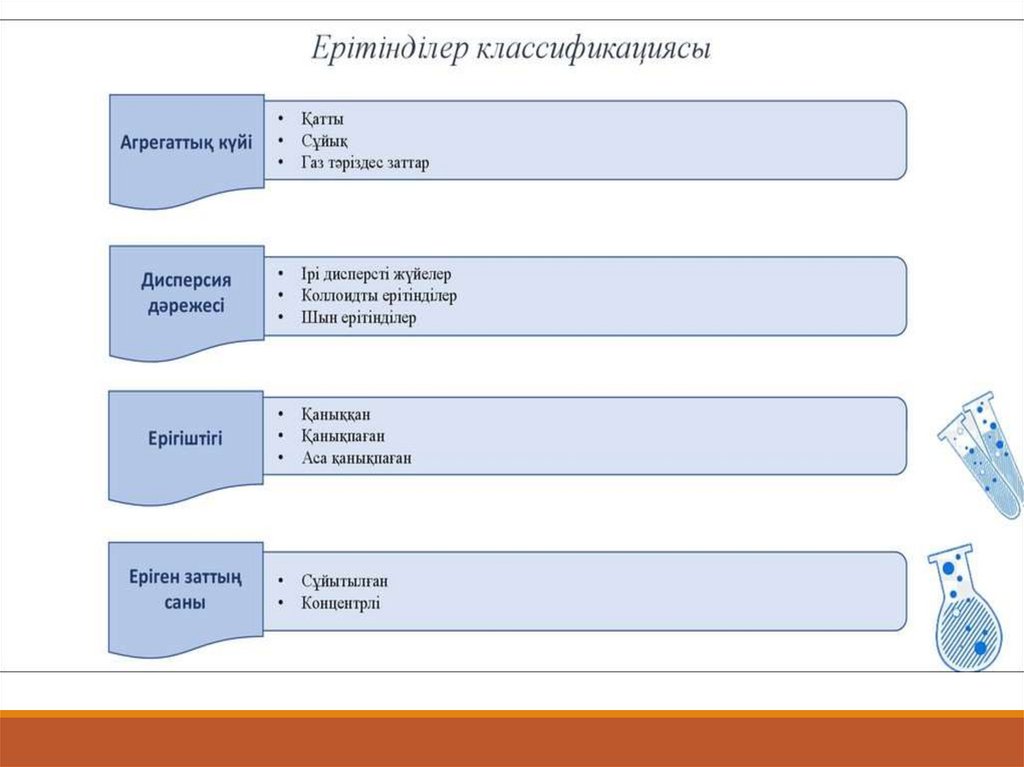
Дисперсті жүйелерді араласатын заттыңұсатылған бөлшегіне қарай үш түрге
бөлеміз.
Жүзгіндер-бөлшектердің мөлшері 100нмден үлкен болса;
Коллоид-1-100нм арасында болса;
Шын немесе молекулалық-1нм-ден кіші
болса
12.
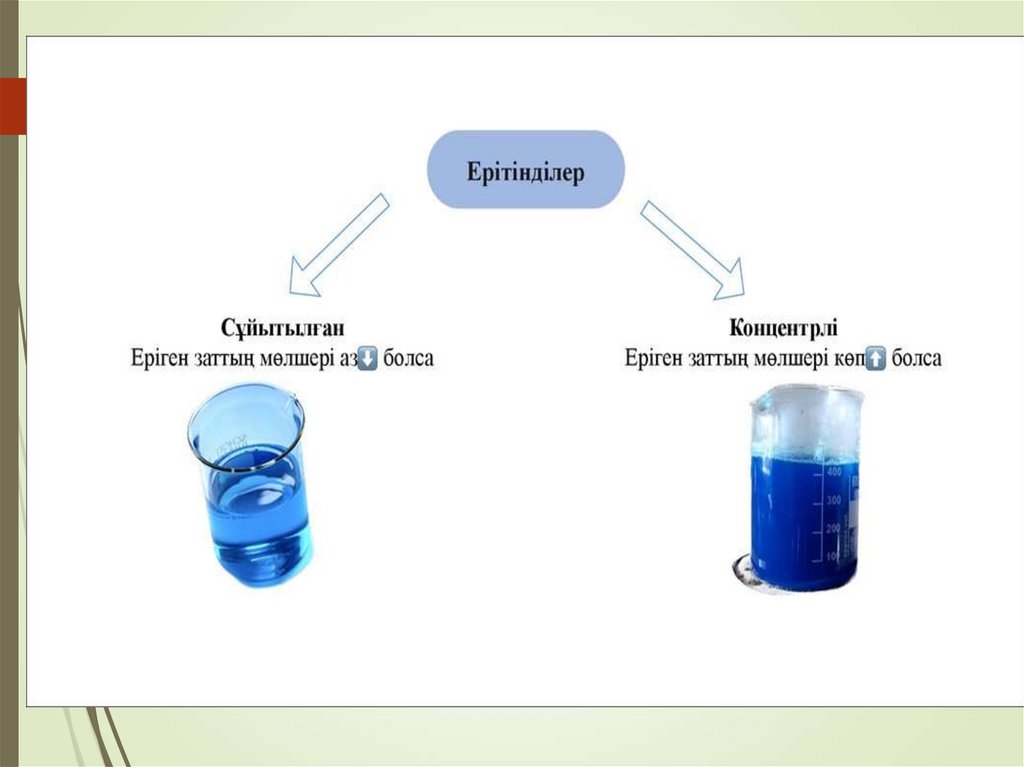
Ерітінділердің еріген заттың мөлшері бойынша жіктелуі:13.
14.
Ерітінділер туралы ілімнің дәрігерлер үшін ерекше мәнібар, себебі негізгі биологиялық сұйықтар –қан плазмасы,
жұлын сұйықтығы, лимфа, несеп, тер, сілекей, судағы
тұздар, көмірсутектер, липидтер тірі ағзада ерітінділер
күйінде болады.
Дәрілік заттар тек ерітінді немесе ағзада еріген күйге
көшкен кезде ғана пайдалы
15.
Медицина үшін ең маңыздысы – сұйық ерітінділер. Тіріағзаның массасы 50-90% судан тұрады.
Су тіршілік процестерінде, атап айтқанда ісіну, осмос т.б.
белсенді роль атқарады, қанда және ұлпаларда онкостық
қысымның белгілі бір шамасын құрайды;
Онкостық қысым (грек. onkos – көлем, масса) – ерітіндідегі
жоғары молекулалы құрамалардың әсерімен түзілген осмостық
қысымның бір бөлігі.Онкостық қысым адамның қан
плазмасындағы осмостық қысымның 0,5%-ын ғана құрайды,
яғни оның мөлшері 25 – 30 мм сын. бағ-на тең Қоректік
заттарды сіңіру, ыдырау өнімдерін бөлу, клеткааралық
сұйықтықты түзу процестері Онкостық қысым арқылы
реттеледі.
Адам ағзасы 20% суды жоғалтқанда жасушаларда болатын
қайтымсыз өзгерістердің нәтижесінде адам қазаға ұшырайды.
16. Ерігіштік
Еру жылуы — заттың бір молі ерігенде бөлінетін несіңірілетін жылу мөлшері (кДж/моль).
Еру жылуы заттың агрегаттық күйіне
тәуелді. Газдар, мыс, аммиак, хлорсутек, т.б. ерігенде
жылу бөлінеді. Ал қатты заттар ерігенде кристалдық
торды бұзу үшін энергия жұмсалып, сырттан жылу
сіңіріледі (эндотермиялық процесс, dH>0).
Кристалдық тордан үзіліп шыққан бөлшектер
еріткішпен әрекеттескенде жылу бөлінеді
(экзотермиялық процесс, dH<0). Ерігенде жылу
сіңірілсе Еру жылуының мәні теріс, ал бөлінсе оң
болады.
17.
Еру өздігінен жүретін үдеріс, олай болса, жүйеніңГиббс энергиясы кішірейеді, яғни ΔGеру<0. Бұл
шамаға энтальпиялық және энтропиялық фактор
әсер етеді. Еру кезінде жүйенің ретсіздік
дәрежесінің артуына байланысты ΔSеру>0 болады.
1 моль зат ерігенде байқалатын термодинамикалық
функциялар өзгерістерін еру энтальпиясы,
энтропиясы деп атайды.
Gеру H еру Т Sеру
а) ΔНеру<0 болғанда, ΔS>0 болуына байланысты, еру өздігінен
жүреді, ΔGеру<0;
ә) ΔНеру>0 болғанда, мына теңсіздік орындалуы шарт: Н T S
олай болса, ΔG<0 болуы үшін температура жоғары болуы қажет.
18.
19.
20.
21.
22.
23.
24.
25. Ерітінділердің коллигативтік қасиеттері
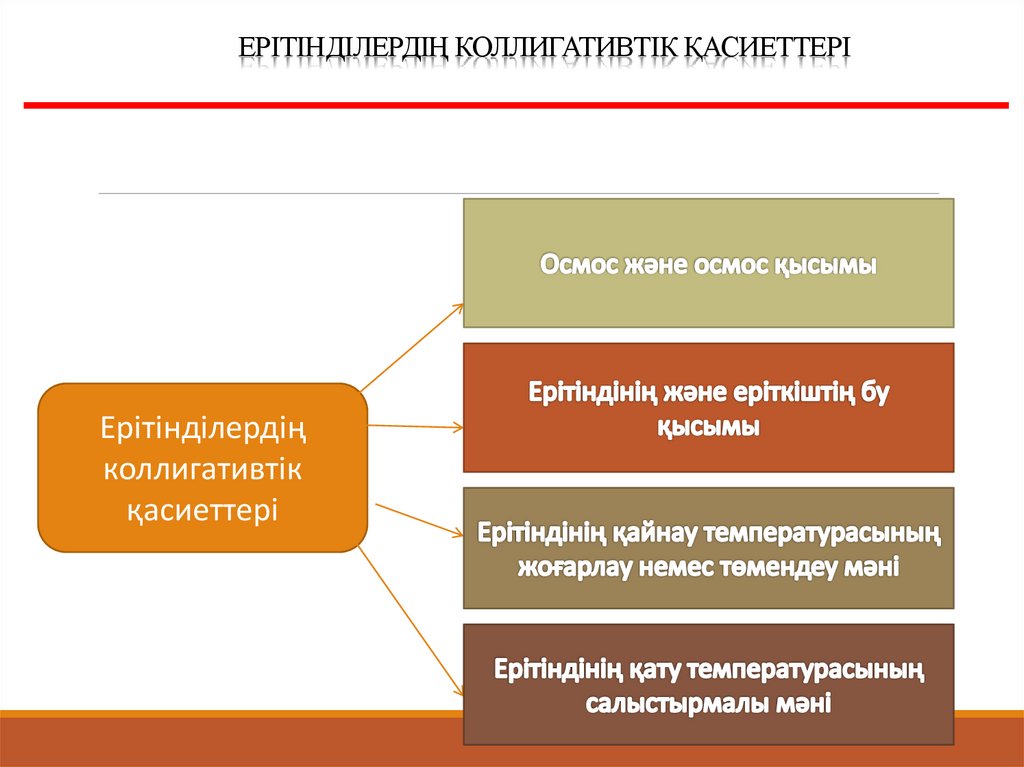
ЕРІТІНДІЛЕРДІҢ КОЛЛИГАТИВТІК ҚАСИЕТТЕРІЕрітінділердің
коллигативтік
қасиеттері
26. Ерітінділердің коллигативті қасиеттері
27.
Ерітіндінің қасиеттеріБір зат екінші затқа ерігенде ерігіштіктің де еріген
заттыңда қасиеттерінде өзгеріс болады. Еріткіштің
өзгеруден тұратын жаңа қасиеттері барлық ерітіндіге
ортақ қасиет болып табылады Мұндай жаңа қасиеттерден
Біз: осмос, ерітінділер буының қысымы, ерітінділердің
қату және қайнау температураларымен танысамыз.
Ерітіндінің осмос қысымы, сол еріген зат газ күйінде
болып , осы температурада , ерітіндінің көлеміндей
көлем алып тұрғандағы туғызатын қысымына тең
(Вант-Гофф заңы)
Еріген зат, ерітіндінің қату температурасын
төмендетіп, қайнау температурасын жоғарылатады.
28.
29.
30.
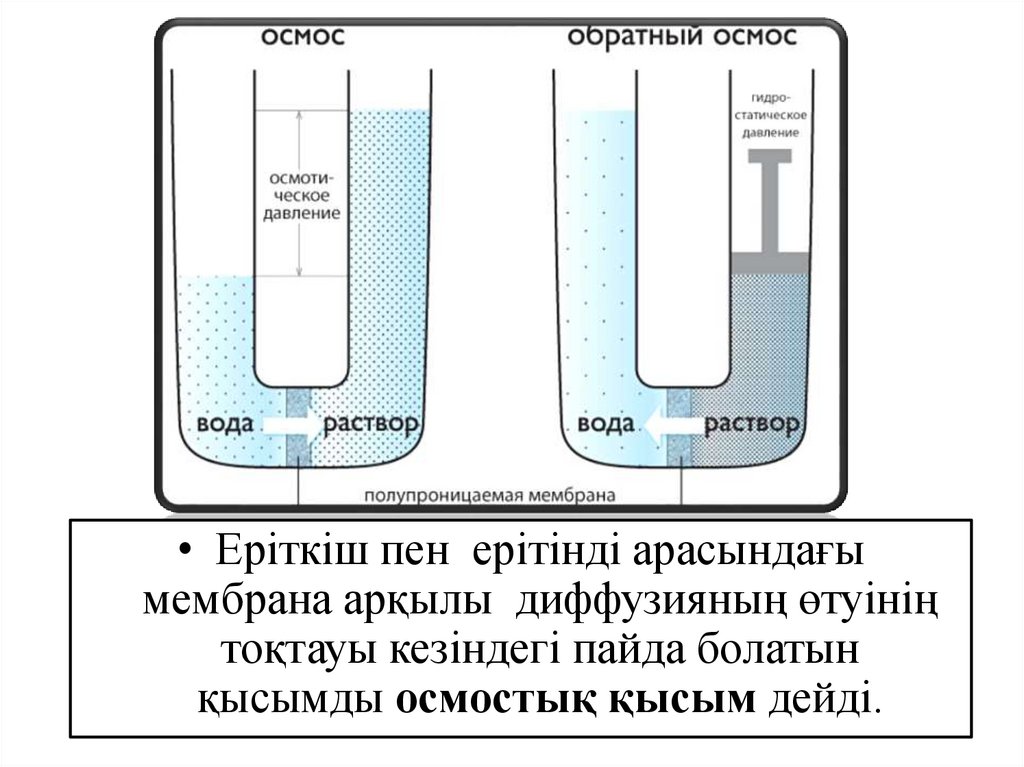
• Еріткіш пен ерітінді арасындағымембрана арқылы диффузияның өтуінің
тоқтауы кезіндегі пайда болатын
қысымды осмостық қысым дейді.
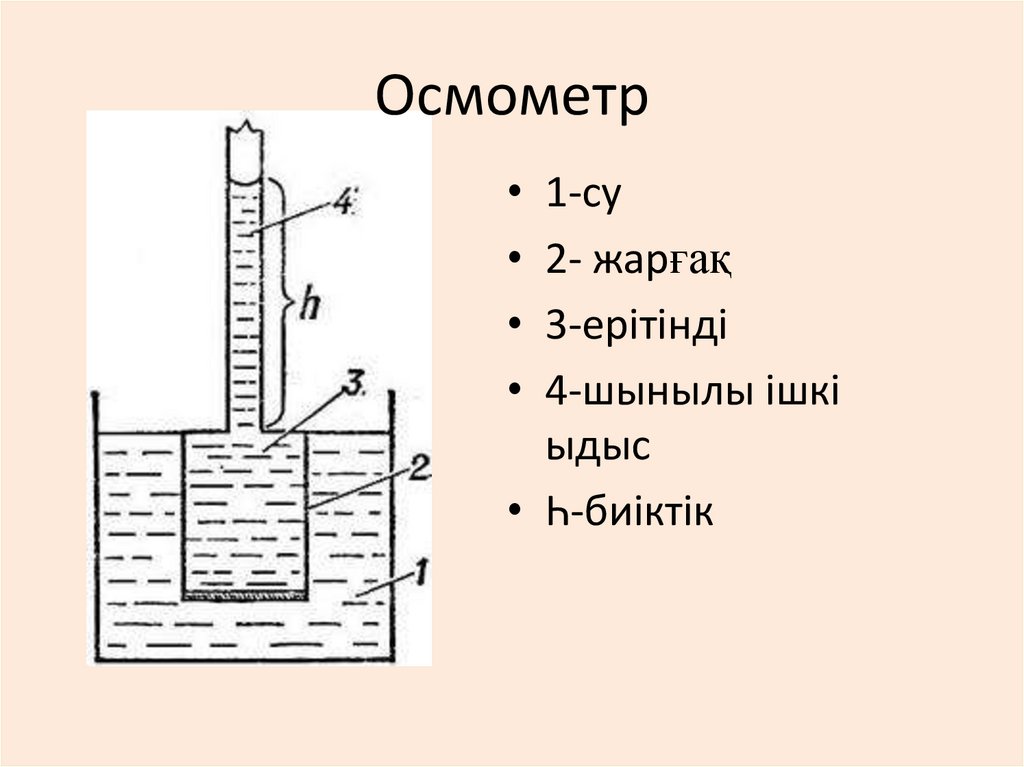
31. Осмометр
• 1-су• 2- жарғақ
• 3-ерітінді
• 4-шынылы ішкі
ыдыс
• Һ-биіктік
32.
33.
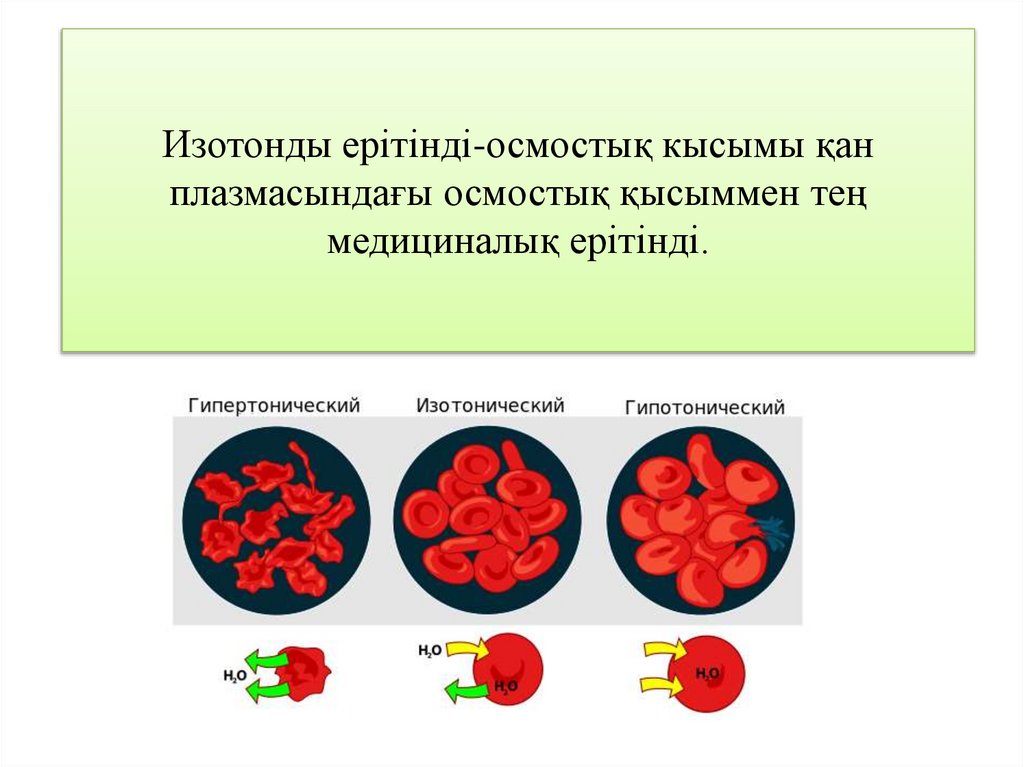
34. Изотонды ерітінді-осмостық кысымы қан плазмасындағы осмостық қысыммен тең медициналық ерітінді.
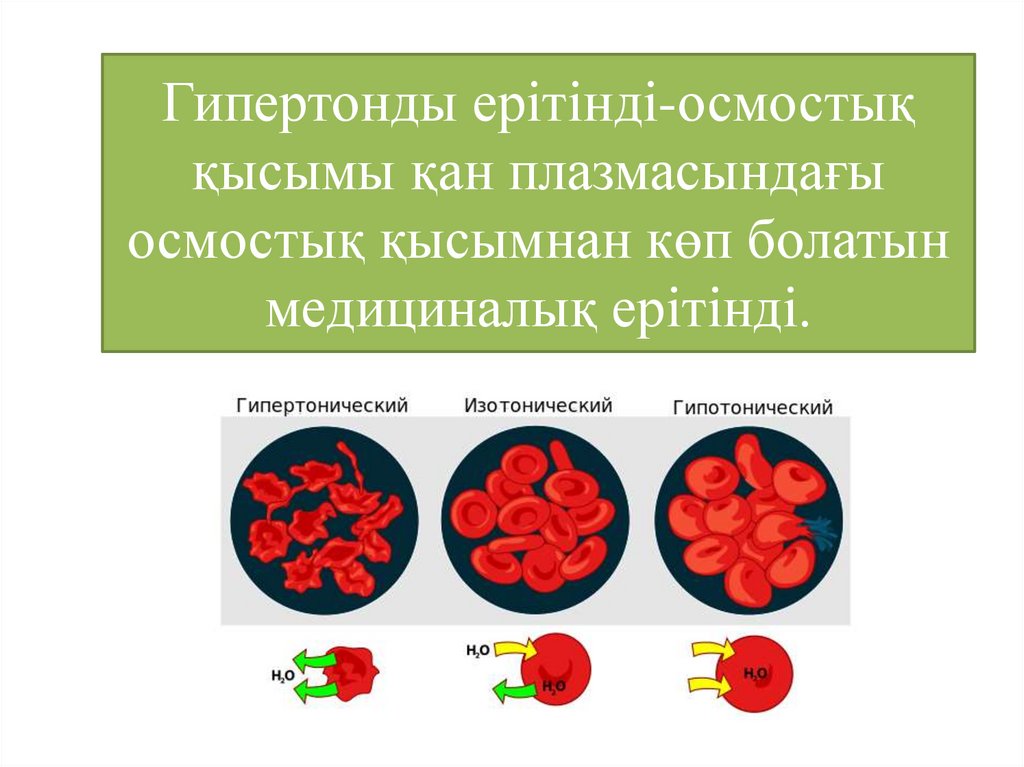
35. Гипертонды ерітінді-осмостық қысымы қан плазмасындағы осмостық қысымнан көп болатын медициналық ерітінді.
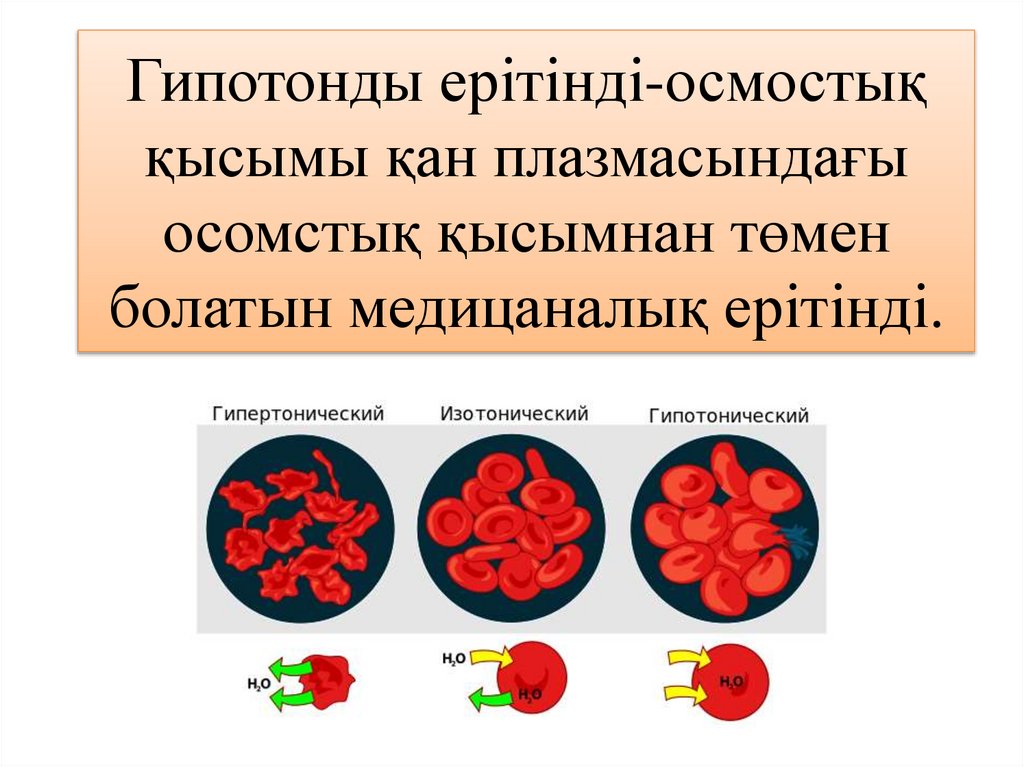
36. Гипотонды ерітінді-осмостық қысымы қан плазмасындағы осомстық қысымнан төмен болатын медицаналық ерітінді.
37. Егер клетка ішіндегі ерітілген заттың концентрациясы клетка сыртындағы сұйықтікінен жоғары болса,онда судан клетка ішінде осмос
жүретінболады,эритроциттер
ісінеді,үлкейеді осының
нәтижесінде қабықша
жыртылады.Бұл құбылыс
ГЕМОЛИЗ деп аталады.
38. Осмос қысымы
• Алғаш рет Вант-Гофф сұйытылған ерітінділердің осмос қысымы ерігензаттың концентрациясына және температураға байланысты екенің
анықтап және оның идеал газға бағынатынын, яғни МенделеевКлапейрон теңдеуі арқылы табуға болатынын анықтады
pV=nRT
• мұндағы P-осмос қысымы, V-ерітіндінің көлемі,
• n-еріген заттың мольдік саны
• R-газ тұрақтысы,
T-абсолютті температура.
Келтірілген теңдеуден осмос қысымын табамыз:
P=nRT/V
Осмосты тоқтататын ерітіндіге сырттан түсіретін қосымша қысымы
осмос қысымы деп аталады. Ерітіндінің осмос қысымы еріген зат сол
температурада газ күйінде болып, ерітіндінің көлеміндей көлем алып
тұрғанда туғызатын қысымына тең. Осмос-еріткіштің өздігінен шала
өткізгіш арқылы сұйық ерітіндіден қою ерітіндіге ауысуы.
39. Ерітінділердің қайнауы мен қатуы
• Ерітінді қату үшін оның бетіндегі еріткіштің қаныққанбу қысымы сәйкес қатты фазаның қысымына тең
болуы керек.Таза еріткіш пен қату температурасының
айырмасын ерітіндінің қату температурасының
төмендеуі
дейді.Ерітіндінің
қайнау
температурасының
жоғарлауы
мен
қату
температурасының
төмендеуі
еріген
заттың
концентрациясына
тура
пропроционалды
тәуелділікте болады.
• Раульдің екінші заңының математикалық өрнегі
мынадай: t=E xC
• E=еріткіштің
эбулиоскопиялық
константантасы,
К=еріткіштің криоскопиялық константасы,
• С=ерітіндінің молярлық концентрациясы
40.
Ерітінділердің қайнаутемпературасының
жоғарылауы
Ерітінді таза еріткішке қарағанда жоғары
температурада қайнайды. Қайнау
температурасының жоғарылауы қаныққан бу
қысымының кемуіне тура тәуелді.
Δtқайнау= Е . Cm
Е-эбуллиоскопиялық тұрақтылық.
Сан мәні (су үшін) 0,51-ға тең.
41.
Қату температурасыныңтөмендеуі
Ерітінді таза еріткішке қарағанда төменірек
температурада қатады.
Қату
температурасының төмендеуі ерітіндідегі
еріген заттың концентрациясына тәуелді.
Δtқату= K . Cm
K-криоскопиялық тұрақтылық.
Сан мәні
(су үшін) 1,86-ға тең.
42.
43.
44.
Негізгі түсініктердің 3 тілдегі атаулары:1) Ерітінділер-растворы-Solutions
2) Электролиттік диссоциация-электролитическая система-electrolytic dissociation
3) Дисперсті жүйе-дисперстическая система-Dispertion is the system
4) Қатты зат-твердая вещь-hard thing
5) Газ-газ-Gas
6) Сұйық-жидкость-liquid
7) Коллоид ерітінді-коллоидный раствор-colloid solution
8) Еріген зат-растворенное вещество-permeate
9) Қанық ерітінді-Насыщенный раствор-Saturated solution
10) Концентрация-концентрация-concentration


































 chemistry
chemistry








