Similar presentations:
Трансплантация фекальной микробиоты как метод лечения кишечного синдрома различной этиологии у детей
1.
Трансплантация фекальноймикробиоты как метод лечения
кишечного синдрома различной
этиологии у детей
к.б.н. Беспятых Юлия Андреевна
Руководитель ЦММиД, зав лабораторией молекулярной медицины ФГБУ
ФНКЦ ФХМ им. Ю.М. Лопухина ФМБА России
Доцент кафедры экспертизы в допинг- и наркоконтроле
РХТУ ИМ. Д.И. Менделеева
Главный внештатный специалист ФМБА по клинической микробиологии
и антибиотикорезистентности по ЦФО
2. ТРАНСПЛАНТАЦИЯ ФЕКАЛЬНОЙ МИКРОБИОТЫ (ТФМ)
Трансплантациякала
(фекотрансплантация,
фекальная
бактериотерапия) представляет собой
восстановление
нормальной
бактериальной флоры кишечника с
помощью стула, полученного от здорового
донора.
3.
ИСТОРИЯ ТФМКитай, IV век
Китай, XVI век
Eisman, 1958
Anna Schwan, 1983
Врач Гэ Хун использовал
материал фекалий для
пациентов с пищевым
отравлением
Врач Ли Ши Чжен
использовал «Желтый» или
«золотой» суп для лечения
ЖКТ
Лечение
псевдомемранозного
энтероколита при помощи
клизм с ФМ
Впервые описана ТФМ
для лечения
клостридиальной инфекции
4.
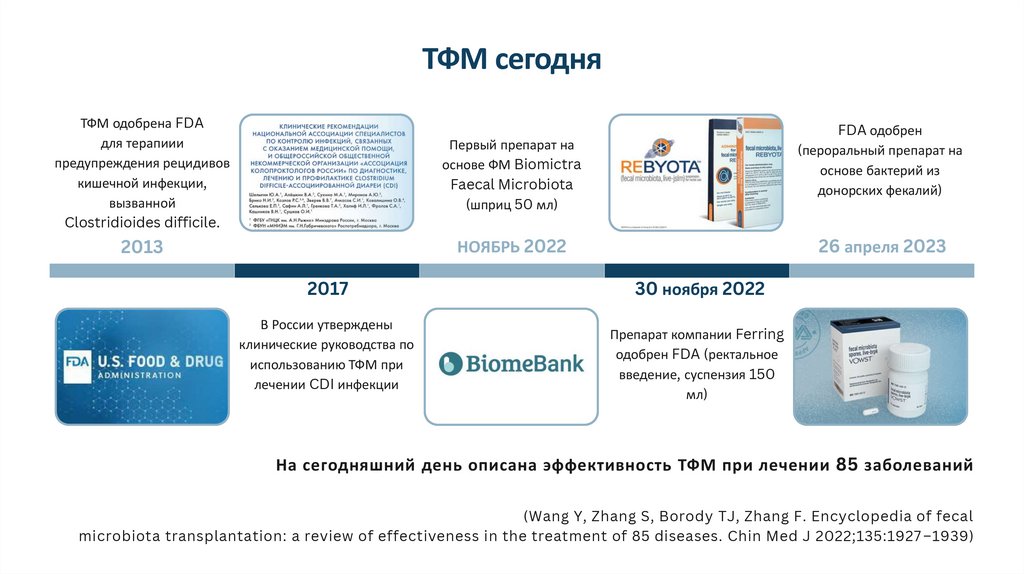
ТФМ сегодняТФМ одобрена FDA
для терапиии
предупреждения рецидивов
кишечной инфекции,
вызванной
Clostridioides difficile.
Первый препарат на
основе ФМ Biomictra
Faecal Microbiota
(шприц 50 мл)
2013
НОЯБРЬ 2022
FDA одобрен
(пероральный препарат на
основе бактерий из
донорских фекалий)
26 апреля 2023
2017
30 ноября 2022
В России утверждены
клинические руководства по
использованию ТФМ при
лечении CDI инфекции
Препарат компании Ferring
одобрен FDA (ректальное
введение, суспензия 150
мл)
На сегодняшний день описана эффективность ТФМ при лечении 85 заболеваний
(Wang Y, Zhang S, Borody TJ, Zhang F. Encyclopedia of fecal
microbiota transplantation: a review of effectiveness in the treatment of 85 diseases. Chin Med J 2022;135:1927 –1939)
5.
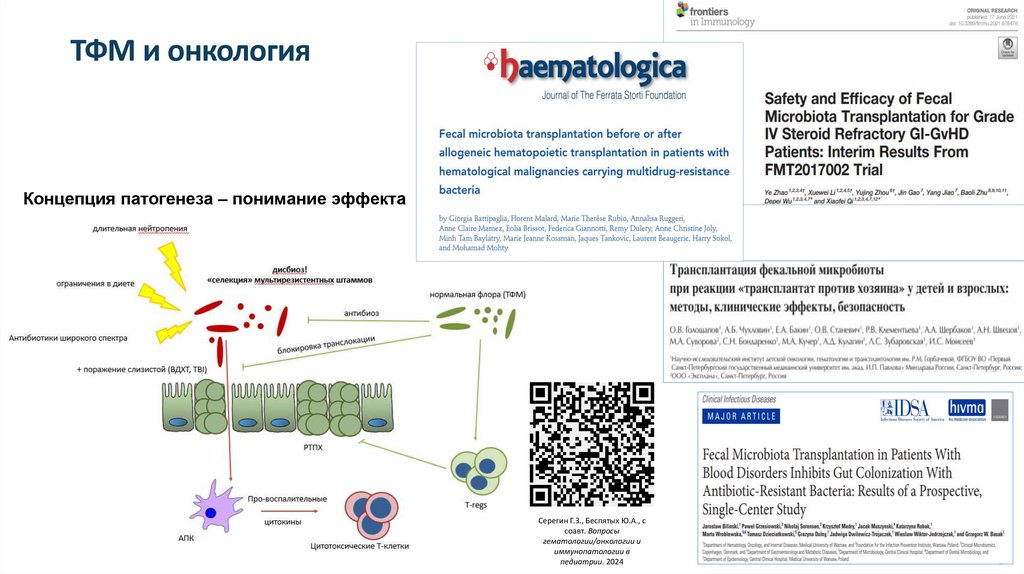
ТФМ и онкологияКонцепция патогенеза – понимание эффекта
Серегин Г.З., Беспятых Ю.А., с
соавт. Вопросы
гематологии/онкологии и
иммунопатологии в
педиатрии. 2024
5
6.
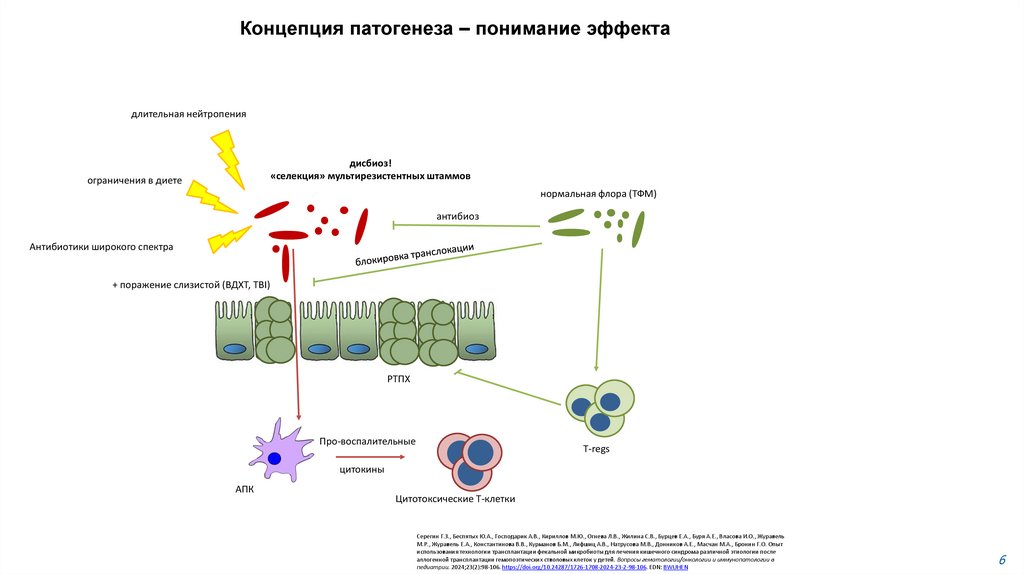
Концепция патогенеза – понимание эффектадлительная нейтропения
дисбиоз!
«селекция» мультирезистентных штаммов
ограничения в диете
нормальная флора (ТФМ)
антибиоз
Антибиотики широкого спектра
+ поражение слизистой (ВДХТ, TBI)
РТПХ
Про-воспалительные
T-regs
цитокины
АПК
Цитотоксические Т-клетки
Серегин Г.З., Беспятых Ю.А., Господарик А.В., Кириллов М.Ю., Огнева Л.В., Жилина С.В., Бурцев Е.А., Буря А.Е., Власова И.О., Журавель
М.Р., Журавель Е.А., Константинова В.В., Курманов Б.М., Лифшиц А.В., Натрусова М.В., Донников А.Е., Масчан М.А., Бронин Г.О. Опыт
использования технологии трансплантации фекальной микробиоты для лечения кишечного синдрома различной этиологии после
аллогенной трансплантации гемопоэтических стволовых клеток у детей. Вопросы гематологии/онкологии и иммунопатологии в
педиатрии. 2024;23(2):98-106. https://doi.org/10.24287/1726-1708-2024-23-2-98-106. EDN: BWUHEN
6
7. ТРАНСПЛАНТАЦИЯ ФЕКАЛЬНОЙ МИКРОБИОТЫ У РЕЦИПИЕНТОВ АЛЛОГЕННОЙ ТРАНСПЛАНТАЦИИ КОСТНОГО МОЗГА И ГЕМОПОЭТИЧЕСКИХ СТВОЛОВЫХ КЛЕТОК
Цель исследования:Профилактика и терапия различных желудочно-кишечных осложнений у пациентов
от 3 до 18 лет после аллогенной трансплантации костного мозга методом трансплантации фекальной
микробиоты.
7
8.
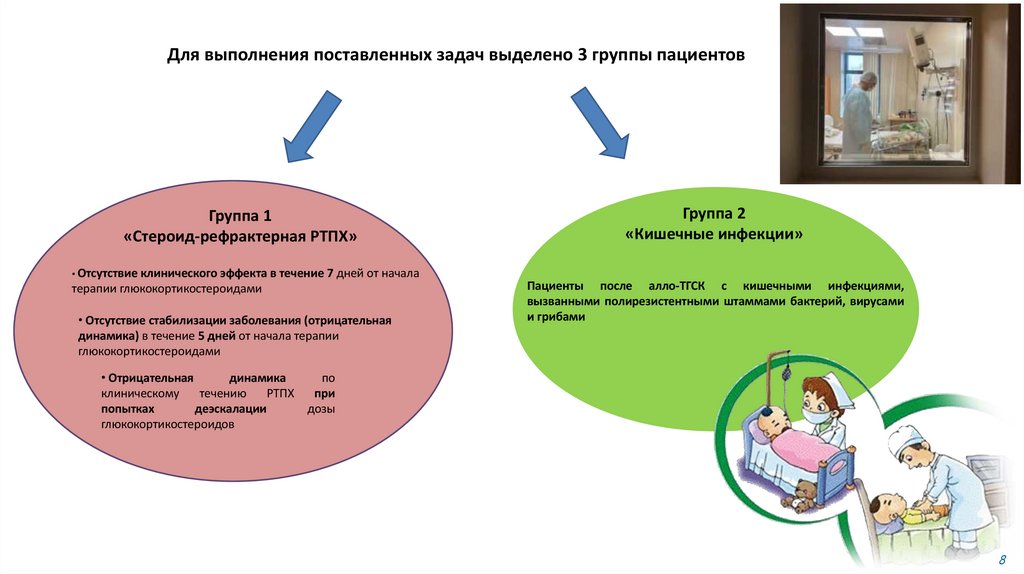
Для выполнения поставленных задач выделено 3 группы пациентовГруппа 1
«Стероид-рефрактерная РТПХ»
• Отсутствие клинического эффекта в течение 7 дней от начала
терапии глюкокортикостероидами
• Отсутствие стабилизации заболевания (отрицательная
динамика) в течение 5 дней от начала терапии
глюкокортикостероидами
• Отрицательная
динамика
клиническому
течению
РТПХ
попытках
деэскалации
глюкокортикостероидов
Группа 2
«Кишечные инфекции»
Пациенты после алло-ТГСК с кишечными инфекциями,
вызванными полирезистентными штаммами бактерий, вирусами
и грибами
по
при
дозы
8
9. Критерии исключения для проведения ТФМ
Отмена показаний к алло-ТГСКВозраст менее 3 лет;
Дополнение к ЛЭК «менее года»
Отсутствие подписанного информированного согласия
Количество нейтрофилов в общем анализе крови <0,5 тыс/мкл, количество лимфоцитов <0,7 тыс/мкл в день
ТФМ и ожидаемое снижение в течение 2 дней после ТФМ
Ожидаемая необходимость в проведении антибактериальной терапии в течение 7 дней после ТФМ
Антибактериальная терапия, проводимая менее чем за 48 часов до процедуры ТФМ
Эпизоды нестабильной гемодинамики в течение не менее чем 1 недели до процедуры
2024
9
10.
Предварительная подготовка реципиента:•Отмена антибиотиков за 48 ч до ТФМ
•Противорвотная терапия в день ТФМ
•Глюкокортикоиды в день ТФМ
•Метабиотик (Инулин/смеси с высоким содержанием глутамина) за 3 дня до ТФМ
•Уровень гранулоцитов – 0,5 тыс/мкл и более
10
11. МАТЕРИАЛ ДЛЯ ТФМ
Назогастральный зондНазоеюнальный зонд
Перорально
Эндоскопическое введение
Жидкая фракция (25-30 мл)
Клизма
Кишечнорастворимые капсулы с
лиофилизированным материалом
2024
11
12. Проведено ТФМ
С июня 2022 года – 54 пациента (возраст от 1 месяца до 17 лет)• Группа 1 (рефрактерная РТПХ кишечника) – 20 пациентов
• Группа 2 (резистентная микрофлора) – 21 пациент
59 процедур:
Жидкая фракция через назогастральный или назоеюнальный зонд – 9
Перорально Капсулы – 23
Жидкая фракция per rectum – 27
2024
12
13.
Клинический эффектГруппа 1 «Стероид-рефрактерная-РТПХ» 18/26
Клинический
эффект
Сроки достижения
клинического
эффекта (день от
ТФМ)
Лабораторный эффект
(оценка
биоразнообразия)дос
тигнут/не достигнут
Доля нормальной
микробиоты (%) до ТФМ
Доля нормальной
микробиоты (%) после
ТФМ
Таксономическое
разнообразие до ТФМ
(шт.)
Таксономическое
разнообразие после ТФМ
(шт.)
Достигнут у 18/26
пациентов
5 – 21 (медиана –
8)
• 19 – да (ПЦР)
• 2 – нет (посев)
• 5– нет (ПЦР)
0 – 100%
Медиана 6.1%
0 – 99.4%
Медиана 86.5%
0 – 14
Медиана – 3 шт
2 – 15
Медиана – 10 шт
нивелирование диареи,
абдоминального болевого синдрома,
гипоальбуминемии
на фоне отмены стероидов
13
14.
Клинический эффектГруппа 2 «Кишечные инфекции» 12/14
Клинический эффект
Сроки достижения
клинического
эффекта (день от
ТФМ)
Лабораторный эффект
(оценка биоразнообразия)
достигнут/не достигнут
Доля нормальной
микробиоты (%) до
ТФМ
Доля нормальной
микробиоты (%) после
ТФМ
Таксономическое
разнообразие до ТФМ
(шт.)
Таксономическое
разнообразие после ТФМ
(шт.)
Достигнут у 12 из 14
пациентов
3 – 20 (Медиана –
7)
• 7 – да (ПЦР)
• 5 – нет (посев)
• 1 – нет (ПЦР)
• 1 – да (посев)
0 – 98 %
Медиана 5.5%
0,8 - 99,1 %
Медиана 97.1%
1- 9
Медиана 3 шт
4 – 15
Медиана 14 шт
(отсутствие эффекта
после второй ТФМ у
одного пациента,
рецидив ОЛЛ)
нивелирование диареи,
абдоминального болевого синдрома,
гипоальбуминемии
нормализация микробиома
14
15.
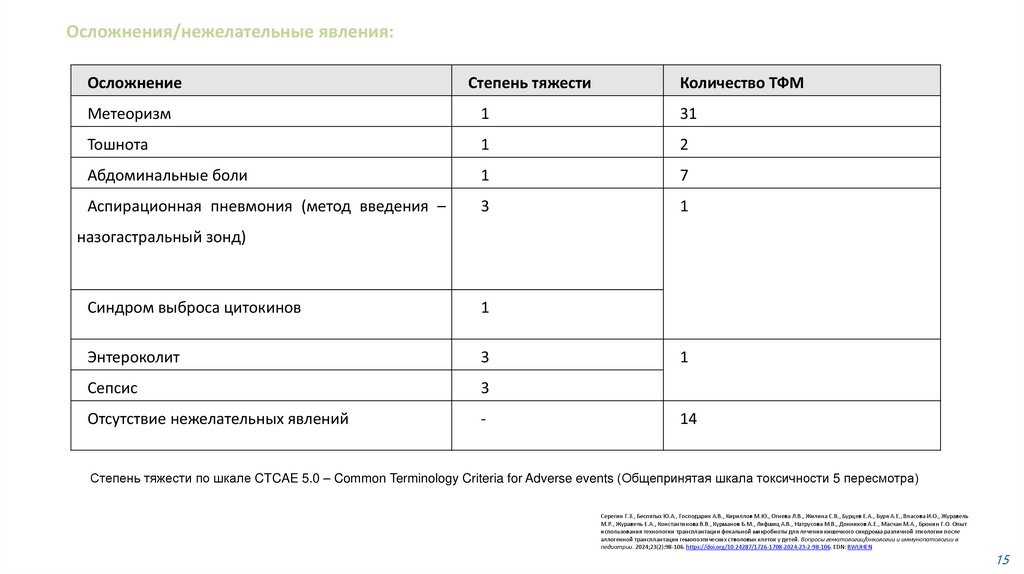
Осложнения/нежелательные явления:Осложнение
Степень тяжести
Количество ТФМ
Метеоризм
1
31
Тошнота
1
2
Абдоминальные боли
1
7
Аспирационная пневмония (метод введения –
3
1
назогастральный зонд)
Синдром выброса цитокинов
1
Энтероколит
3
Сепсис
3
Отсутствие нежелательных явлений
-
1
14
Степень тяжести по шкале CTCAE 5.0 – Common Terminology Criteria for Adverse events (Общепринятая шкала токсичности 5 пересмотра)
Серегин Г.З., Беспятых Ю.А., Господарик А.В., Кириллов М.Ю., Огнева Л.В., Жилина С.В., Бурцев Е.А., Буря А.Е., Власова И.О., Журавель
М.Р., Журавель Е.А., Константинова В.В., Курманов Б.М., Лифшиц А.В., Натрусова М.В., Донников А.Е., Масчан М.А., Бронин Г.О. Опыт
использования технологии трансплантации фекальной микробиоты для лечения кишечного синдрома различной этиологии после
аллогенной трансплантации гемопоэтических стволовых клеток у детей. Вопросы гематологии/онкологии и иммунопатологии в
педиатрии. 2024;23(2):98-106. https://doi.org/10.24287/1726-1708-2024-23-2-98-106. EDN: BWUHEN
15
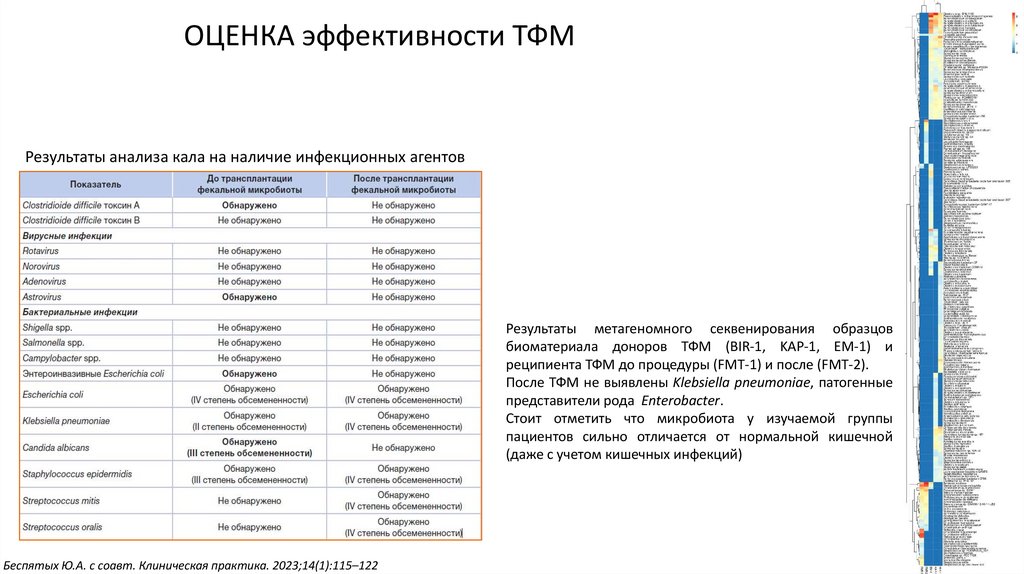
16. ОЦЕНКА эффективности ТФМ
Результаты анализа кала на наличие инфекционных агентовРезультаты метагеномного секвенирования образцов
биоматериала доноров ТФМ (BIR-1, KAP-1, EM-1) и
реципиента ТФМ до процедуры (FMT-1) и после (FMT-2).
После ТФМ не выявлены Klebsiella pneumoniae, патогенные
представители рода Enterobacter.
Стоит отметить что микробиота у изучаемой группы
пациентов сильно отличается от нормальной кишечной
(даже с учетом кишечных инфекций)
Беспятых Ю.А. с соавт. Клиническая практика. 2023;14(1):115–122
16
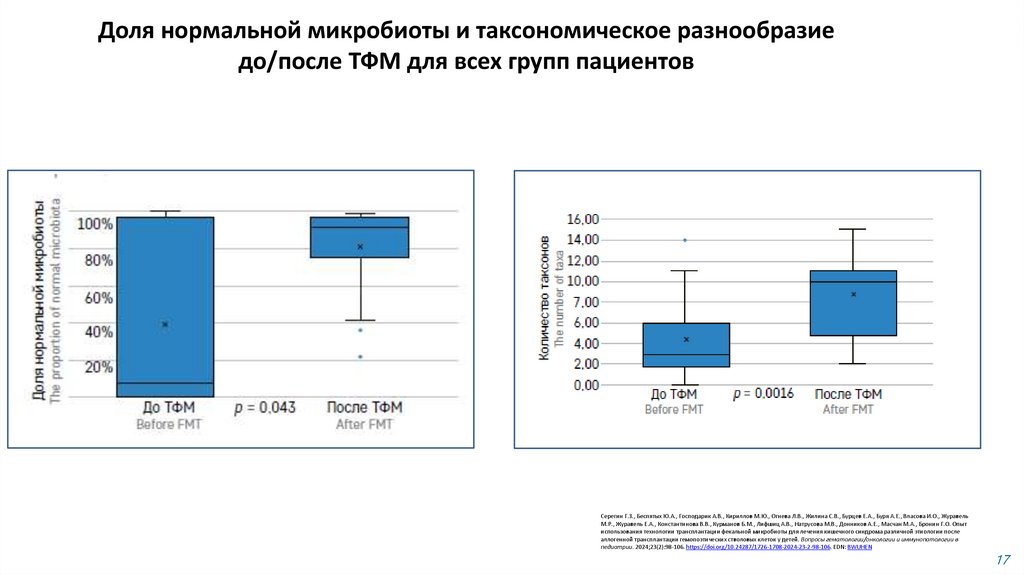
17.
Доля нормальной микробиоты и таксономическое разнообразиедо/после ТФМ для всех групп пациентов
Серегин Г.З., Беспятых Ю.А., Господарик А.В., Кириллов М.Ю., Огнева Л.В., Жилина С.В., Бурцев Е.А., Буря А.Е., Власова И.О., Журавель
М.Р., Журавель Е.А., Константинова В.В., Курманов Б.М., Лифшиц А.В., Натрусова М.В., Донников А.Е., Масчан М.А., Бронин Г.О. Опыт
использования технологии трансплантации фекальной микробиоты для лечения кишечного синдрома различной этиологии после
аллогенной трансплантации гемопоэтических стволовых клеток у детей. Вопросы гематологии/онкологии и иммунопатологии в
педиатрии. 2024;23(2):98-106. https://doi.org/10.24287/1726-1708-2024-23-2-98-106. EDN: BWUHEN
17
18. Общая динамика изменения содержания КЦЖК в стуле
Уровень ацетата, изобутирата, бутирата иобщего содержания КЦЖК показал тенденцию
к росту, что может свидетельствовать о
повышении
представленности
родов
Bifidobacteria,
Ruminococcus,
Bacteroides,
Lachnospira, Fusobacterium и Lactobacillus в
ходе терапии
Значимо увеличился уровень пропионата, что
может говорить о росте представленности
Veillonella, Propionnibacterium, Arachnia,
Anaerovibrio в физиологических границах
нормы
Не отмечалось изменения уровня валерата,
капроната, а также изовалерата, что
свидетельствует об отсутствии избыточного
роста
представителей
Megasphaera,
Clostridium, Coprococcus, Fusobacterium
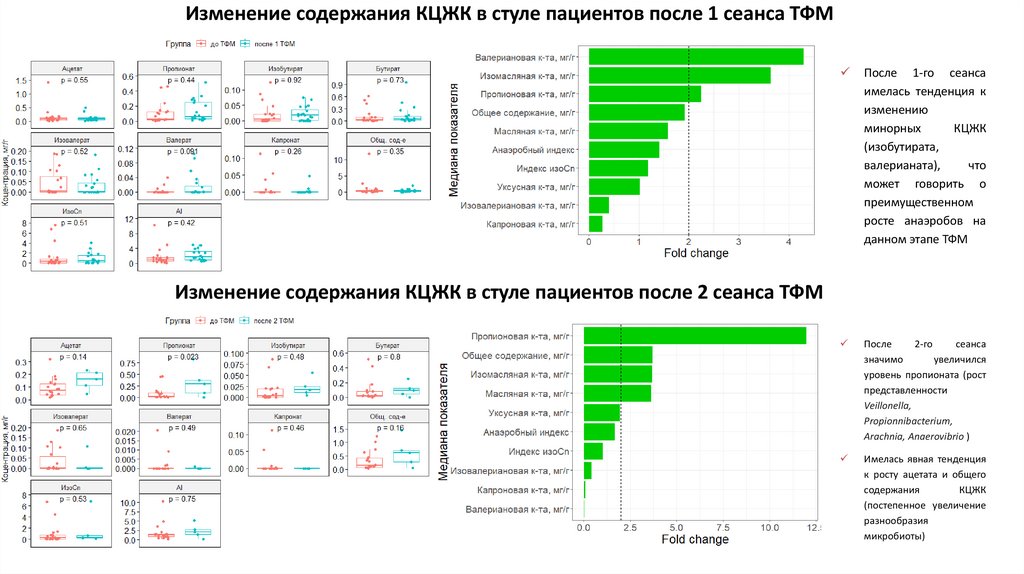
19. Изменение содержания КЦЖК в стуле пациентов после 1 сеанса ТФМ
После 1-го сеансаимелась тенденция к
изменению
минорных
КЦЖК
(изобутирата,
валерианата),
что
может говорить о
преимущественном
росте анаэробов на
данном этапе ТФМ
После
2-го
сеанса
значимо
увеличился
уровень пропионата (рост
представленности
Veillonella,
Propionnibacterium,
Arachnia, Anaerovibrio )
Имелась явная тенденция
к росту ацетата и общего
содержания
КЦЖК
(постепенное увеличение
разнообразия
микробиоты)
Изменение содержания КЦЖК в стуле пациентов после 2 сеанса ТФМ
20. Take-home message
Методы введения в целом равны по эффективности, per rectum и через капсулы видятся более «безопасным»вариантом
Отсутствие эрадикации определенного агента не всегда коррелирует с достижением клинического эффекта
(эффект достигается, патоген персистирует)
Нарушение диеты, «быстрая» отмена базовой ИСТ после достижения эффекта – путь к реактивации кишечного
синдрома
Трансплантация
фекальной
микробиоты
является
многообещающим и безопасным методом терапии реципиентов
алло-ТГСК со «стероид-рефрактерной» желудочно-кишечной
формой
РТПХ
и
инфекционными
желудочно-кишечными
осложнениями после алло-ТГСК
20
21.
1. Методы введения в целом равны по эффективности, per rectum и через капсулывидятся более «безопасным» вариантом;
2. Отсутствие эрадикации определенного агента не всегда коррелирует с достижением
клинического эффекта (эффект достигается, патоген персистирует);
3. Нарушение диеты, «быстрая» отмена базовой ИСТ после достижения эффекта – путь
к реактивации кишечного синдрома;
Собственные данные авторов
21
22.
Серегин Георгий Зурабовичврач-детский онколог
к.м.н., доцент Бронин Глеб Олегович
заведующий отделением, врач-гематолог
Журавель Евгений Андреевич
врач-детский онколог
22













 medicine
medicine








