Similar presentations:
Ионная, ковалентная, водородная, металлическая химические связи (Химия. 8 класс)
1. Ионная, ковалентная, водородная, металлическая химические связи
ИОННАЯ, КОВАЛЕНТНАЯ,ВОДОРОДНАЯ, МЕТАЛЛИЧЕСКАЯ
ХИМИЧЕСКИЕ СВЯЗИ
Химия 8 класс
2. Гипотеза урока
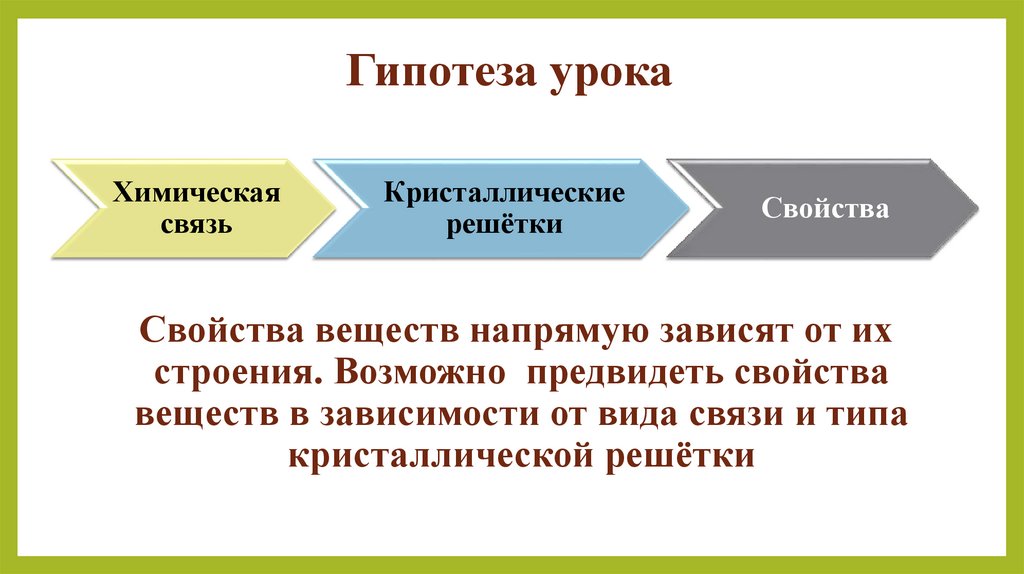
Химическаясвязь
Кристаллические
решётки
Свойства
Свойства веществ напрямую зависят от их
строения. Возможно предвидеть свойства
веществ в зависимости от вида связи и типа
кристаллической решётки
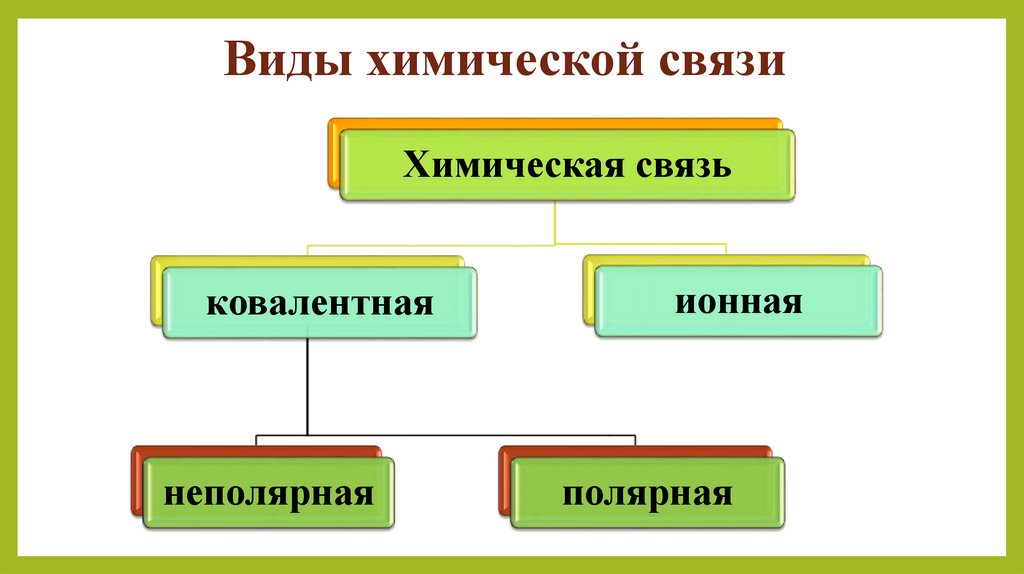
3. Виды химической связи
Химическая связьковалентная
неполярная
ионная
полярная
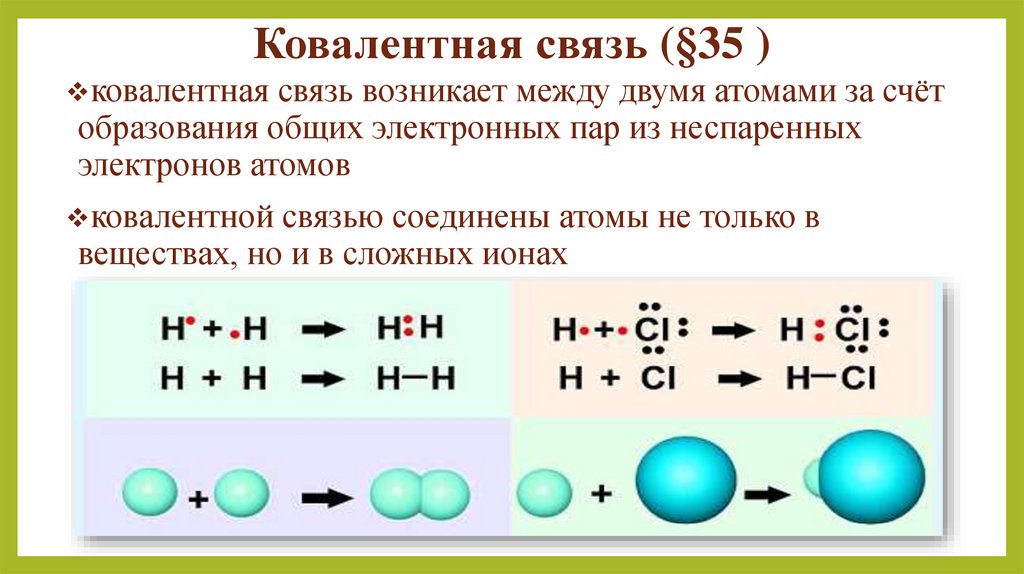
4. Ковалентная связь (§35 )
ковалентная связь возникает между двумя атомами за счётобразования общих электронных пар из неспаренных
электронов атомов
ковалентной связью соединены атомы не только в
веществах, но и в сложных ионах
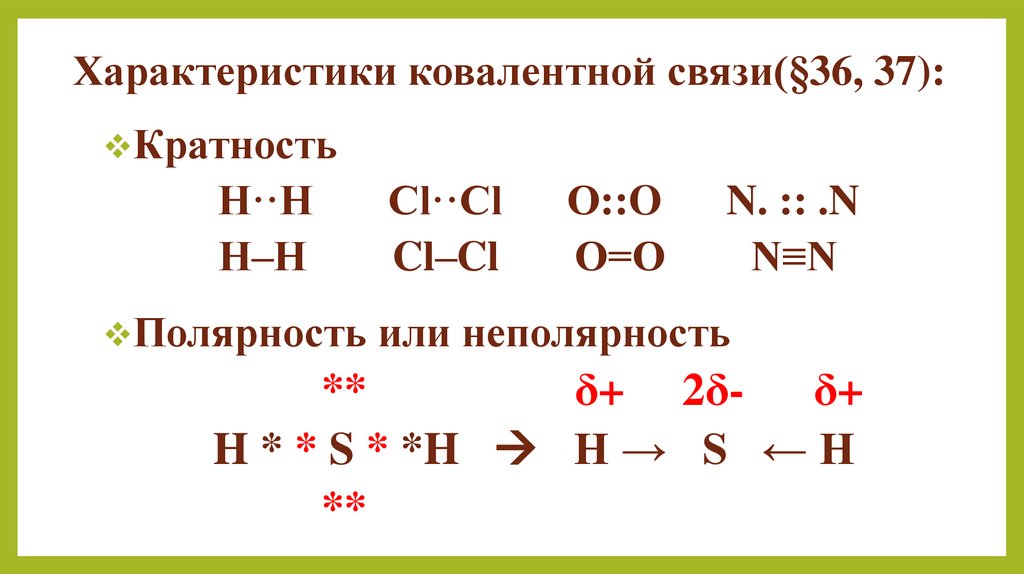
5. Характеристики ковалентной связи(§36, 37):
КратностьH··H
Н–Н
Cl··Cl
Cl–Cl
О::O
О=О
N. :: .N
N≡N
Полярность или неполярность
**
δ+ 2δδ+
H * * S * *H H → S ← H
**
6. Механизмы образования ковалентной связи
ОбменныйДонорно-акцепторный (ионы аммония и гидроксония)
7. Ионная связь (§34 )
Атомы могут терять электроны, присоединять их ипревращаться в заряженіые частицы — ионы
Li – e– → Li+;
F + e– → F–;
Ионы бывают простыми и сложными
Простой ион образован одним химическим элементом:
Н+ , Ca2+ , Fe3+
Сложные ионы образованы двумя и больше элементами:
OH- , CO32-, PO43 Атомы в них соединены ковалентной связью
8.
9. Ионная связь (§34 )
Ионы с противоположными зарядами под действиемэлектростатических сил соединяются вместе; между
ними возникает ионная связь
Ионная связь довольно прочная
MgO, Al2O3, Ca(OH)2, BaCl2, Li3N
10. Водородная связь
Электростатическое взаимодействиемежду молекулами при участии атомов
водорода называют водородной
связью.
Водородная связь образуется между
молекулами, в которых атомы водорода
соединяются с атомами самых
электроотрицательных элементов:
фтора, кислорода, азота
11.
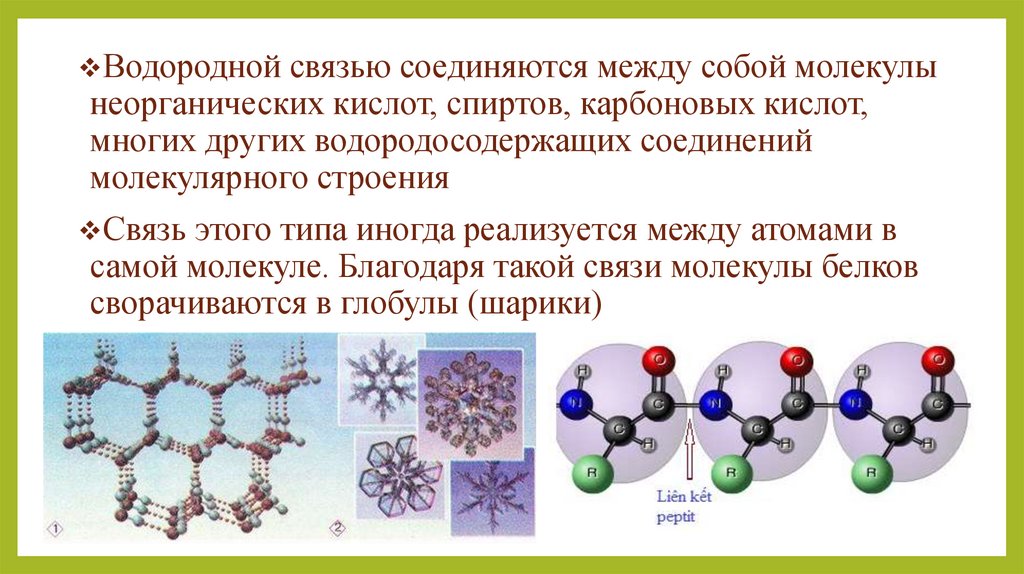
Водородной связью соединяются между собой молекулынеорганических кислот, спиртов, карбоновых кислот,
многих других водородосодержащих соединений
молекулярного строения
Связь этого типа иногда реализуется между атомами в
самой молекуле. Благодаря такой связи молекулы белков
сворачиваются в глобулы (шарики)
12. Металлическая связь (иногда представляют как разновидность ионной связи)
В металлах (простые вещества) атомырасположены очень плотно
Эти атомы и превращаются в катионы
Электроны теряют «свои» атомы и
становятся свободными, общими для
образца металла
Связь между катионами в металле,
осуществляется за счёт этих свободных
электронов и называется металлической
13. Домашнее задание
§ 34 повторить§ 35-37 учить
подготовиться к тесту







 chemistry
chemistry








