Similar presentations:
Растворы полимеров
1. РАСТВОРЫ ПОЛИМЕРОВ
2.
Полимеры и низкомолекулярные жидкости могут образовывать истинныерастворы (РП), коллоидные системы и студни (гели).
РП имеют формальное сходство с коллоидными системами - наличие в
низкомолекулярной жидкости больших по размеру частиц. Однако, в
отличие от коллоидных растворов в истинных – полимер молекулярнодиспергирован.
Истинные РП и коллоидные растворы имеют ряд принципиальных
различий:
- термодинамическая устойчивость РП и термодинамическая
неустойчивость коллоидных систем;
- однофазность растворов полимеров и двухфазность
коллоидных систем;
- агрегативная устойчивость РП и агрегативная неустойчивость
коллоидных систем;
- обратимость свойств РП и необратимость свойств коллоидных систем.
Огромная разница в размерах м/у
макромолекулами и молекулами растворителя, а
также цепное строение молекул растворяемого
вещества
3.
Свойства растворов полимеров (РП)1. Растворению
набухание.
полимеров
всегда
предшествует
2. РП имеют аномально высокую вязкость.
3. В РП чрезвычайно медленно протекают процессы
установления равновесия.
4. Малые количества посторонних веществ (примесей) в
РП могут резко изменить свойства раствора.
5. Свойства РП зависят от молекулярной массы полимера
и геометрических характеристик макромолекул.
4.
КЛАССИФИКАЦИЯ РАСТВОРОВ ПОЛИМЕРОВразбавленные (а)
полуразбавленные (умеренно-концентрированные) (б)
концентрированные растворы полимеров (в)
студни (гели)
пластифицированные системы.
5.
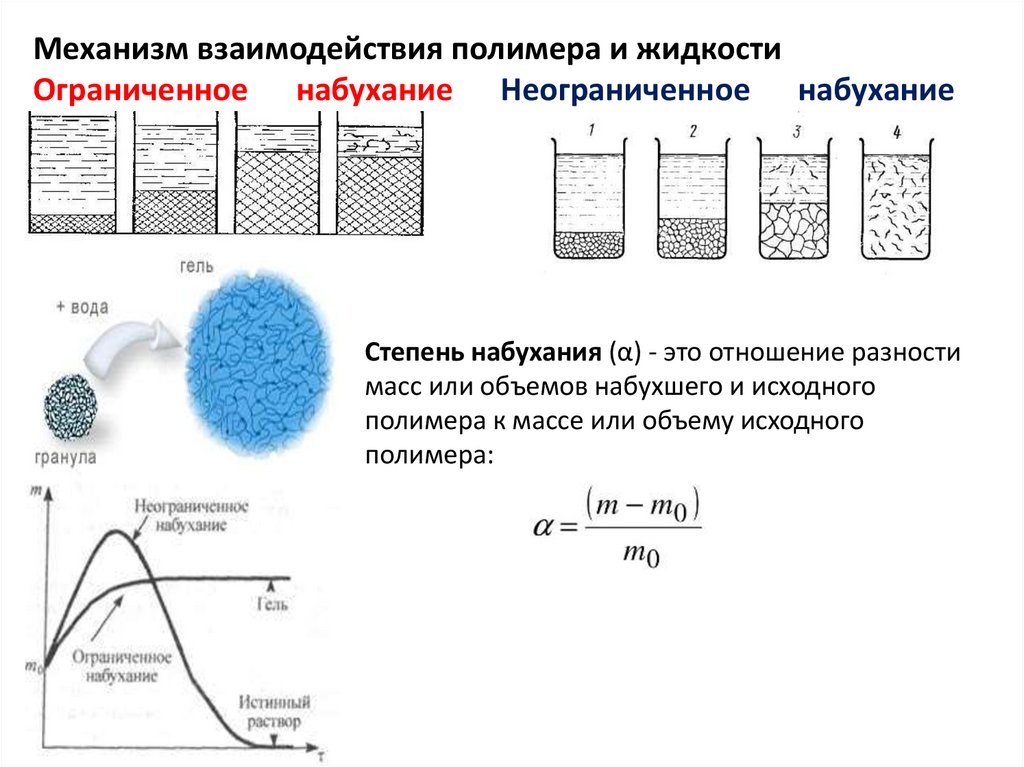
Механизм взаимодействия полимера и жидкостиОграниченное набухание Неограниченное набухание
Cтепень набухания (α) - это отношение разности
масс или объемов набухшего и исходного
полимера к массе или объему исходного
полимера:
6.
Факторы, влияющие на процесс растворенияполимеров
1. Природа полимера и растворителя (химическое
строение , структура, полярность компонентов раствора)
2. Гибкость полимерной цепи (возможности
сегментальной подвижности)
3. Молекулярная масса (чем выше ММ, тем растворимость
полимеров ниже)
4. Температура растворения (неоднозначное влияние)
7.
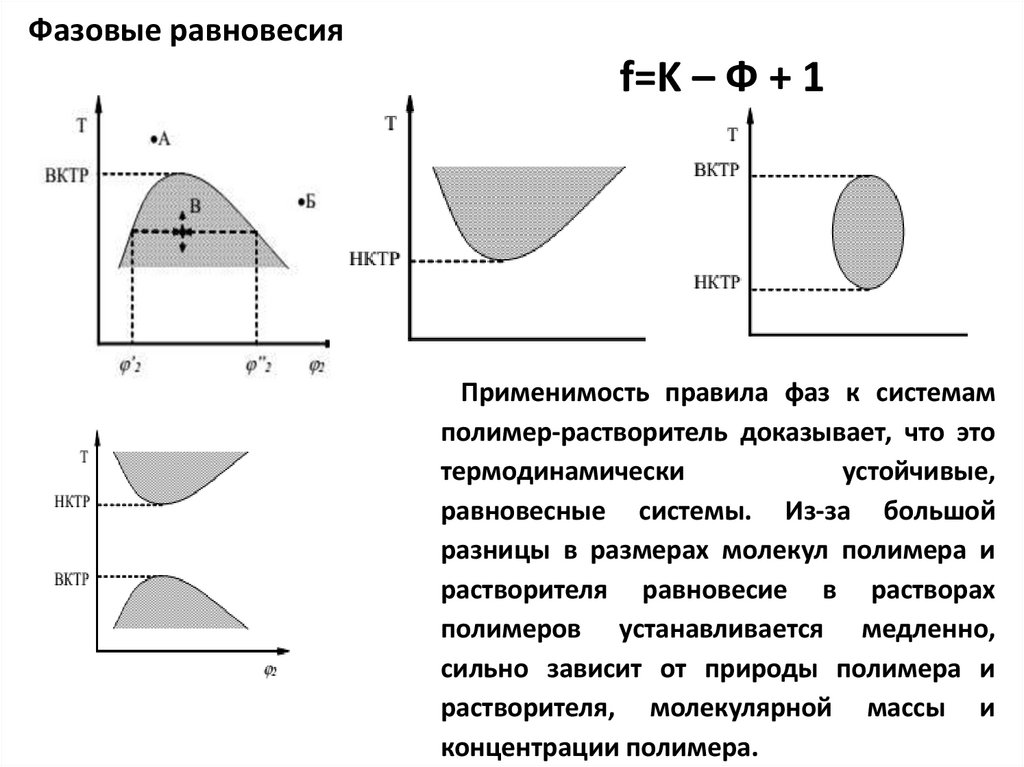
Фазовые равновесияf=K – Ф + 1
Применимость правила фаз к системам
полимер-растворитель доказывает, что это
термодинамически
устойчивые,
равновесные системы. Из-за большой
разницы в размерах молекул полимера и
растворителя равновесие в растворах
полимеров устанавливается медленно,
сильно зависит от природы полимера и
растворителя, молекулярной массы и
концентрации полимера.
8.
Особенности термодинамики полимерных растворовG = H–T S<0,
где H=Hр-ра– Hкомп – изменение энтальпии системы при
растворении; S = Sр-ра– Sкомп – изменение энтропии
системы при растворении.
Самопроизвольное растворение полимера возможно в
следующих случаях:
H<0 и S>0 - экзотермическое растворение.
H<0 и S<0, при условии H > T S - растворение
экзотермическое, но сопровождается уменьшением энтропии.
H>0 и S>0, при условии H < T S - растворение происходит за
счет возрастания энтропии и сопровождается поглощением тепла,
т.е. растворение эндотермическое.
H=0 и S>0. Растворение происходит за счет возрастания энтропии
и сопровождается нулевым тепловым эффектом (атермическое
растворение).
9.
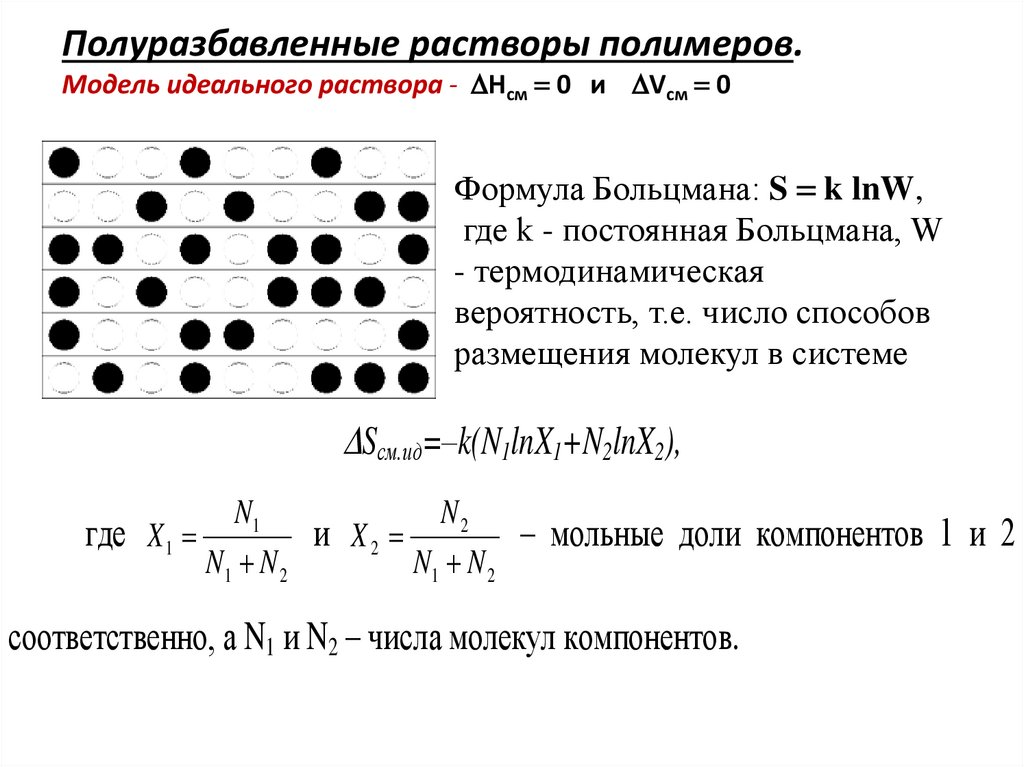
Полуразбавленные растворы полимеров.Модель идеального раствора - Нсм 0 и Vсм 0
Формула Больцмана: S k lnW,
где k - постоянная Больцмана, W
- термодинамическая
вероятность, т.е. число способов
размещения молекул в системе
Sсм.ид=–k(N1lnX1+N2lnX2),
N1
N2
где X 1
и X2
– мольные доли компонентов 1 и 2
N1 N 2
N1 N 2
соответственно, а N1 и N2 – числа молекул компонентов.
10.
Модели полимерных растворов.Модель полимерного раствора по Флори и Хаггинсу
ДОПУЩЕНИЯ:
Макромолекула состоит из Z отрезков – сегментов
Сегмент занимает ячейку, эквивалентную
молекуле растворителя
Энтропия смешения определяется числом
способов расположения молекул р-ля и сегментов
Следует учитывать, что число перестановок –
ограничено, т.к. сегменты связаны в цепь
В отличие от идеального раствора, при расчете энтропии смешения
полимерного раствора необходимо учесть значительную разницу в
размерах макромолекул и молекул растворителя
Энтропия смешения N1 молекул растворителя и N2 цепей, каждая из
которых состоит из Z сегментов:
Sсм. k(N1 ln 1 N2ln 2),
где 1 и 2 - объемные доли растворителя и полимера.
11.
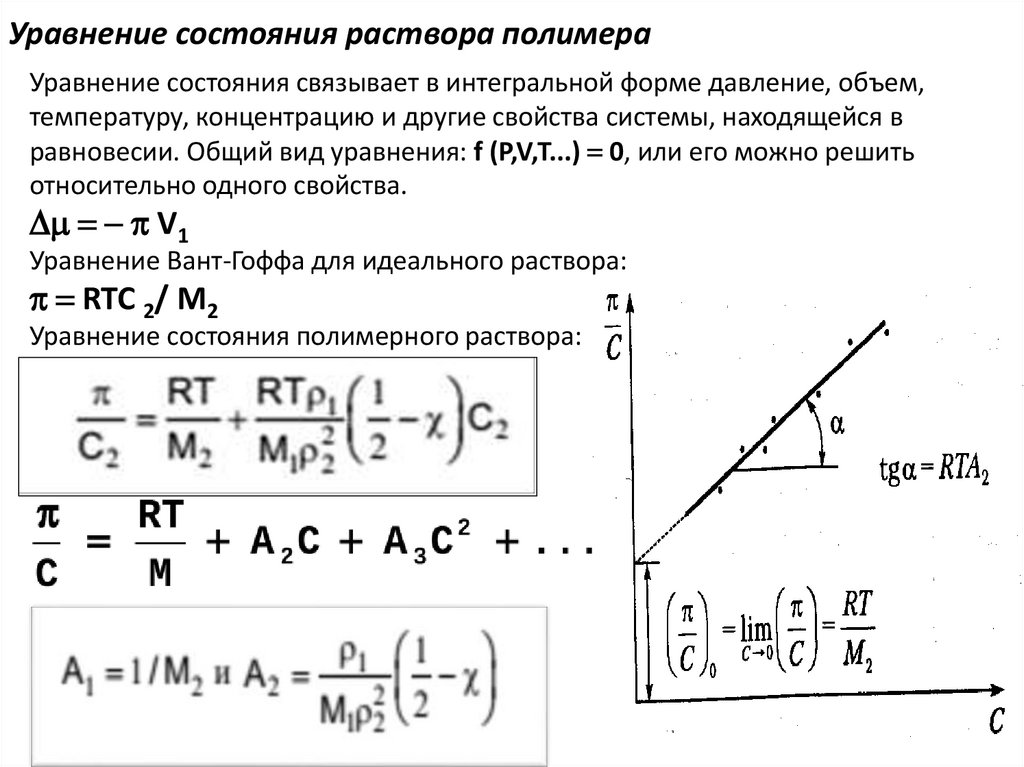
Уравнение состояния раствора полимераУравнение состояния связывает в интегральной форме давление, объем,
температуру, концентрацию и другие свойства системы, находящейся в
равновесии. Общий вид уравнения: f (P,V,T...) 0, или его можно решить
относительно одного свойства.
V1
Уравнение Вант-Гоффа для идеального раствора:
RTC 2/ M2
Уравнение состояния полимерного раствора:
12.
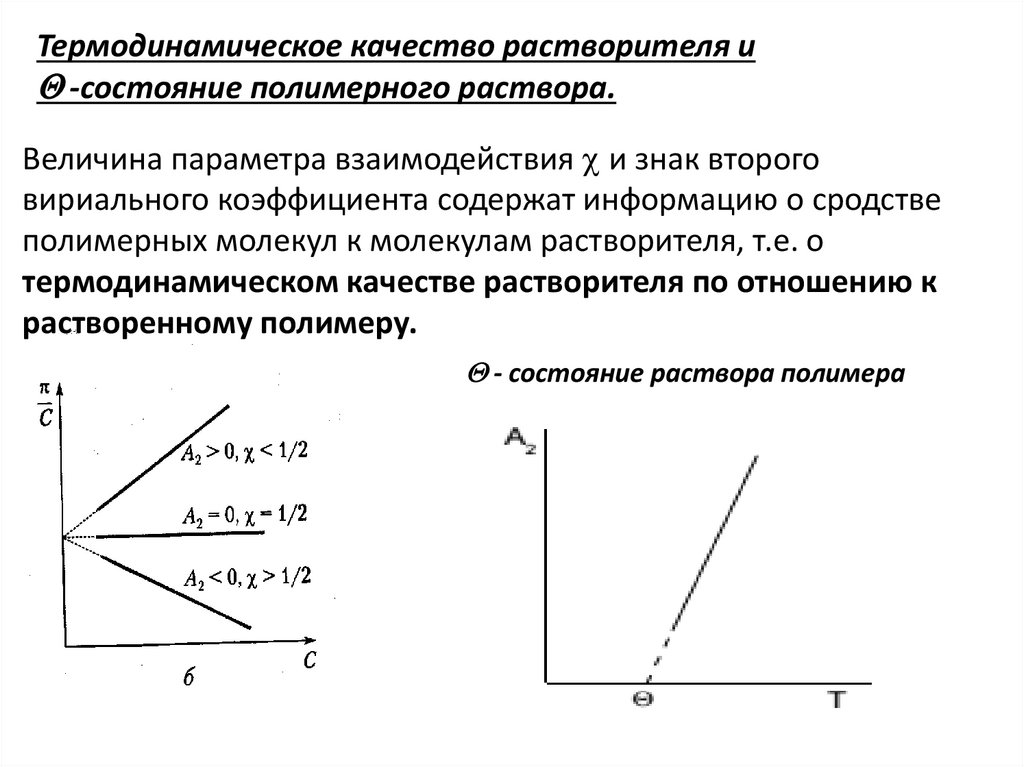
Термодинамическое качество растворителя и-состояние полимерного раствора.
Величина параметра взаимодействия и знак второго
вириального коэффициента содержат информацию о сродстве
полимерных молекул к молекулам растворителя, т.е. о
термодинамическом качестве растворителя по отношению к
растворенному полимеру.
- состояние раствора полимера
13.
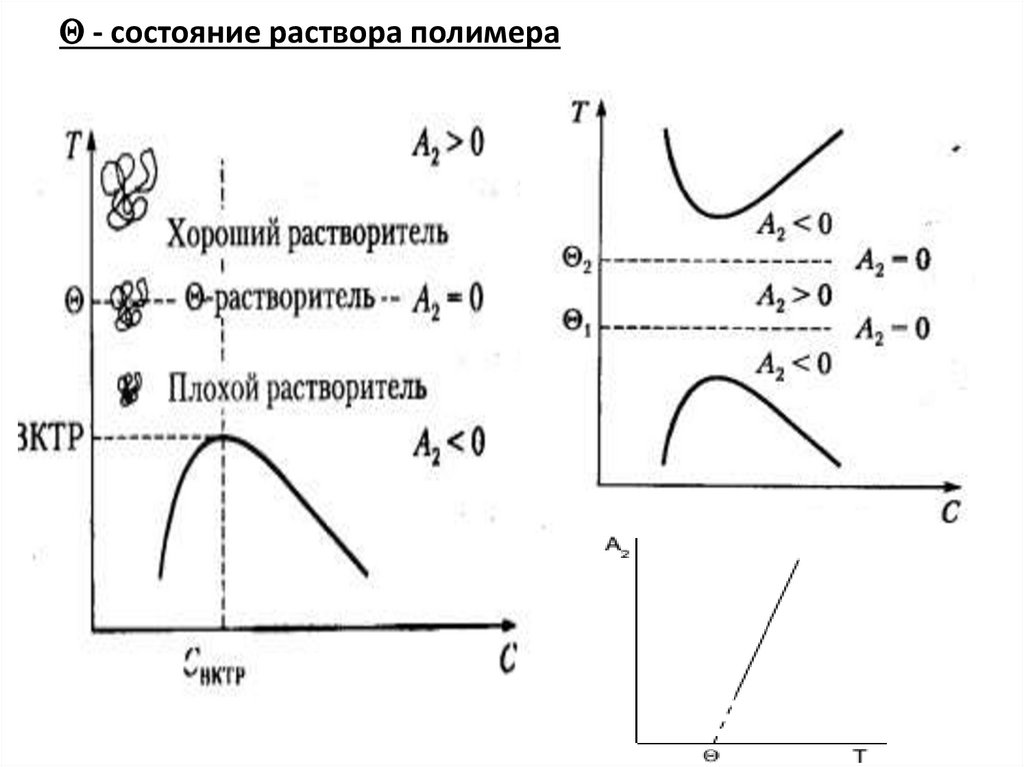
- состояние раствора полимера14.
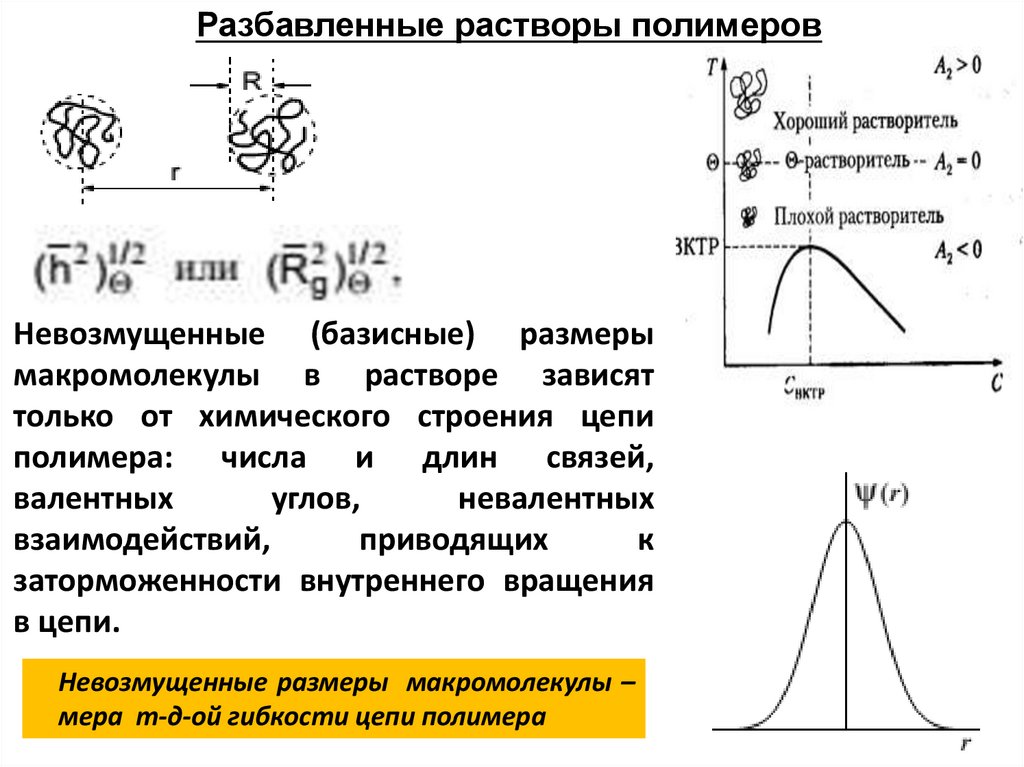
Разбавленные растворы полимеровНевозмущенные (базисные) размеры
макромолекулы в растворе зависят
только от химического строения цепи
полимера: числа и длин связей,
валентных
углов,
невалентных
взаимодействий,
приводящих
к
заторможенности внутреннего вращения
в цепи.
Невозмущенные размеры макромолекулы –
мера т-д-ой гибкости цепи полимера
15.
Коэффициент набухания макромолекулыh
h
2
2
1
1
2
2
при T (в хорошем растворителе) 1
при T
А2>0
при T
А2<0
T
16.
ГИДРОДИНАМИЧЕСКИЕ СВОЙСТВА РАСТВОРОВ ПОЛИМЕРОВ (РП)Одна из основных фундаментальных задач науки о полимерах
- установление связи между химическим строением
макромолекул и их конформацией. Изучение РП позволяет
получать следующие характеристики: молекулярная масса,
размеры клубков, коэффициент набухания, степень
полидисперсности и др.
17.
Вязкость разбавленных растворов полимеров. Природа вязкостиразбавленных полимерных растворов
η р-ра ~ ММ, Т, С, т-д качество растворителя и др.
Гидродинамические свойства РП проявляются в процессе течения.
Вязкость характеризует силы внутреннего трения жидкостей, т.е.
способность жидкости сопротивляться силе, вызывающей её течение.
Вязкость - мера энергии, рассеиваемой в форме теплоты в процессе
течения жидкости.
- большие затраты энергии на преодоление сил
взаимодействия полимер-полимер и полимеррастворитель при течении;
- макромолекула в ламинарном потоке растворителя
оказывается разными своими частями в слоях,
движущихся с разными скоростями. В результате
молекула испытывает действие момента сил, который
заставляет ее вращаться в потоке, что требует
дополнительной затраты энергии.
d
dx
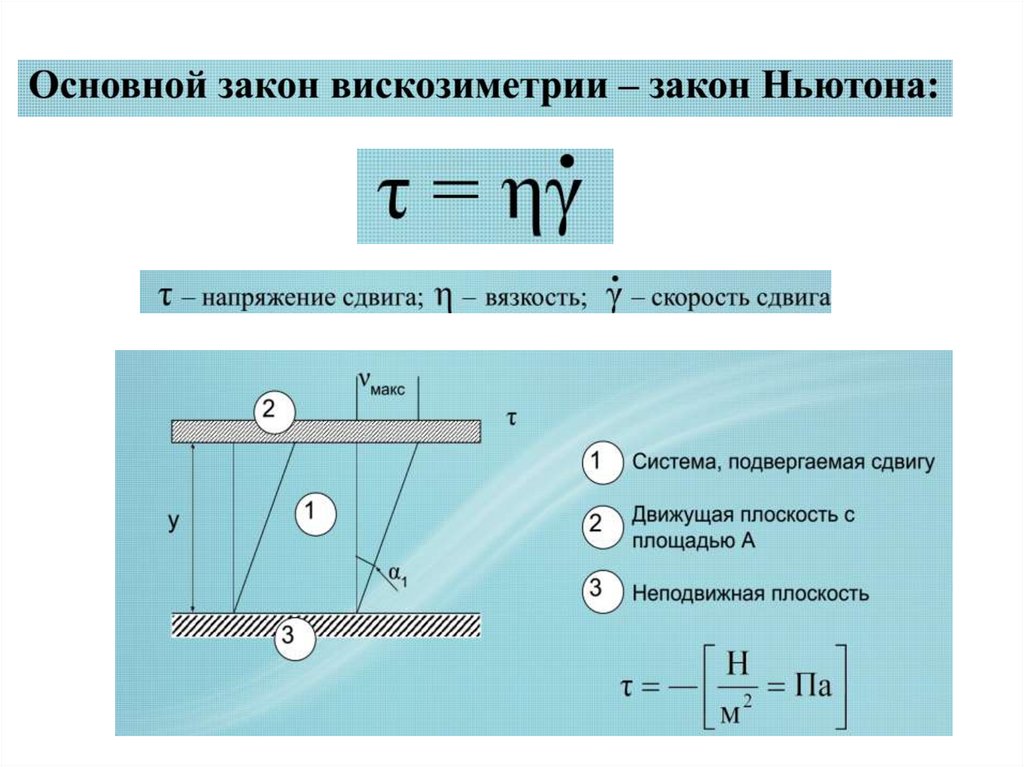
18.
Вискозиметрический метод исследованиярастворов полимеров
r 4 Pt
Q
Уравнение Пуазейля
8 l
Относительная вязкость:
отн
Удельная вязкость:
Приведенная вязкость:
( – o)/ o = ( уд)
Характеристическая вязкость:
уд
lim C 0
C
Уравнение Хаггинса
уд
С
t
0 t0
K' C
2
уд/С = пр
19.
Вискозиметрический метод определения ММ полимеровУравнение Марка-Куна-Хаувинка:
[ ] = K Ma
K = 10-2–10-5, зависит от температуры, природы полимера и
растворителя, полидисперсности. Разветвленности, тактичности и
др.
a - связан с конформацией макромолекулы в растворе и зависит
от всех факторов, влияющих на конформацию цепи – т-д качества
растворителя
и
температуры.
Для
компактных
частиц
(эйнштейновских
непроницаемых,
сплошных,
невзаимодействующих частиц), a=0; для гауссовых клубков в условиях a=0.5; для гибких макромолекул в хороших
растворителях a=0.6–0.8; для жестких макромолекул, т.е.
протекаемых клубков, a=1.0–1.5; для палочкообразных частиц
a=1.7–2.0.
В общем случае постоянная a изменяется в пределах: 0 a 2.
20.
Связь характеристической вязкости с размерами клубков иММ полимеров
1 2.5
Формула Эйнштейна
0
где – объемная доля растворенного вещества; 2.5 – коэффициент, учитывающий
гидродинамическое взаимодействие жесткой сферической частицы со средой.
2
3
2
Формула Флори-Фокса для
h
характеристической
вязкости полимера в M
растворителе
Ф – константа Флори, не зависит от свойств полимера.
2
2
Ф = 2.84х10 21
h ZА
h
3
2
M
3
2
1
3
21.
Характеристика концентрированности растворов полимеровПри [ ] с 1 раствор считается разбавленным (с 0.01-1%), макромолекулы
разделены растворителем и контакты между ними незначительны.
При [ ] с 10 раствор является умеренно концентрированным, для такого
раствора характерно взаимодействие и взаимное проникновение
макромолекулярных клубков.
При [ ] с 10 раствор является высоко концентрированным.
Макромолекулы в таком растворе настолько сближены и переплетены, что
образуют пространственную флуктуационную сетку зацеплений.
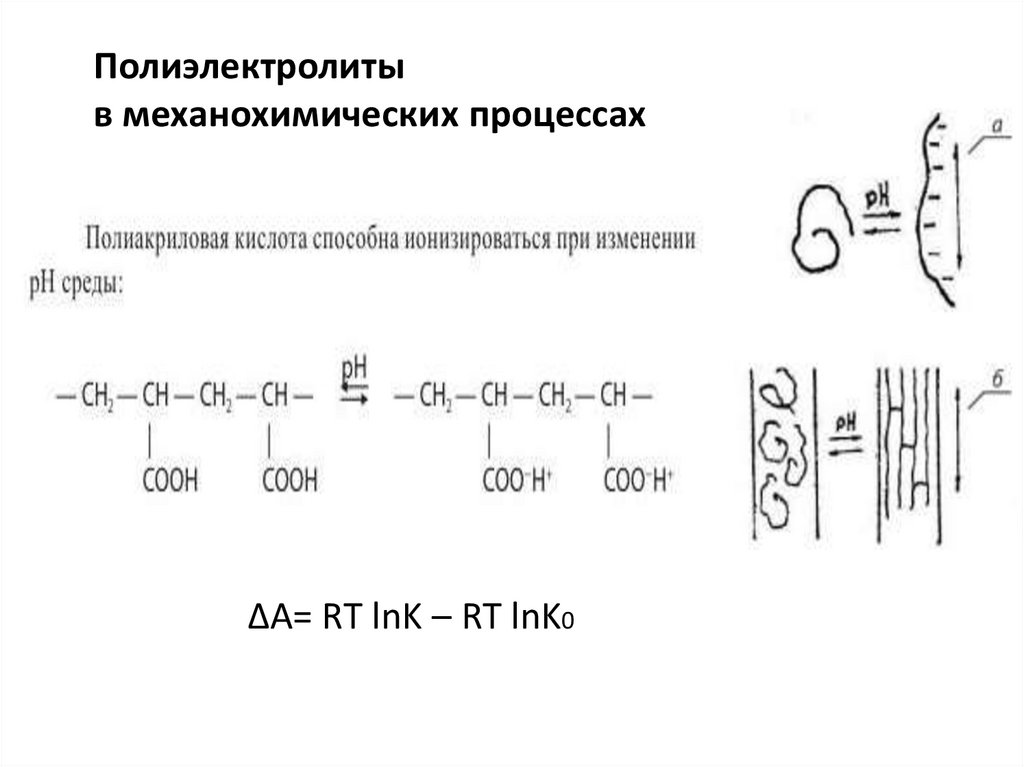
22.
Полиэлектролитыв механохимических процессах
ΔA= RT lnK – RT lnK0
23. КОНЦЕНТРИРОВАННЫЕ РАСТВОРЫ ПОЛИМЕРОВ
24.
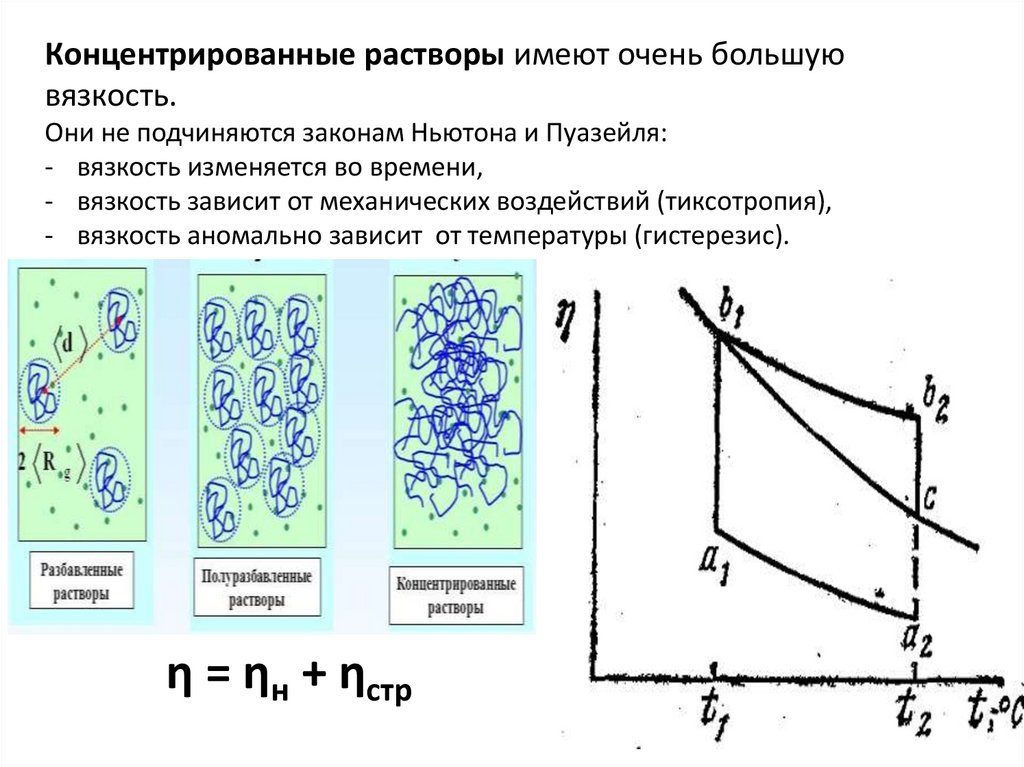
Концентрированные растворы имеют очень большуювязкость.
Они не подчиняются законам Ньютона и Пуазейля:
- вязкость изменяется во времени,
- вязкость зависит от механических воздействий (тиксотропия),
- вязкость аномально зависит от температуры (гистерезис).
η = ηн + ηстр
25.
26.
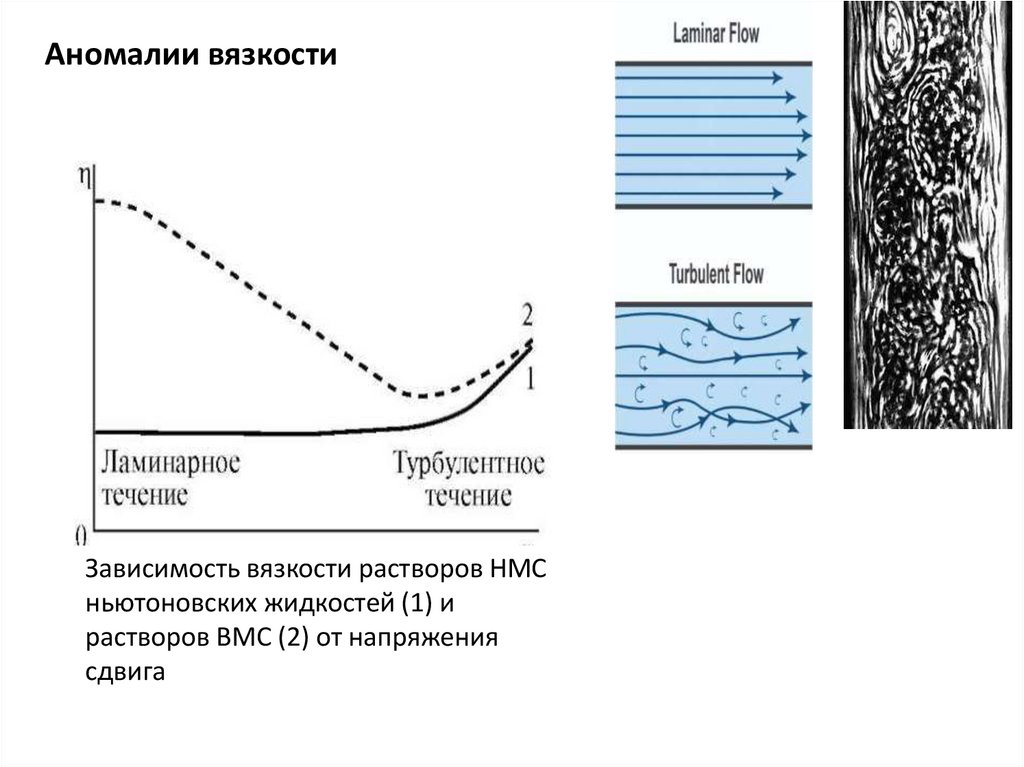
Аномалии вязкостиЗависимость вязкости растворов НМС
ньютоновских жидкостей (1) и
растворов ВМС (2) от напряжения
сдвига
27.
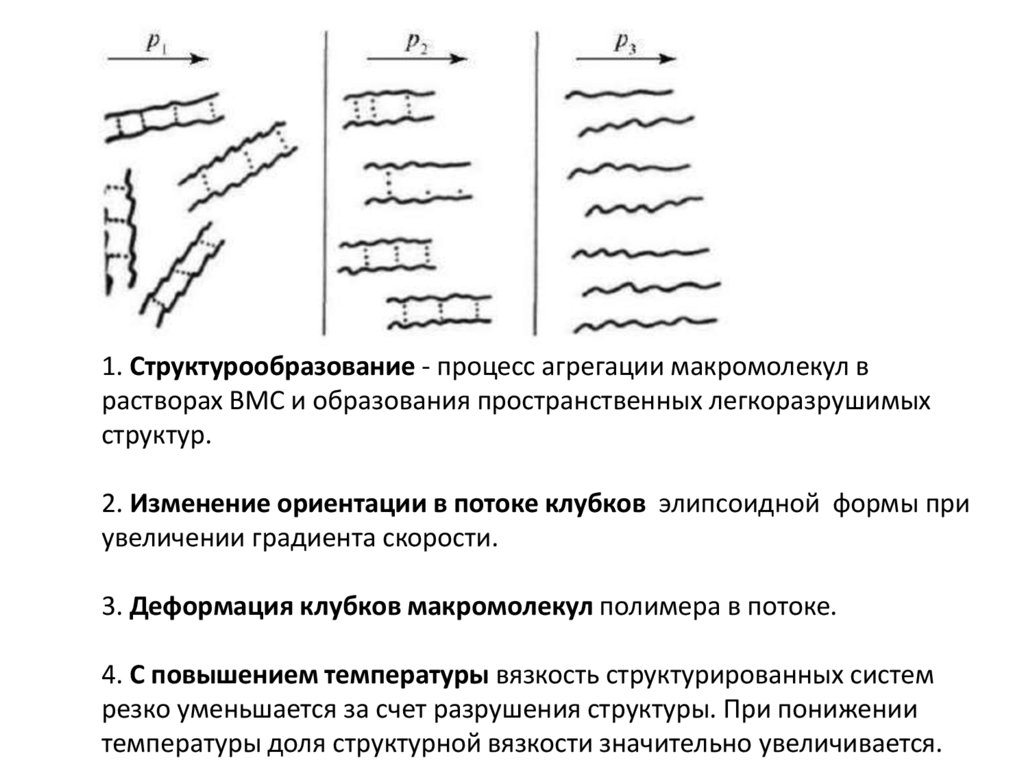
1. Структурообразование - процесс агрегации макромолекул врастворах ВМС и образования пространственных легкоразрушимых
структур.
2. Изменение ориентации в потоке клубков элипсоидной формы при
увеличении градиента скорости.
3. Деформация клубков макромолекул полимера в потоке.
4. С повышением температуры вязкость структурированных систем
резко уменьшается за счет разрушения структуры. При понижении
температуры доля структурной вязкости значительно увеличивается.
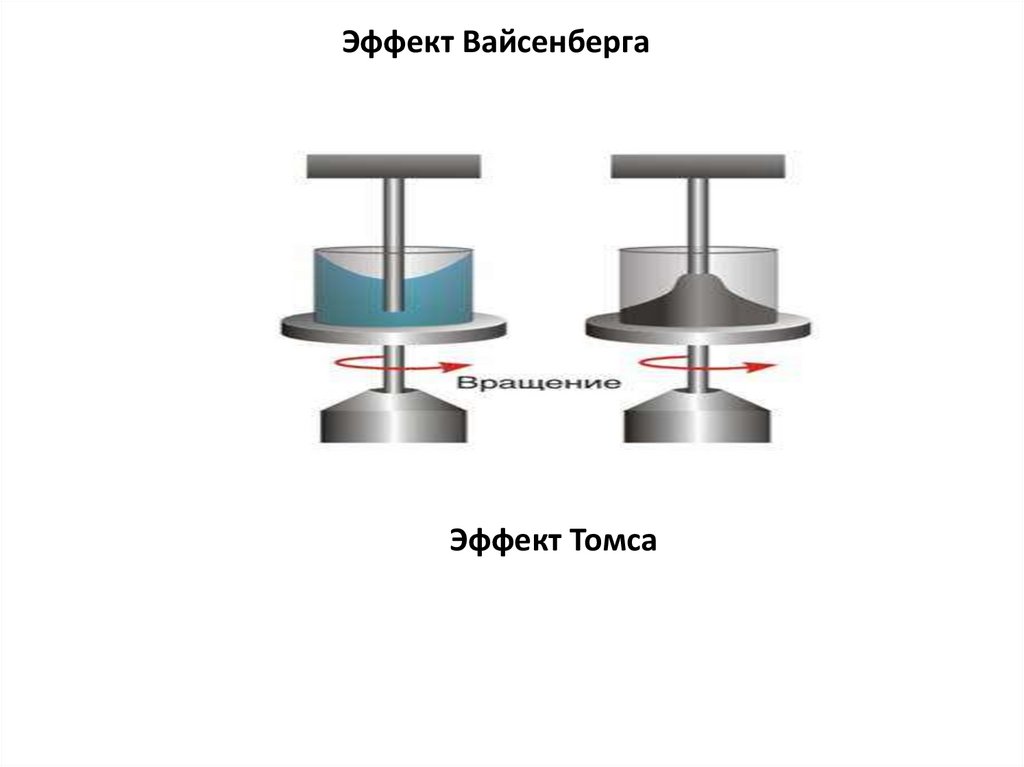
28.
Эффект ВайсенбергаЭффект Томса
29.
Причины возникновения аномалий вязкости1. Структурообразование – процесс агрегации
макромолекул в растворах ВМС и образование
пространственных легко разрушаемых структур
2. Изменение ориентации в потоке клубков-элипсоидов
при увеличении скорости сдвига.
3. Деформация клубков в потоке жидкости
4. Влияние температуры на вязкость за счет разрушения
или восстановления структуры полимерного раствора
(флуктуационной сетки зацеплений)
30.
Студень– гомогенная система, состоящая из ВМС (высокомолекулярная система) ирастворителя. При образовании студней между макромолекулами полимера возникают
молекулярные силы сцепления, приводящие к образованию пространственного
сетчатого каркаса, ячейки которого заполнены жидким раствором. Образование студня
можно рассматривать как начальную стадию коагуляции или как начало процесса
разделения раствора ВМС на две фазы. Студни преимущественно образуются
высокополимерами с гибкими макромолекулами. Благодаря гибкости пространственной
сетки студень при высушивании легко деформируется, сжимается, так что можно
высушиванием получить совершенно сухой полимер, который сохраняет эластичность.
Он снова способен набухать в подходящем растворителе. Процесс обратим и может
быть повторен неоднократно.
Классификация К студням первого типа относят набухшие в р-рителях сетчатые
полимеры.Такие студни обратимо деформируются в широком интервале т-р от точки
кристаллизации р-рителя до начала термич. распада р-рителя или полимера при
высоких т-рах. Все студни первого типа - однофазные системы. Студни второго
типа – с отчетливо выраженным двухфазным состоянием. Они возникают в
результате распада однофазных р-ров полимеров на две фазы, первая из к-рых,
содержащая большое кол-во полимера, образует преим. непрерывный каркас, а вторая
фаза с очень низкой концентрацией полимера включена в этот каркас в виде дисперсии.
Образуются из р-ров белковых в-в, при осаждении полимеров в ходе их переработки в
изделия (напр., в хим. волокна, в частности при созревании вискозы), из водных р-ров
метил- и оксиэтилцеллюлозы. Фазовый распад связан с изменением активности растворителя вследствие введения "нерастворителя" или резкого изменения Т.
31.
Пластификация (механизмы, правила мольных иобъемных долей) – самостоятельно.



















 chemistry
chemistry








