Similar presentations:
Аминокислоты
1.
Аминокислоты2.
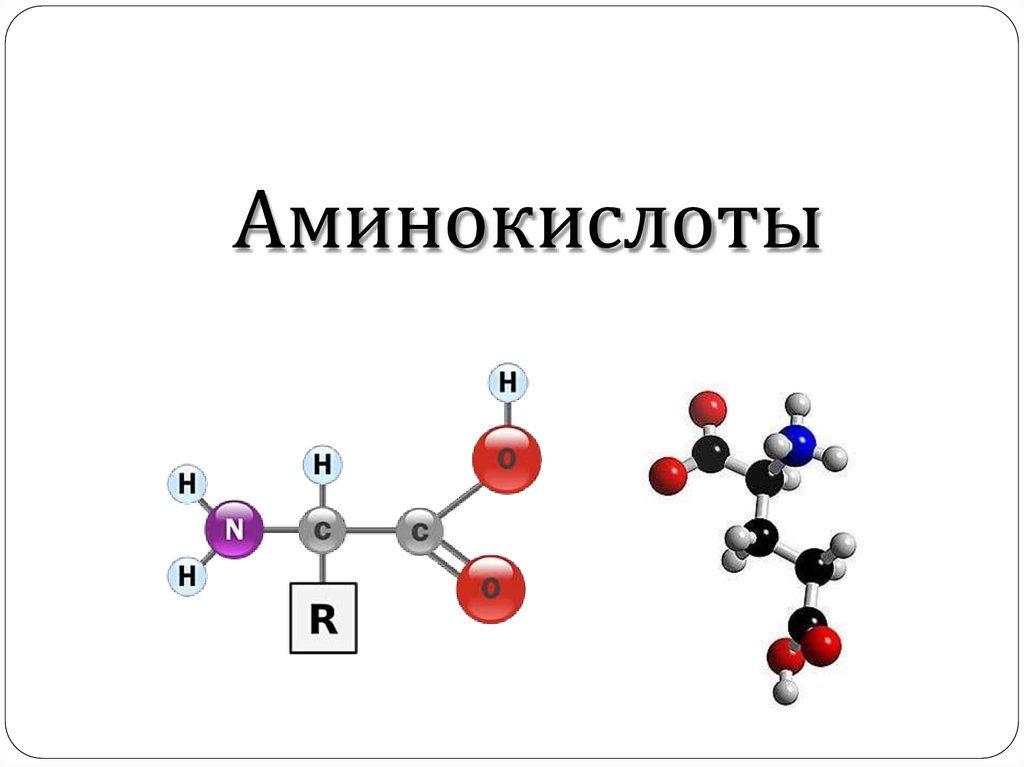
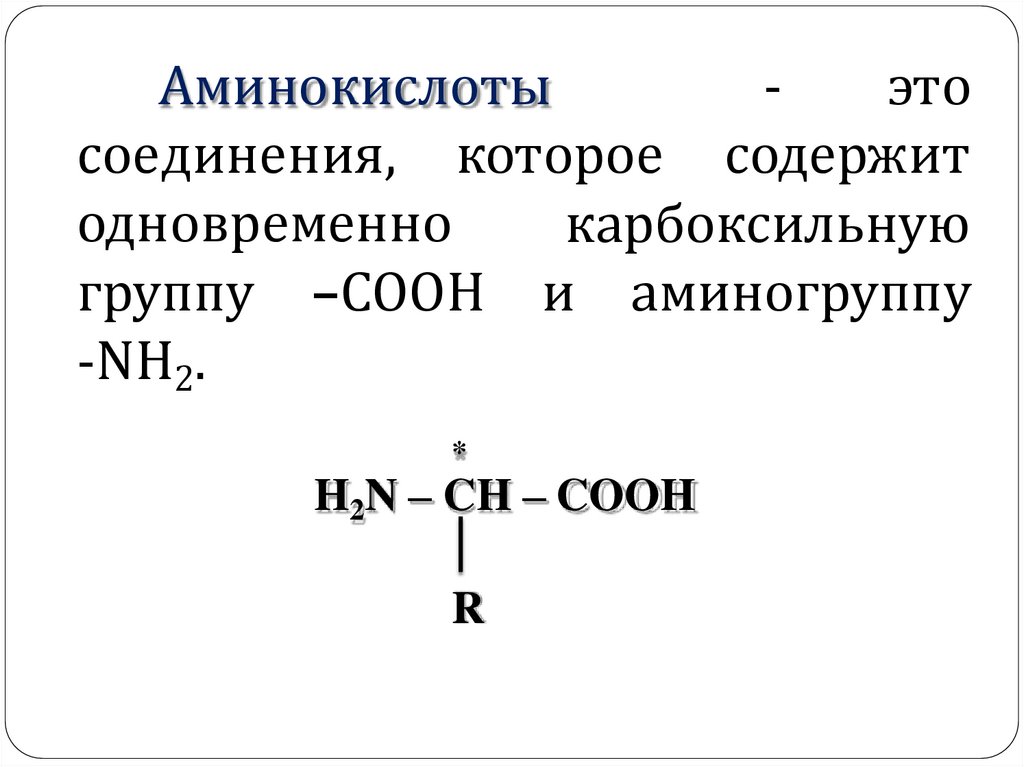
Аминокислотыэто
соединения, которое содержит
одновременно
карбоксильную
группу –СООН и аминогруппу
-NH2.
*
H2N – CH – COOH
R
3.
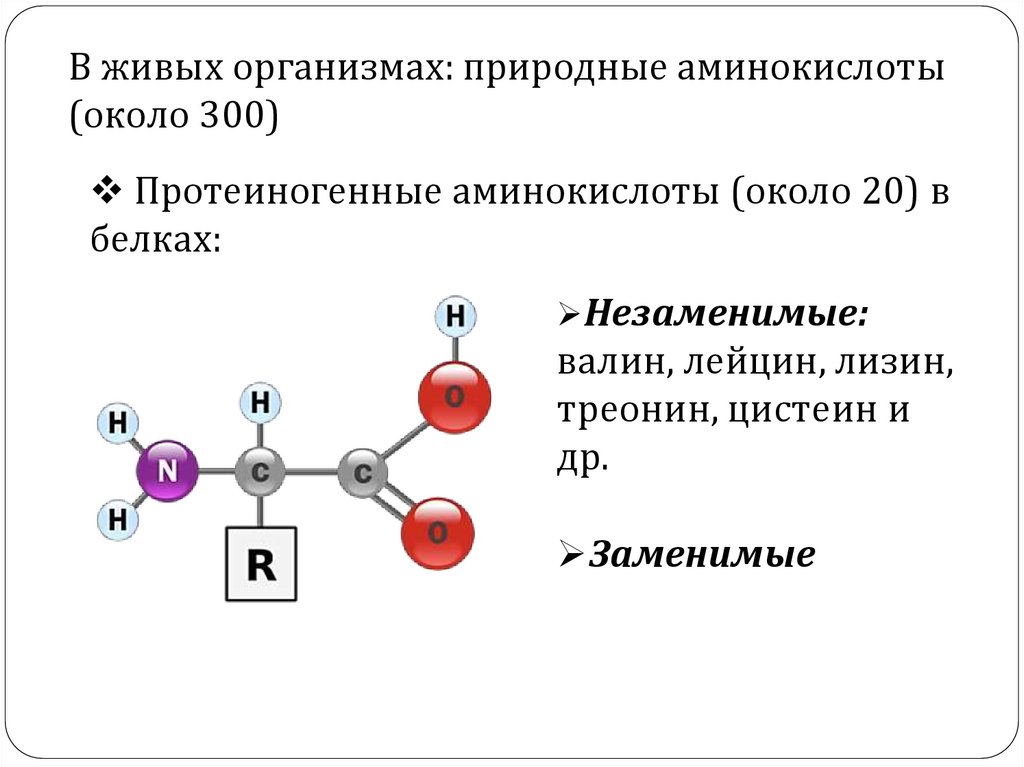
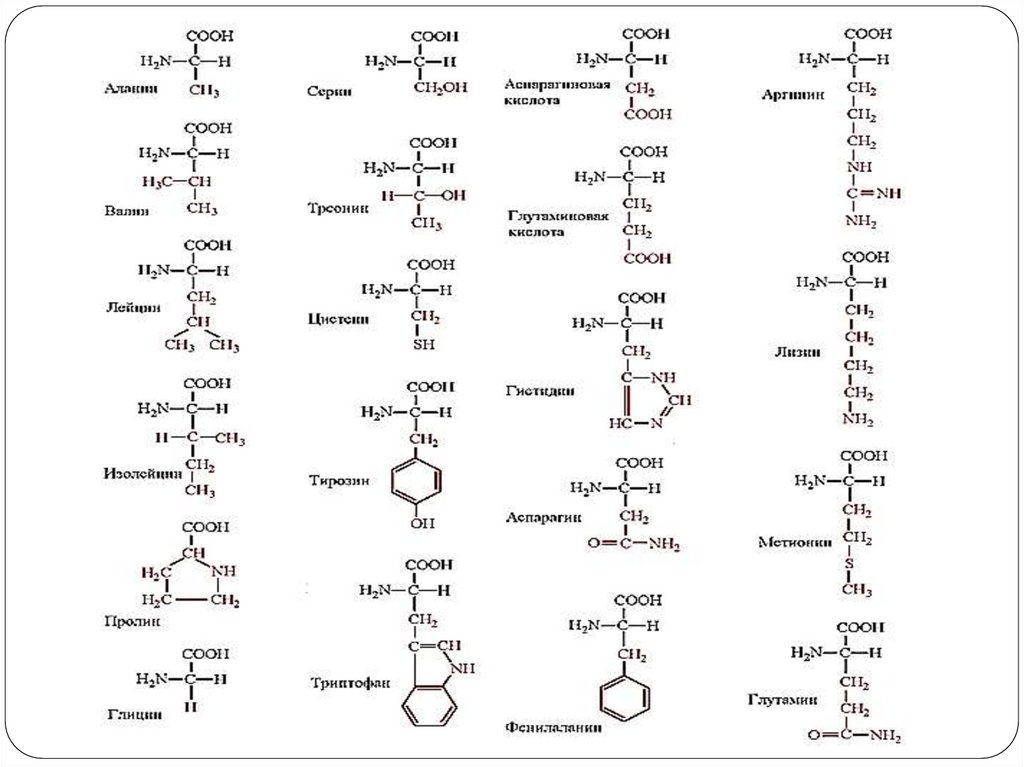
В живых организмах: природные аминокислоты(около 300)
Протеиногенные аминокислоты (около 20) в
белках:
Незаменимые:
валин, лейцин, лизин,
треонин, цистеин и
др.
Заменимые
4.
5.
Систематическая номенклатура(ИЮПАК)
По
систематической
номенклатуре
названия
аминокислот образуются из названий соответствующих
кислот прибавлением приставки амино и указанием места
расположения
аминогруппы
по
отношению
к
карбоксильной группе.
6.
Рациональная номенклатураК тривиальному названию карбоновой кислоты
добавляется приставка амино с указанием
положения аминогруппы буквой греческого
алфавита.
7.
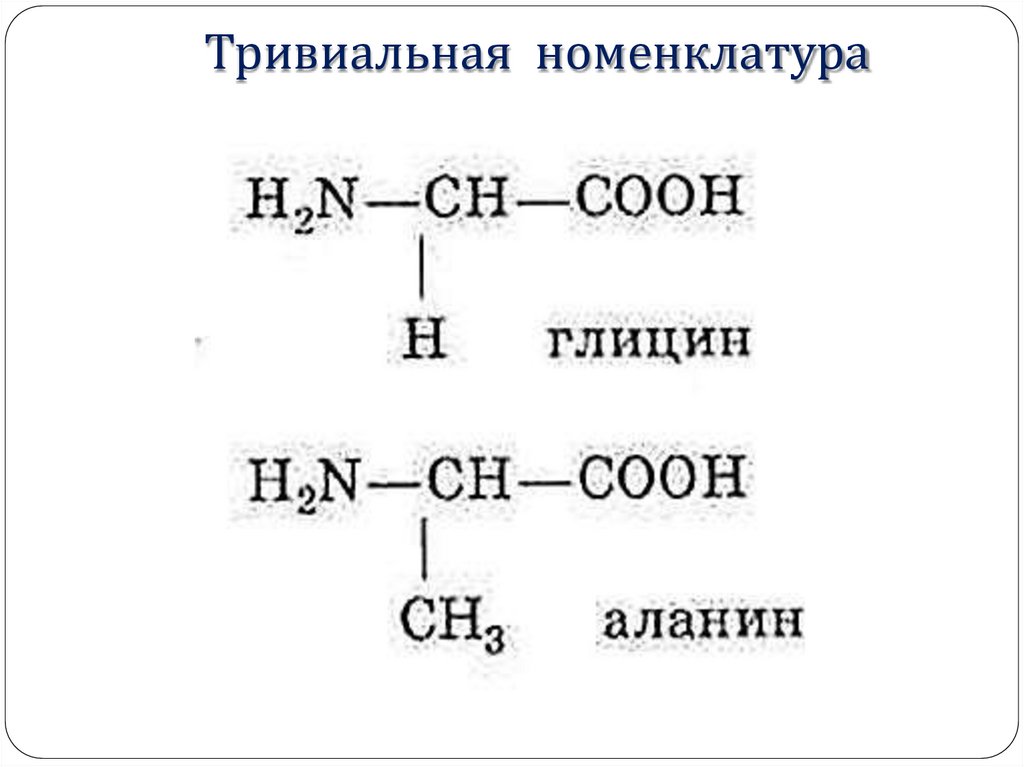
Тривиальная номенклатура8.
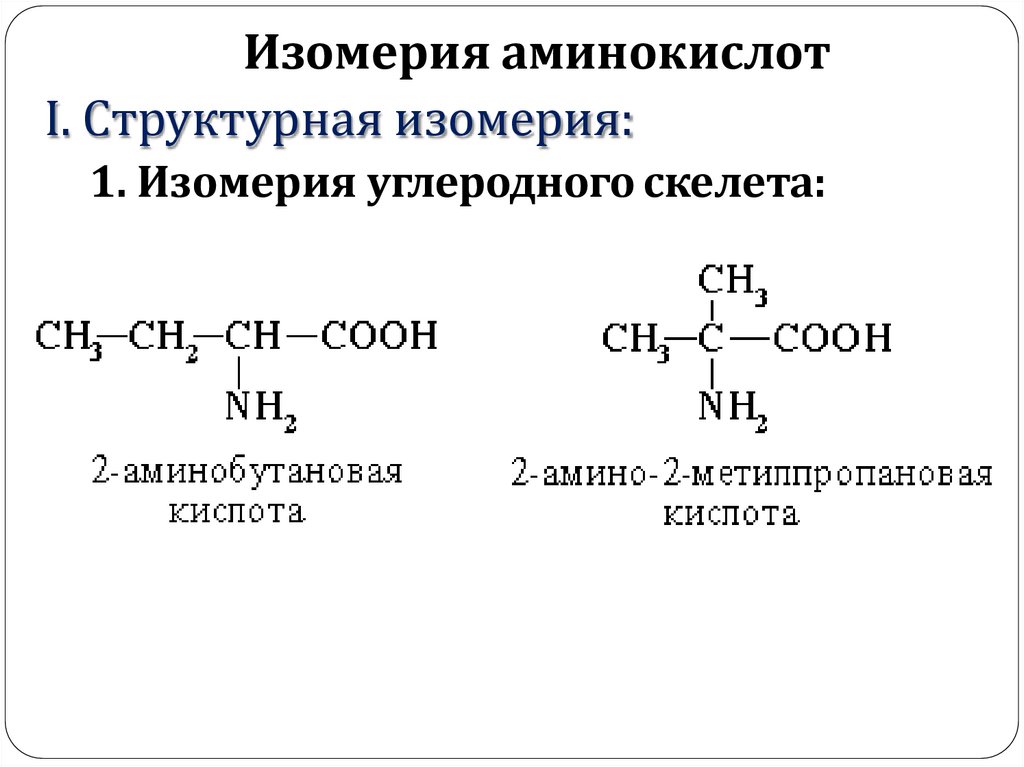
Изомерия аминокислотI. Структурная изомерия:
1. Изомерия углеродного скелета:
9.
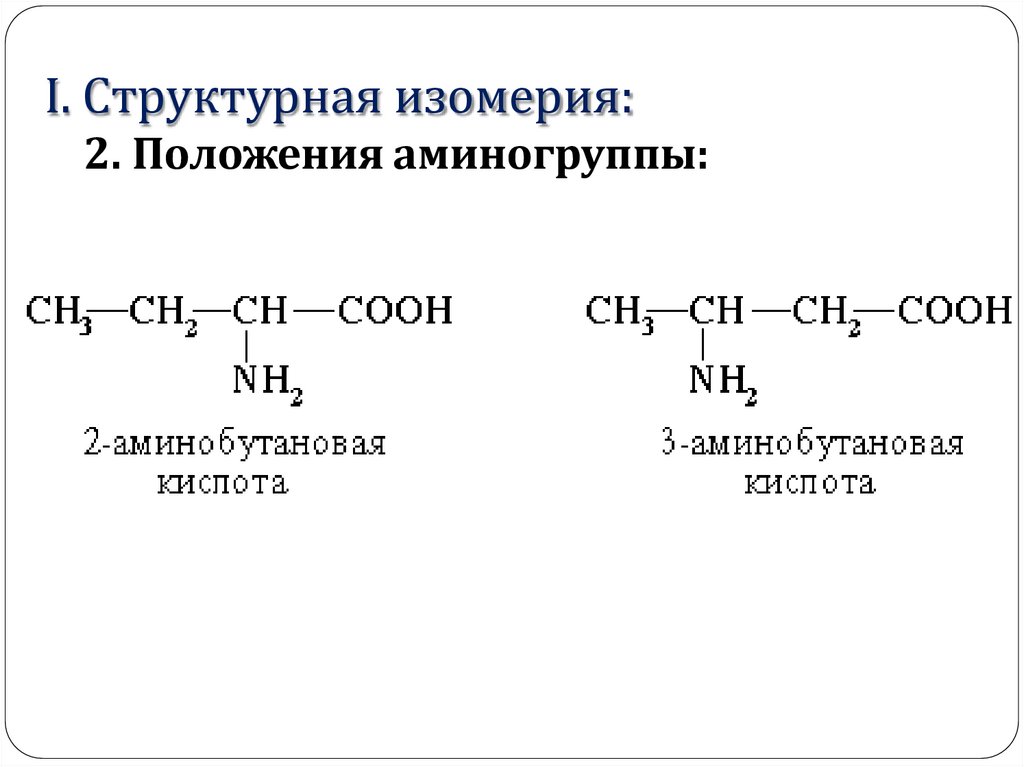
I. Структурная изомерия:2. Положения аминогруппы:
10.
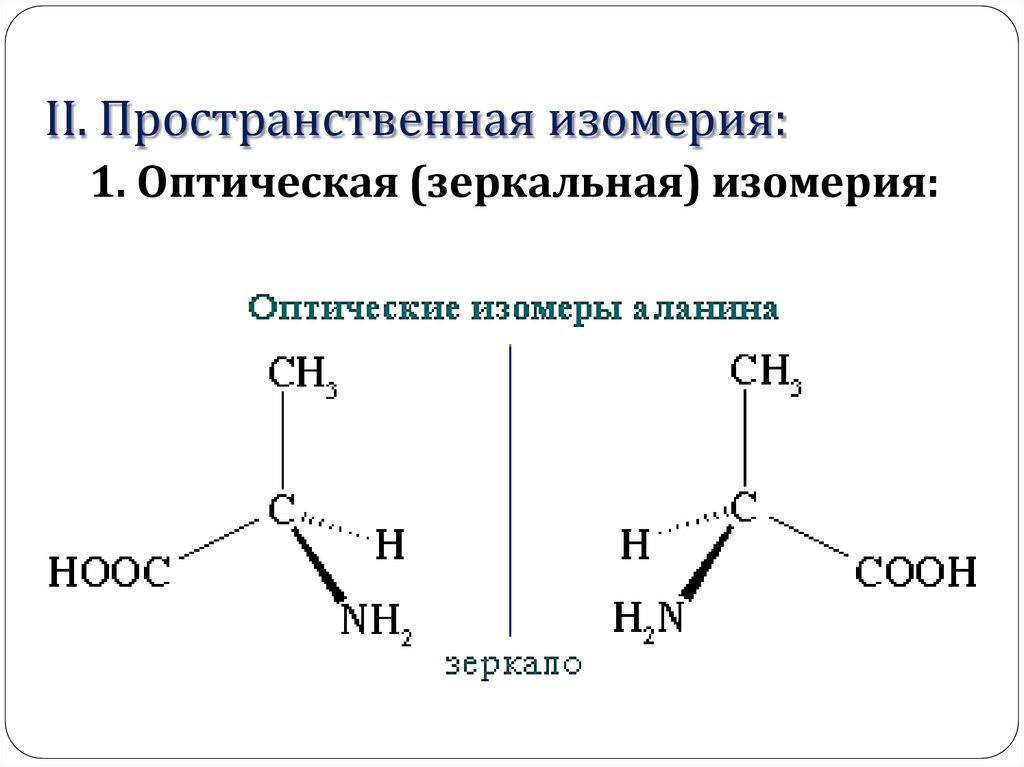
II. Пространственная изомерия:1. Оптическая (зеркальная) изомерия:
11.
ОПТИЧЕСКАЯ ИЗОМЕРИЯЗеркало Венеры (1898)
Все объекты этой картине имеют зеркальные
отражения.
12.
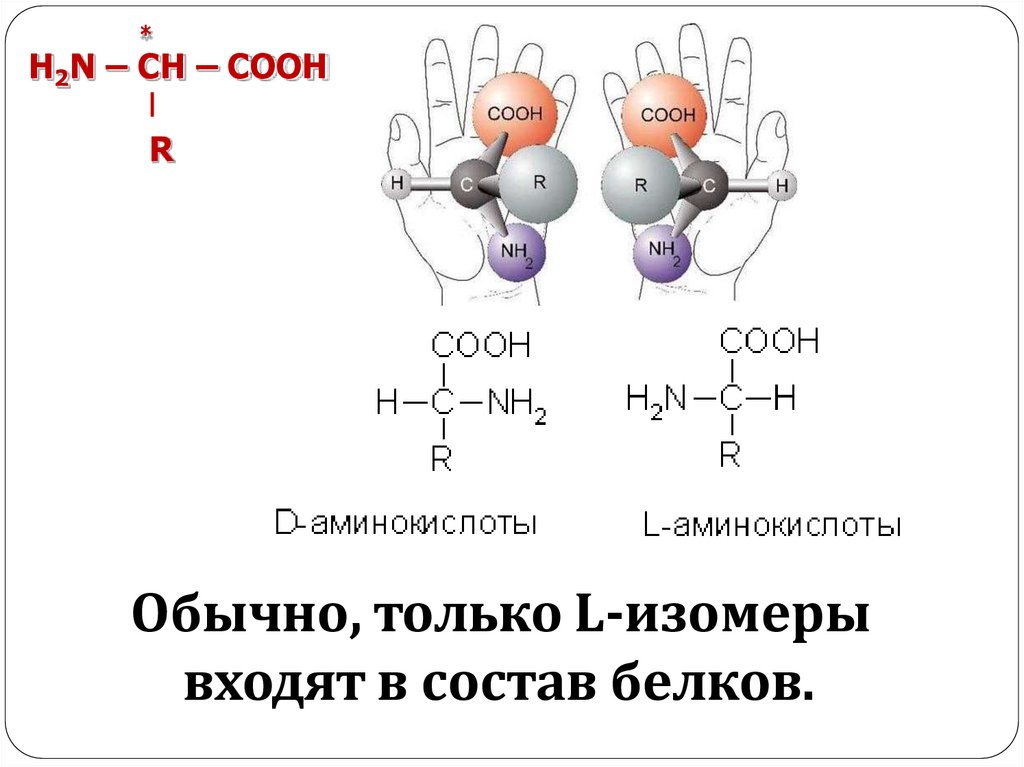
*H2N – CH – COOH
R
Обычно, только L-изомеры
входят в состав белков.
13.
Физические свойствааминокислот:
Аминокислоты
–
твердые
кристаллические
вещества
с
высокой tпл, при плавлении
разлагаются. Хорошо растворимы
в
воде,
водные
растворы
электропроводны.
14.
Химические свойствааминокислот:
Аминокислоты
проявляют
свойства оснований за счет
аминогруппы и свойства кислот
за счет карбоксильной группы, т.е.
являются
амфотерными
соединениями.
15.
I. Кислотные свойства –СООН1) С основаниями
NH2–CH2–COOH+NaOH→NH2–CH2–COONa+H2O
2) С металлами
2NH2–CH2–COOH+Mg→(NH2–CH2–COO)2Mg+H2
3) Реакция этерификации
16.
II. Основные свойства -NH2С кислотами
NH2–CH2–COOH+НСl→[NH3–CH2–COOH ]+СlВывод : органические амфотерные соединения
17.
III.Свойства,
взаимодействием
групп
определяемые
функциональных
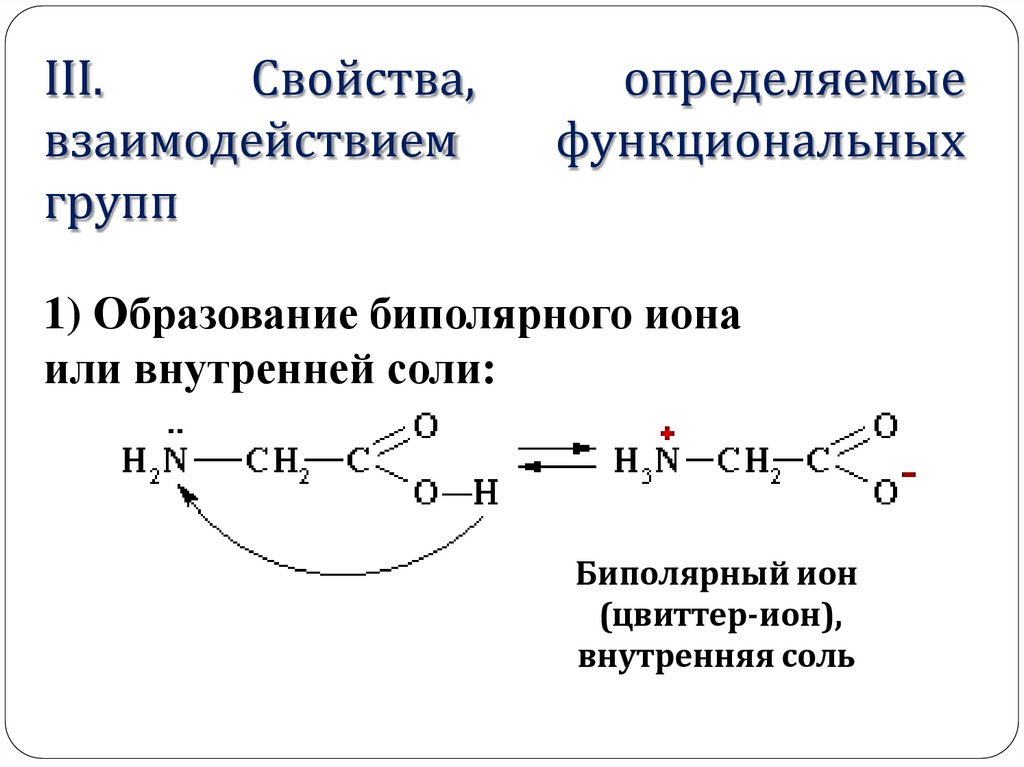
1) Образование биполярного иона
или внутренней соли:
Биполярный ион
(цвиттер-ион),
внутренняя соль
18.
III.Свойства,
взаимодействием
групп
определяемые
функциональных
2) Реакция поликонденсации (образование
пептидов) - взаимодействие аминокислот
между собой:
19.
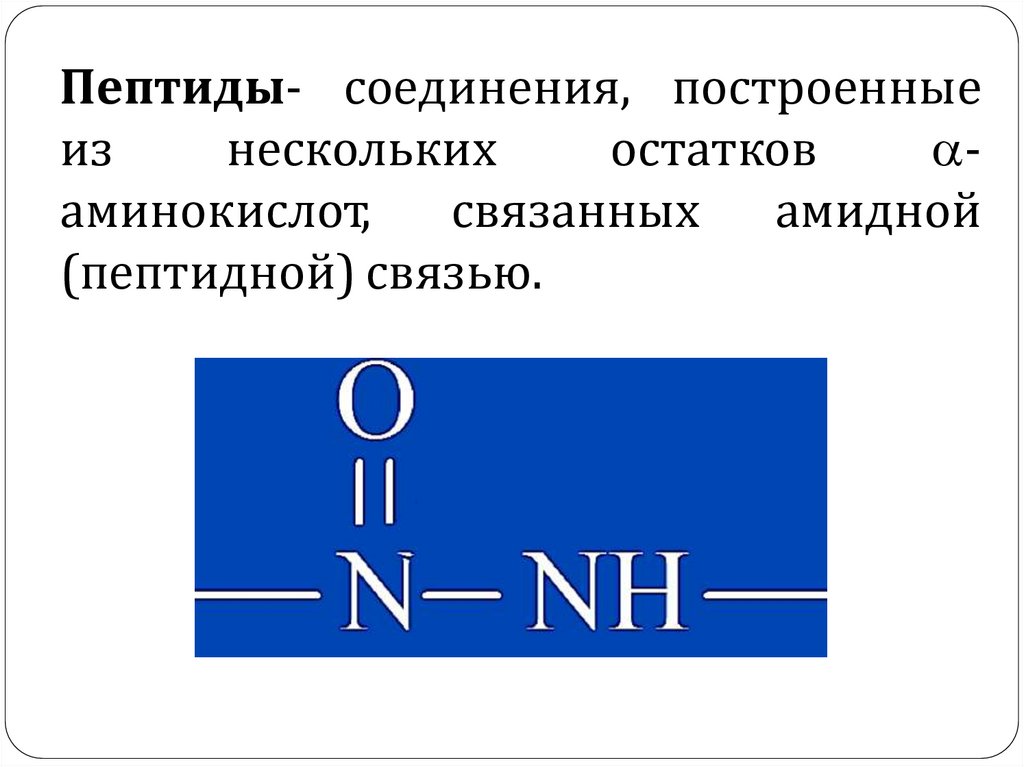
Пептиды- соединения, построенныеиз
нескольких
остатков
аминокислот,
связанных амидной
(пептидной) связью.
20.
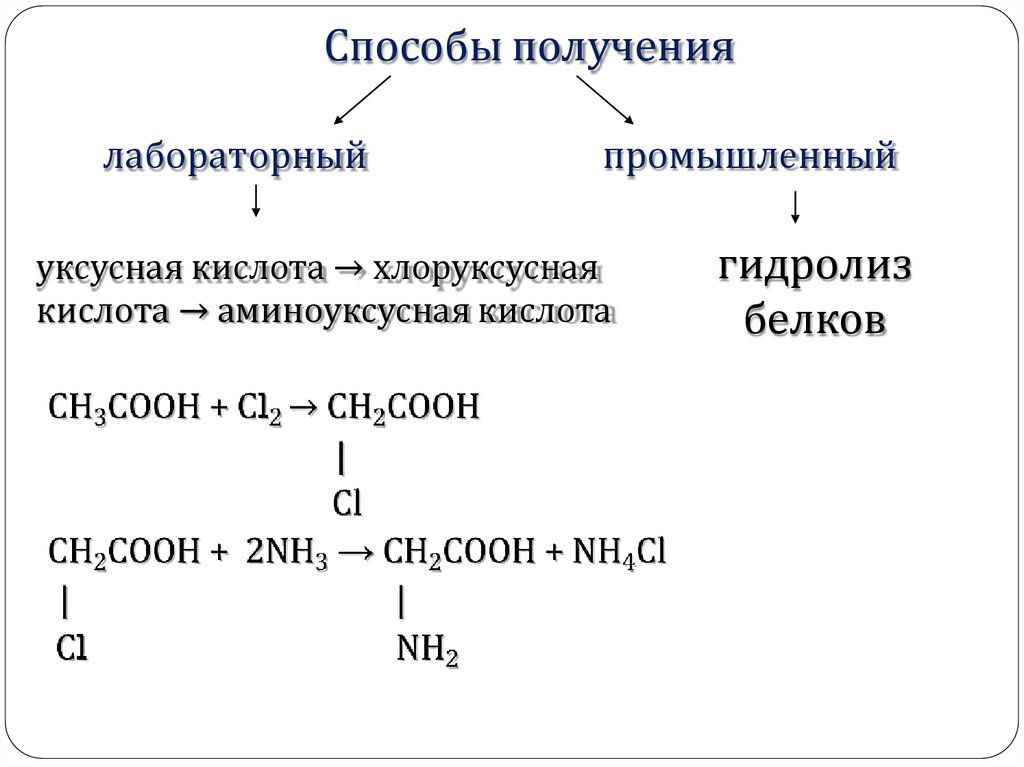
Способы получениялабораторный
промышленный
уксусная кислота → хлоруксусная
кислота → аминоуксусная кислота
гидролиз
белков
21.
БИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ22.
БИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ23.
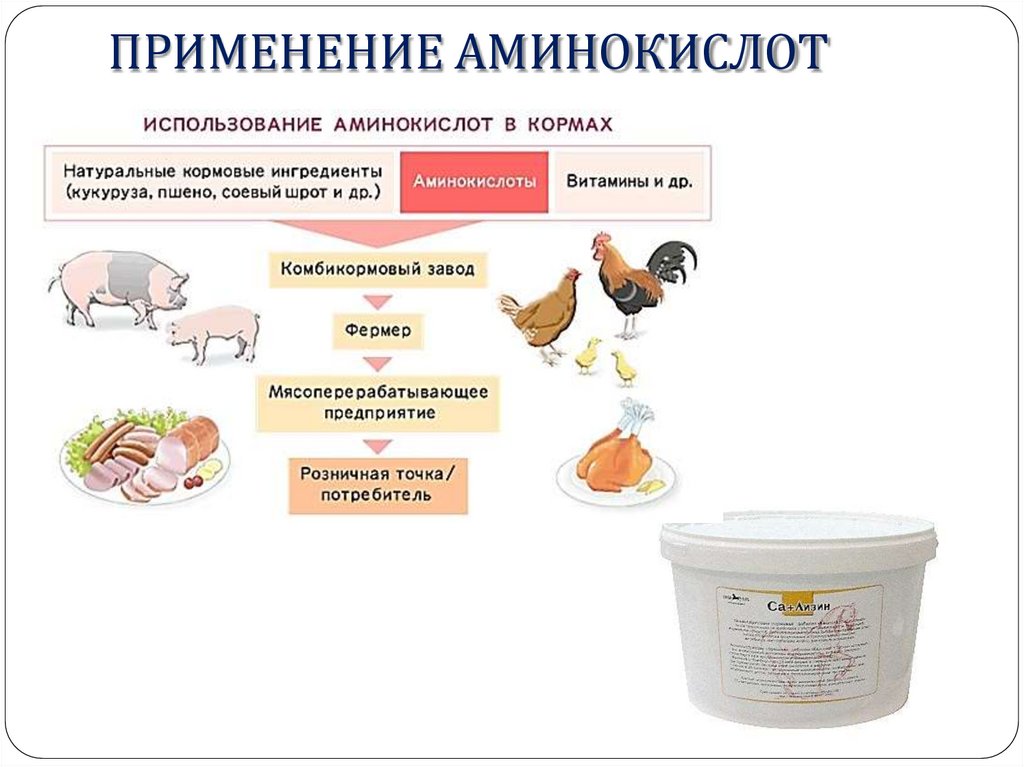
ПРИМЕНЕНИЕ АМИНОКИСЛОТ24.
ПРИМЕНЕНИЕ АМИНОКИСЛОТ25.
ПРИМЕНЕНИЕ АМИНОКИСЛОТ26.
ПРИМЕНЕНИЕ АМИНОКИСЛОТУСИЛИТЕЛИ ВКУСА И АРОМАТА - глутаминовая
кислота (Е620) или ее соли - (Е621)
27.
Домашнее задание:§17














 chemistry
chemistry