Similar presentations:
Холестерол. Переваривание экзогенного холестерола
1.
ПЯТИГОРСКИЙ МЕДИКО-ФАРМАЦЕВТИЧЕСКИЙ ИНСТИТУТ филиал федерального государственного бюджетного образовательного учреждения высшего образования«ВОЛГОГРАДСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙУНИВЕРСИТЕТ»
Министерства здравоохранения Российской Федерации
Кафедра микробиологии и иммунологии с курсом биологической химии
Лектор: к.б.н , старший преподаватель
Харитонова О.В.
Пятигорск
2022
2.
ХолестеролХолестерол относится к группе
соединений, имеющих в своей основе
циклопентанпергидрофенантреновое
кольцо, и является ненасыщенным
спиртом.
Стероид, характерный только для животных организмов
Синтезируется во многих тканях человека, но основное место синтеза –
печень. В печени синтезируется – 50%, в тонком кишечнике – 15-20%,
остальной холестерол синтезируется в коже, коре надпочечников,
половых железах
С пищей в сутки поступает в среднем 300-500 мг, а синтезируется в
организме около 1 г
3.
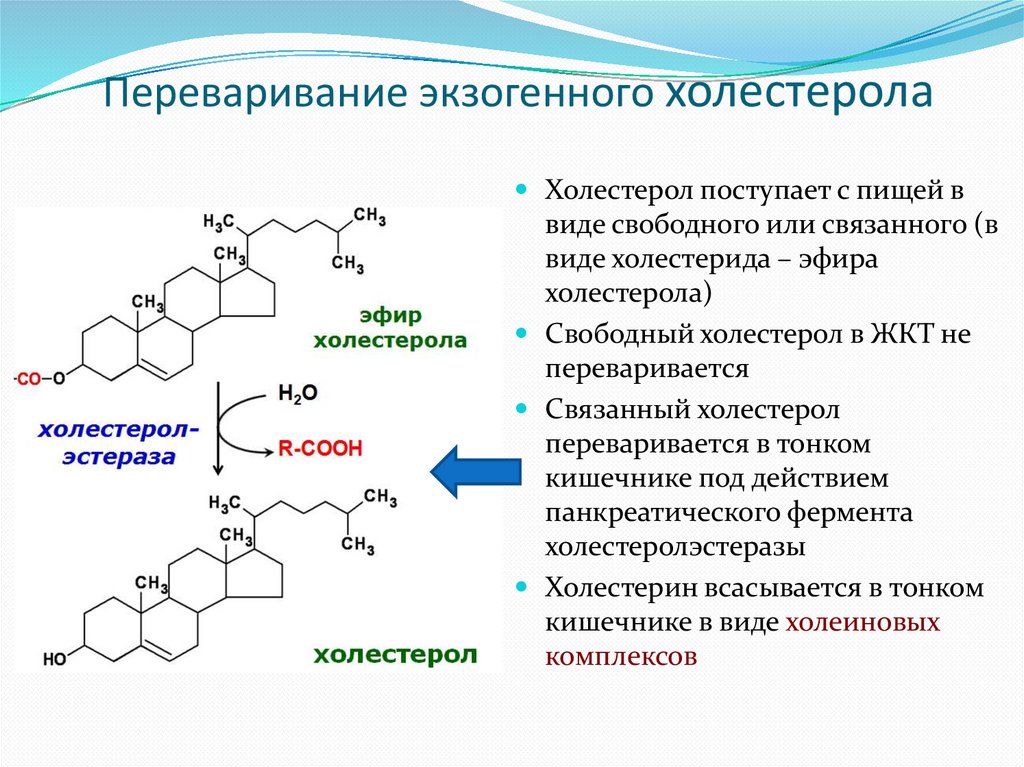
Переваривание экзогенного холестеролаХолестерол поступает с пищей в
виде свободного или связанного (в
виде холестерида – эфира
холестерола)
Свободный холестерол в ЖКТ не
переваривается
Связанный холестерол
переваривается в тонком
кишечнике под действием
панкреатического фермента
холестеролэстеразы
Холестерин всасывается в тонком
кишечнике в виде холеиновых
комплексов
4.
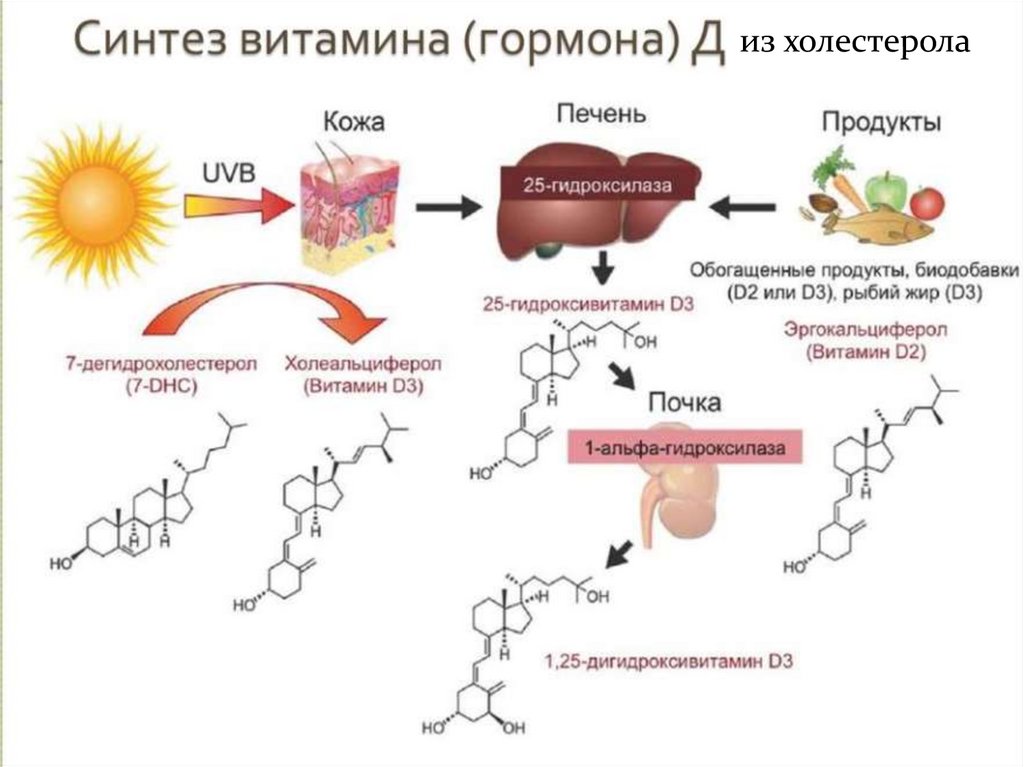
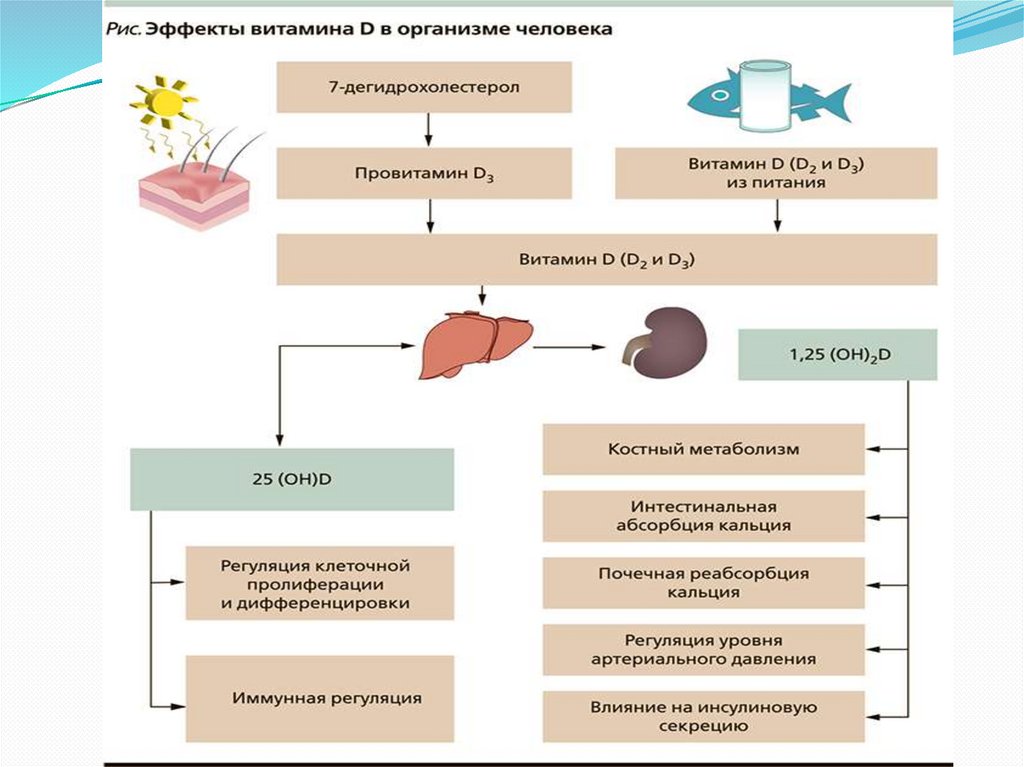
Холестерол выполняет много функций, а именно онвходит в состав всех мембран клеток и влияет на их
свойства, служит исходным субстратом в синтезе
желчных кислот и стероидных гормонов.
Холестерол за счет своей гидроксильной группы может
образовывать эфиры с высшими жирными кислотами.
Этерифицированный холестерол преобладает в крови
и запасается в небольших количествах в некоторых
типах клеток, использующих его как субстрат для
синтеза других веществ (стероидных гормонов,
витамина Д и желчных кислот).
Холестерол и его эфиры – гидрофобные молекулы,
поэтому они транспортируются кровью только в
составе различных типов липопротеинов (ЛП).
5.
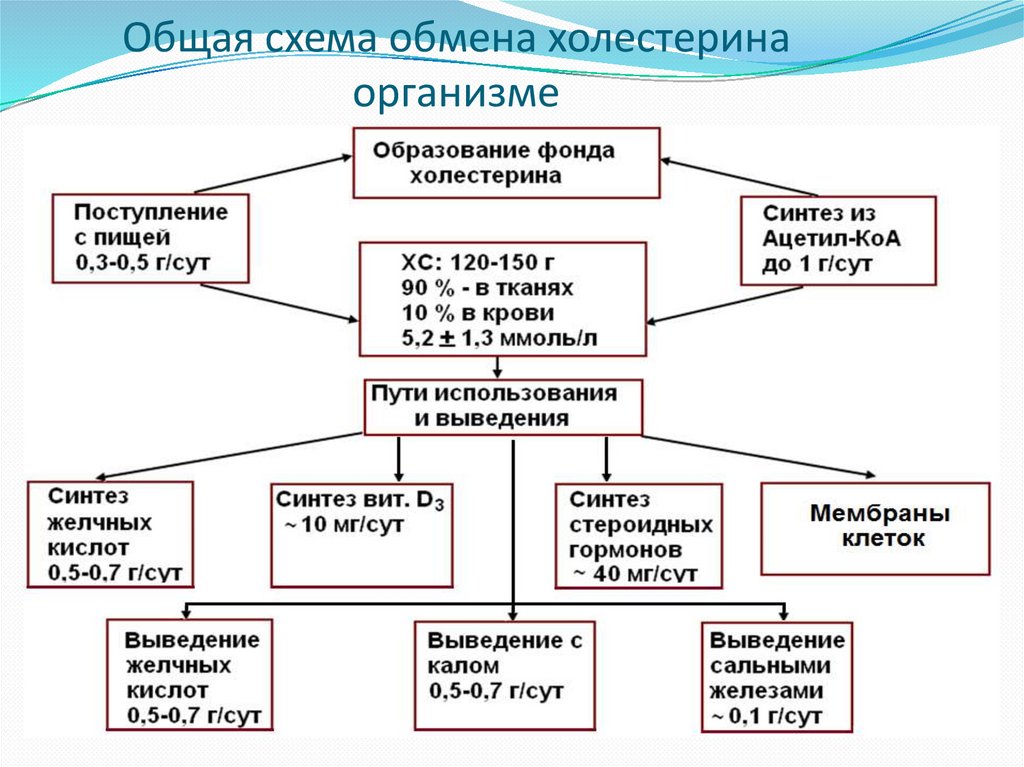
Общая схема обмена холестеринаорганизме
6.
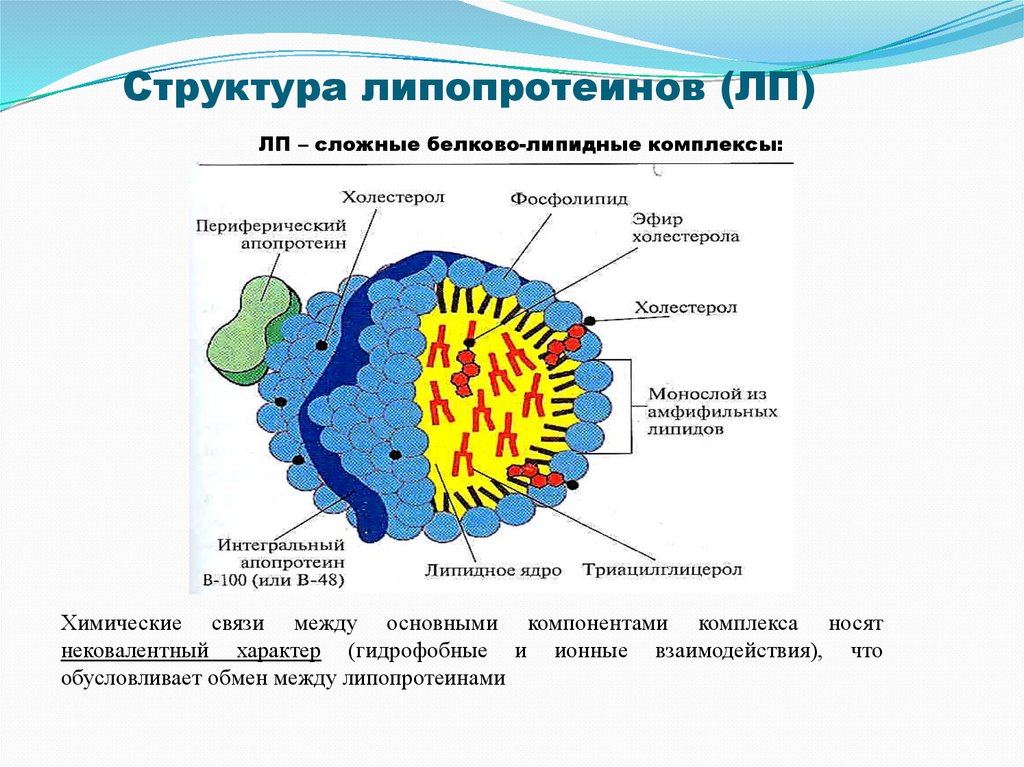
Структура липопротеинов (ЛП)ЛП – сложные белково-липидные комплексы:
Химические связи между основными компонентами комплекса носят
нековалентный характер (гидрофобные и ионные взаимодействия), что
обусловливает обмен между липопротеинами
6
7.
Транспортные формы холестеринаЛПНП (β-липопротеины)
ЛПОНП (пре-β-липопротеины)
ЛПНП+ЛПОНП
- атерогенные липопротеины
ЛПВП (альфа- ЛП) - антиатерогенные
липопротеины
8.
Биологическая роль ЛПТранспорт липидов:
ХМ (хиломикроны) – экзогенный жир из кишечника в
ткани
ЛПОНП (липопротеины очень низкой плотности) –
эндогенный жир, синтезированный в печени
ЛПНП (липопротеины низкой плотности) –
холестерин из печени в ткани через В, Е-рецепторы
ЛПВП (липопротеины высокой плотности) –
холестерин из тканей и ЛПНП в печень («обратный»
транспорт) при участии рецептора SR-BI и АТФ-связанных
кассетных транспортеров семейства ABC
Транспорт стероидных и тиреоидных гормонов,
жирорастворимых витаминов, ксенобиотиков,
лекарственных препаратов, генетического материала
8
9.
Синтез холестеролаРеакции синтеза холестерола происходят в цитозоле клеток. Это
один из самых длинных метаболических путей в организме
человека. Включает порядка 100 последовательных реакций. Всего
в обмене холестерола участвуют около 300 разных белков.
Источником всех атомов углерода в молекуле является
ацетил-SКоА, поступающий сюда из митохондрий в составе
цитрата, также как при синтезе жирных кислот. При
биосинтезе холестерола затрачивается 18 молекул АТФ и 13 молекул
восстановленного НАДФН+Н+.
Однако, условно в биосинтезе холестерина можно выделить 3
стадии:
1.
2.
3.
превращение ацетил-КоА в мевалоновую кислоту
образование из мевалоновой кислоты - сквалена
циклизация сквалена в холестерин
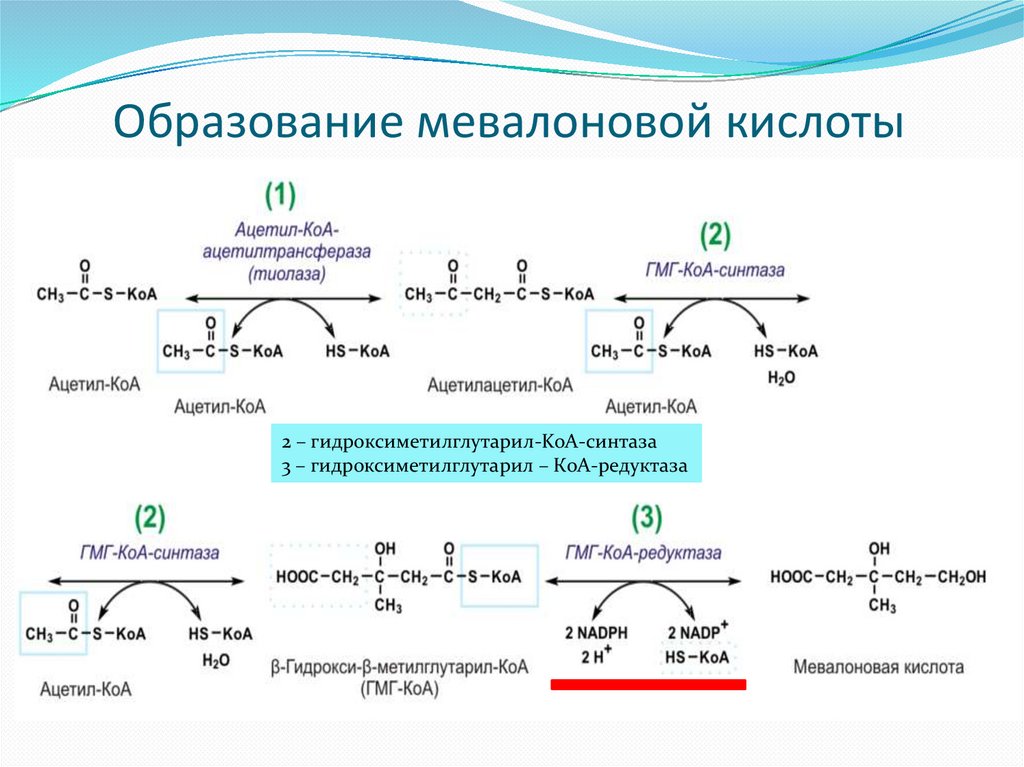
10.
Образование мевалоновой кислоты2 – гидроксиметилглутарил-KoA-синтаза
3 – гидроксиметилглутарил – КоА-редуктаза
11.
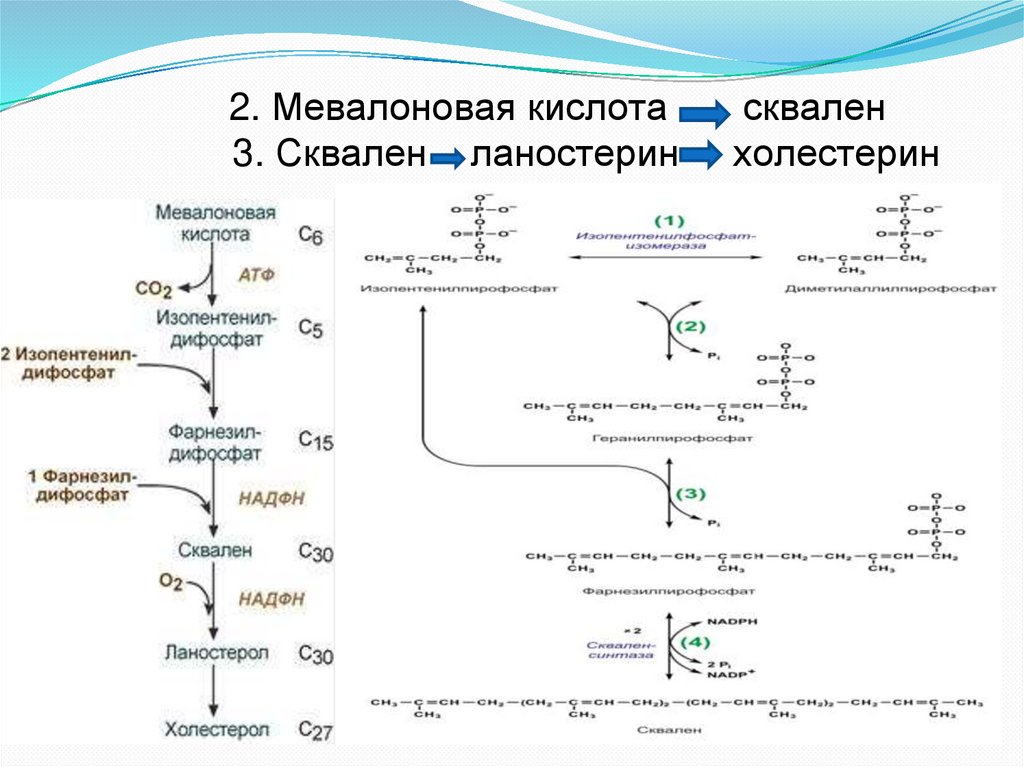
2. Мевалоновая кислота3. Сквален ланостерин
сквален
холестерин
12.
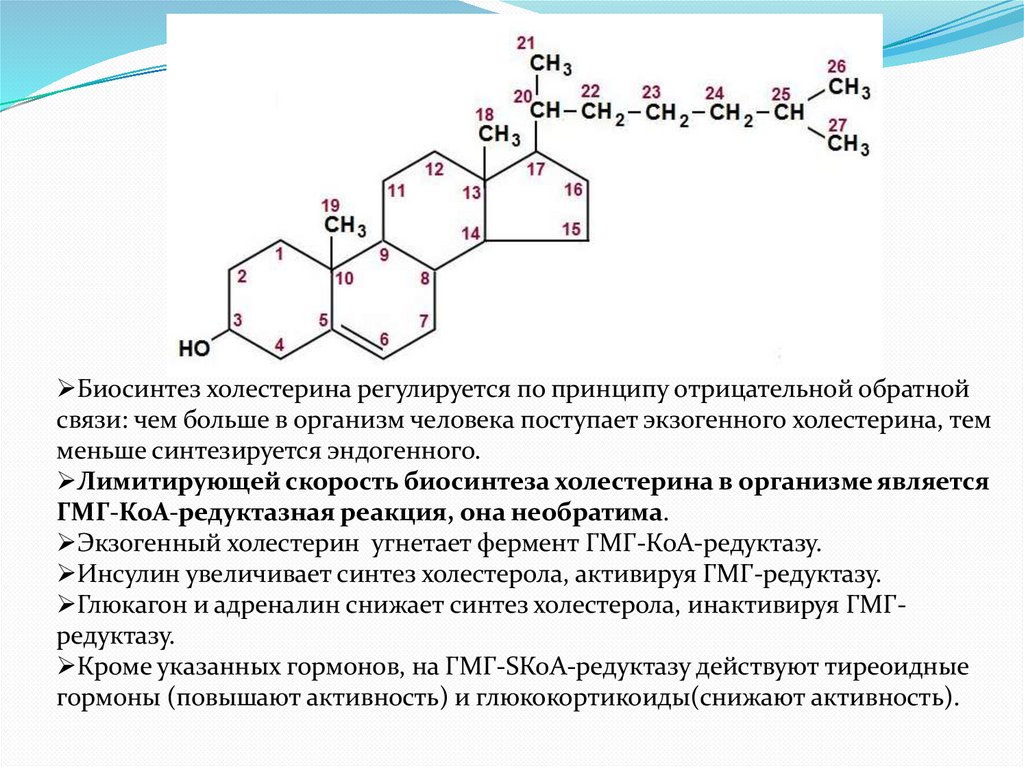
Биосинтез холестерина регулируется по принципу отрицательной обратнойсвязи: чем больше в организм человека поступает экзогенного холестерина, тем
меньше синтезируется эндогенного.
Лимитирующей скорость биосинтеза холестерина в организме является
ГМГ-КоА-редуктазная реакция, она необратима.
Экзогенный холестерин угнетает фермент ГМГ-КоА-редуктазу.
Инсулин увеличивает синтез холестерола, активируя ГМГ-редуктазу.
Глюкагон и адреналин снижает синтез холестерола, инактивируя ГМГредуктазу.
Кроме указанных гормонов, на ГМГ-SКоА-редуктазу действуют тиреоидные
гормоны (повышают активность) и глюкокортикоиды(снижают активность).
13.
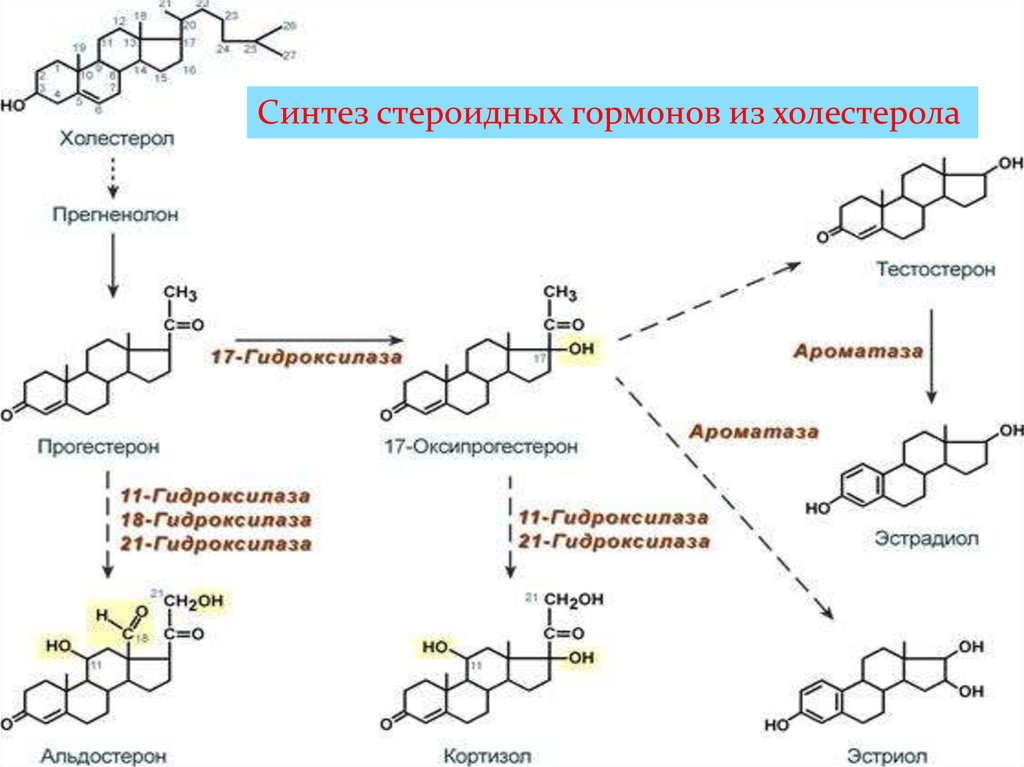
Синтез стероидных гормонов из холестерола14.
Образование желчных кислот из холестролаидет в эндоплазматическом ретикулуме при участии цитохрома
Р450, кислорода, НАДФН и аскорбиновой кислоты. 75%
холестерина, образуемого в печени, участвует в синтезе
желчных кислот.
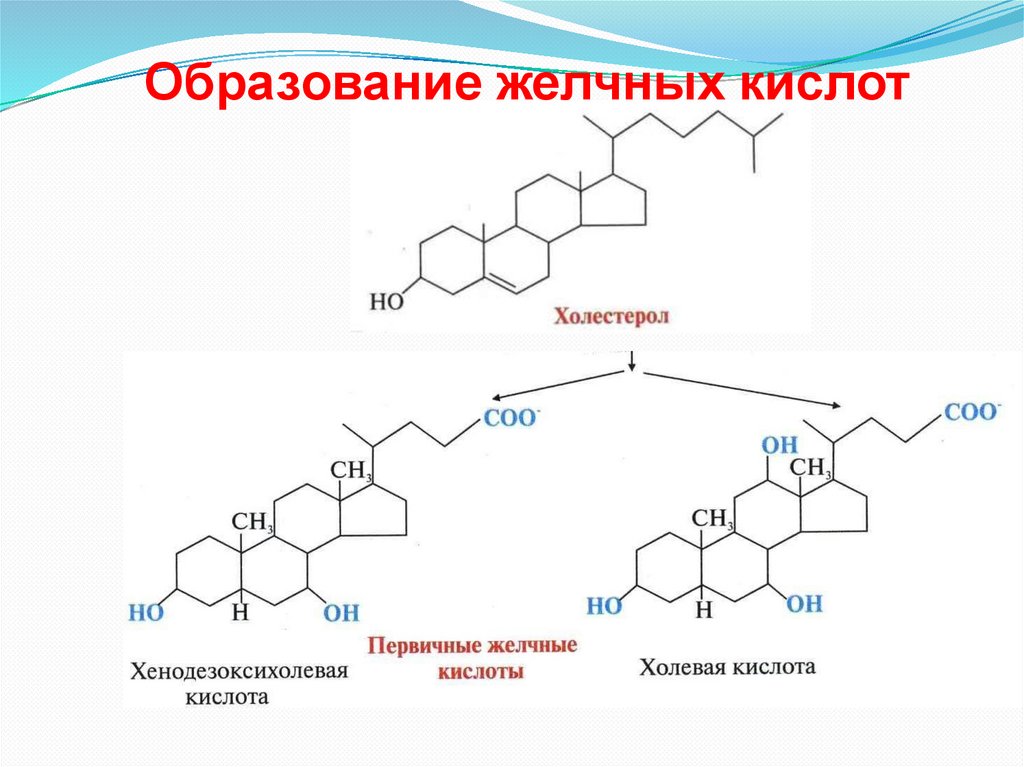
В печени синтезируются первичные желчные кислоты:
холевая (3α, 7β, 12α, гидроксилирована по С3, С7, С12),
хенодезоксихолевая (3α, 7α, гидроксилирована по С3, С7).
Затем они образуют парные желчные киcлоты – конъюгаты с
глицином (гликопроизводные) и с таурином
(тауропроизводные), в соотношении 3:1 соответственно.
В кишечнике под действием микрофлоры эти желчные кислоты
теряют OH-группу при С7 и превращаются во вторичные
желчные кислоты:
холевая в дезоксихолевую (3α, 12α, гидроксилирована
по С3 и С12),
хенодезоксихолевая в литохолевую (3α, гидроксилирована
только по С3)
15.
Образование желчных кислот16.
Желчные кислотывторичные
парные
17.
из холестерола18.
19.
20.
Выведение холестеролаСтруктурная
основа
холестерола
–
кольца
циклопентанпергидрофенантрена – не может быть расщеплена до
углекислого газа и воды, как другие органические компоненты
поступающие с пищей или синтезированные в организме.
Поэтому основное количество холестерола выводится в виде
желчных кислот.
Некоторое количество желчных кислот выделяется в неизменном
виде, а часть подвергается действию ферментов бактериальной
флоры кишечника. Продукты их разрушения (в основном
вторичные желчные кислоты) выводятся из организма
Часть молекул холестерола в кишечнике под действием ферментов
флоры восстанавливается по двойной связи в кольце В, в
результате чего образуется 2 типа молекул – холестанол и
копростанол, выводимые с фекалиями.
В сутки из организма выводится от 1,0 до 1,3 г холестерола,
основная часть удаляется с фекалиями.
21.
Нарушения обмена липидовПриобретенные
Патология обмена
нейтральных жиров
1. Ожирение
2. Жировое
перерожде
ние печени
Патология
обмена
холестерола
Врожденные
Дислипопро- Сфинголипидозы
теинемии
1. Желчекаме
н ная
болезнь
2. Атеросклероз
22.
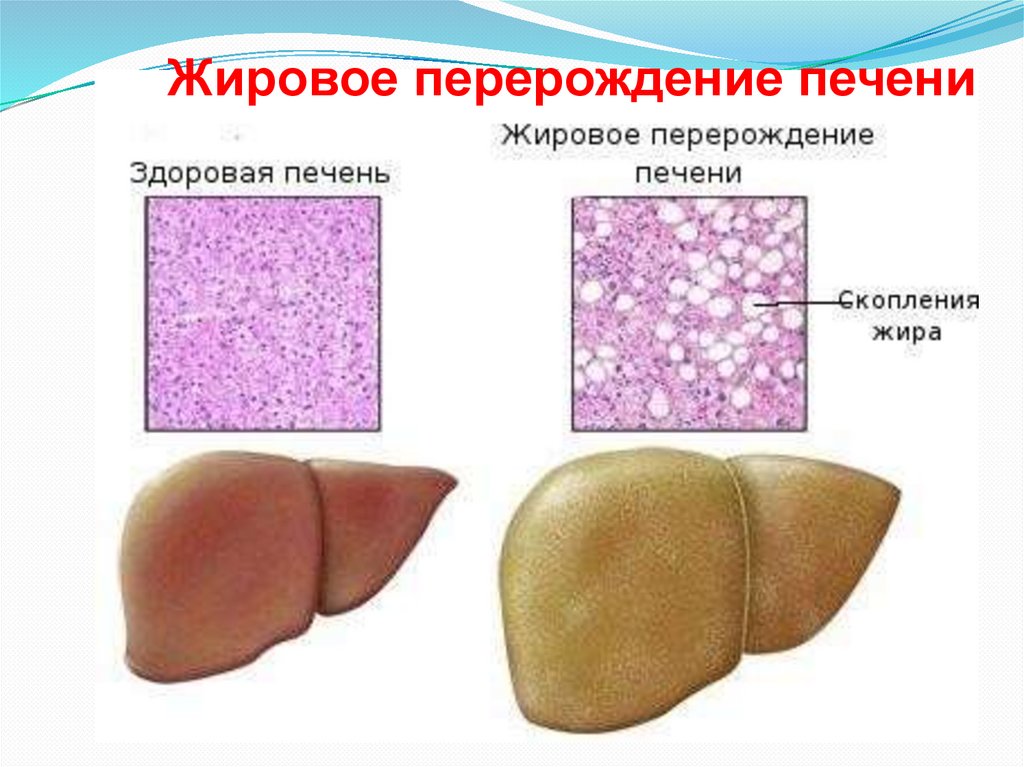
Жировое перерождение печени23.
Жировая инфильтрация печени (жировой гепатоз, стеатозпечени, жировая дистрофия) заключается в накоплении в цитозоле и
межклеточном пространстве печени триацилглицеролов в виде
жировых капель и в функциональной невозможности клеток их
удалить.
Главной причиной жировой инфильтрации печени является
метаболический блок синтеза ЛПОНП. Так как ЛПОНП включают
разнородные соединения, то блок может возникнуть на разных
уровнях синтеза:
нарушение секреции липопротеинов в кровь – патологии
мембран гепатоцитов при активации перекисного окисления липидов
вследствие недостаточности антиоксидантных систем (в первую
очередь гиповитаминозы С, А, Е, дефицит цинка и железа),
часто причиной может быть относительная недостаточность
апобелков и фосфолипидов при избытке ТАГ,
недостаток апобелков – нехватка белка или незаменимых
аминокислот в пище, воздействие токсинов и ингибиторов синтеза
белка,
снижение синтеза фосфолипидов – отсутствие липотропных
факторов (витаминов, метионина, полиненасыщенных жирных
кислот), из-за чего не формируется оболочка липопротеинов,
блок сборки липопротеиновых частиц в ЭПР при воздействии
токсинов (наример, хлороформ, мышьяк, свинец),
24.
НАРУШЕНИЯ ОБМЕНАХОЛЕСТЕРИНА
ЖЕЛЧНОКАМЕННАЯ
БОЛЕЗНЬ
АТЕРОСКЛЕРОЗ
25.
Причины жѐлчно-каменнойболезни
Избыток холестерина в пище
Гиперкалорийное питание
Повышенный синтез холестерина в печени
Снижение синтеза жѐлчных кислот
Снижение синтеза фосфолипидов
Застой жѐлчи
Нарушение гепатоэнтеральной циркуляции
жѐлчных кислот
Воспалительные заболевания жѐлчного
пузыря
26.
АтеросклерозАтеросклероз – это отложение холестерина и его эфиров в
соединительной ткани стенок артерий, в которых выражена
механическая нагрузка на стенку (по убыванию воздействия):
абдоминальная аорта, коронарная артерия, подколенная артерия,
бедренная артерия, тибиальная артерия, грудная аорта, дуга
грудной аорты, сонные артерии.
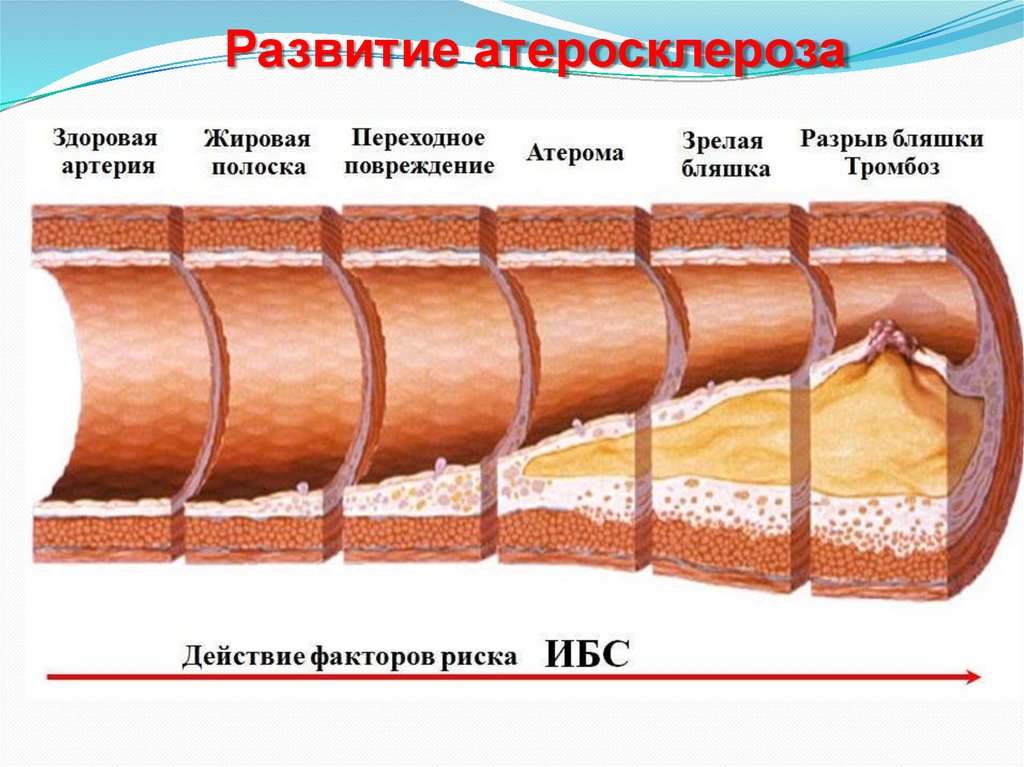
Стадии атеросклероза
Морфологически выделяют четыре стадии атеросклероза. Первая
и вторая стадии распространены широко и при правильном питании
являются обратимыми, 3 и 4 стадии уже имеют клиническое
значение и необратимы.
1 стадия – повреждение эндотелия
Это "долипидная" стадия, обнаруживается даже у годовалых детей.
Изменения этой стадии неспецифичны и ее могут вызывать:
дислипопротеинемия, гипертензия, повышение вязкости крови,
курение, вирусные и бактериальные инфекции, свинец, кадмий и
т.п.
На этой стадии в эндотелии создаются зоны повышенной
проницаемости и клейкости. Внешне это проявляется в
разрыхлении и истончении (вплоть до исчезновения) защитного
гликокаликса на поверхности эндотелиоцитов, расширении
межэндотелиальных щелей. Это приводит к усилению выхода
моноцитов и липопротеинов (ЛПНП и ЛПОНП) в интиму.
27.
2 стадия – стадия начальных измененийОтмечается у большинства детей и молодых людей.
Поврежденный эндотелий и активированные тромбоциты
вырабатывают медиаторы воспаления, факторы роста,
эндогенные окислители. В результате через поврежденный
эндотелий в интиму сосудов еще более активно проникают
моноциты и способствуют развитию воспаления. При этом ЛПНП,
попавшие под интиму, начинают изменяться
(модифицироваться), т.е. подвергаются окислению,
гликозилированию, ацетилированию.
Моноциты, преобразуясь в макрофаги, активно поглощают
измененные липопротеины при участии "мусорных" рецепторов
(scavenger ['skævɪnʤə] receptors). Таким образом, поглощение
модифицированных ЛПНП макрофагами идет без участия апоВ100-рецепторов, а, значит, нерегулируемо.
При поглощении модифицированных липопротеинов макрофаги
активируются, выделяют цитокины и разнообразные факторы
роста, которые стимулируют деление гладкомышечных клеток,
синтез межклеточного вещества, и играют роль в развитии
атеросклеротической бляшки.
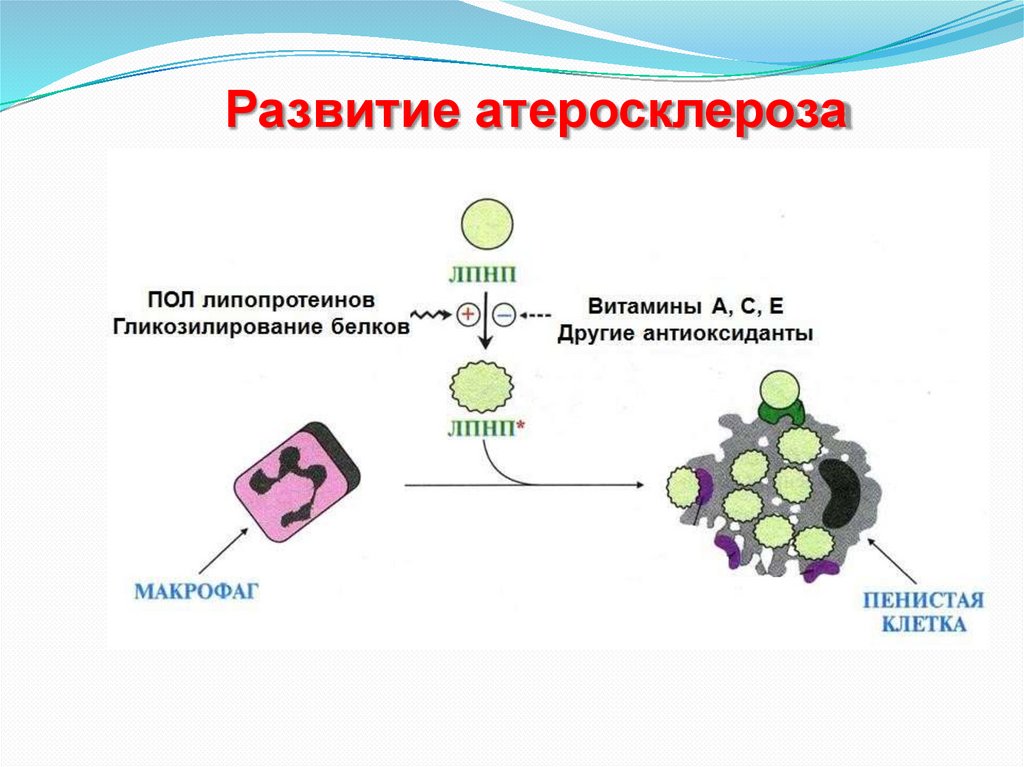
28.
Окисление ЛПНП нарастает при недостаточной активностиантиоксидантных систем – гиповитаминозах Е и С,
нехватке металлов (железо, селен, медь, цинк), входящих
в состав антиоксидантных ферментов каталазы,
пероксидазы, супероксиддисмутазы.
Гликозилирование белков ЛПНП ускоряется при сахарном
диабете или при других хронических гипергликемиях.
Такие модифицированные липопротеины теряют
способность связываться с апоВ-100-рецептором и
проникать в клетки-мишени и, в результате,
накапливаются в крови и в интиме сосудов.
Под действием факторов роста гладкомышечные клетки
медии мигрируют в интиму и начинают пролиферировать,
превращаясь в макрофагоподобные клетки. Они также
накапливают модифицированные ЛПНП.
Накопление липидов в макрофагах быстро исчерпывает
невысокие возможности клеток по утилизации свободного
и этерифицированного ХС. Они переполняются стероидами
и превращаются в пенистые клетки. Внешне на эндотелии
появляются липидные пятна и полоски.
29.
3 стадия – стадия поздних измененийПродолжают развертываться и приобретают масштабность
события, начавшиеся на второй стадии.
Внешне проявляется как выступание поверхности в
просвет сосуда. Стадия дополнительно характеризуется
следующими особенностями:
увеличение количества коллагена, эластина и
гликозаминогликанов, т.е. накопление межклеточного
вещества,
пролиферация и гибель пенистых клеток (апоптоз),
накопление в межклеточном пространстве свободного ХС
и этерифицированного ХС,
инкапсулирование холестерола и формирование
фиброзной бляшки.
4 стадия – стадия осложнений
На этой стадии происходят:
кальцификация бляшки и ее изъязвление, приводящее к
эмболии сосудов,
тромбоз из-за адгезии и активации тромбоцитов, разрыв
сосуда.
30.
Атерогенные факторыдислипидемия
гипертензия
табакокурение
атеросклероз
ожирение
гиподинамия
сахарный диабет
31.
Развитие атеросклероза32.
Развитие атеросклероза33.
Ожирение – чрезмерное накопление нейтрального(резервного) жира.
Причины:
Чрезмерное питание, в особенности углеводами;
Эндокринные заболевания;
Наследственная патология
Нарушение обмена липопротеинов
Наследственные заболевания, приводящие к
гиперлипопротеинемии или гиполипопротеинемии
Гиперлипопротеинемии:
I тип. Гиперхиломикронемия. Характеризуется медленным
выведением хиломикронов, которые постепенно
накапливаются в крови. Резко увеличивается в крови
концентрация триглицеридов.
34.
II тип. Гипер-β-липопротеинемия.IIа – характеризуется увеличением в
крови преимущественно ЛПНП
IIб – характеризуется одновременным
увеличением в крови ЛПНП и ЛПОНП.
При этом типе значительно возрастает
концентрация холестерина в крови, что
увеличивает вероятность развития атеросклероза
35.
III тип. Дис-β-липопротеинемия.Характеризуется появлением в крови
липопротеинов с необычно высоким содержанием
холестерина. Такие липопротеины накапливаются
в крови вследствие нарушения превращения
ЛПОНП в ЛПНП
IV тип. Гиперпре- β-липопротеинемия.
Характеризуется значительным ростом ЛПОНП
при нормальном содержании в крови ЛПНП. При
этом уровень холестерина повышен
незначительно.
V тип. Гиперпре- β-липопротеинемия и
хиломикронемия.
Характеризуется одновременным ростом в крови
содержания ЛПОНП и ХМ
36.
Болезни накопления липидов (Липидозы)Сфинголипидозы – в тканях, в особенности в
нервной, накапливаются сфинголипиды.
При этом нарушен распад запасаемых липидов,
тогда как скорость биосинтеза сфинголипидов
сравнима со скоростью биосинтеза их у здоровых
людей





















 biology
biology








