Similar presentations:
Люпус-нефрит: сучасні діагностичні критерії, перспективи лікування (Рекомендації EULAR, ACR)
1.
Люпус-нефрит:сучасні діагностичні
критерії, перспективи
лікування
(Рекомендації EULAR, ACR)
Шаповал І.І.
2.
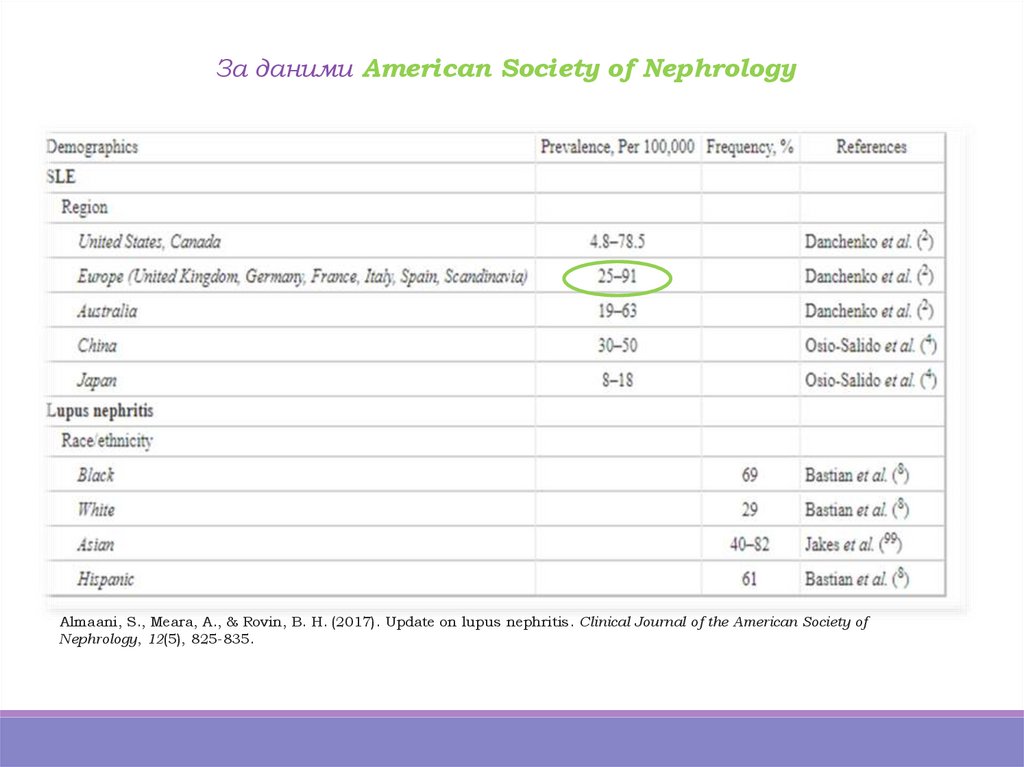
За даними American Society of NephrologyAlmaani, S., Meara, A., & Rovin, B. H. (2017). Update on lupus nephritis. Clinical Journal of the American Society of
Nephrology, 12(5), 825-835.
3.
1997ACR
revised
criteria
Наявність
4 з 11
критеріїв
підтверджують
діагноз СЧВ
Tan EM, Cohen AS, Fries JF, Masi AT, McShane DJ, Rothfield NF, et al. The 1982 revised criteria for
the classification of systemic lupus erythematosus. Arthritis Rheum 1982;25:1271---7. and Hochberg
MC. Updating the American College of Rheumatology revised criteria for the classification of systemic
lupus erythematosus [letter]. Arthritis Rheum 1997;40:1725.
4.
2012SLICC
criteria
Наявність
4 з 11 критеріїв
підтверджують
діагноз СЧВ
5.
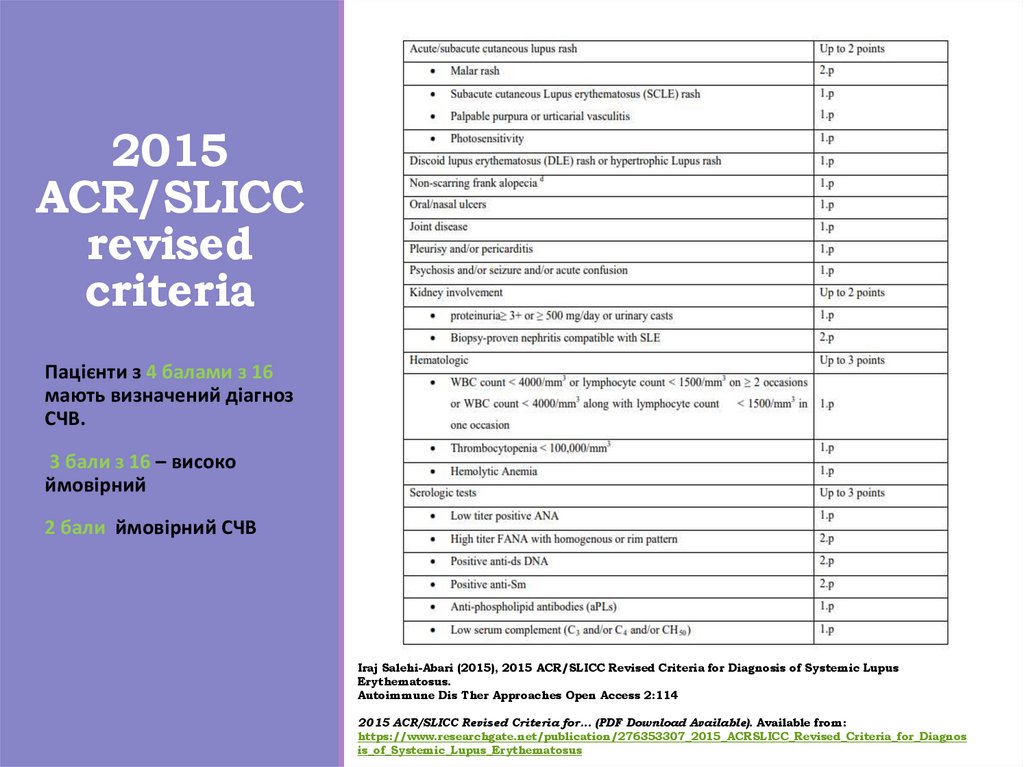
2015ACR/SLICC
revised
criteria
Пацієнти з 4 балами з 16
мають визначений діагноз
СЧВ.
3 бали з 16 – високо
ймовірний
2 бали ймовірний СЧВ
Iraj Salehi-Abari (2015), 2015 ACR/SLICC Revised Criteria for Diagnosis of Systemic Lupus
Erythematosus.
Autoimmune Dis Ther Approaches Open Access 2:114
2015 ACR/SLICC Revised Criteria for... (PDF Download Available). Available from:
https://www.researchgate.net/publication/276353307_2015_ACRSLICC_Revised_Criteria_for_Diagnos
is_of_Systemic_Lupus_Erythematosus
6.
New SLE Criteria Under Development:A Joint Effort of the ACR & EULAR
"SLE is a heterogeneous disease, a disease without a gold standard for
diagnosis," said Sindhu Johnson, MD, PhD, from the University of
Toronto.
Available
on
JUNE 2018
Johnson S. European League Against Rheumatism and American College of Rheumatology present new SLE classification criteria at the 2017 ACR/ARHP
annual meeting. Presentation at: ACR/ARHP 2017 Annual Meeting; November 3-8, 2017; San Diego, CA.
7.
8.
Покази для нефробіопсії при СЧВБудь-яке ураження нирок, зокрема, наявність
персистуючої протеїнурії≥0,5 г/добу (С),
особливо з клубочковою гематурією та
лейкоцитурією є показом для біопсії нирок.
Результати
біопсії
повинні
оцінюватись
згідно
класифікації ISN/RPS 2003
Dooley MA. Clinical and epidemiologic features of lupus nephritis. Wallace DJ, Hahn BH, eds. Dubois' Lupus Erythematosus and Related Syndromes. 8th ed.
Philadelphia,PA: Elsevier Saunders; 2013. 438-54.
Grande JP, Balow JE. Renal biopsy in lupus nephritis. Lupus. 1998. 7(9):611-7.
9.
Класифікація ЛН (ISN/RPS 2003)International Society of Nephrology/Renal Pathology Society
Class I – Мінімальний мезангіальний ЛН
Class II – Мезангіо-проліферативний ЛН
Class III – Фокальний проліферативний ЛН (<50% клубочків)
ІІІ (А) - активний фокальний проліферативний ЛН
ІІІ (А/С) – активний проліферативний зі склерозом ЛН
ІІІ (С) – неактивний з фокальним склерозом ЛН
Class IV–Дифузний проліферативний ЛН (50% або > клубочків)
IV (A), IV (A/C), IV (C)
Class V – Мембранозний ЛН
Class VI – Склерозуючий ЛН (>90% склерозованих клубочків)
Weening JJ, D'Agati VD, Schwartz MM, et al. The classification of glomerulonephritis in systemic lupus
erythematosus revisited. J Am Soc Nephrol. Feb 2004;15(2):241-50.
10.
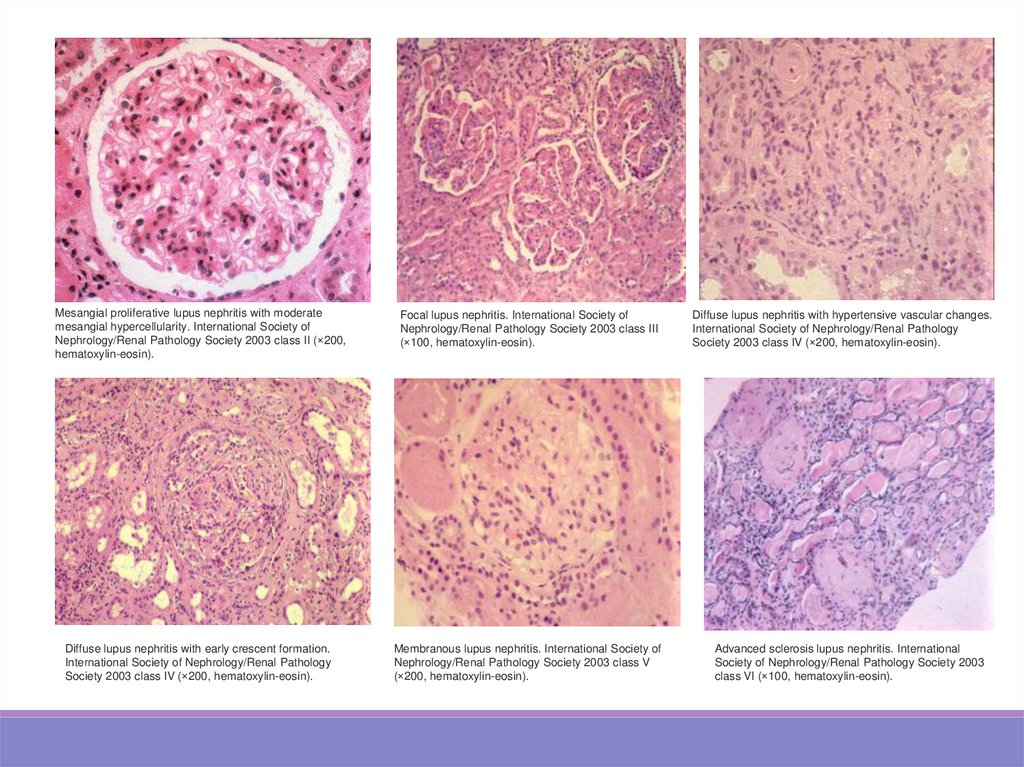
Mesangial proliferative lupus nephritis with moderatemesangial hypercellularity. International Society of
Nephrology/Renal Pathology Society 2003 class II (×200,
hematoxylin-eosin).
Focal lupus nephritis. International Society of
Nephrology/Renal Pathology Society 2003 class III
(×100, hematoxylin-eosin).
Diffuse lupus nephritis with hypertensive vascular changes.
International Society of Nephrology/Renal Pathology
Society 2003 class IV (×200, hematoxylin-eosin).
Diffuse lupus nephritis with early crescent formation.
International Society of Nephrology/Renal Pathology
Society 2003 class IV (×200, hematoxylin-eosin).
Membranous lupus nephritis. International Society of
Nephrology/Renal Pathology Society 2003 class V
(×200, hematoxylin-eosin).
Advanced sclerosis lupus nephritis. International
Society of Nephrology/Renal Pathology Society 2003
class VI (×100, hematoxylin-eosin).
11.
Показидо імуносупресивної терапії
Для початку імуносупресивної терапії слід керуватися
результатами біопсії нирок (А).
Імунодепресанти рекомендовані в класі IIIA або IIIA/С (±V)
та IVA або IVA/С (±V), а також в V класі ЛН, якщо рівень
протеїнурії перевищує 1 г/добу, не зважаючи на
оптимальне використання блокаторів РААС
12.
Мета−збереження функції нирок,
−профілактика загострень хвороби,
−попередження ускладнень,
−поліпшення якості життя і виживання.
Прогностичне значення повної ниркової відповіді (Б/Кр <50
мг/ммоль і нормальною або майже нормальною ШКФ)
Прогностичне значення часткової ниркової відповіді
(зниження протеїнурії і нормальною або майже нормальною
ШКФ ≥50%)
13.
EULARRecommendations
2012
14.
Індукційна терапія ЛНДля пацієнтів з IIIA або IIIA/С (±V) та IVA або IVA/С (±V) класами
ЛН:
мофетилу мікофенолат- 3 г/день 6 міс. (А)
або
циклофосфамід – загальна доза 3г на 3 міс. (В) в комбінації з
ГКС.
Для більшої ефективності розпочинають з пульс-терапії
метилпреднізолоном 500-750 мг в/в №3 з подальшим
переходом на пероральний прийом преднізолону 0,5 мг/кг/день
(4 тижні), знижуючи дозу до <10 мг/день за 4-6 міс.
15.
Індукційна терапія ЛНДля пацієнтів з IIIA або IIIA/С (±V) та IVA або IVA/С (±V) класами ЛН та
факторами несприятливого перебігу:
−зниженням функції нирок
−появою півмісяців
−фібриноїдним некрозом
Використовують мофетилу мікофенолат- 3 г/день 6 міс.
або
циклофосфамід – в більш високих дозах в/в (0,75-1 г/м2) щомісяця
протягом 6 міс. або перорально (2-2,5 мг/кг/день) протягом 3 міс.
в комбінації з ГКС (пульс-терапія метилпреднізолоном з подальшим
переходом на пероральний прийом преднізолону 1 мг/кг/день)
16.
Індукційна терапія ЛНДля пацієнтів з V класом ЛН з нефротичним синдромом:
мофетилу мікофенолат- 3 г/день 6 міс.
в комбінації з пероральним прийомом преднізолону
0,5 мг/кг/день.
Циклофосфамід, циклоспорин, такролімус або
ритуксимаб рекомендовані як альтернативний
варіант для нон-респондерів.
17.
Індукційна терапія ЛНЯк альтернатива мофетилу мікофенолату та
циклофосфаміду може розглядатися азатіоприн у дозі 2
мг/кг/день у окремих пацієнтів без несприятливих
прогностичних факторів та за умов, коли дані препарати:
−протипоказані
−непереносимість до ММФ, ЦФ
−недоступні
18.
Підтримуюча терапія ЛННизькі дози
мофетилу мікофенолату- 2 г/день ( не > 3 років)
або
азатіоприну– 2 мг/кг/день ( не > 3 років)
в комбінації з низькими дозами
преднізолону 5-7,5 мг/день.
У випадку рефрактерності до стандартної терапії:
ЦФ
ММФ або ММФ
ЦФ або ритуксимаб
19.
Допоміжна терапія ЛНІнгібітори АПФ або БРА - хворим з протеїнурією (білок/креатинін
сечі>50 мг/ммоль) або гіпертензією
Статини- хворим з дисліпідемією (цільовий рівень ЛПНЩ-ХС 2,58
ммоль/л (100 мг/дл))
Гідроксихлорохін (200-400 мг/добу)- для попередження загострень
та зниження кардіоваскулярних та ренальних ризиків
Ацетилсаліцилова кислота- у хворих з наявністю антифосфоліпідних
АТ
Антикоагулянти – у хворих з нефротичним синдромом з рівнем
альбуміну <20 г/л
20.
Моніторинг і прогноз ЛНАктивний ЛН слід регулярно контролювати шляхом
визначення в кожний візит: маси тіла, артеріального
тиску, сироваткового креатиніну і ШКФ, сироваткового
альбумін, протеїнурія, сечового осаду (мікроскопічна
оцінка), сироваткових рівнів С3 і С4, сироваткові рівні
анти-ДНК антитіл і загального аналізу крові.
Візити повинні бути заплановані кожні 2-4 тижні
протягом перших 2-4 місяців після постановки діагнозу
або загострення, а потім залежно до відповіді на
лікування протягом усього життя, принаймні кожні 3-6
місяців.
Повторна нефробіопсія може використовуватись у
випадках
погіршення стану або рефрактерності до
імуносупресивної або біологічної терапії (нездатність
знизити протеїнурію ≥50%, персистуюча протеїнурія
більше 1 року та/або погіршення ШКФ), або при рецидиві
21.
ACR Guidelines2012
22.
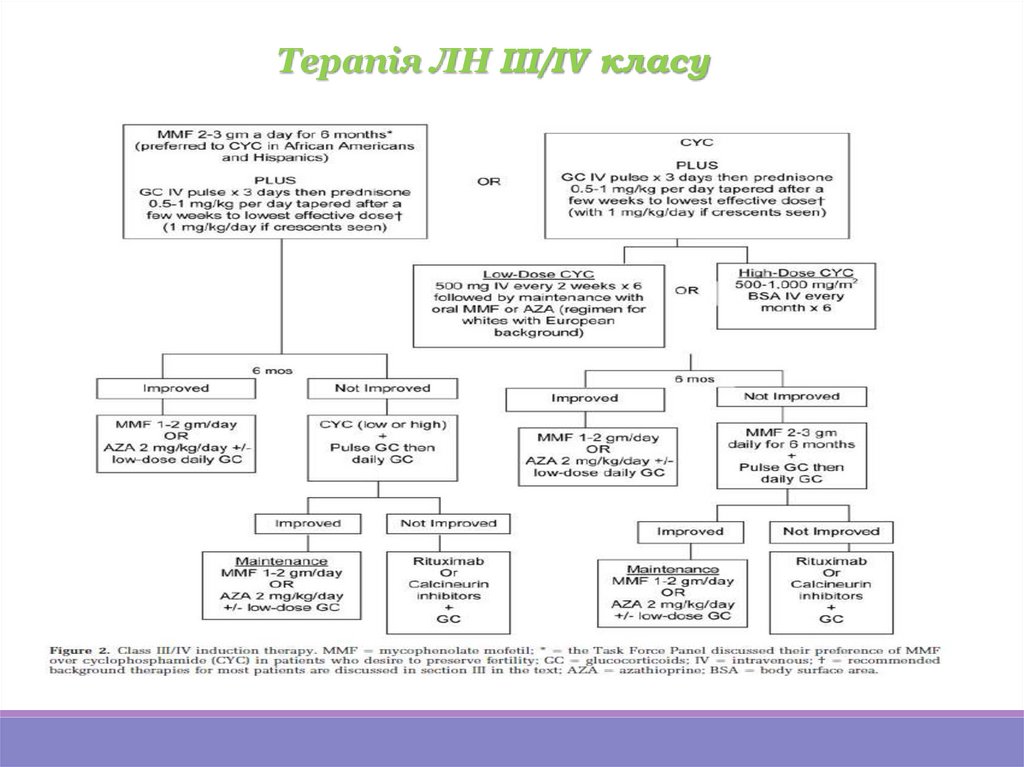
Терапія ЛН III/IV класу23.
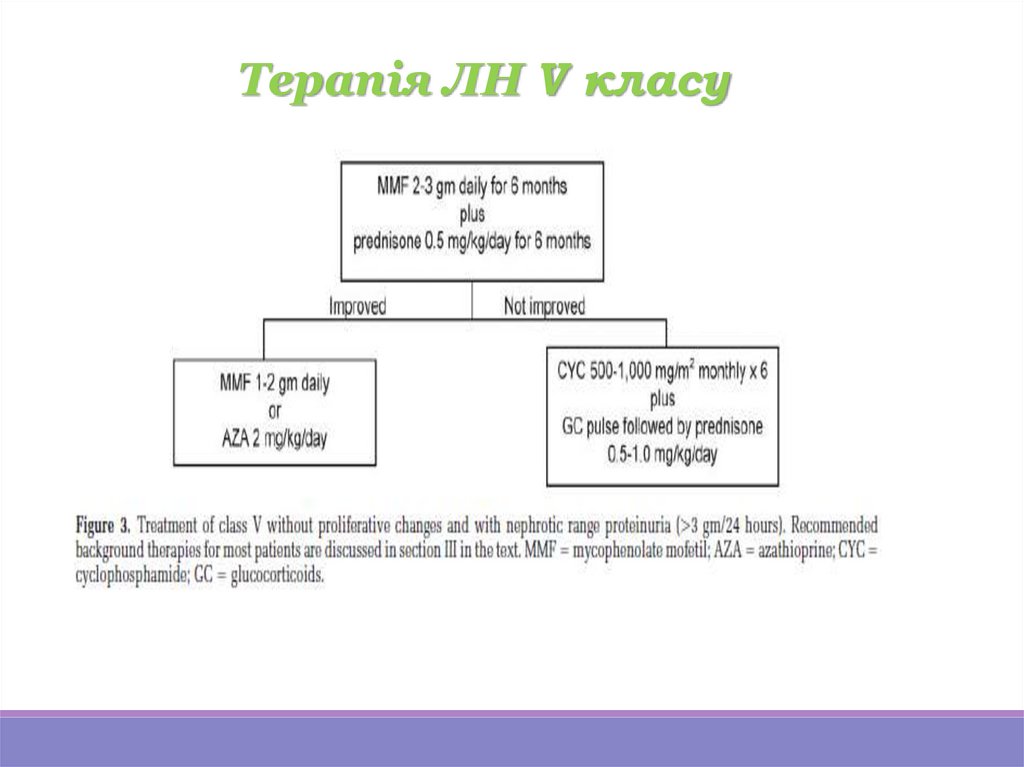
Терапія ЛН V класу24.
Перспективи лікування ЛН та СЧВРитуксимаб (анти-CD20 моноклональні антитіла) ефективний препарат як для лікування СЧВ, так і ЛН
Silverman GJ. Anti-CD20 therapy in systemic lupus erythematosus: a step closer to the clinic. Arthritis Rheum. 2005 Feb. 52(2):371-7.
Looney RJ, Anolik JH, Campbell D, Felgar RE, Young F, Arend LJ. B cell depletion as a novel treatment for systemic lupus erythematosus: a phase I/II dose-escalation trial of rituximab. Arthritis Rheum. 2004 Aug.
50(8):2580-9.
Leandro MJ, Cambridge G, Edwards JC, Ehrenstein MR, Isenberg DA. B-cell depletion in the treatment of patients with systemic lupus erythematosus: a longitudinal analysis of 24 patients. Rheumatology
(Oxford). 2005 Dec. 44(12):1542-5.
Ng KP, Leandro MJ, Edwards JC, Ehrenstein MR, Cambridge G, Isenberg DA. Repeated B cell depletion in treatment of refractory systemic lupus erythematosus. Ann Rheum Dis. 2006 Jul. 65(7):942-5.
Merrill JT, Neuwelt CM, Wallace DJ, et al. Efficacy and safety of rituximab in moderately-to-severely active systemic lupus erythematosus: the randomized, double-blind, phase II/III systemic lupus
erythematosus evaluation of rituximab trial. Arthritis Rheum. 2010 Jan. 62(1):222-33.
Rovin BH, Furie R, Latinis K, Looney RJ, Fervenza FC, Sanchez-Guerrero J, et al. Efficacy and safety of rituximab in patients with active proliferative lupus nephritis: the Lupus Nephritis Assessment with
Rituximab study. Arthritis Rheum. 2012 Apr. 64 (4):1215-26.
Белімумаб (Бенліста) (моноклональні антитіла проти стимулятора B-лімфоцитів BLyS)
затверджено FDA для застосування у пацієнтів з активним СЧВ
Kirou KA, Salmon JE, Crow MK. Soluble mediators as therapeutic targets in systemic lupus erythematosus: cytokines, immunoglobulin receptors, and the complement system. Rheum Dis Clin North Am. 2006
Feb. 32(1):103-19, ix.
Wallace DJ, Stohl W, Furie RA, et al. A phase II, randomized, double-blind, placebo-controlled, dose-ranging study of belimumab in patients with active systemic lupus erythematosus. Arthritis Rheum. 2009 Sep
15. 61(9):1168-78.
Jacobi AM, Huang W, Wang T, et al. Effect of long-term belimumab treatment on B cells in systemic lupus erythematosus: extension of a phase II, double-blind, placebo-controlled, dose-ranging study. Arthritis
Rheum. 2010 Jan. 62(1):201-10.
Воклоспорин (новий інгібітор кальційневрину) відбувається III фаза клінічного дослідження
Harrison P. Novel Regimen Showing Promise, a First in Lupus Nephritis. Medscape Medical News. Available at https://www.medscape.com/viewarticle/872186. November 21, 2016; Accessed: November 16,
2017.
Aurinia Renal Response in Active Lupus With Voclosporin (AURORA). ClinicalTrials.gov. Available at https://clinicaltrials.gov/ct2/show/NCT03021499. November 2017; Accessed: November 16, 2017.
Атацісепт (гібридний білок TACI-Ig, який інгібує BLyS та ліганд, що викликає проліферацію) у
дослідженні було продемонстровано дозозалежне зниження рівня В-клітин та імуноглобулінів.
Dall'Era M, Chakravarty E, Wallace D, et al. Reduced B lymphocyte and immunoglobulin levels after atacicept treatment in patients with systemic lupus erythematosus: results of a multicenter, phase Ib,
double-blind, placebo-controlled, dose-escalating trial. Arthritis Rheum. 2007 Dec. 56(12):4142-50.
Абетімус (толероген B-лімфоцитів) виявився неефективним у запобіганні загострень ЛН, хоча знижував
рівень анти-ДНК-антитіл. Furie R. Abetimus sodium (riquent) for the prevention of nephritic flares in patients with systemic lupus erythematosus. Rheum Dis Clin North Am. 2006 Feb.
32(1):149-56, x.
Антицитокінові терапії спрямовані проти :Інтерферону-α, ІЛ -1, ІЛ-6, ІЛ-10, іФНП-α
Kirou KA, Salmon JE, Crow MK. Soluble mediators as therapeutic targets in systemic lupus erythematosus: cytokines, immunoglobulin receptors, and the complement
system. Rheum Dis Clin North Am. 2006 Feb. 32(1):103-19, ix.
25.
Дякую заувагу!



















 medicine
medicine