Similar presentations:
Обмен белков
1.
Обмен белков2. Азотистый баланс
АЗОТИСТЫЙ БАЛАНСРавновесие
Положительный
Отрицательный
3. Источники и пути расходования аминокислот
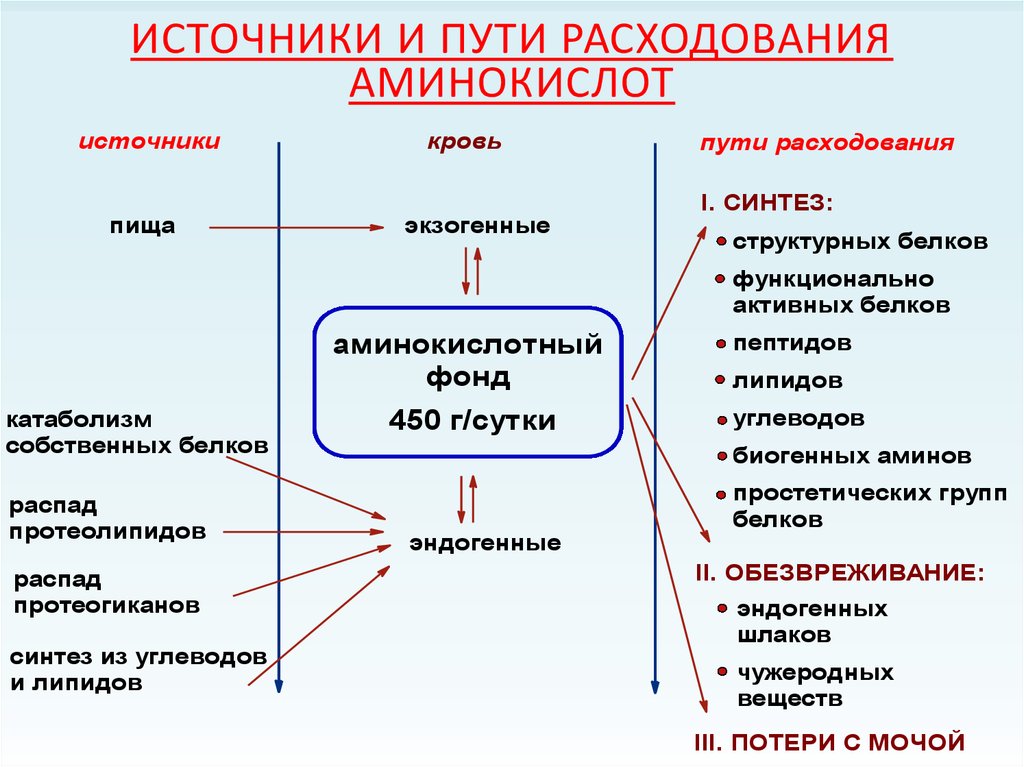
ИСТОЧНИКИ И ПУТИ РАСХОДОВАНИЯАМИНОКИСЛОТ
источники
пища
кровь
экзогенные
пути расходования
I. CИНТЕЗ:
структурных белков
функционально
активных белков
катаболизм
собственных белков
распад
протеолипидов
распад
протеогиканов
синтез из углеводов
и липидов
аминокислотный
фонд
пептидов
450 г/сутки
углеводов
липидов
биогенных аминов
эндогенные
простетических групп
белков
II. ОБЕЗВРЕЖИВАНИЕ:
эндогенных
шлаков
чужеродных
веществ
III. ПОТЕРИ С МОЧОЙ
4. Заменимые и незаменимые аминокислоты
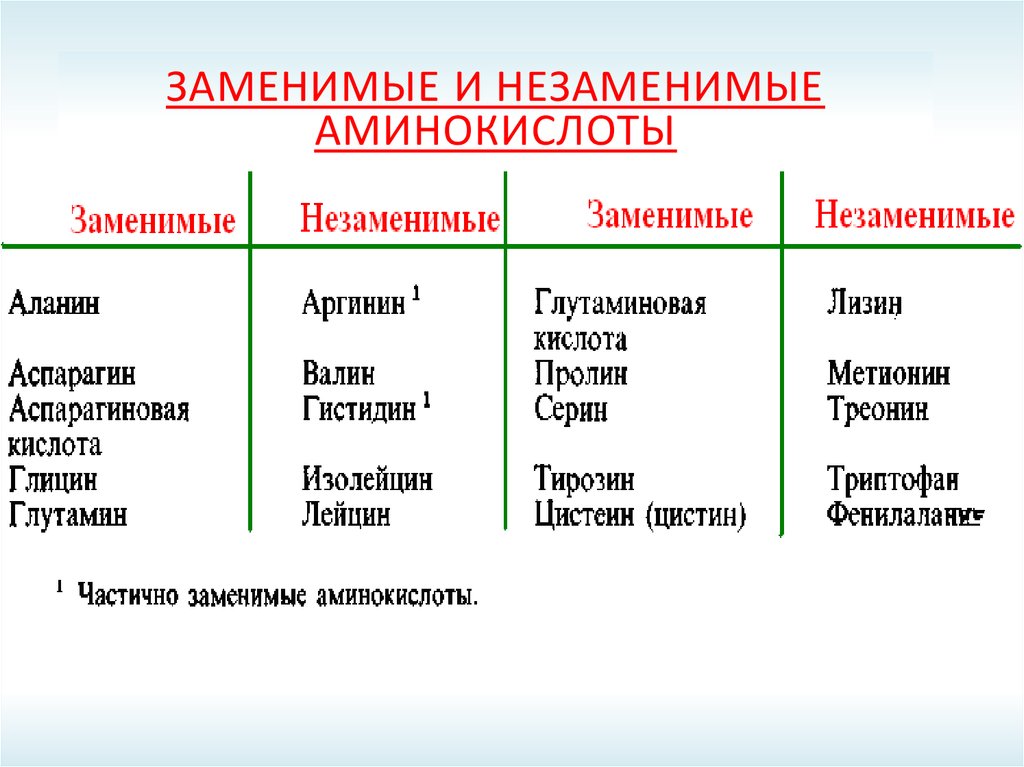
ЗАМЕНИМЫЕ И НЕЗАМЕНИМЫЕАМИНОКИСЛОТЫ
5. Количество белка в некоторых пищевых продуктах
КОЛИЧЕСТВО БЕЛКА В НЕКОТОРЫХПИЩЕВЫХ ПРОДУКТАХ
6. Содержание незаменимых аминокислот в белках различного происхождения
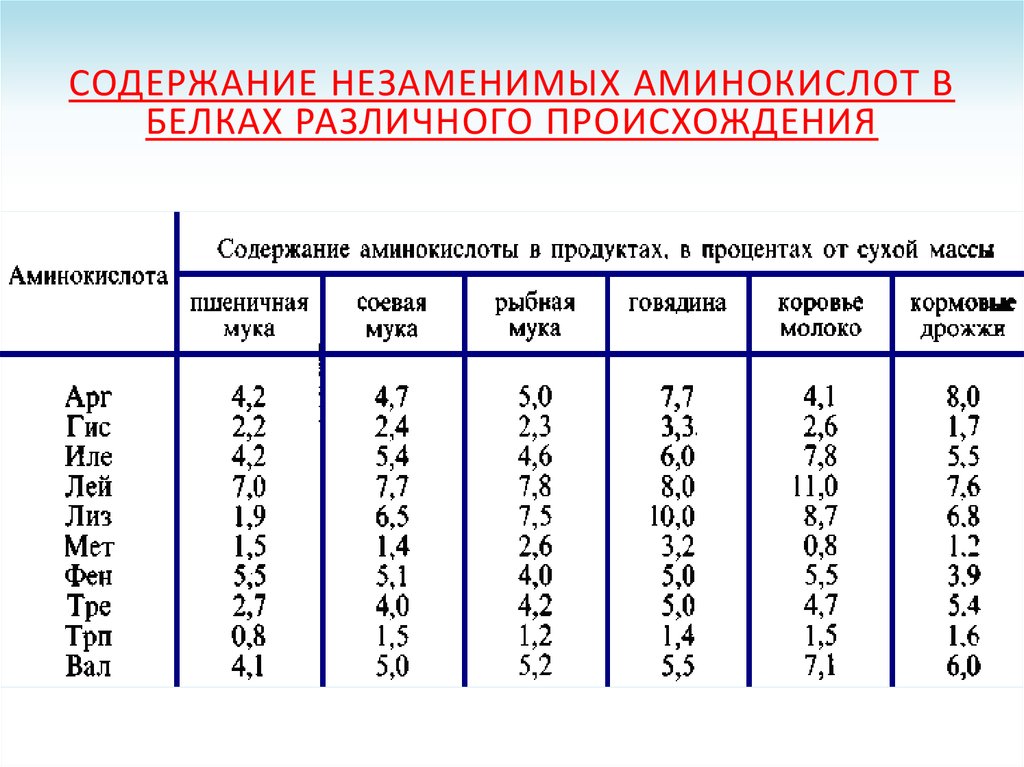
СОДЕРЖАНИЕ НЕЗАМЕНИМЫХ АМИНОКИСЛОТ ВБЕЛКАХ РАЗЛИЧНОГО ПРОИСХОЖДЕНИЯ
7. Протеиназы ЖКТ
ПРОТЕИНАЗЫ ЖКТЭндопептидазы
Экзопептидазы
Пепсин;
Карбоксипептидазы А и В;
Реннин;
Аминопептидазы;
Гастриксин;
Дипептидазы;
Трипсин;
Трипептидазы.
Химотрипсин;
Эластаза.
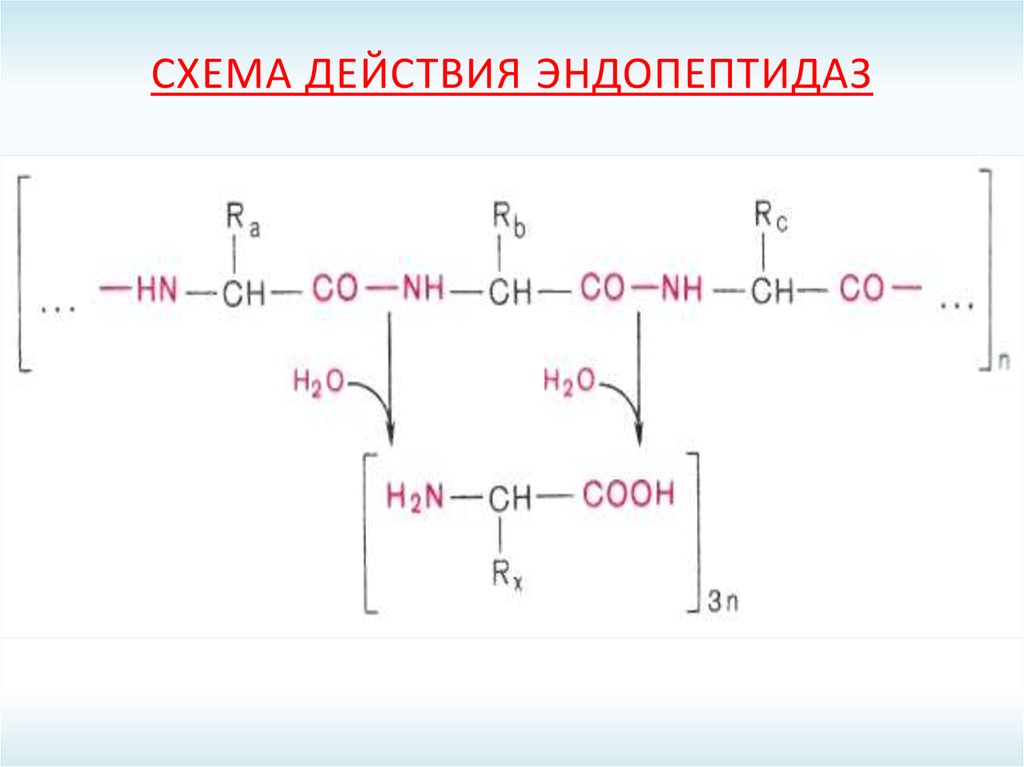
8. Схема действия эндопептидаз
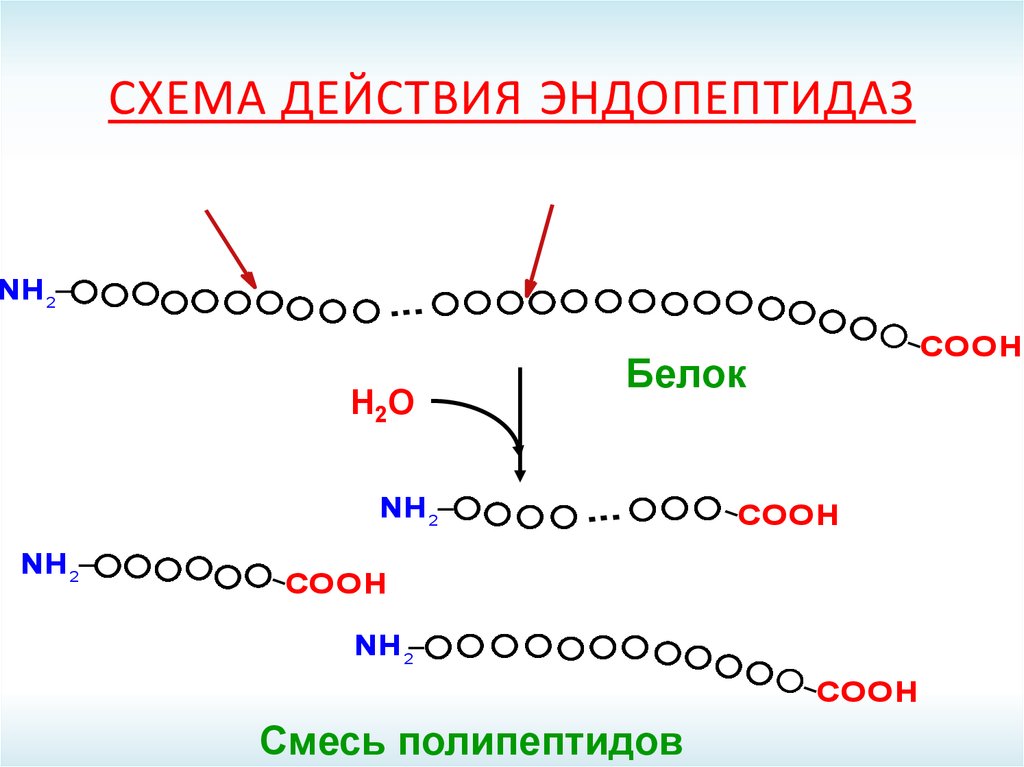
СХЕМА ДЕЙСТВИЯ ЭНДОПЕПТИДАЗ9. Схема действия эндопептидаз
СХЕМА ДЕЙСТВИЯ ЭНДОПЕПТИДАЗNН 2
...
Белок
Н2О
NН 2
NН 2
COOH
...
COOH
COOH
NН 2
COOH
Смесь полипептидов
10. Схема действия экзопептидаз
СХЕМА ДЕЙСТВИЯ ЭКЗОПЕПТИДАЗ11. Схема действия экзопептидаз
СХЕМА ДЕЙСТВИЯ ЭКЗОПЕПТИДАЗNН 2
...
COOH
аминопептидаза
Белок
Н2О
NН 2
карбоксипептидаза
...
COOH
NН 2
COOH
Свободные
аминокислоты
NН 2
COOH
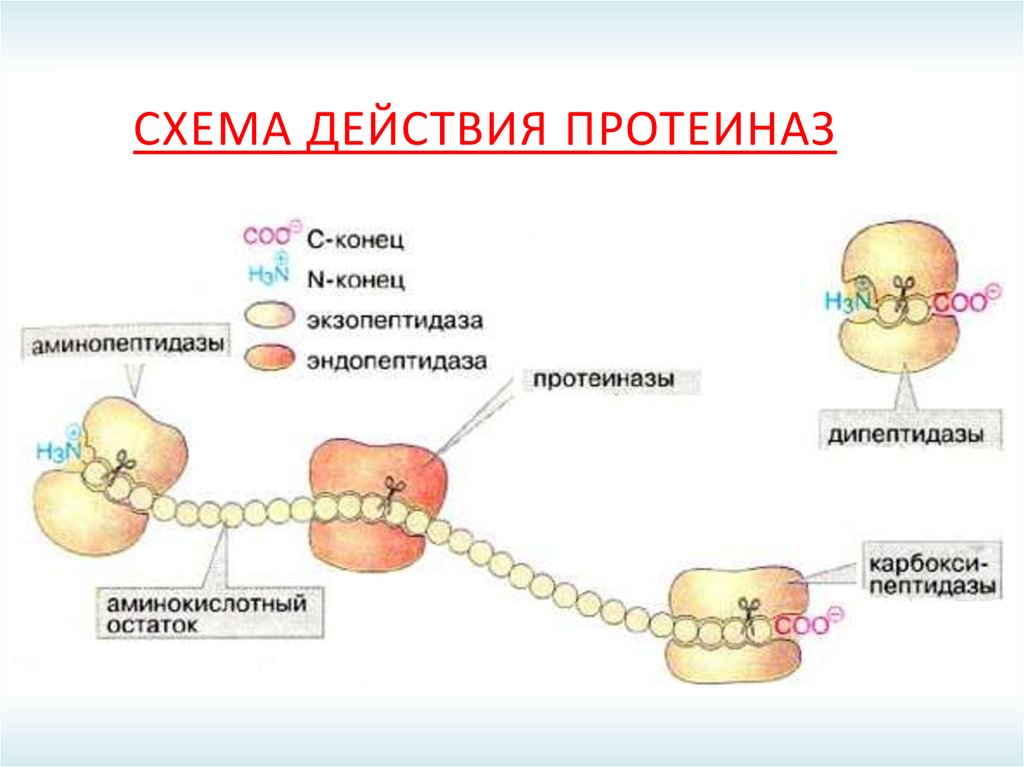
12. Схема действия протеиназ
СХЕМА ДЕЙСТВИЯ ПРОТЕИНАЗ13.
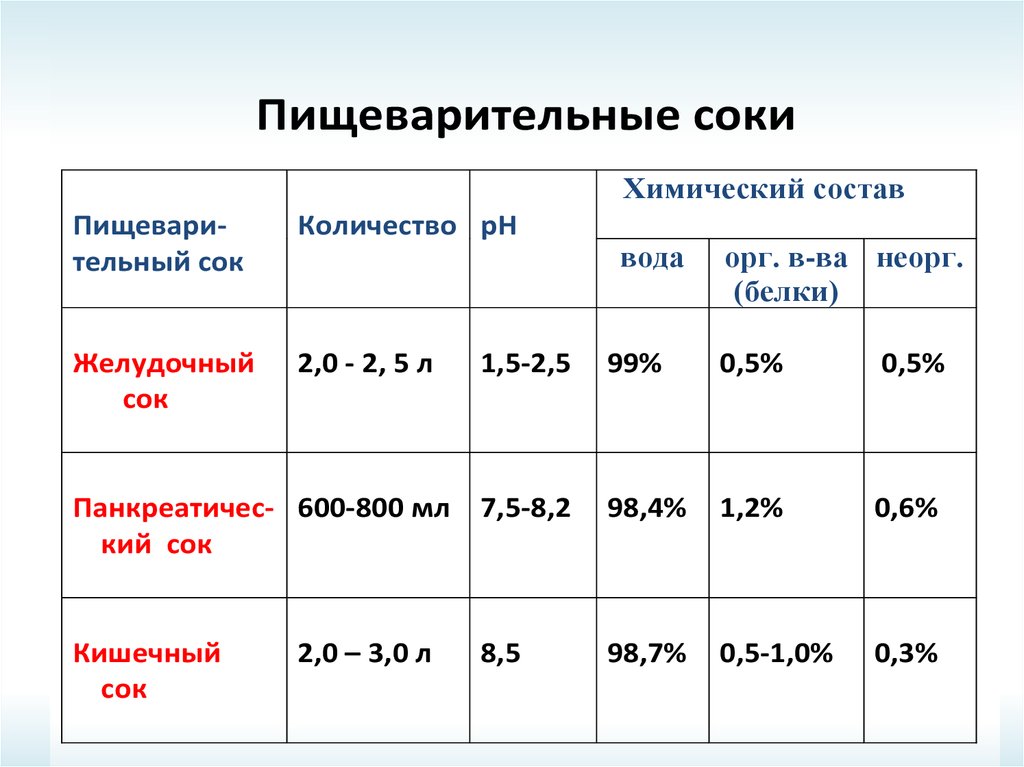
Пищеварительные сокиХимический состав
Пищеварительный сок
Количество рН
Желудочный
сок
2,0 - 2, 5 л
вода
орг. в-ва неорг.
(белки)
1,5-2,5
99%
0,5%
0,5%
Панкреатичес- 600-800 мл
кий сок
7,5-8,2
98,4%
1,2%
0,6%
Кишечный
сок
8,5
98,7%
0,5-1,0%
0,3%
2,0 – 3,0 л
14. Протеиназы желудочно-кишечного тракта
ПРОТЕИНАЗЫ ЖЕЛУДОЧНО-КИШЕЧНОГОТРАКТА
Источник
Фермент
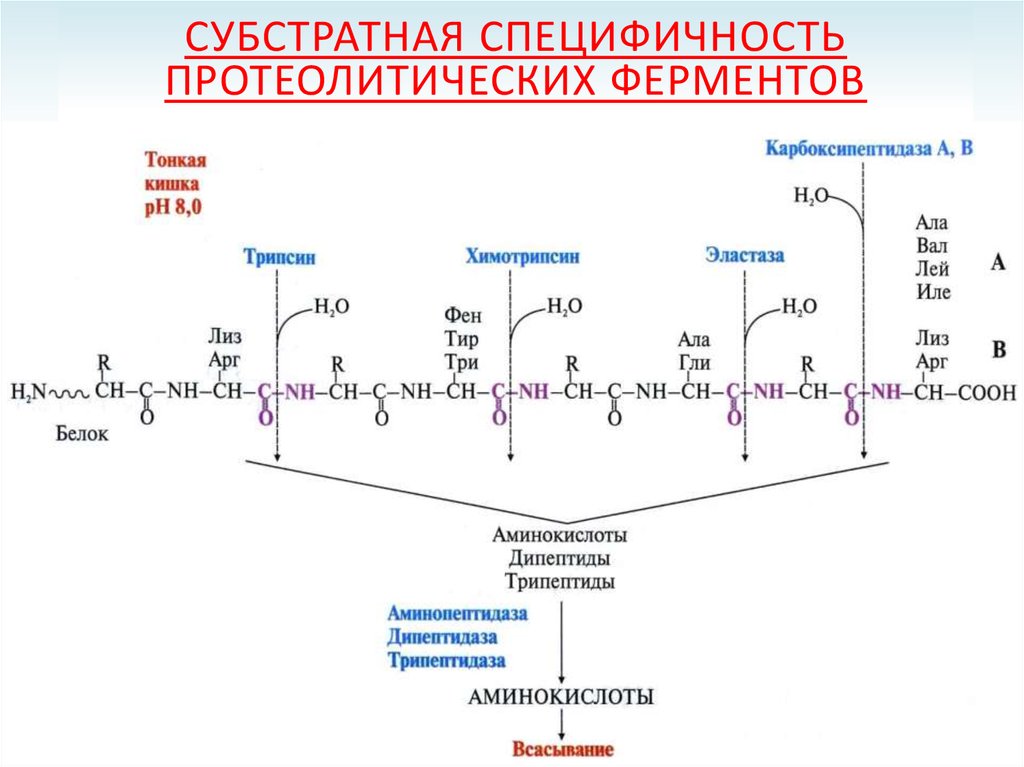
Субстратная
специфичность
Желудочный пепсин
сок
реннин
гастриксин
Панкреатический сок
трипсин
эндопептидазы
химотрипсин
коллагеназа
эластаза
карбоксипептидаза
Кишечный
сок
аминопептидаза
трипептидазы
дипептидазы
экзопептидазы
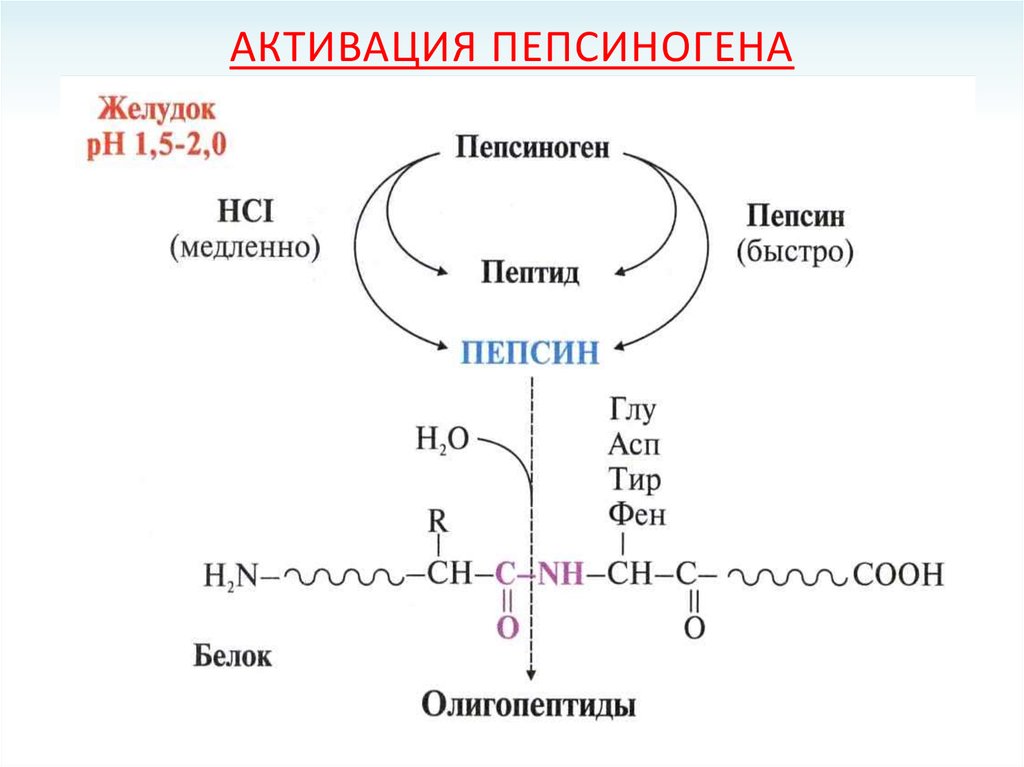
15. Активация пепсиногена
АКТИВАЦИЯ ПЕПСИНОГЕНА16. Секреция соляной кислоты в желудке
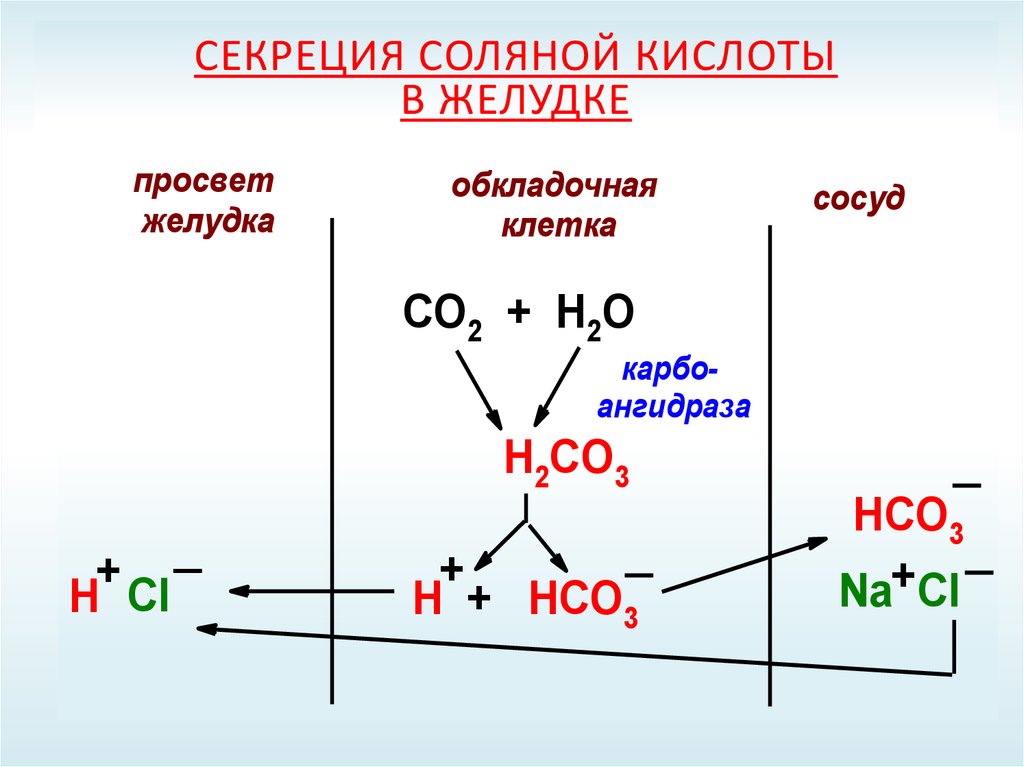
СЕКРЕЦИЯ СОЛЯНОЙ КИСЛОТЫВ ЖЕЛУДКЕ
просвет
желудка
обкладочная
клетка
сосуд
СО2 + Н2О
карбоангидраза
Н2СО3
+
H Cl
+
Н + НСО3
НСО3
Na+Cl
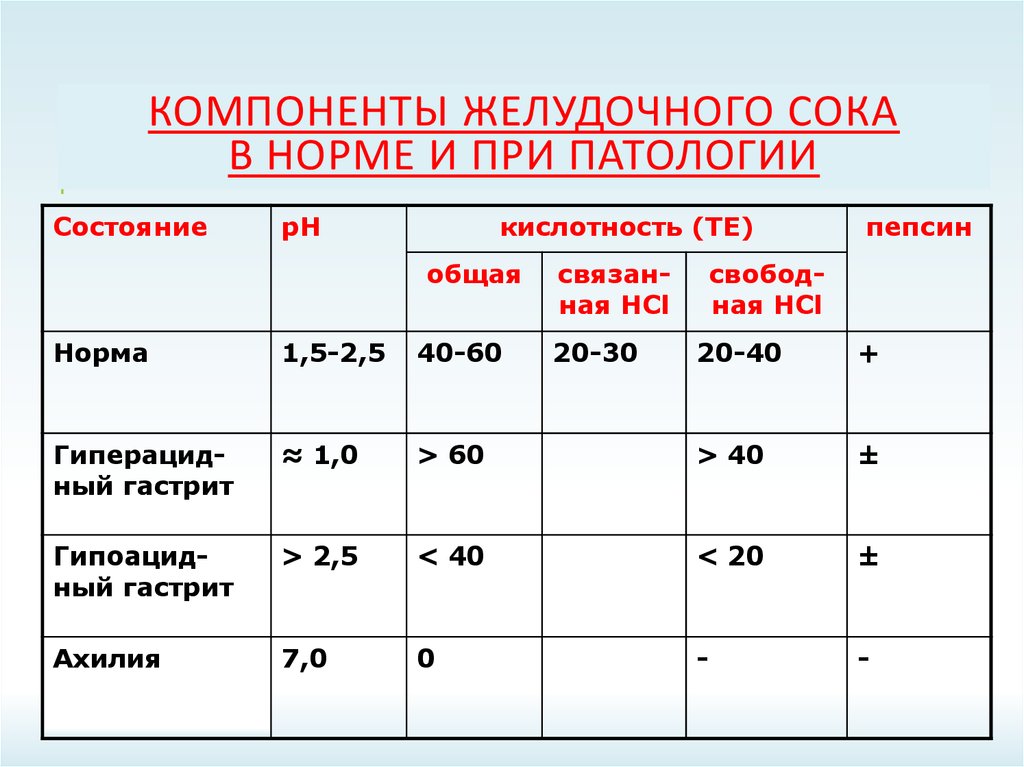
17. Компоненты желудочного сока в норме и при патологии
КОМПОНЕНТЫ ЖЕЛУДОЧНОГО СОКАВ НОРМЕ И ПРИ ПАТОЛОГИИ
Состояние
рН
кислотность (ТЕ)
общая
Норма
1,5-2,5
40-60
Гиперацидный гастрит
≈ 1,0
Гипоацидный гастрит
Ахилия
связанная НСl
20-30
пепсин
свободная HCl
20-40
+
> 60
> 40
±
> 2,5
< 40
< 20
±
7,0
0
-
-
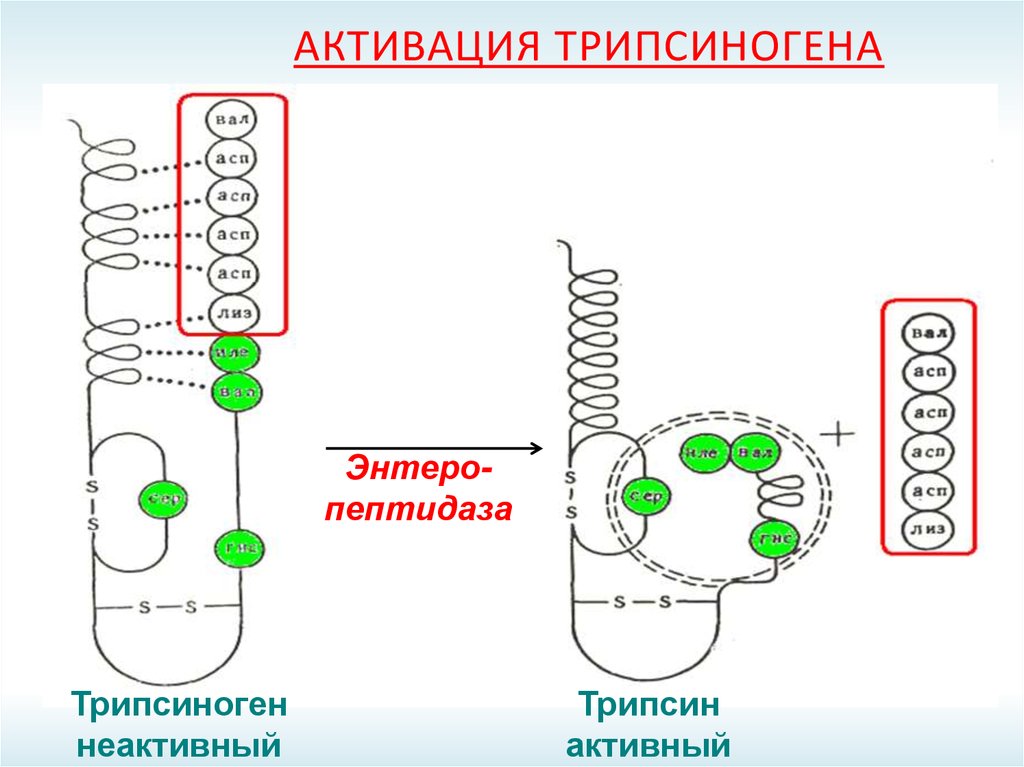
18. Активация трипсиногена
АКТИВАЦИЯ ТРИПСИНОГЕНАЭнтеропептидаза
Трипсиноген
неактивный
Трипсин
активный
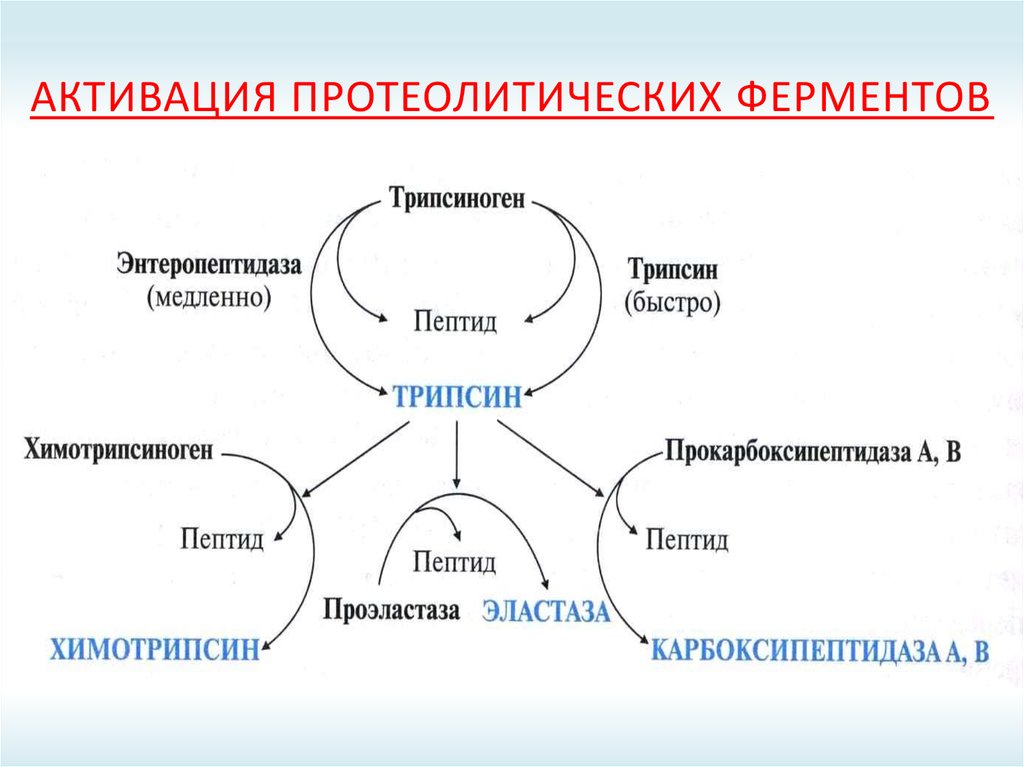
19. Активация протеолитических ферментов
АКТИВАЦИЯ ПРОТЕОЛИТИЧЕСКИХ ФЕРМЕНТОВ20. Субстратная специфичность протеолитических ферментов
СУБСТРАТНАЯ СПЕЦИФИЧНОСТЬПРОТЕОЛИТИЧЕСКИХ ФЕРМЕНТОВ
21.
22.
Советский учёный, специалист вобласти физиологии, вегетативных
функций и их регуляции.
Академик АН СССР по отделению
физиологии (1984). Впервые описал
пристеночное пищеварение,
механизмы самопереваривания.
Исследовал эволюцию пищеварител
ьной функции.
Александр Михайлович
Уголев
Работа А. М. Уголева «Пристеночное
(контактное) мембранное
пищеварение» была признана
как научное открытие и внесена
в Государственный реестр открытий
СССР под № 15 с приоритетом от
декабря 1958 г.За свои работы — в
1990 году был награждён золотой
медалью им. И. И. Мечникова.
23. Схема последовательных конформационных взаимодействий ферментной и транспортной частей функционирующего ферментно- транспортного комп
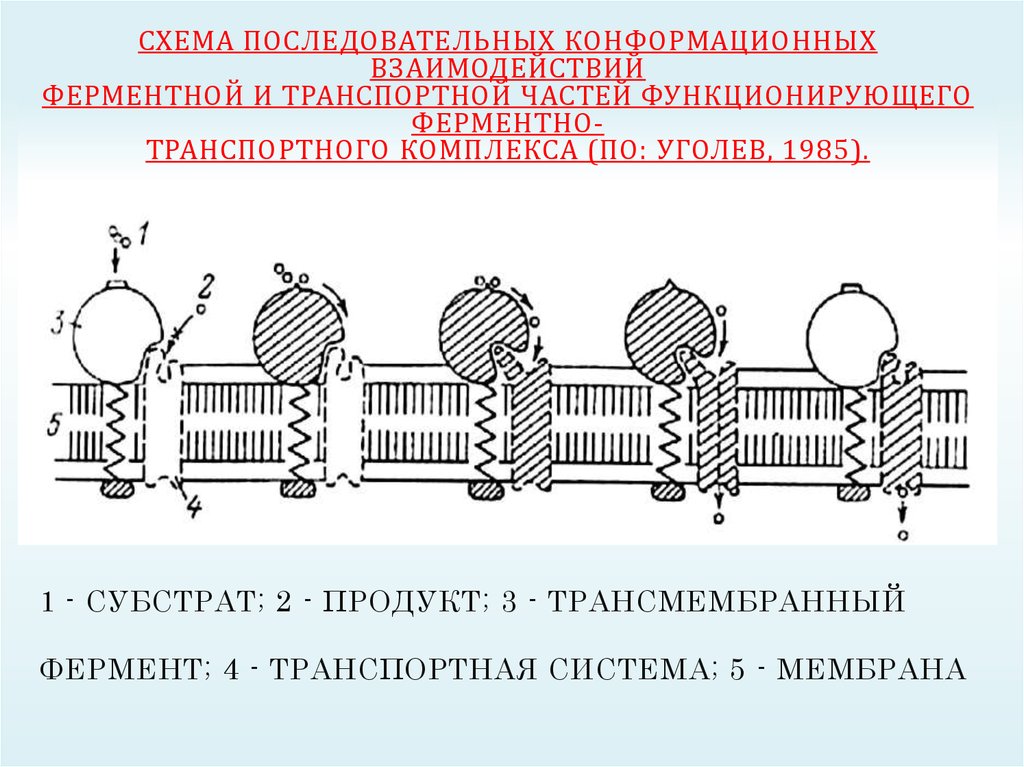
СХЕМА ПОСЛЕДОВАТЕЛЬНЫХ КОНФОРМАЦИОННЫХВЗАИМОДЕЙСТВИЙ
ФЕРМЕНТНОЙ И ТРАНСПОРТНОЙ ЧАСТЕЙ ФУНКЦИОНИРУЮЩЕГО
ФЕРМЕНТНОТРАНСПОРТНОГО КОМПЛЕКСА (ПО: УГОЛЕВ, 1985).
1 - СУБСТРАТ; 2 - ПРОДУКТ; 3 - ТРАНСМЕМБРАННЫЙ
ФЕРМЕНТ; 4 - ТРАНСПОРТНАЯ СИСТЕМА; 5 - МЕМБРАНА
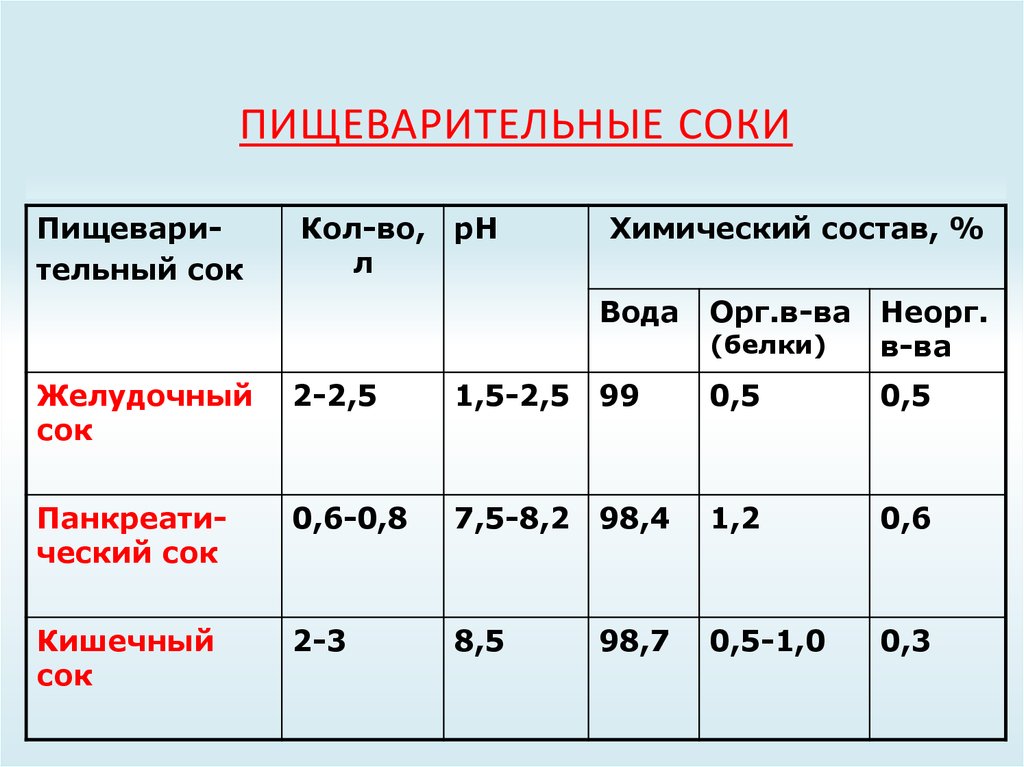
24. Пищеварительные соки
ПИЩЕВАРИТЕЛЬНЫЕ СОКИПищеварительный сок
Кол-во,
л
рН
Химический состав, %
Вода
Орг.в-ва
(белки)
Неорг.
в-ва
Желудочный
сок
2-2,5
1,5-2,5
99
0,5
0,5
Панкреатический сок
0,6-0,8
7,5-8,2
98,4
1,2
0,6
Кишечный
сок
2-3
8,5
98,7
0,5-1,0
0,3
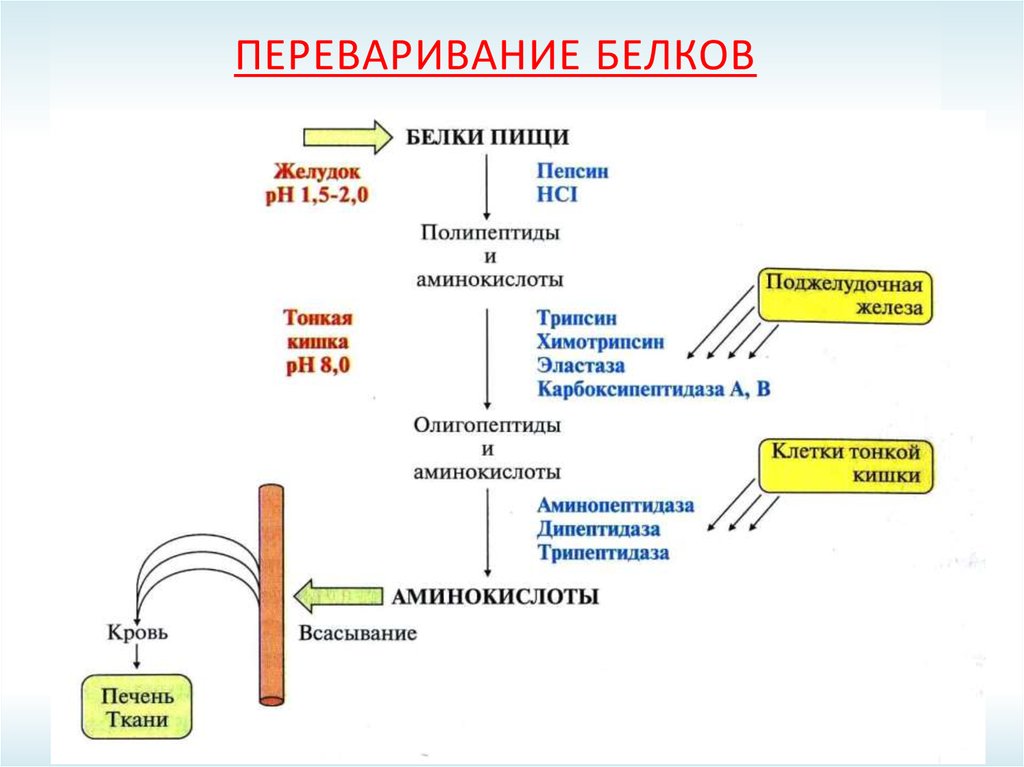
25. Переваривание белков
ПЕРЕВАРИВАНИЕ БЕЛКОВ26.
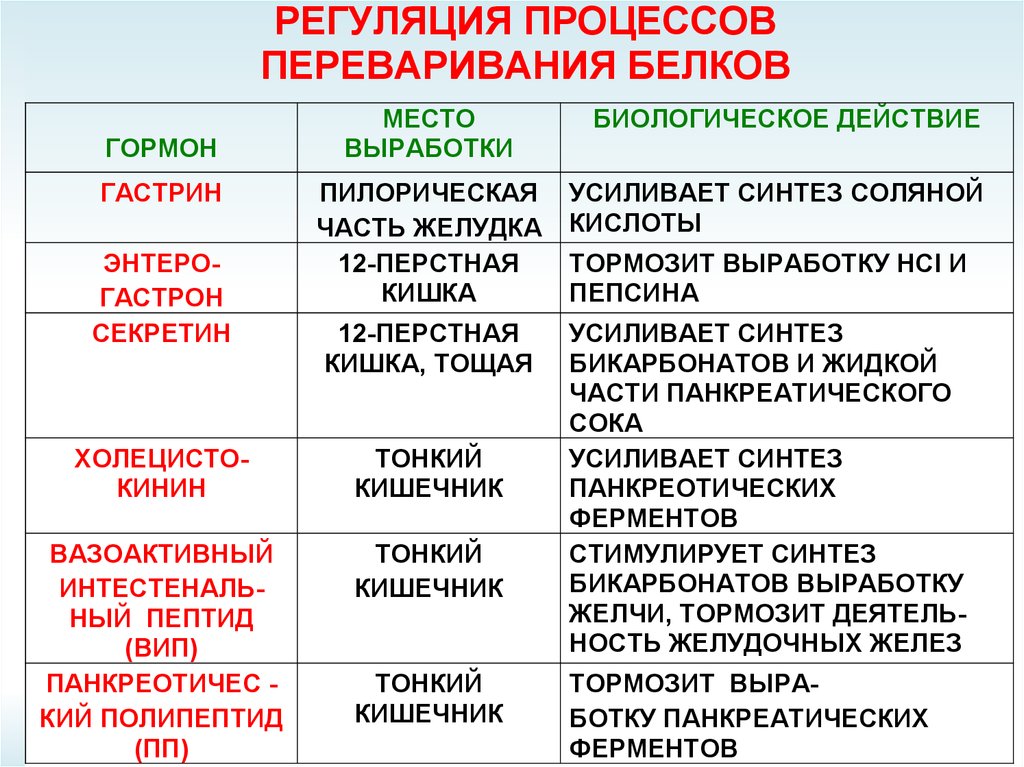
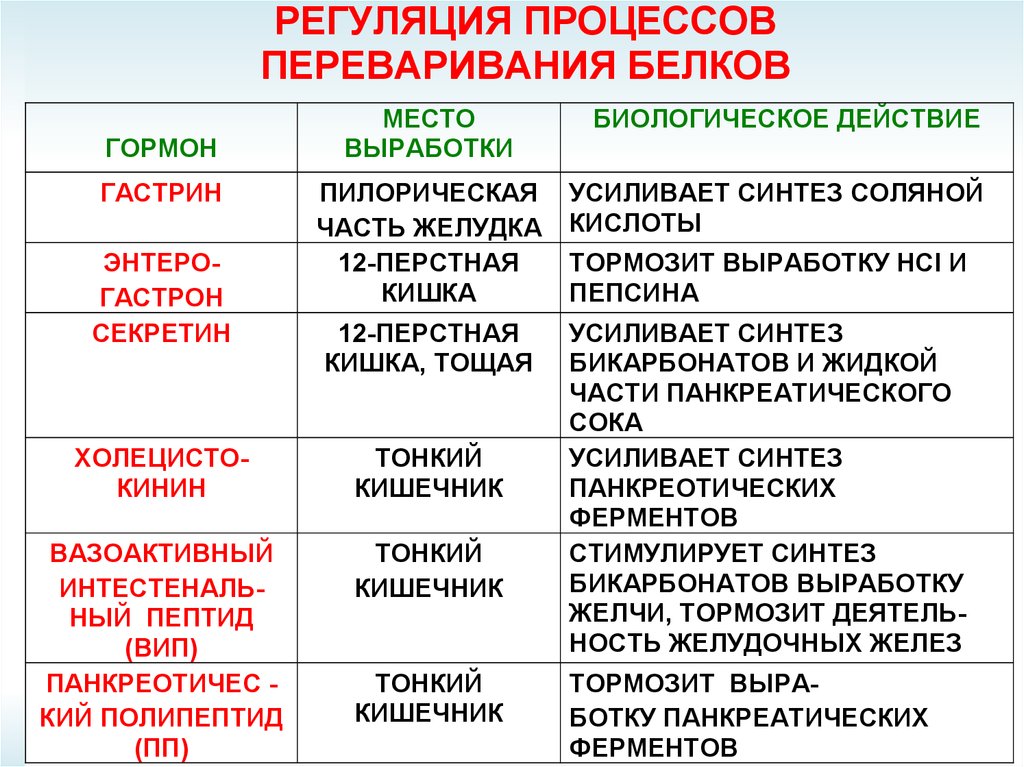
РЕГУЛЯЦИЯ ПРОЦЕССОВПЕРЕВАРИВАНИЯ БЕЛКОВ
ГОРМОН
ГАСТРИН
ЭНТЕРОГАСТРОН
СЕКРЕТИН
МЕСТО
ВЫРАБОТКИ
ПИЛОРИЧЕСКАЯ
ЧАСТЬ ЖЕЛУДКА
12-ПЕРСТНАЯ
КИШКА
12-ПЕРСТНАЯ
КИШКА, ТОЩАЯ
ХОЛЕЦИСТОКИНИН
ТОНКИЙ
КИШЕЧНИК
ВАЗОАКТИВНЫЙ
ИНТЕСТЕНАЛЬНЫЙ ПЕПТИД
(ВИП)
ПАНКРЕОТИЧЕС КИЙ ПОЛИПЕПТИД
(ПП)
ТОНКИЙ
КИШЕЧНИК
ТОНКИЙ
КИШЕЧНИК
БИОЛОГИЧЕСКОЕ ДЕЙСТВИЕ
УСИЛИВАЕТ СИНТЕЗ СОЛЯНОЙ
КИСЛОТЫ
ТОРМОЗИТ ВЫРАБОТКУ НСI И
ПЕПСИНА
УСИЛИВАЕТ СИНТЕЗ
БИКАРБОНАТОВ И ЖИДКОЙ
ЧАСТИ ПАНКРЕАТИЧЕСКОГО
СОКА
УСИЛИВАЕТ СИНТЕЗ
ПАНКРЕОТИЧЕСКИХ
ФЕРМЕНТОВ
СТИМУЛИРУЕТ СИНТЕЗ
БИКАРБОНАТОВ ВЫРАБОТКУ
ЖЕЛЧИ, ТОРМОЗИТ ДЕЯТЕЛЬНОСТЬ ЖЕЛУДОЧНЫХ ЖЕЛЕЗ
ТОРМОЗИТ ВЫРАБОТКУ ПАНКРЕАТИЧЕСКИХ
ФЕРМЕНТОВ
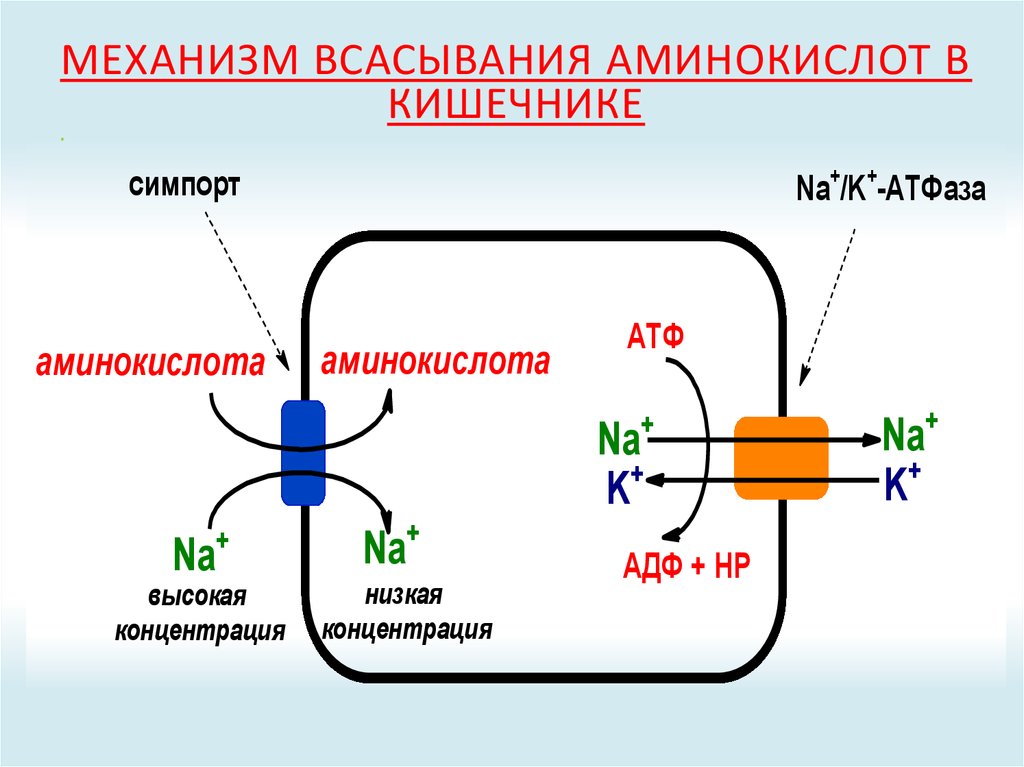
27. Механизм всасывания аминокислот в кишечнике
МЕХАНИЗМ ВСАСЫВАНИЯ АМИНОКИСЛОТ ВКИШЕЧНИКЕ
симпорт
аминокислота
Na+/K+-АТФаза
аминокислота
АТФ
+
Na
K+
Na
+
высокая
концентрация
Na+
низкая
концентрация
АДФ + НР
Na
K+
+
28.
29. УБИКВИНТИН
Убиквитин - играет решающуюроль в процессе утилизации
белков присоединяясь к тому
белку, который нужно
уничтожить. Вход в протеасому
обычно закрыт, и попасть в нее
может только белок,
отмеченный специальной
меткой, в этом случае вход в
протеасому открывается. Роль
такой «черной» метки играет
убиквитин. Этот процесс
прикрепления убиквитина к
молекуле белка, подлежащего
ликвидации, назвали
«поцелуем смерти».
30.
1.2.
3.
4.
5.
6.
31. УБИКВИНТИН
Структура убиквитина. Боковые цеписеми остатков лизина показаны жёлтым
Идентификаторы
Символ
Pfam
ubiquitin
InterPro
IPR000626
PROSITE
PDOC00271
SCOP
1aar
SUPERFAMILY
1aar
PF00240
Убиквити́н (от англ. ubiquitous —
вездесущий) консервативный белок
эукариот, участвующий
в регуляции процессов
внутриклеточной деградации других
белков, а также их функций.
Он присутствует почти во всех
тканях многоклеточных эукариот, а также
у одноклеточных эукариотических
организмов.
Убиквитин был открыт в
1975 году Гидеоном Голдштейном с
соавторами[1] и охарактеризован в 70—
80-х годах XX века
В 2004 году Аарон Чехановер, Аврам
Гершко и Ирвин Роуз были
удостоены Нобелевской премии по
химии «за открытие убиквитинопосредованной деградации белка»
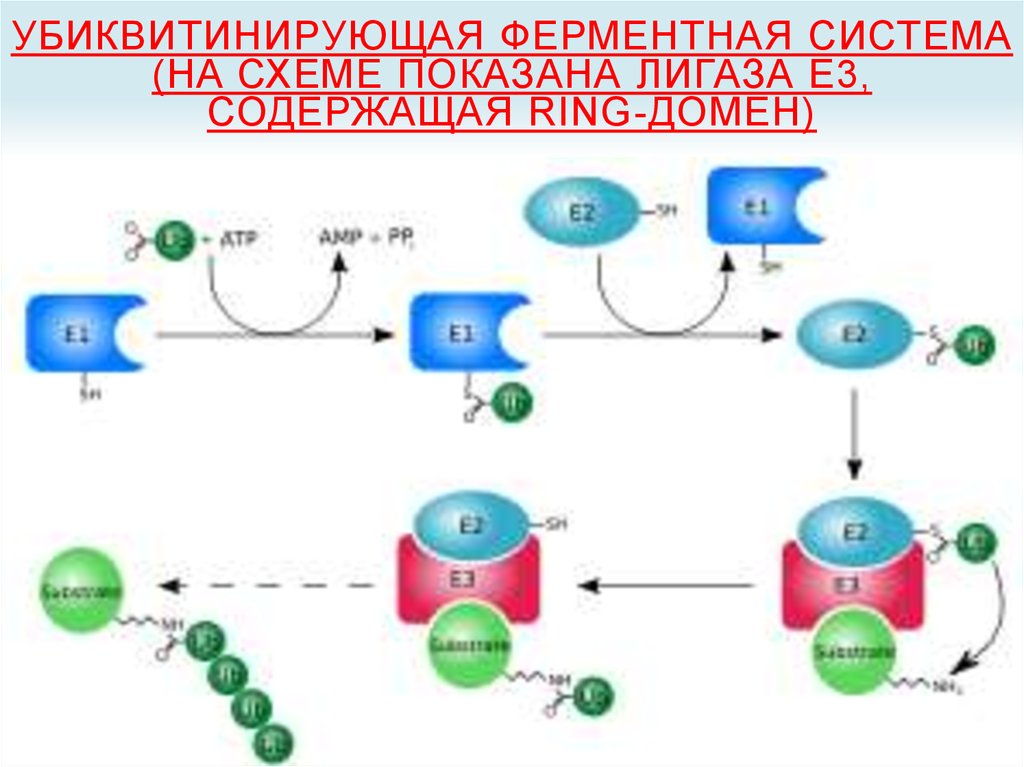
32. Убиквитинирующая ферментная система (на схеме показана лигаза E3, содержащая RING-домен)
УБИКВИТИНИРУЮЩАЯ ФЕРМЕНТНАЯ СИСТЕМА(НА СХЕМЕ ПОКАЗАНА ЛИГАЗА E3,
СОДЕРЖАЩАЯ RING-ДОМЕН)
33.
РЕГУЛЯЦИЯ ПРОЦЕССОВПЕРЕВАРИВАНИЯ БЕЛКОВ
ГОРМОН
ГАСТРИН
ЭНТЕРОГАСТРОН
СЕКРЕТИН
МЕСТО
ВЫРАБОТКИ
ПИЛОРИЧЕСКАЯ
ЧАСТЬ ЖЕЛУДКА
12-ПЕРСТНАЯ
КИШКА
12-ПЕРСТНАЯ
КИШКА, ТОЩАЯ
ХОЛЕЦИСТОКИНИН
ТОНКИЙ
КИШЕЧНИК
ВАЗОАКТИВНЫЙ
ИНТЕСТЕНАЛЬНЫЙ ПЕПТИД
(ВИП)
ПАНКРЕОТИЧЕС КИЙ ПОЛИПЕПТИД
(ПП)
ТОНКИЙ
КИШЕЧНИК
ТОНКИЙ
КИШЕЧНИК
БИОЛОГИЧЕСКОЕ ДЕЙСТВИЕ
УСИЛИВАЕТ СИНТЕЗ СОЛЯНОЙ
КИСЛОТЫ
ТОРМОЗИТ ВЫРАБОТКУ НСI И
ПЕПСИНА
УСИЛИВАЕТ СИНТЕЗ
БИКАРБОНАТОВ И ЖИДКОЙ
ЧАСТИ ПАНКРЕАТИЧЕСКОГО
СОКА
УСИЛИВАЕТ СИНТЕЗ
ПАНКРЕОТИЧЕСКИХ
ФЕРМЕНТОВ
СТИМУЛИРУЕТ СИНТЕЗ
БИКАРБОНАТОВ ВЫРАБОТКУ
ЖЕЛЧИ, ТОРМОЗИТ ДЕЯТЕЛЬНОСТЬ ЖЕЛУДОЧНЫХ ЖЕЛЕЗ
ТОРМОЗИТ ВЫРАБОТКУ ПАНКРЕАТИЧЕСКИХ
ФЕРМЕНТОВ
34. Катаболизм аминокислот
ОБЩИЕ ПУТИКАТАБОЛИЗМА
СО2
R
ИНДИВИДУАЛЬНЫЕ
ПУТИ
КАТАБОЛИЗМА
СН COOH
NH2
потеря
аминогруппы
- NH3
карбоновые
кислоты
декарбоксилирование
биогенные
амины
ин
и
ам
дез вание
ро
- NH2
п ер
еа
ров миниани
е
-кетокислоты
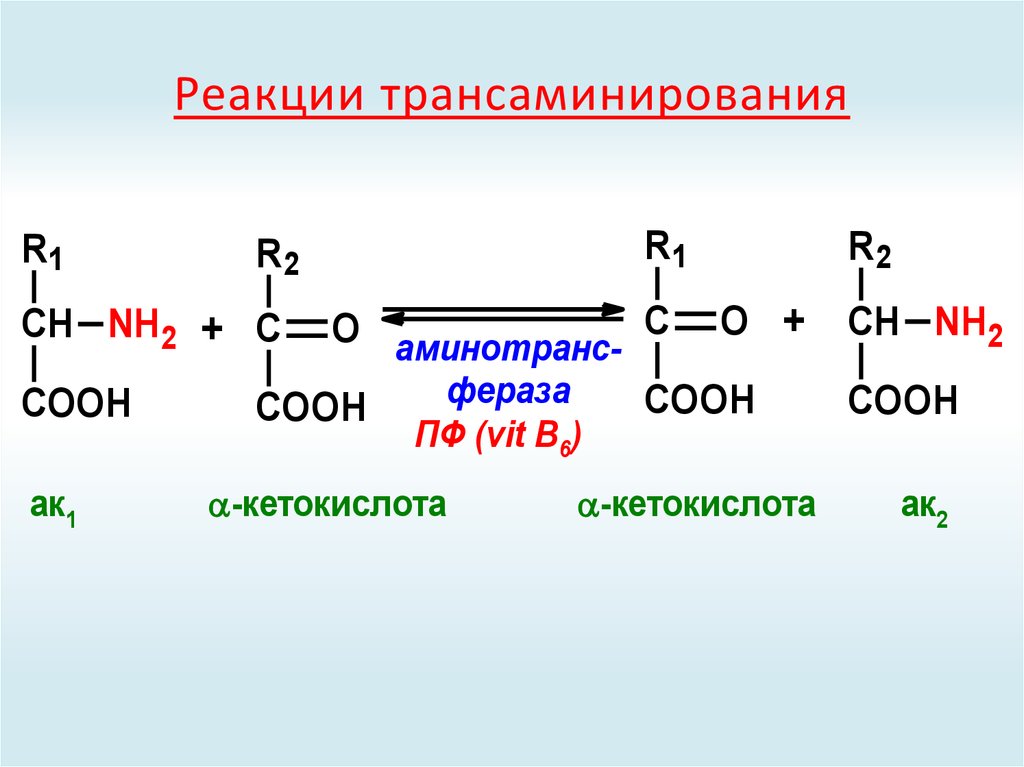
35. Реакции трансаминирования
R1R1
R2
O аминотранс- С O +
фераза
COOH
COOH
R2
СН NH2 + С
СН NH2
COOH
COOH
ак1
ПФ (vit B6)
-кетокислота
-кетокислота
ак2
36. Реакции трансаминирования
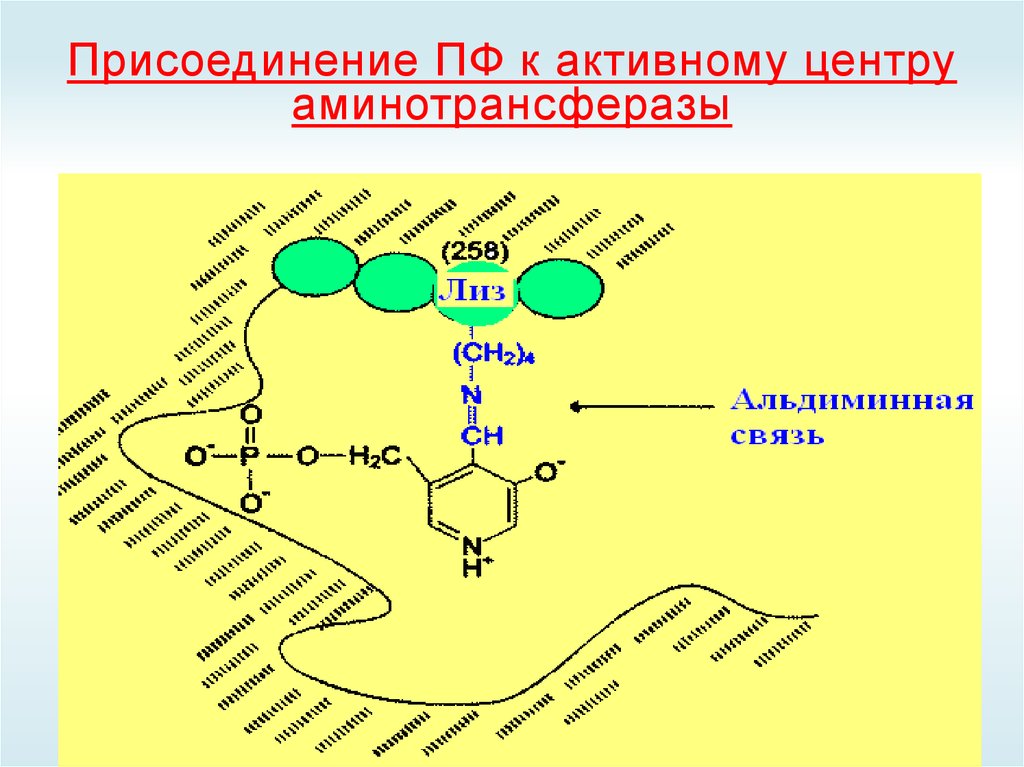
37. Присоединение ПФ к активному центру аминотрансферазы
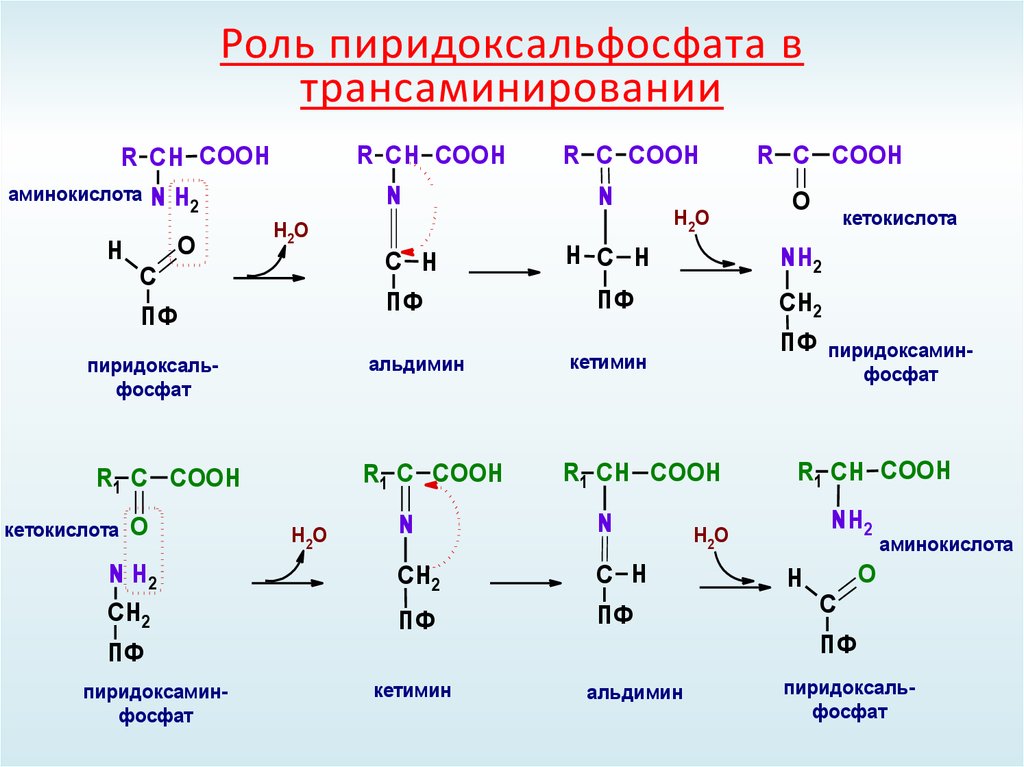
38. Роль пиридоксальфосфата в трансаминировании
R СН COOHR СН COOH
аминокислота
H
N Н2
O
N
Н2О
С H
С
ПФ
ПФ
альдимин
пиридоксальфосфат
R1 С COOH
R1 С COOH
R С COOH
N
H С H
СН2
С H
СН2
ПФ
ПФ
кетимин
фосфат
R1 СН COOH
NН2
Н2О
H
аминокислота
O
С
ПФ
ПФ
пиридоксаминфосфат
ПФ пиридоксамин-
R1 СН COOH
N Н2
Н2О
кетокислота
СН2
кетимин
N
O
O
NН2
ПФ
N
кетокислота
Н2О
R С COOH
альдимин
пиридоксальфосфат
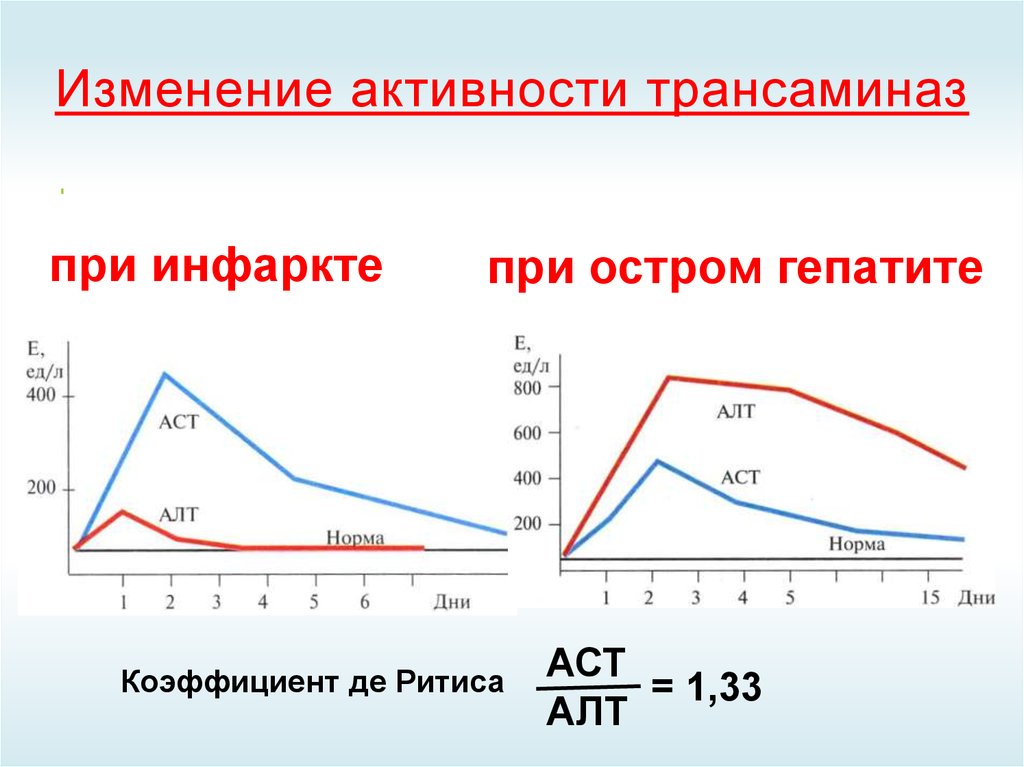
39. Изменение активности трансаминаз
при инфарктепри остром гепатите
Коэффициент де Ритиса
АСТ
= 1,33
АЛТ
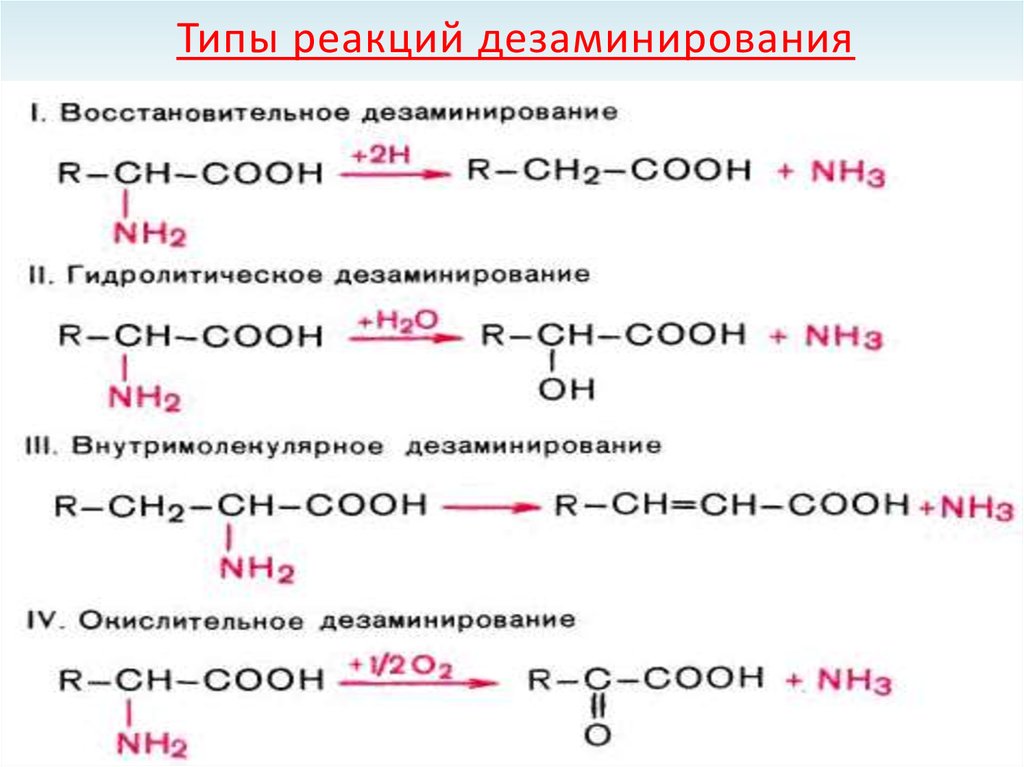
40. Типы реакций дезаминирования
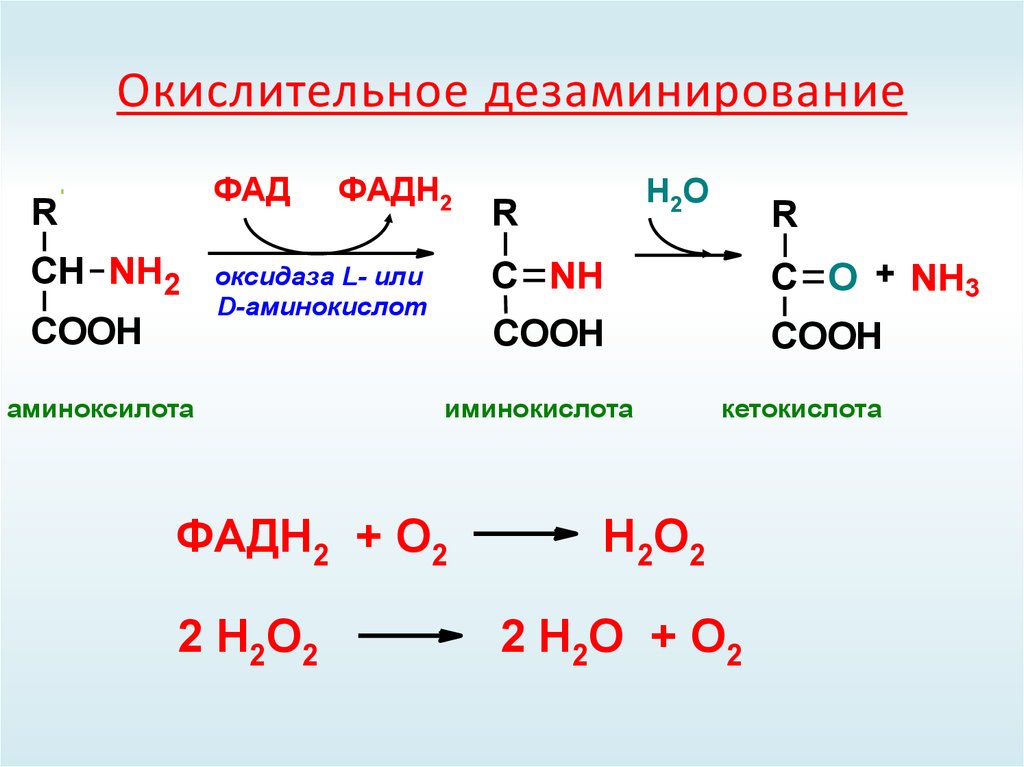
41. Окислительное дезаминирование
ФАДR
СН NH2
COOH
ФАДН2
оксидаза L- или
D-аминокислот
аминоксилота
R
R
С NH
С O + NH3
COOH
COOH
иминокислота
ФАДН2 + О2
2 Н2О2
Н2О
кетокислота
Н2О2
2 Н2О + О2
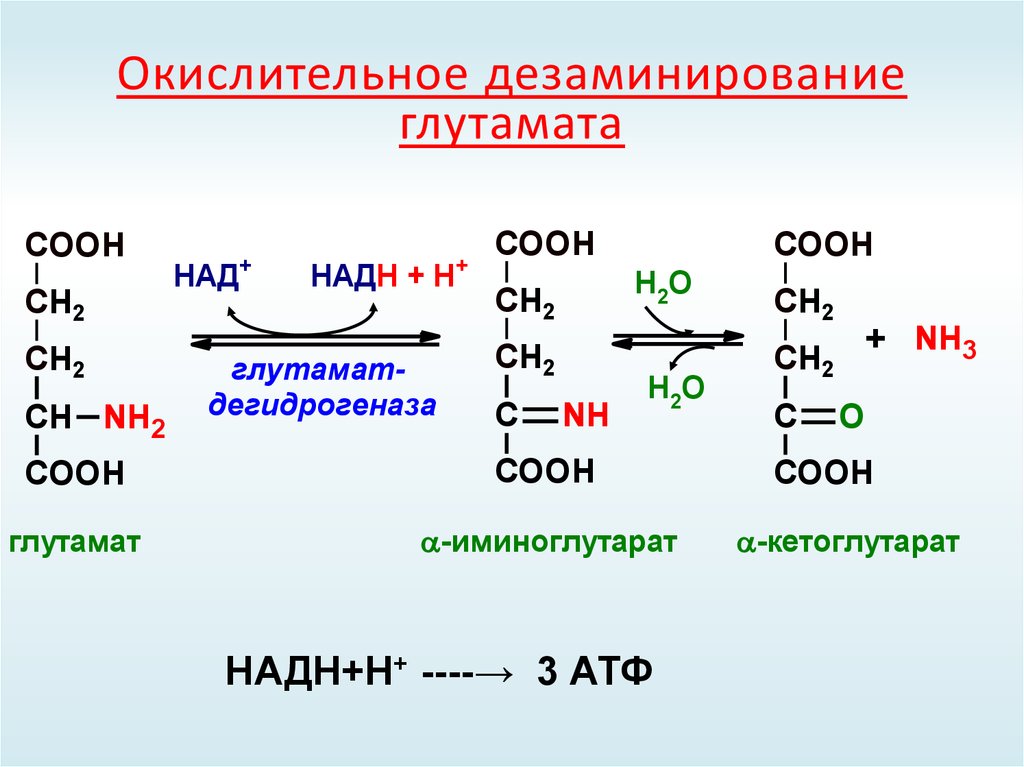
42. Окислительное дезаминирование глутамата
COOHCH2
CH2
СН NH2
COOH
глутамат
+
НАД
НАДН + Н
глутаматдегидрогеназа
+
COOH
Н2О
CH2
CH2
С
COOH
NH
Н2О
COOH
-иминоглутарат
НАДН+Н+ ----→ 3 АТФ
CH2
+ NH3
CH2
С
O
COOH
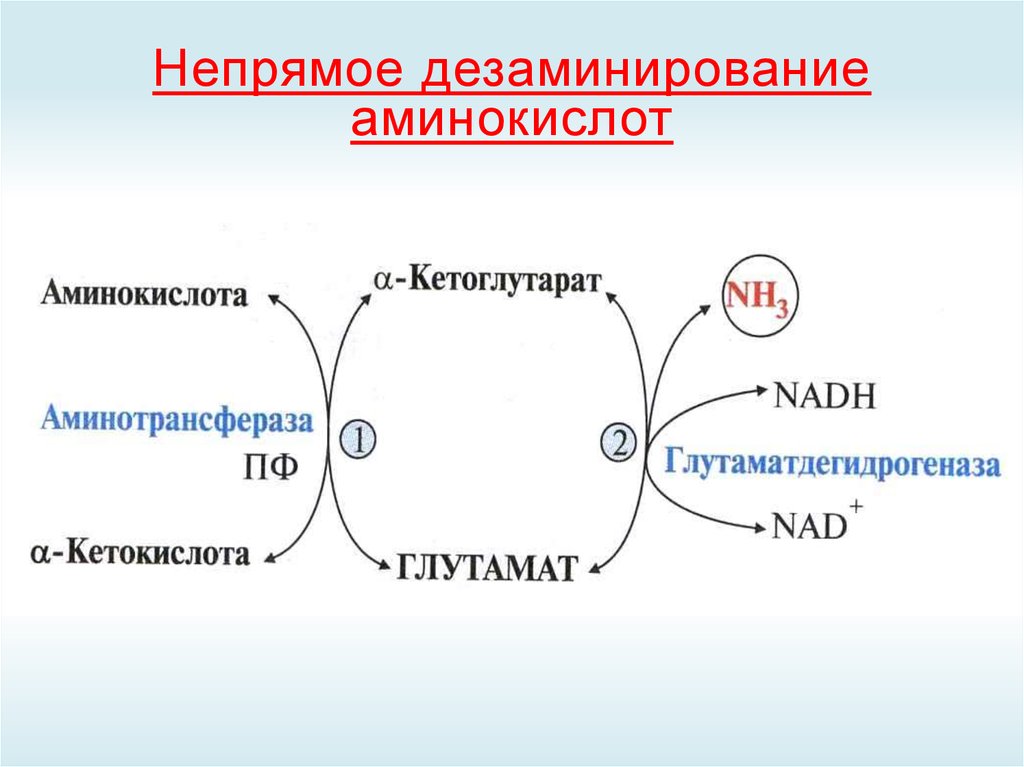
-кетоглутарат
43. Непрямое дезаминирование аминокислот
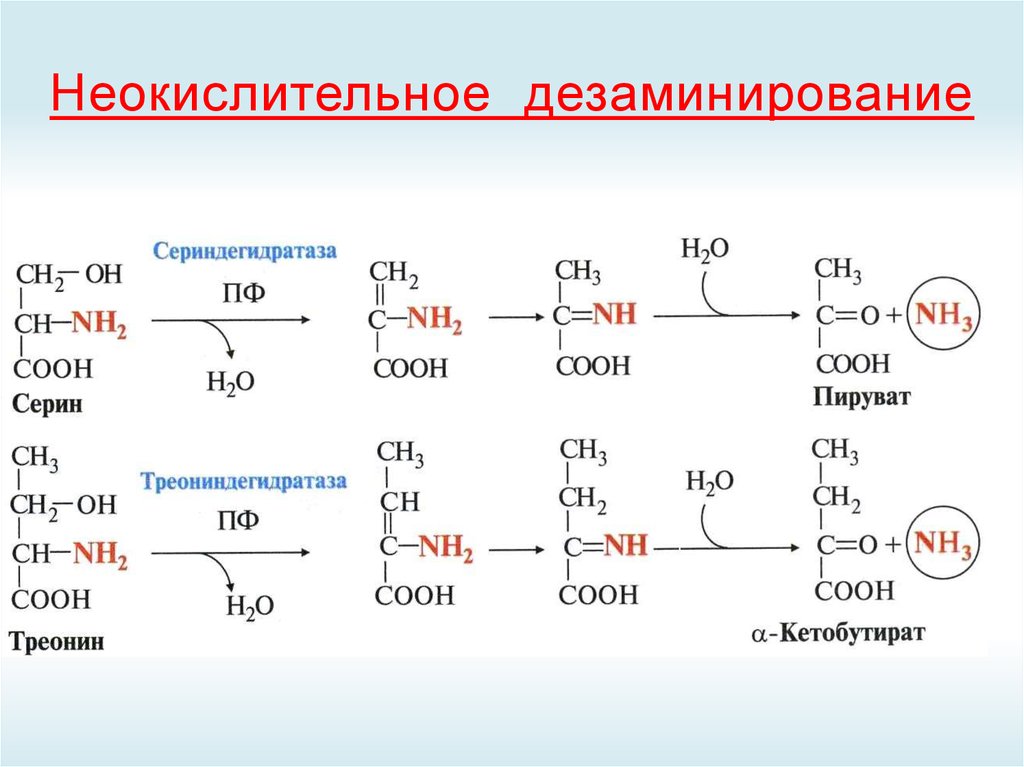
44. Неокислительное дезаминирование
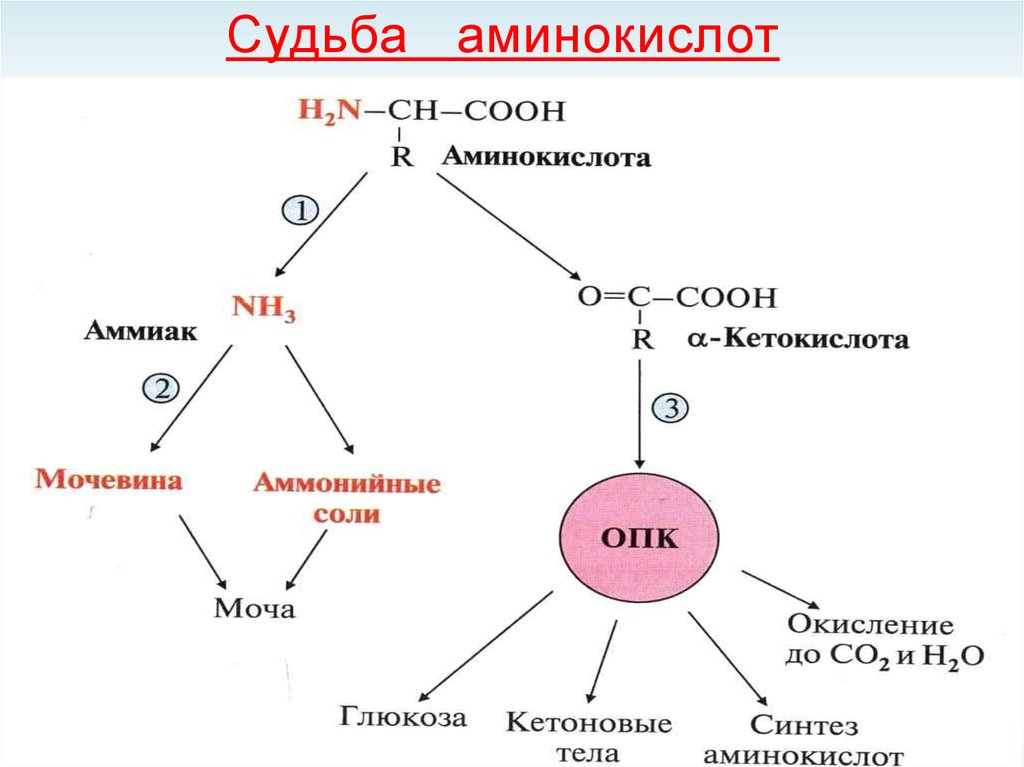
45. Судьба аминокислот
46. Реакции декарбоксилирования
СО2R СН COO H
NH2
декарбоксилаза
ПФ (vit B6)
аминоксилота
COOH
СН2
СН2
СН NH2
COOH
глу
R СН2 NH2
биогенный амин
СО 2
декарбоксилаза
ПФ (vit B6)
COOH
СН2
СН2
СН2 NH2
-аминомасляная к-та
(ГАМК)
47. Декарбоксилирование гетероциклических аминокислот
СН 2N
СН COOH
NH2
NH
гистидин
СО 2
СН 2
N
гистидиндекарбоксилаза
ПФ (vit B6)
СН 2
NH2
NH
гистамин
СН 2 СН COOH
NH2
NH
триптофан
1/2 О2
гидроксилаза
СО2
HO
СН 2 СН COOH
NH
NH2
декарбоксилаза
HO
СН 2 СН 2
NH
NH2
ПФ (vit B6)
5-окситриптофан
серотонин
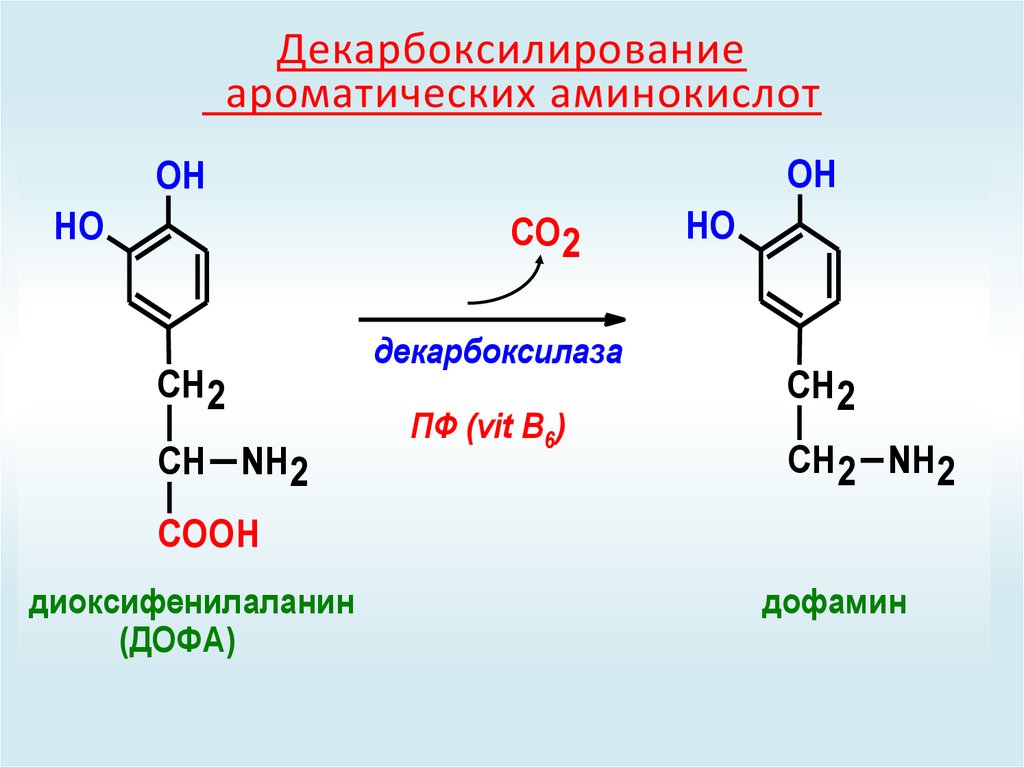
48. Декарбоксилирование ароматических аминокислот
OHOH
СО2
HO
СН2
СН NH2
декарбоксилаза
ПФ (vit B6)
HO
СН2
СН 2 NH2
COOH
диоксифенилаланин
(ДОФА)
дофамин
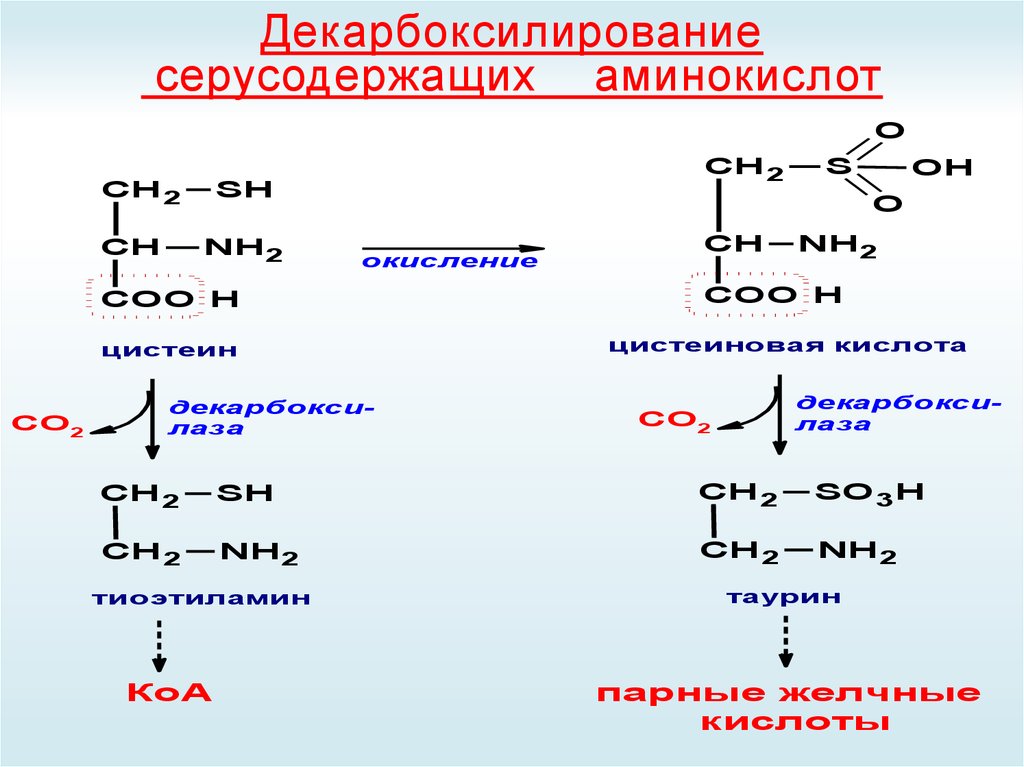
49. Декарбоксилирование серусодержащих аминокислот
OСН 2
СН
СН 2
SH
NH2
OH
O
окисление
COO H
цистеин
СО2
S
декарбоксилаза
СН
NH2
COO H
цистеиновая кислота
декарбоксилаза
СО2
СН 2
SH
СН 2
SO 3 H
СН 2
NH2
СН 2
NH2
тиоэтиламин
КоА
таурин
парные желчные
кислоты
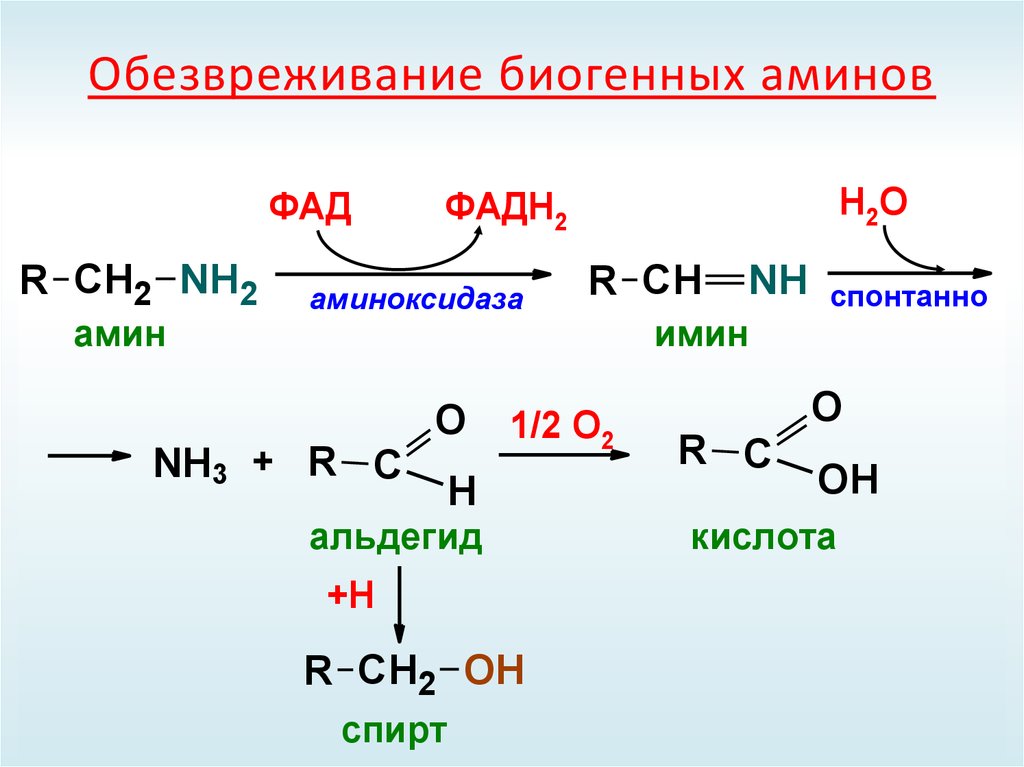
50. Обезвреживание биогенных аминов
ФАДR СН2 NH2
амин
аминоксидаза
NH3 + R С
Н2О
ФАДН2
O
1/2 О2
H
альдегид
+Н
R СН2 OH
спирт
R СН
NH
имин
спонтанно
O
R С
ОН
кислота
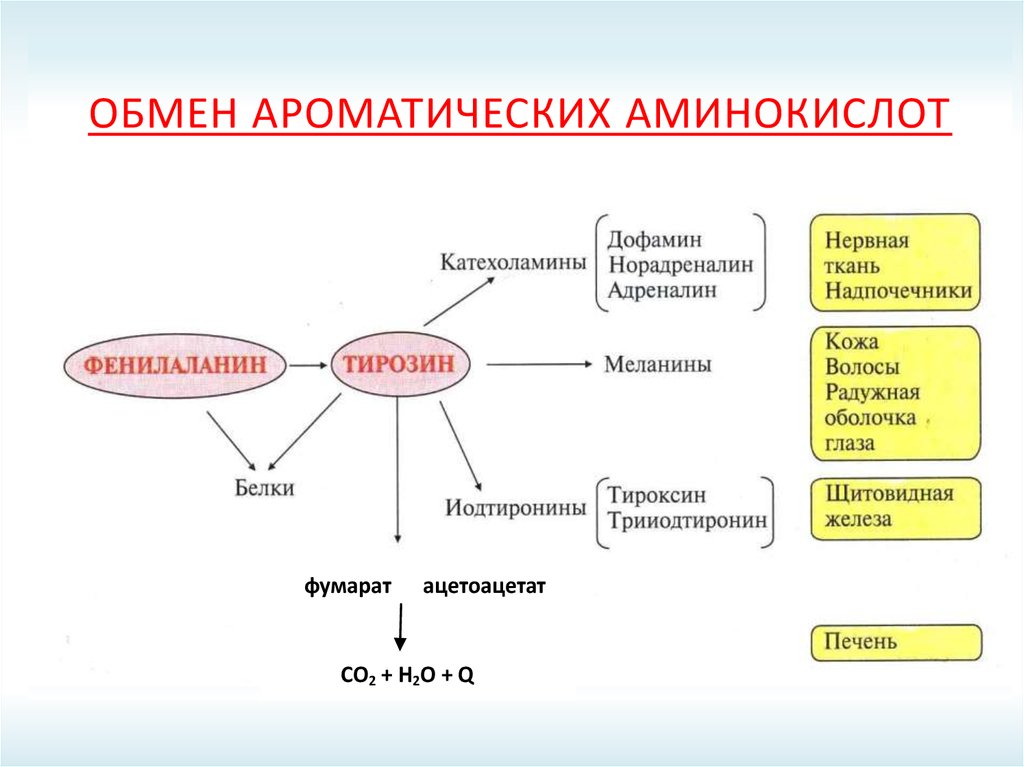
51. Обмен ароматических аминокислот
ОБМЕН АРОМАТИЧЕСКИХ АМИНОКИСЛОТфумарат
ацетоацетат
СО2 + Н2О + Q
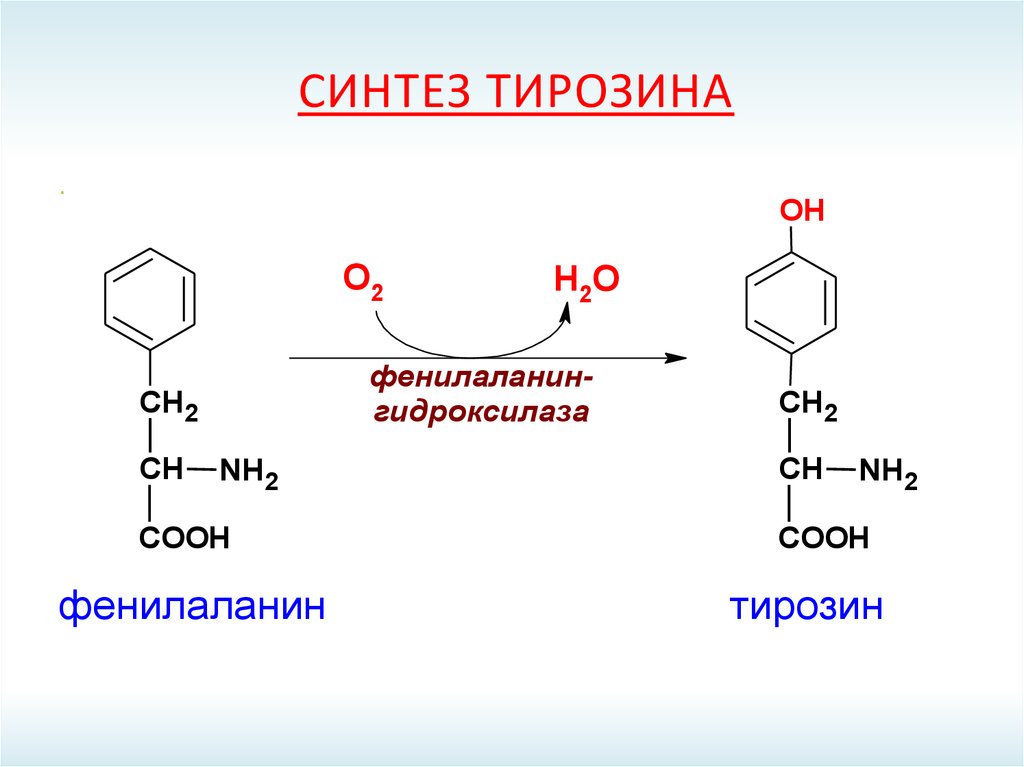
52. Синтез тирозина
СИНТЕЗ ТИРОЗИНАOH
О2
фенилаланингидроксилаза
СН2
СН
Н2О
NH2
COOH
фенилаланин
СН2
СН
NH2
COOH
тирозин
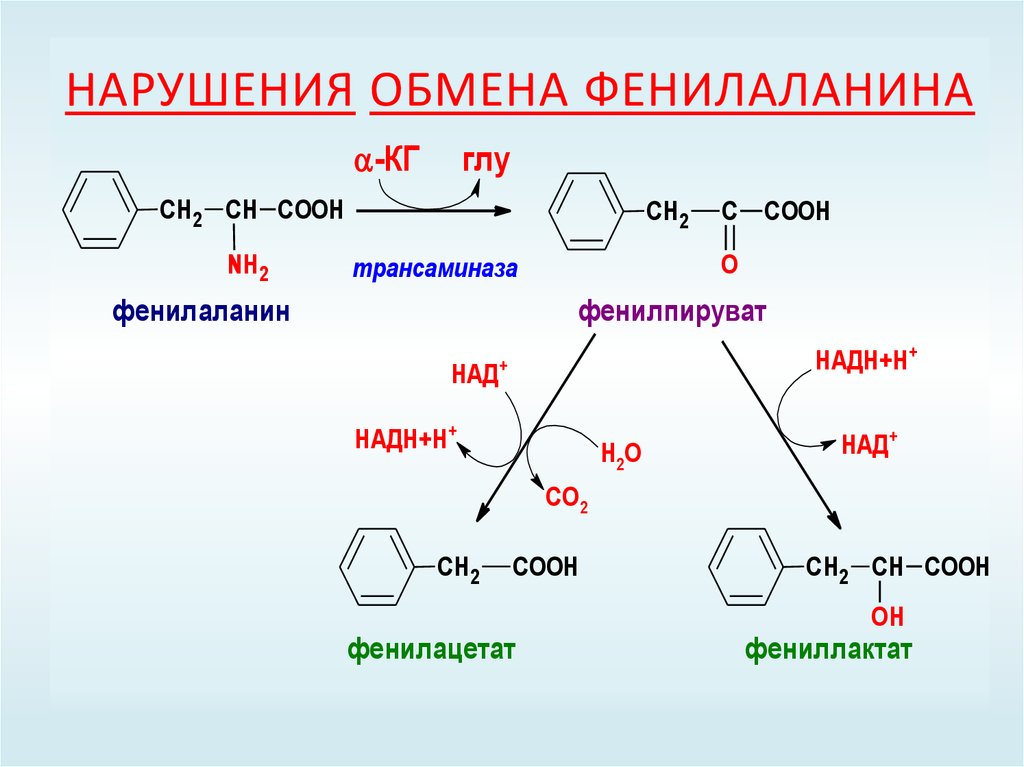
53. Нарушения обмена фенилаланина
НАРУШЕНИЯ ОБМЕНА ФЕНИЛАЛАНИНА-КГ
глу
СН2 СН COOH
NH2
СН2
трансаминаза
фенилаланин
С
COOH
O
фенилпируват
НАД
НАДН+Н+
+
НАДН+Н+
Н2 О
НАД+
СО2
СН2
COOH
фенилацетат
СН2 СН COOH
OH
фениллактат
54. Синтез катехоламинов
СИНТЕЗ КАТЕХОЛАМИНОВО2
СН2
OH
OH
OH
Н 2О
СО2
OH
тирозингидроксилаза
СН2
СН NH2
СН NH2
COOH
COOH
тирозин
ДОФА-декарбоксилаза
ДОФА
Н2О
дофамингидроксилаза
СН2
СН2 NH2
дофамин
OH
OH
О2
OH
SАМ
OH
СН OH
SАГ
метилтрансфераза
СН2 NH2
норадреналин
OH
СН
OH
СН2 NH
адреналин
CH3
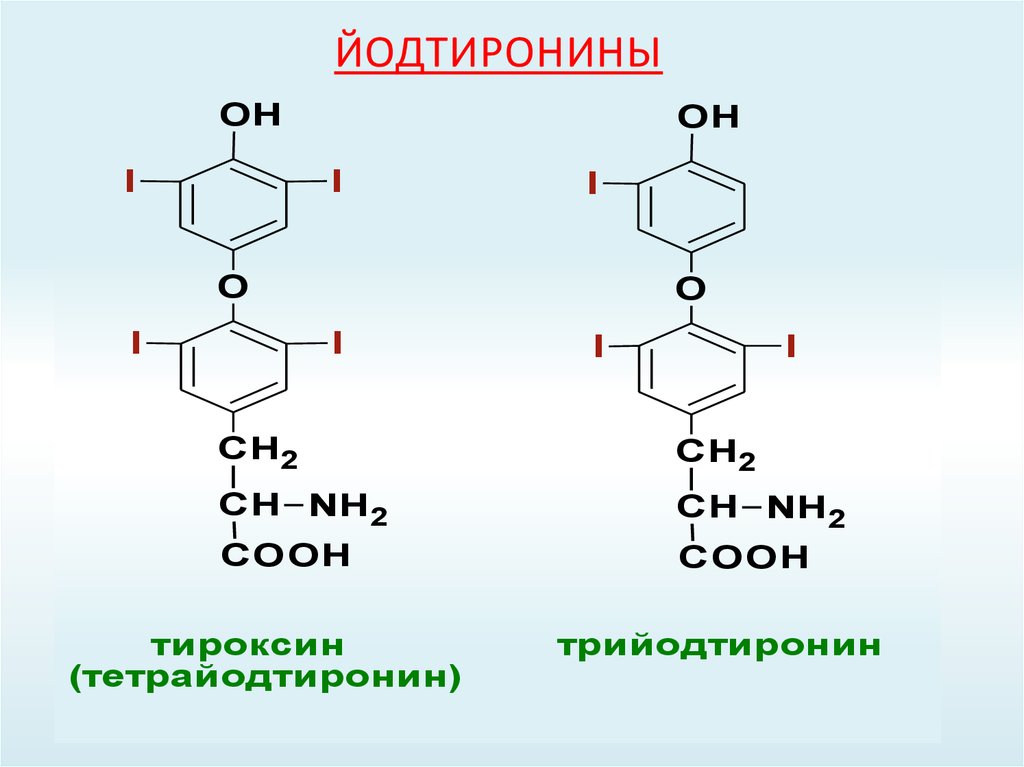
55. Йодтиронины
ЙОДТИРОНИНЫOH
I
OH
I
I
O
I
O
I
I
I
СН2
СН2
СН NH2
СН NH2
COOH
COOH
тироксин
(тетрайодтиронин)
трийодтиронин
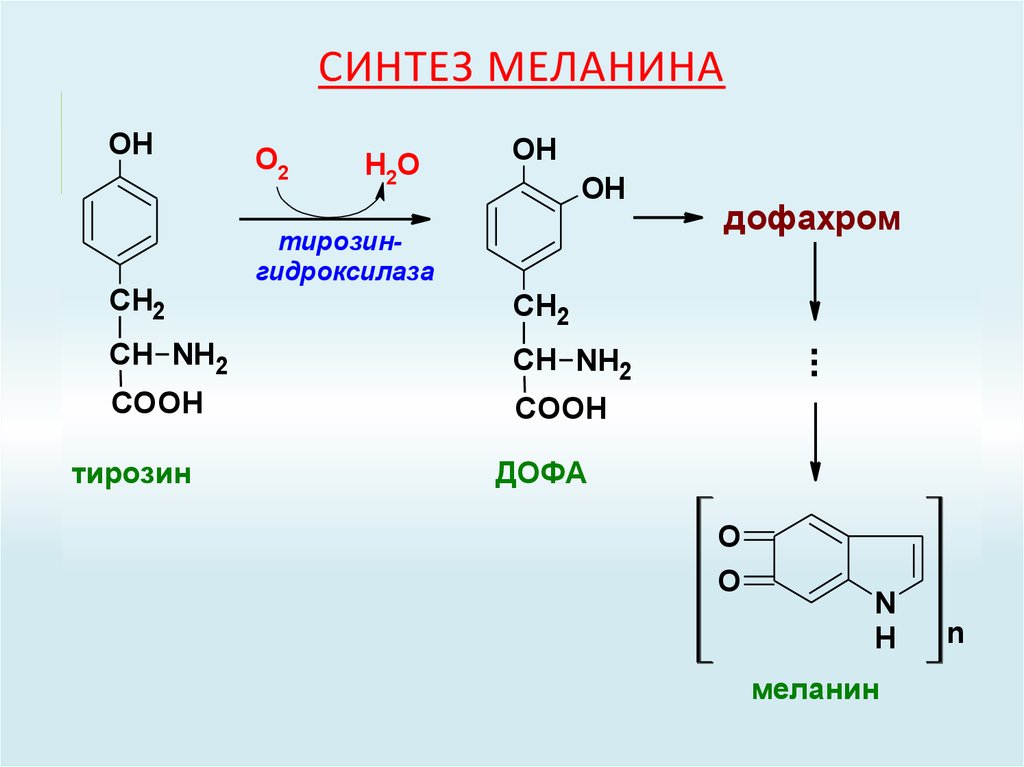
56. Синтез меланина
СИНТЕЗ МЕЛАНИНАСН2
О2
Н2О
OH
OH
тирозингидроксилаза
СН2
СН NH2
СН NH2
COOH
COOH
тирозин
дофахром
...
OH
ДОФА
O
O
N
H
меланин
n
57. Распад тирозина
РАСПАД ТИРОЗИНАOH
OH
OH
-КГ
глу
...
трансаминаза
СН2
СН NH2
С
COOH
COOH
тирозин
OH
O
п-гидроксифенилпируват
...
СН2
СН2 COOH
COOH
COOH
СН
гомогентезиновая
кислота
+
СН2
СН
С
COOH
COOH
фумарат
O
ацетоацетат
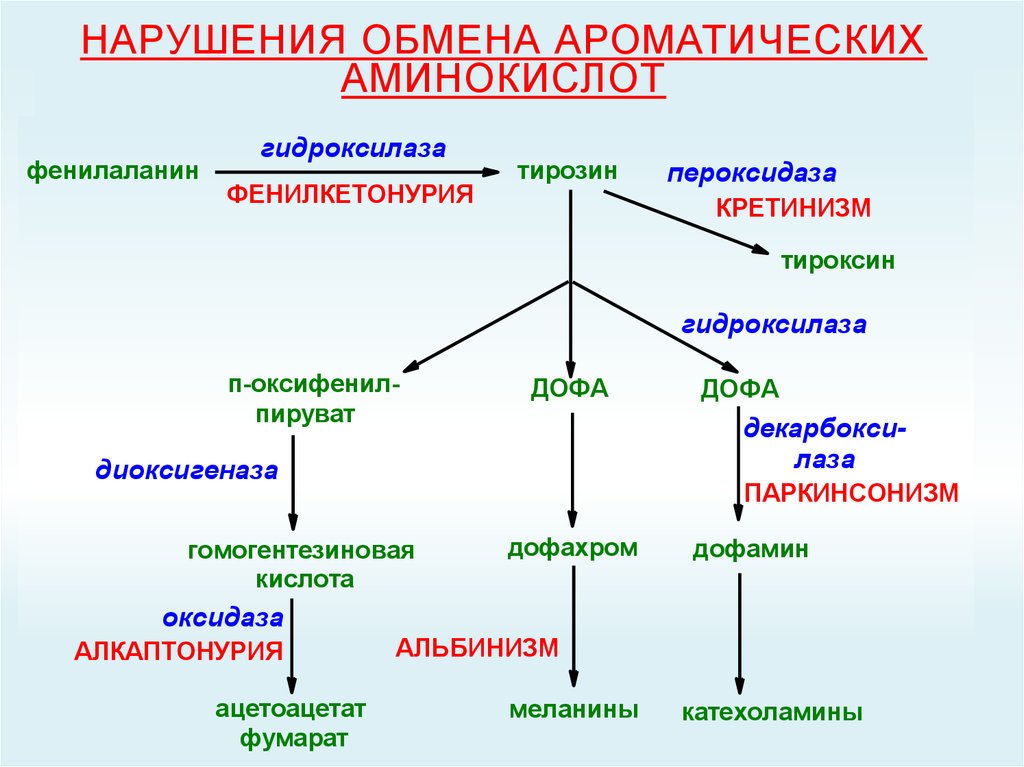
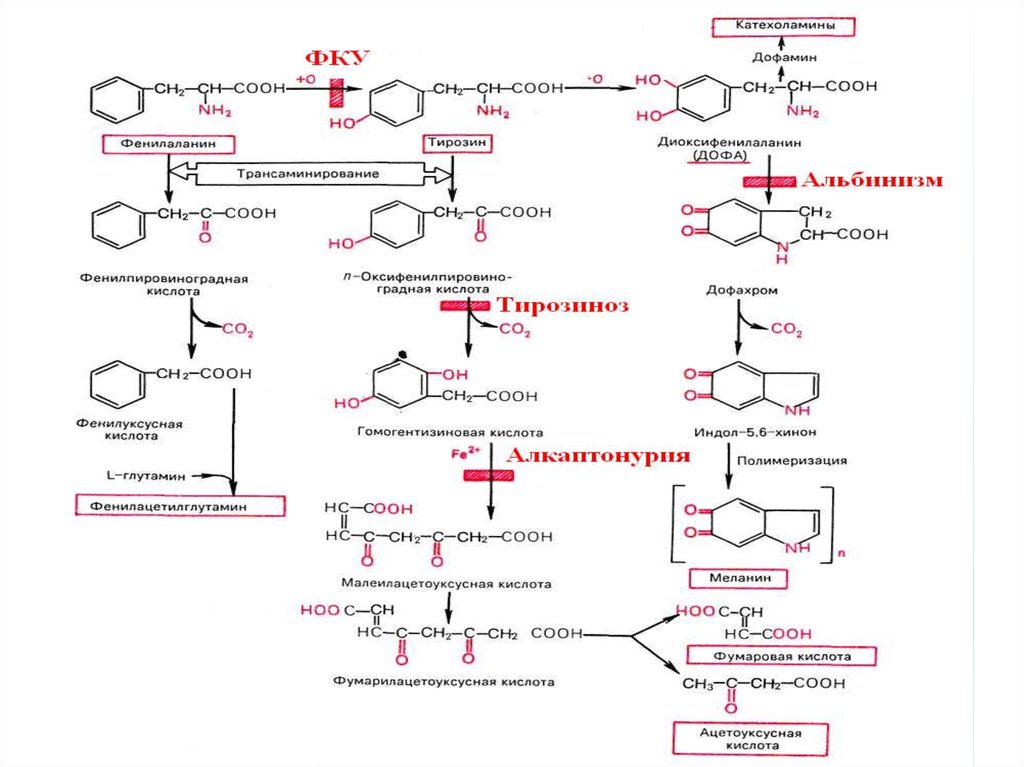
58. НАРУШЕНИЯ ОБМЕНА АРОМАТИЧЕСКИХ АМИНОКИСЛОТ
фенилаланингидроксилаза
ФЕНИЛКЕТОНУРИЯ
тирозин
пероксидаза
КРЕТИНИЗМ
тироксин
гидроксилаза
п-оксифенилпируват
ДОФА
ДОФА
декарбоксилаза
диоксигеназа
ПАРКИНСОНИЗМ
гомогентезиновая
кислота
дофахром
дофамин
оксидаза
АЛКАПТОНУРИЯ
ацетоацетат
фумарат
АЛЬБИНИЗМ
меланины
катехоламины
59.
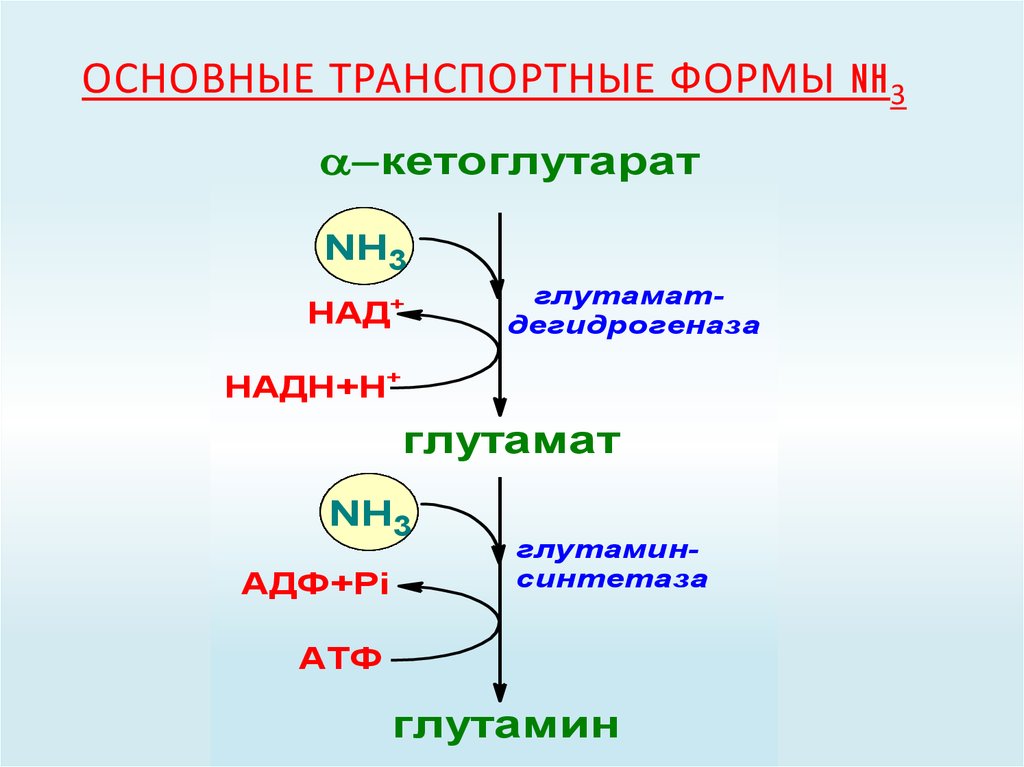
60. Основные транспортные формы NH3
ОСНОВНЫЕ ТРАНСПОРТНЫЕ ФОРМЫ NH3кетоглутарат
NH3
+
НАД
глутаматдегидрогеназа
НАДН+Н+
глутамат
NH3
АДФ+Рi
глутаминсинтетаза
АТФ
глутамин
61. Метаболизм глутамина в кишечнике
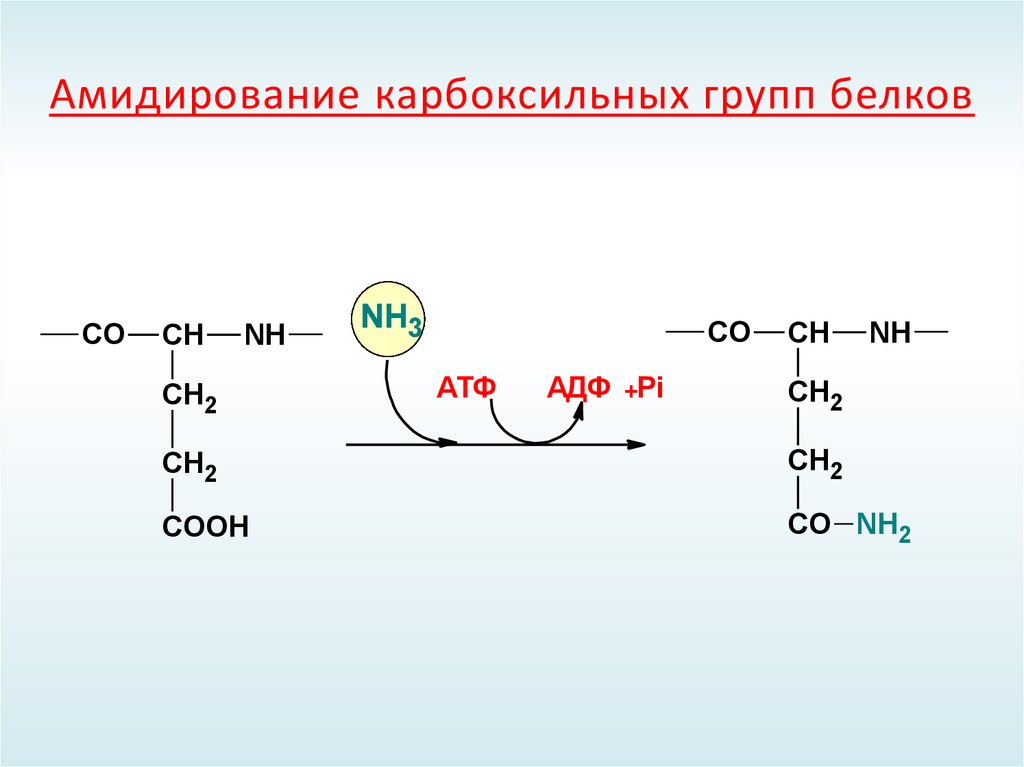
МЕТАБОЛИЗМ ГЛУТАМИНА В КИШЕЧНИКЕ62. Амидирование карбоксильных групп белков
H3CCO
СН
NH
СН2
NH3
H3C
CH3
АТФ
АДФ +Рi
CO
СН
NH
СН2
СН2
СН2
COOH
CO NH2
CH3
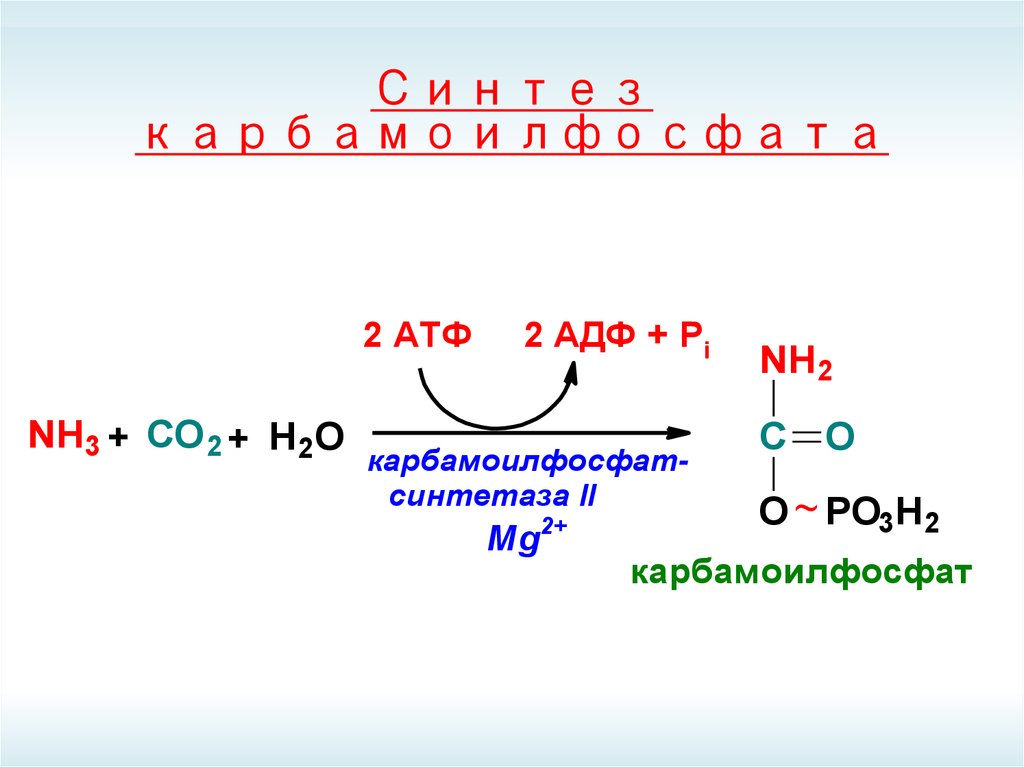
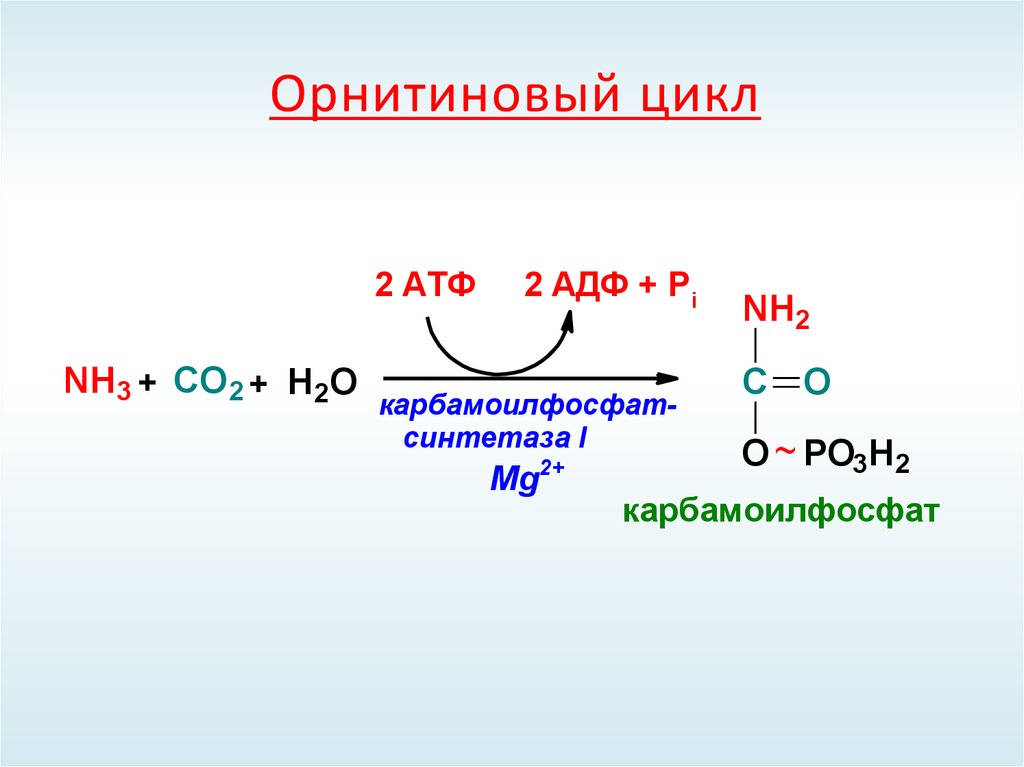
63. Синтез карбамоилфосфата
2 АТФNH3 + СО 2 + Н2О
2 АДФ + Pi
карбамоилфосфатсинтетаза II
2+
Мg
NH2
С O
O ~ PO3H2
карбамоилфосфат
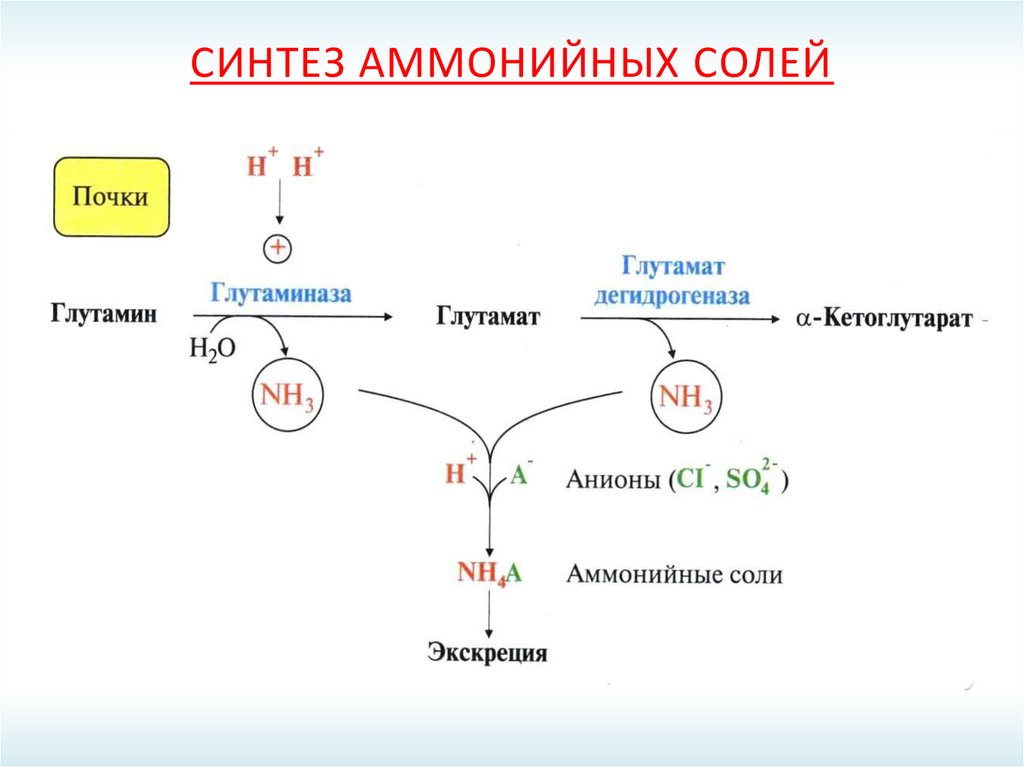
64. Синтез аммонийных солей
СИНТЕЗ АММОНИЙНЫХ СОЛЕЙ65. Орнитиновый цикл
2 АТФNH3 + СО 2 + Н2О
2 АДФ + Pi
карбамоилфосфатсинтетаза I
2+
Мg
NH2
С O
O ~ PO3H2
карбамоилфосфат
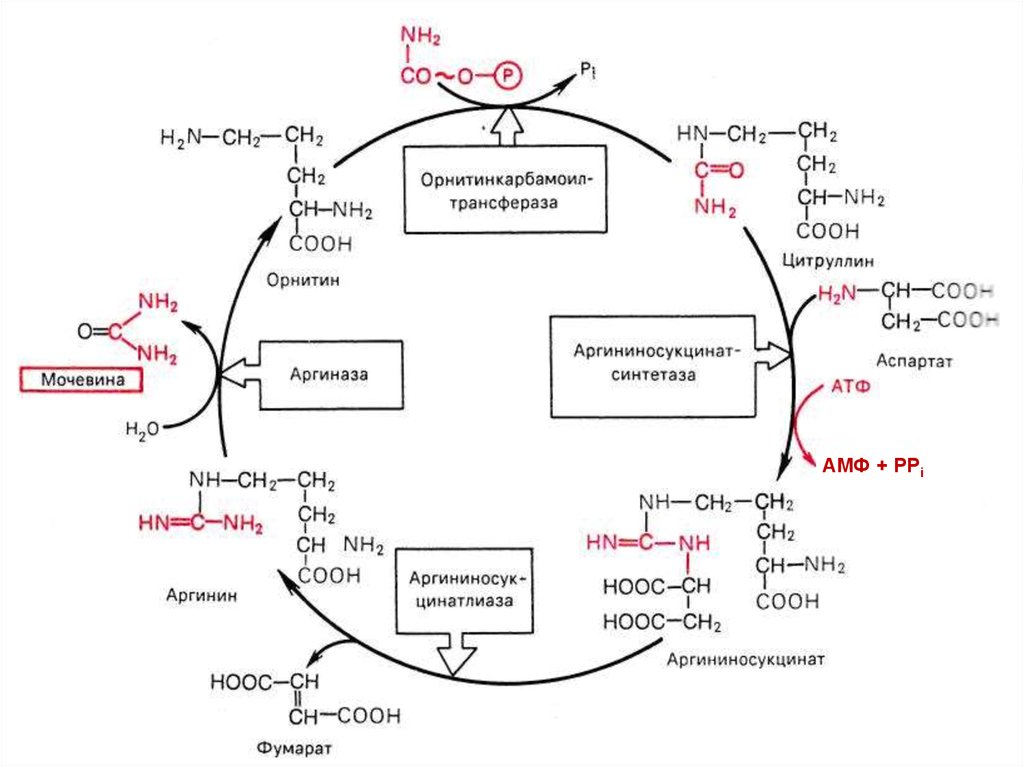
66.
NH2NH2
С O
Н3РО4
(СН2)3
+
O ~ PO3H2
карбамоилфосфат
СН NH2
орнитинкарбамоил
трансфераза
NH2
С O
NH
(СН2)3
COOH
СН NH2
орнитин
COOH
цитруллин
67.
NH2С O
NH
H2N СН
+
(СН2)3
СН2
COOH
COOH
NH2
COOH
АТФ
АМФ + РPi
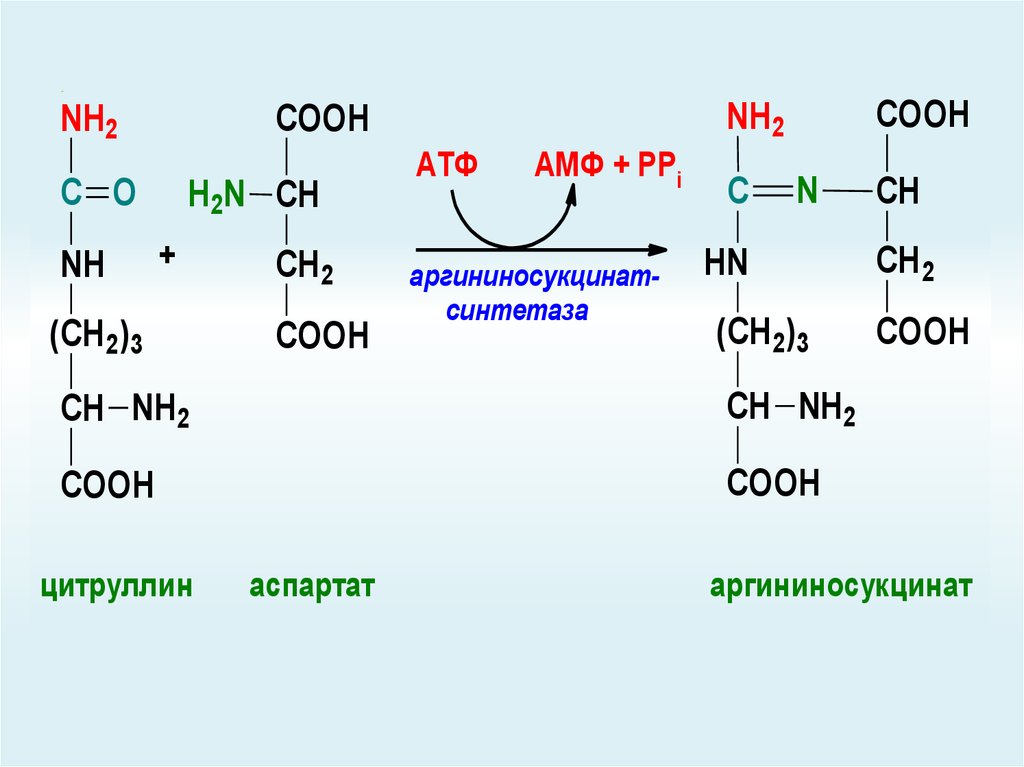
аргининосукцинатсинтетаза
С
N
HN
(СН2)3
СН NH2
СН NH2
COOH
COOH
цитруллин
аспартат
СН
СН2
COOH
аргининосукцинат
68.
COOHNH2
С
N
NH2
СН
HN
СН2
(СН2)3
COOH
С NH
аргининосукцинатлиаза
СН
NH
(СН2)3
СН NH2
СН NH2
COOH
COOH
аргининосукцинат
COOH
аргинин
+
СН
COOH
фумарат
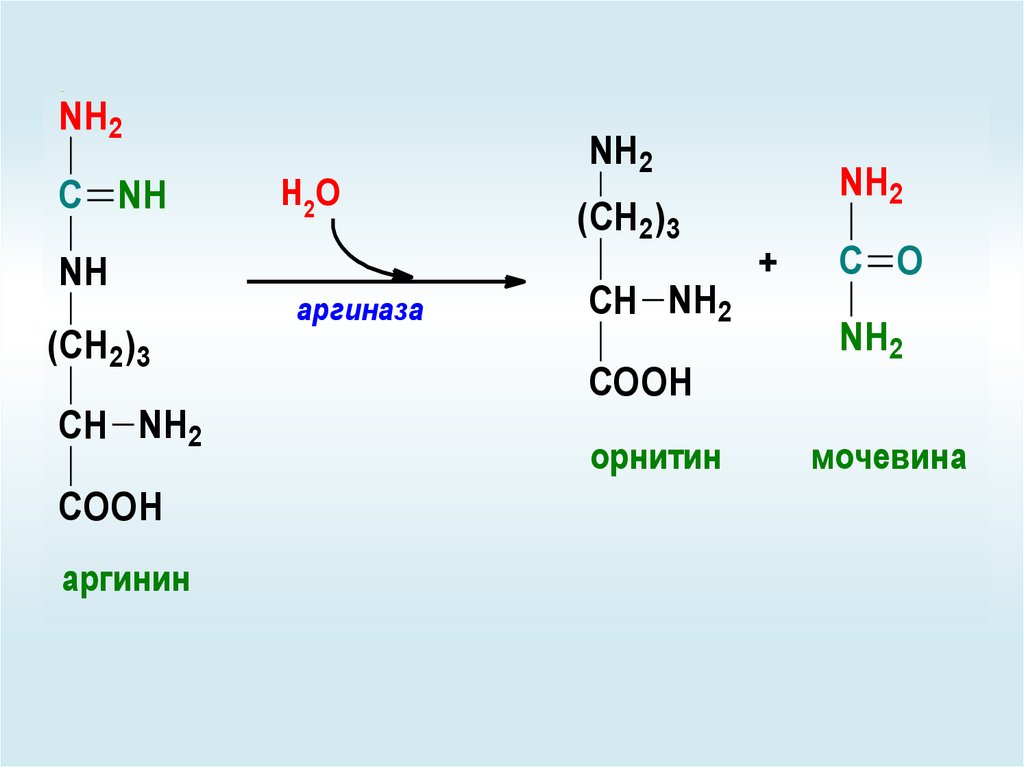
69.
NH2С NH
NH
(СН2)3
СН NH2
COOH
аргинин
Н2О
аргиназа
NH2
NH2
(СН2)3
СН NH2
+
С O
NH2
COOH
орнитин
мочевина
70.
АМФ + РРi71. Нарушения синтеза мочевины
ГИПЕРАММОНИЕМИЯI типа
NH3 + СО2 + 2 АТ Ф
H2 N
С
карбамоилфосфатсинтетаза
карбамоил+ 2 АДФ + 2 Рi
фосфат
карбамоилтрансфераза
NH2
O
ГИПЕРАММОНИЕМИЯ
II типа
орнитин-
орнитин
Н2О
аргинин
цитруллин
аспартат
АТФ
фумарат
аргининсукцинатсинтетаза
аргининсукцинатлиаза
АРГИНИНЯНТАРНАЯ
АМИНОАЦИДУРИЯ
аргинин-янтарная
кислота
ЦИТРУЛЛИНЕМИЯ
72. Нарушение синтеза и выведения мочевины
НАРУШЕНИЕ СИНТЕЗА И ВЫВЕДЕНИЯМОЧЕВИНЫ
УРЕМИЯ
ПРОДУКЦИОННАЯ
РЕТЕНЦИОННАЯ
ПОЧЕЧНАЯ
ВНЕПОЧЕЧНАЯ
73. Количество азотсодержащих веществ в моче (%) при нормальном белковом питании
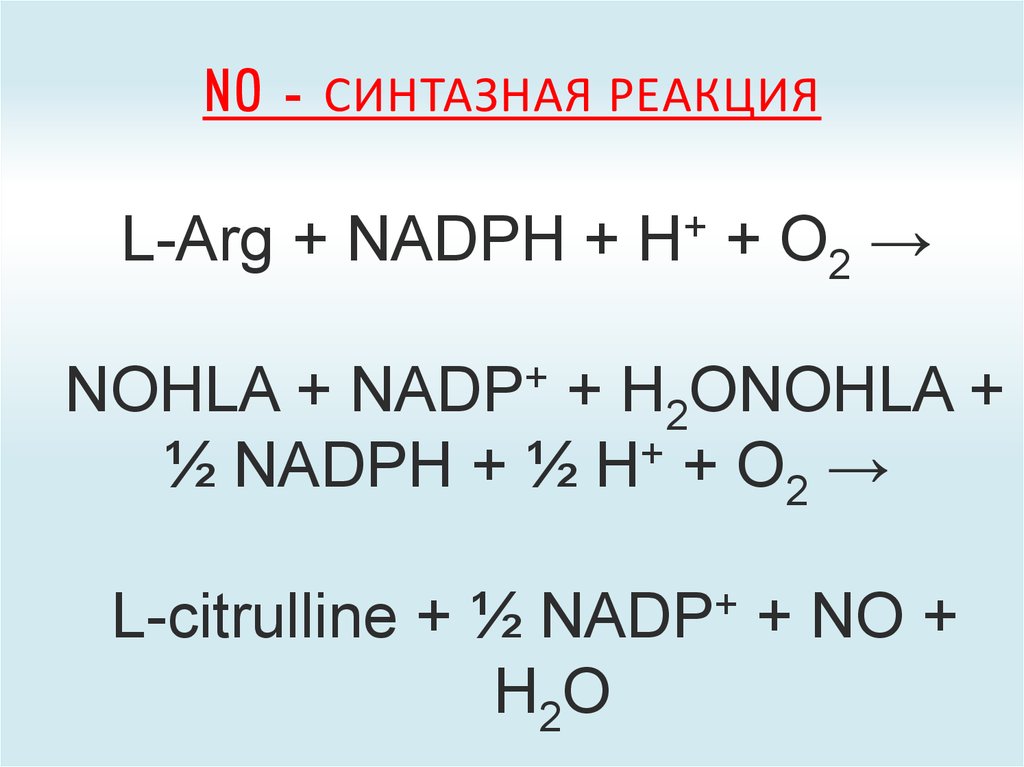
74. NO - СИНТАЗНАЯ РЕАКЦИЯ
L-Arg + NADPH + H+ + O2 →NOHLA + NADP+ + H2ONOHLA +
½ NADPH + ½ H+ + O2 →
L-citrulline + ½ NADP+ + NO +
H2 O
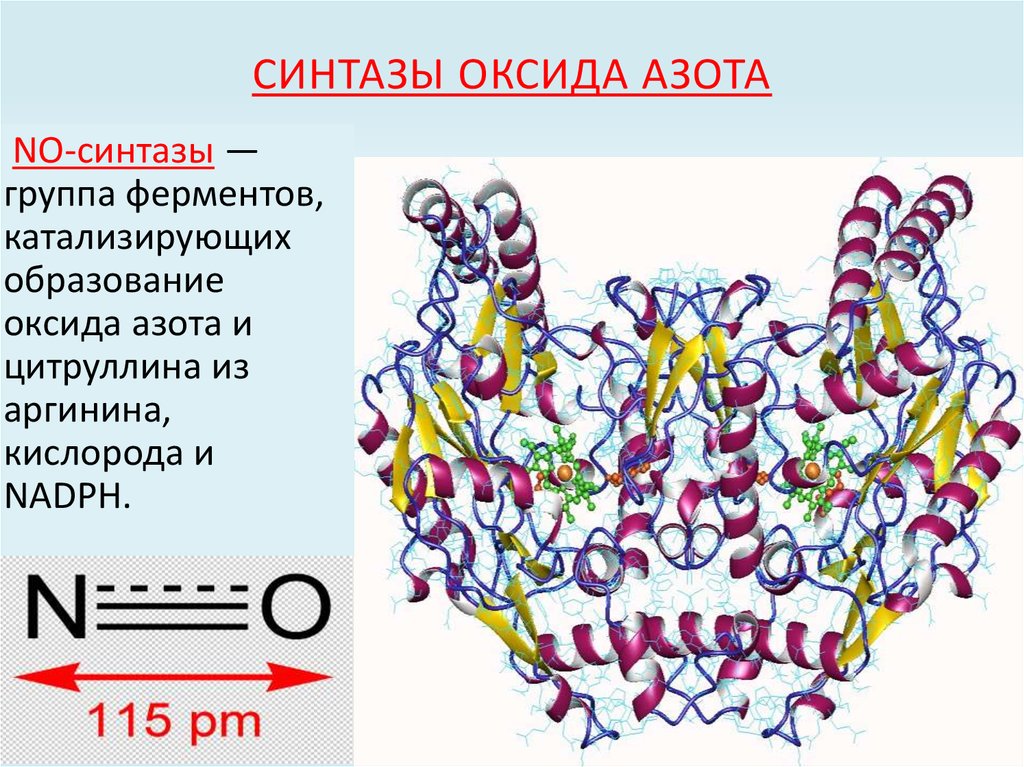
75. СИНТАЗЫ ОКСИДА АЗОТА
NO-синтазы —группа ферментов,
катализирующих
образование
оксида азота и
цитруллина из
аргинина,
кислорода и
NADPH.
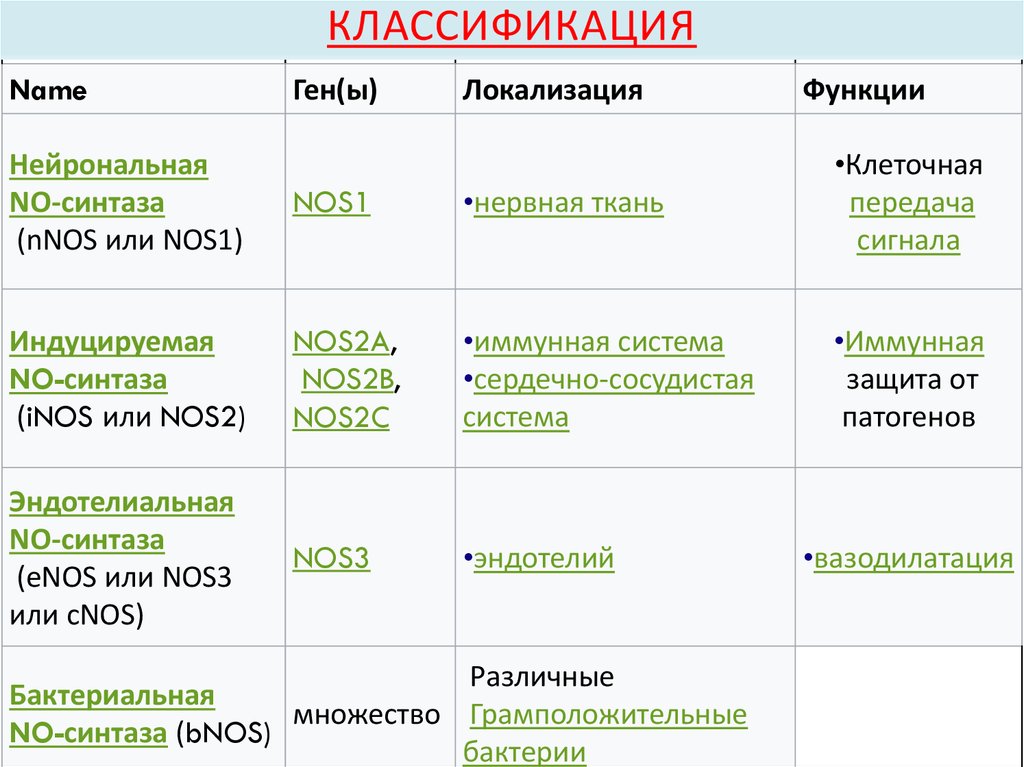
76. Классификация
КЛАССИФИКАЦИЯName
Ген(ы)
Локализация
Функции
Нейрональная
NO-синтаза
(nNOS или NOS1)
NOS1
•нервная ткань
•Клеточная
передача
сигнала
Индуцируемая
NO-синтаза
(iNOS или NOS2)
NOS2A,
NOS2B,
NOS2C
•иммунная система
•сердечно-сосудистая
система
•Иммунная
защита от
патогенов
Эндотелиальная
NO-синтаза
(eNOS или NOS3
или cNOS)
NOS3
•эндотелий
Различные
Бактериальная
множество Грамположительные
NO-синтаза (bNOS)
бактерии
•вазодилатация
























 biology
biology








