Similar presentations:
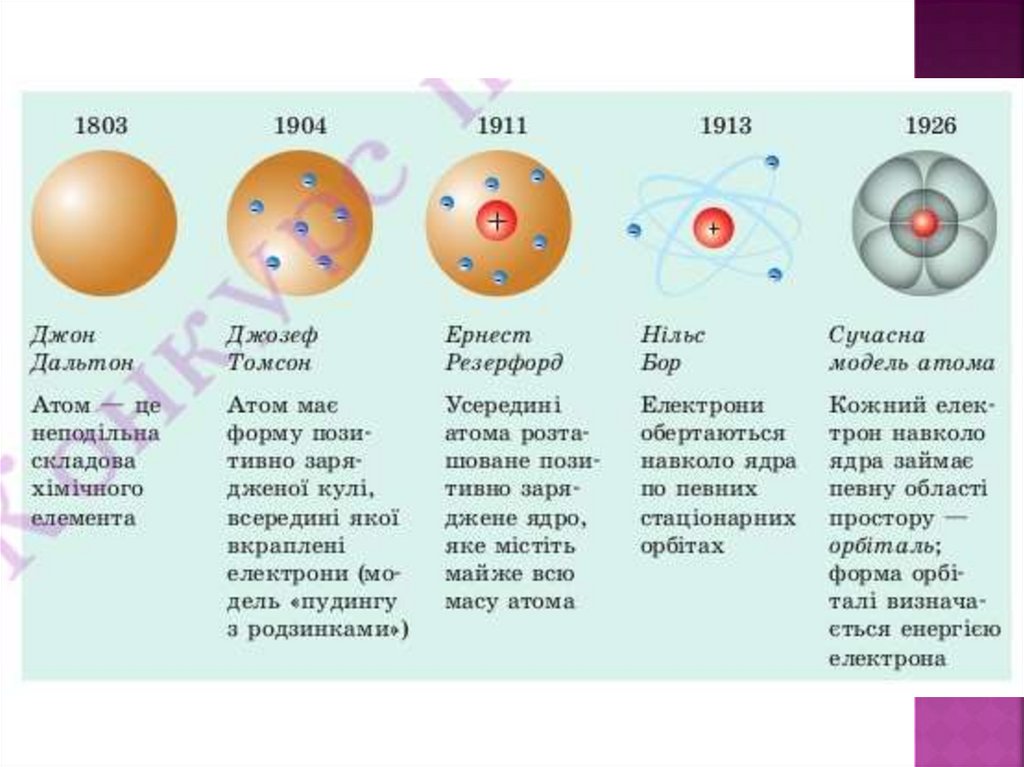
Сучасна модель атома
1.
Вчитель фізики: Мар’єнкоАнна Олександрівна
2.
Увага! Умовні позначення:Текст
Текст
- Просто читати! Ця промова
для тих, хто був відсутній на
Zoom конференції
- Обов’язково законспектувати!
Малюнки перемальовувати за бажанням
3.
Дж. Дж. Томсон(1856–1940), англійський фізик, що
отримав Нобелевську премію з
фізики за роботи, що призвели до
відкриття електрона (1897 р).
Модель будови атома
Дж. Томсона - «пудинг»
4.
Ернест Резерфорд(1871–1937) — видатний
англійський фізик. Заклав
основи
вчення
про
радіоактивність і будову
атома, здійснив першу
ядерну
реакцію,
передбачив
існування
нейтрона.
5.
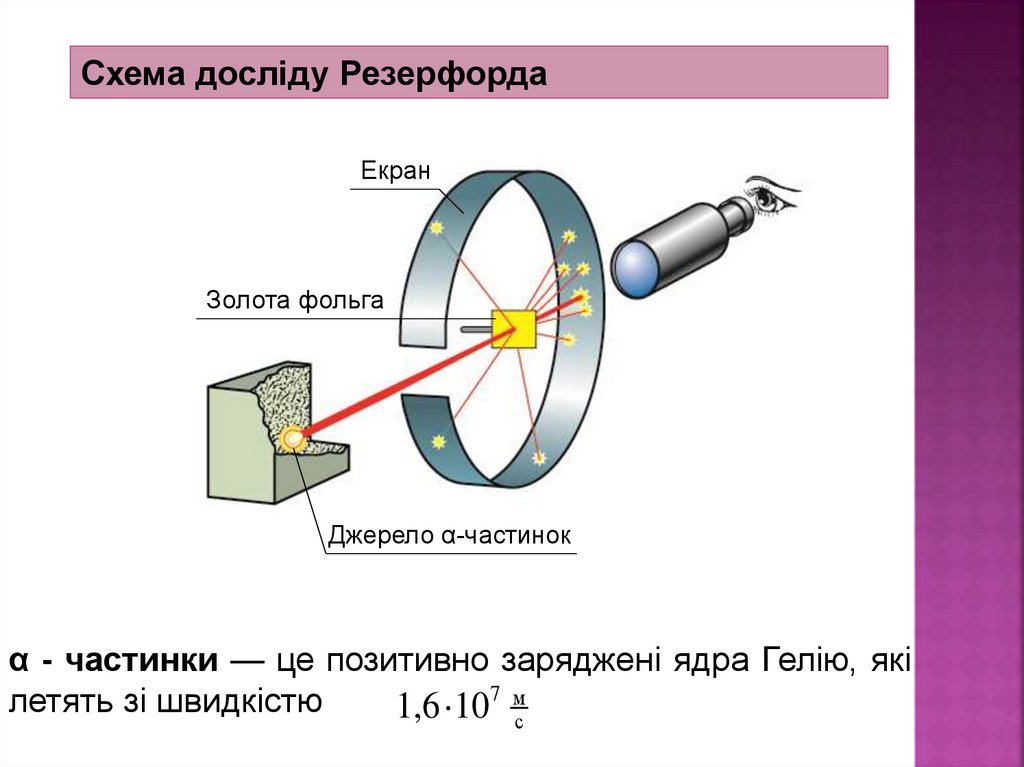
Схема досліду РезерфордаЕкран
Золота фольга
Джерело α-частинок
α - частинки — це позитивно заряджені ядра Гелію, які
летять зі швидкістю
1,6 107 мс
6.
Дослід Резерфорда:Для досліду вчений використав речовину, із якої із
великою швидкістю вилітали позитивно-заряджені
частинки – так звані α - частинки (альфа частинки).
Вузький пучок α – частинок зі свинцевого контейнера
спрямувався на тонку золоту фольгу, а далі потрапляв в
екран, покритий шаром кристалів цинк сульфіду. Якщо
в такий екран улучала α – частинка, то в місці її
влучання відбувався слабкий спалах світла. Учений
спостерігав спалахи за допомогою мікроскопа та
реєстрували влучання α – частинок в екран.
У результаті дослідів було з’ясовано, що переважна
більшість α – частинок проходить крізь золоту фольгу, не
змінюючи напрямку руху, деякі відхиляються від
початкової траєкторії.
7. Схема досліду Резерфорда
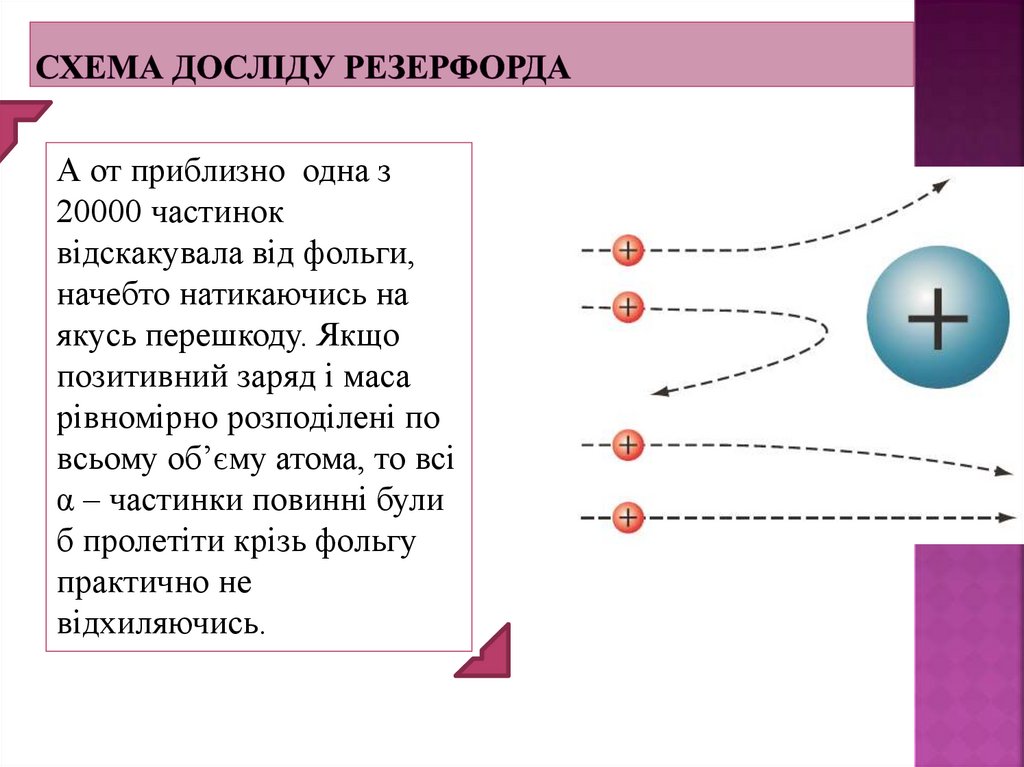
А от приблизно одна з20000 частинок
відскакувала від фольги,
начебто натикаючись на
якусь перешкоду. Якщо
позитивний заряд і маса
рівномірно розподілені по
всьому об’єму атома, то всі
α – частинки повинні були
б пролетіти крізь фольгу
практично не
відхиляючись.
8.
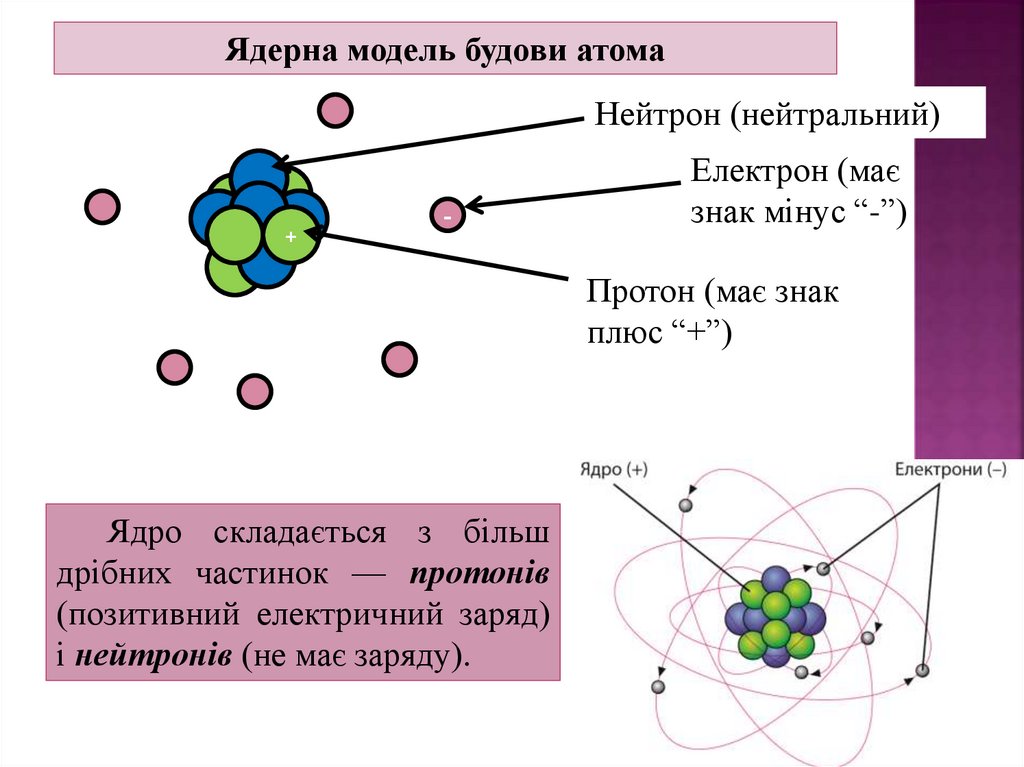
Ядерна модель будови атомаНейтрон (нейтральний)
+
-
Електрон (має
знак мінус “-”)
Протон (має знак
плюс “+”)
Ядро складається з більш
дрібних частинок — протонів
(позитивний електричний заряд)
і нейтронів (не має заряду).
9.
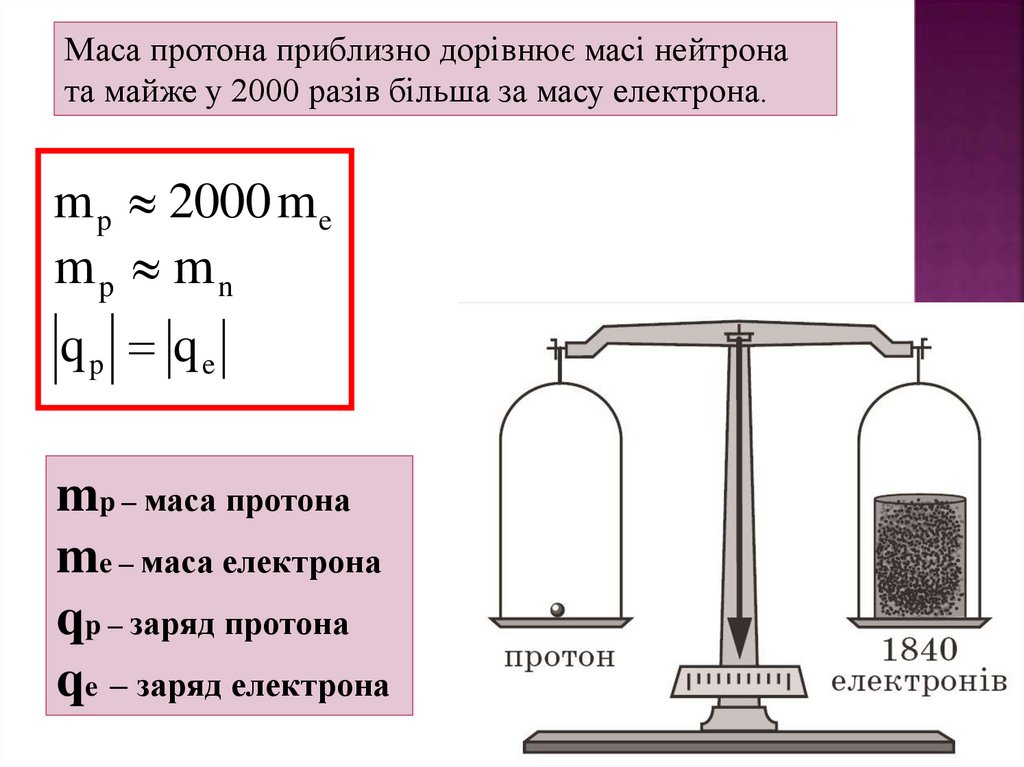
Маса протона приблизно дорівнює масі нейтроната майже у 2000 разів більша за масу електрона.
m p 2000 m e
mp mn
qp qe
mp – маса протона
me – маса електрона
qp – заряд протона
qe – заряд електрона
10.
11.
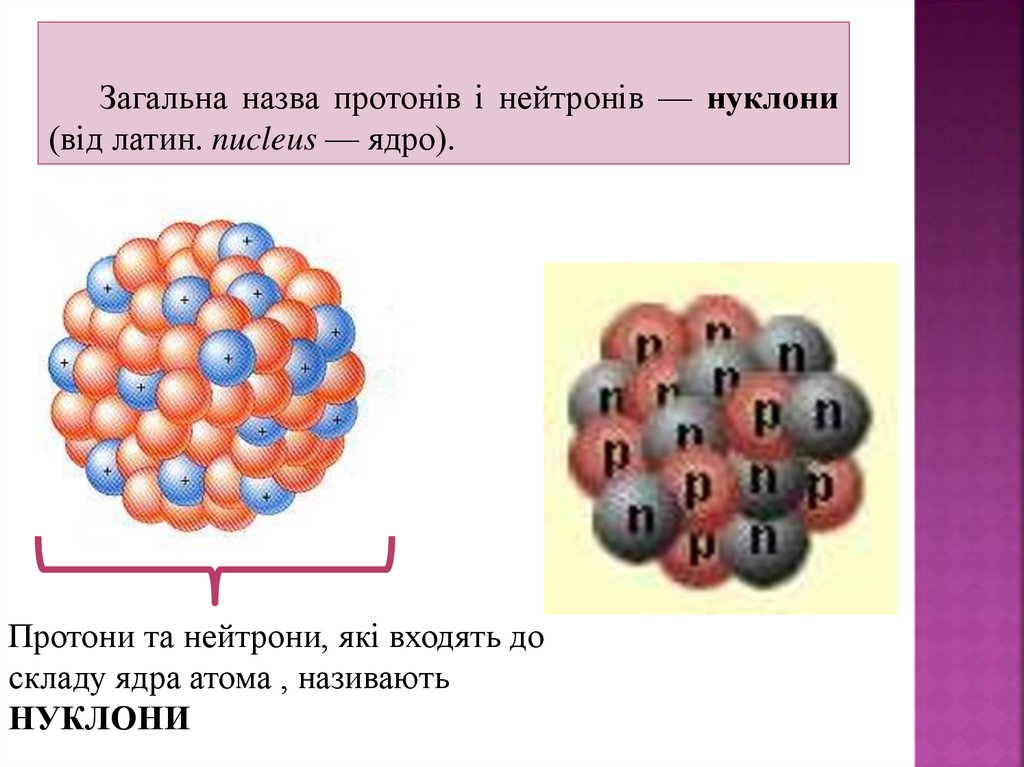
Загальна назва протонів і нейтронів — нуклони(від латин. nucleus — ядро).
Протони та нейтрони, які входять до
складу ядра атома , називають
НУКЛОНИ
12.
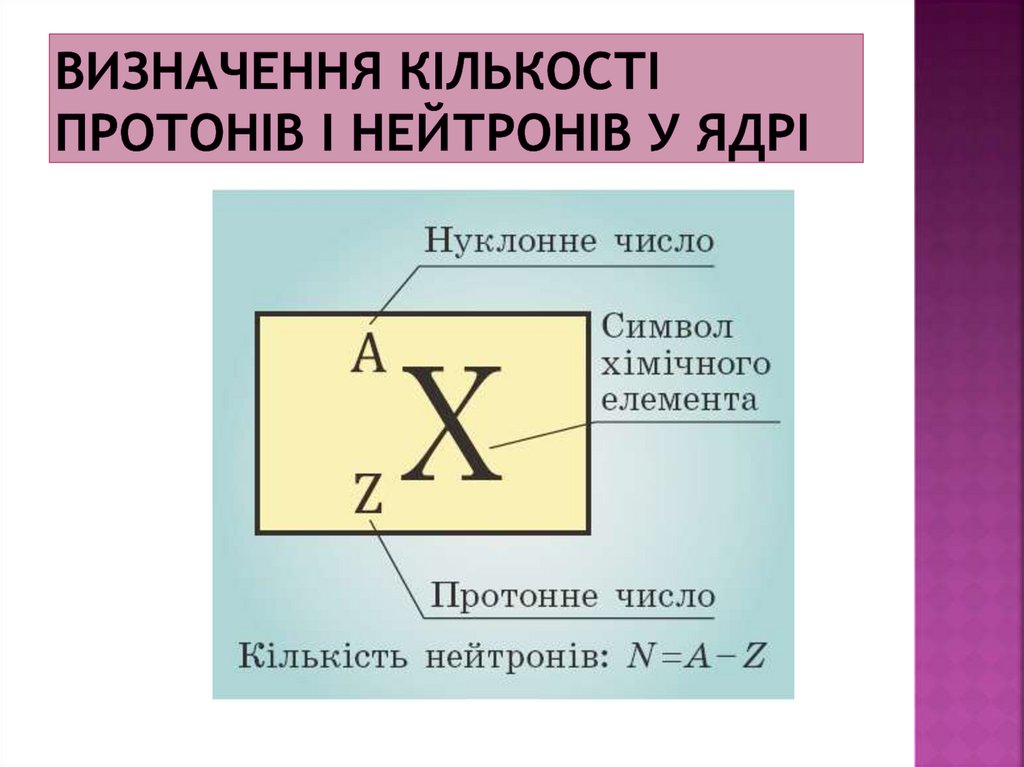
Z (зарядове (протонне)протонів у ядрі атома
число)
–
кількість
N – кількість нейтронів у ядрі атома
А (нуклонне (масове) число) – сумарна кількість
нейтронів і протонів у ядрі атома
Нуклонне (масове) число A, яке визначає атомну
масу елемента, дорівнює сумі чисел нейтронів N і
протонів Z у ядрі:
A Z N
13. Визначення кількості протонів і нейтронів у ядрі
14. Завдання
42
He
238
92
U
масове число
4
протони
2
нейтрони
2
масове число
238
протони
92
нейтрони
238 - 92=146
15.
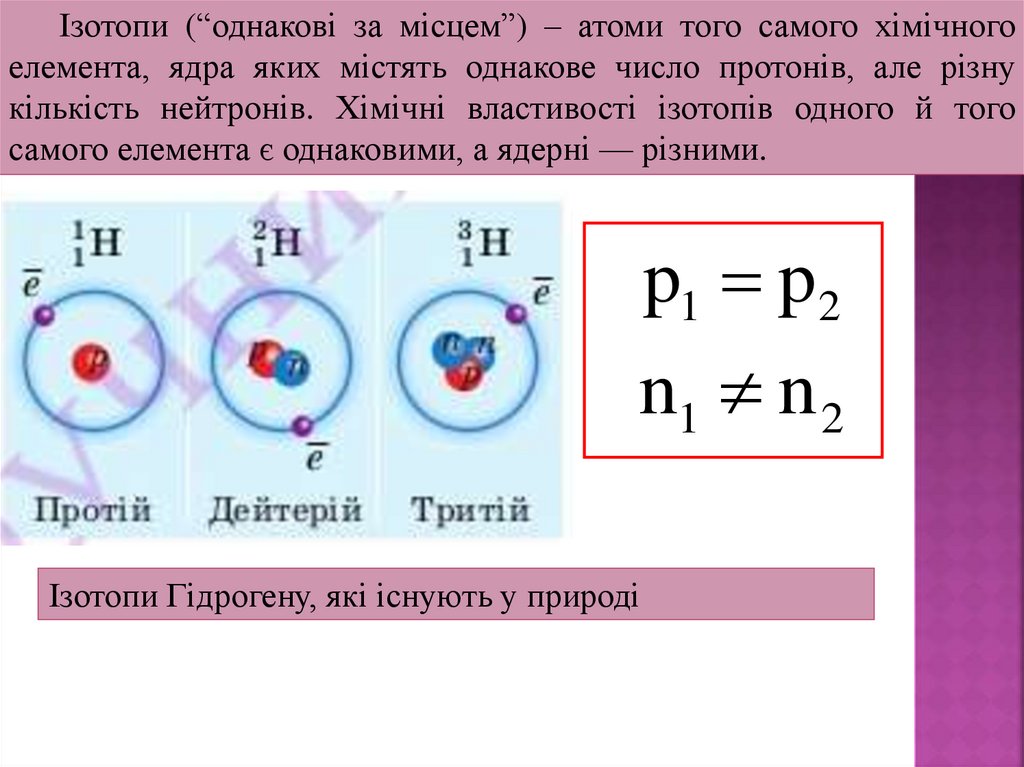
Ізотопи (“однакові за місцем”) – атоми того самого хімічногоелемента, ядра яких містять однакове число протонів, але різну
кількість нейтронів. Хімічні властивості ізотопів одного й того
самого елемента є однаковими, а ядерні — різними.
p1 p2
n1 n 2
Ізотопи Гідрогену, які існують у природі
16.
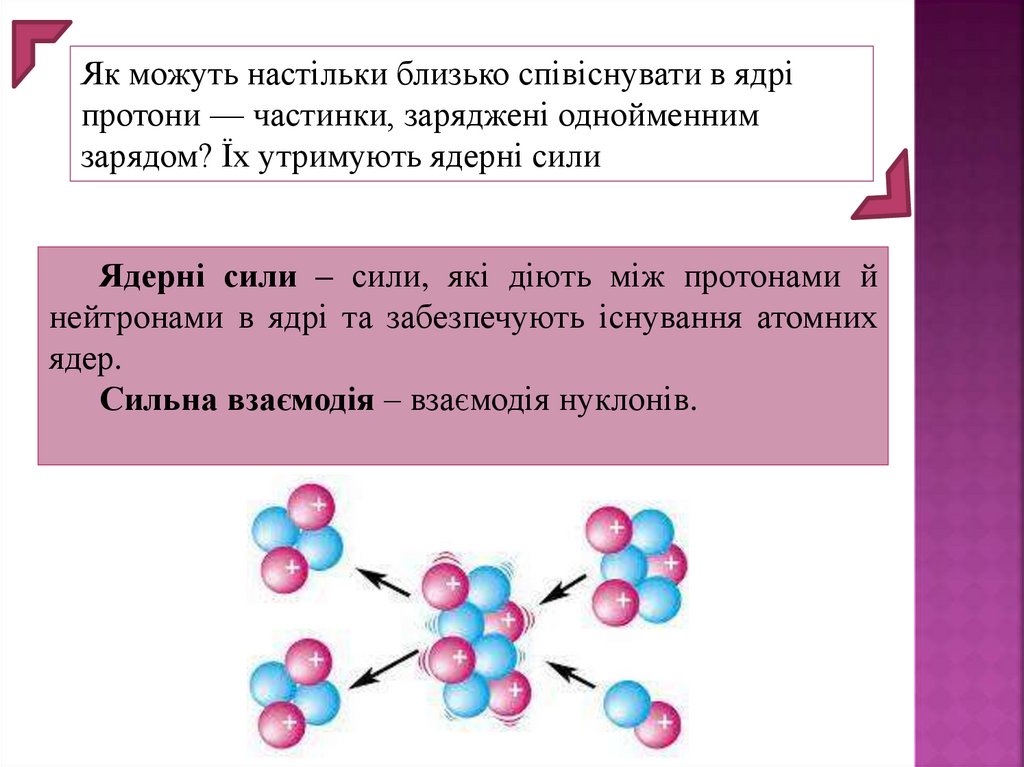
Як можуть настільки близько співіснувати в ядріпротони — частинки, заряджені однойменним
зарядом? Їх утримують ядерні сили
Ядерні сили – сили, які діють між протонами й
нейтронами в ядрі та забезпечують існування атомних
ядер.
Сильна взаємодія – взаємодія нуклонів.
17.
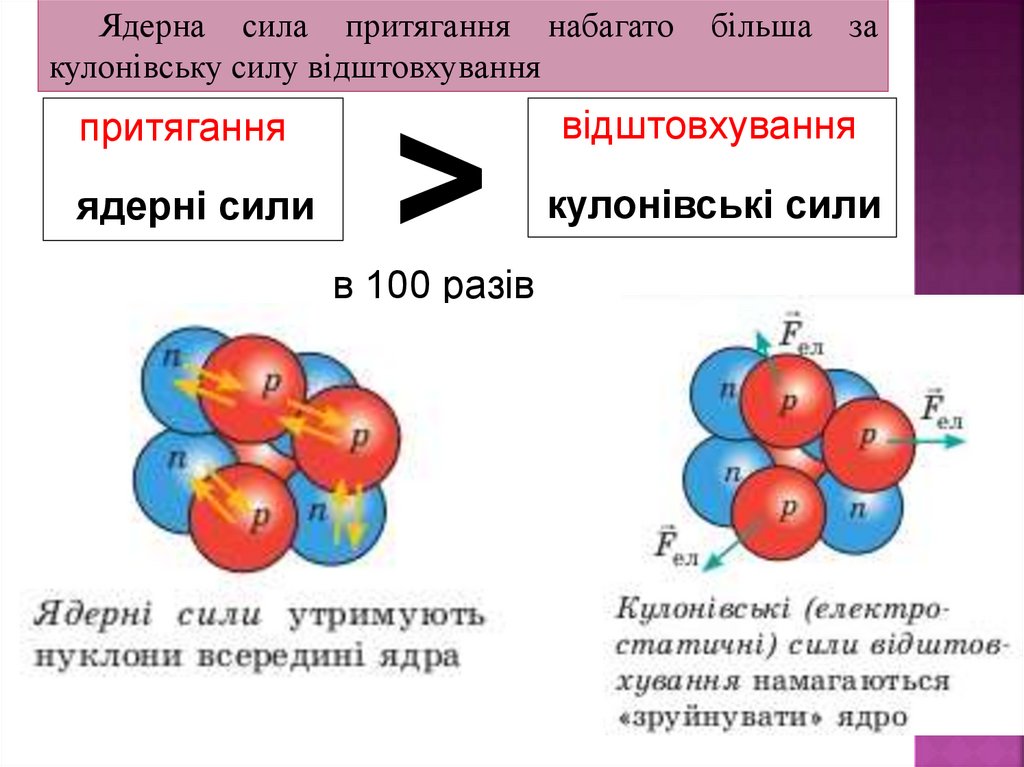
Ядерна сила притягання набагатокулонівську силу відштовхування
притягання
ядерні сили
>
в 100 разів
більша
за
відштовхування
кулонівські сили
18.
Основні властивості ядерних силЄ тільки силами притягання;
Є близькодіючими (ядерні сили між нуклонами
виявляються на відстані приблизно рівних розмірам
нуклонів);
Не залежать від заряду (на однаковій відстані сили,
що діють між двома протонами, між двома
нейтронами або між протоном і нейтроном, є
однаковими);
Мають властивість насичення (нуклон виявляється
здатним до ядерної взаємодії одночасно лише з
невеликою кількістю нуклонів-”сусідів”).
19.
Дякую за вашуувагу!








 physics
physics








