Similar presentations:
Химический состав живых организмов. Спирты
1.
Химический составживых организмов.
Спирты
2.
Кислородсодержащиеорганические
соединения
органические
соединения,
содержащие С, Н, О.
Функциональная группа – группа
атомов, определяющая характерные
свойства и принадлежность вещества
к определенному классу соединений.
3.
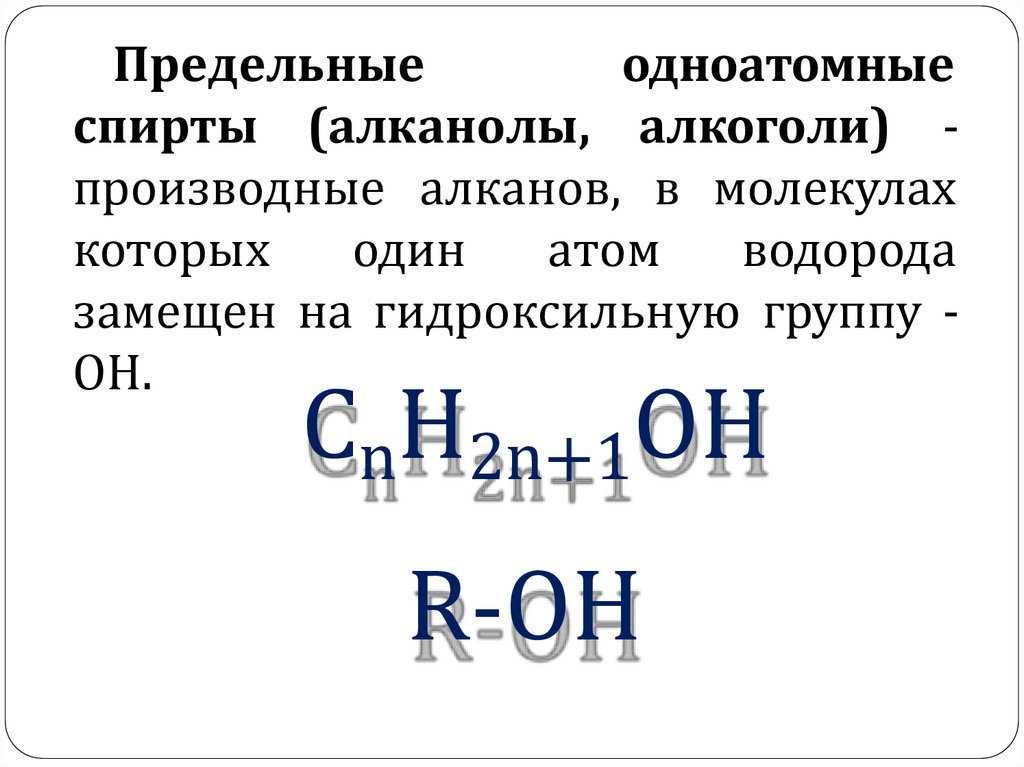
Предельныеодноатомные
спирты (алканолы, алкоголи) производные алканов, в молекулах
которых
один
атом
водорода
замещен на гидроксильную группу ОН.
СnH2n+1OH
R-ОН
4.
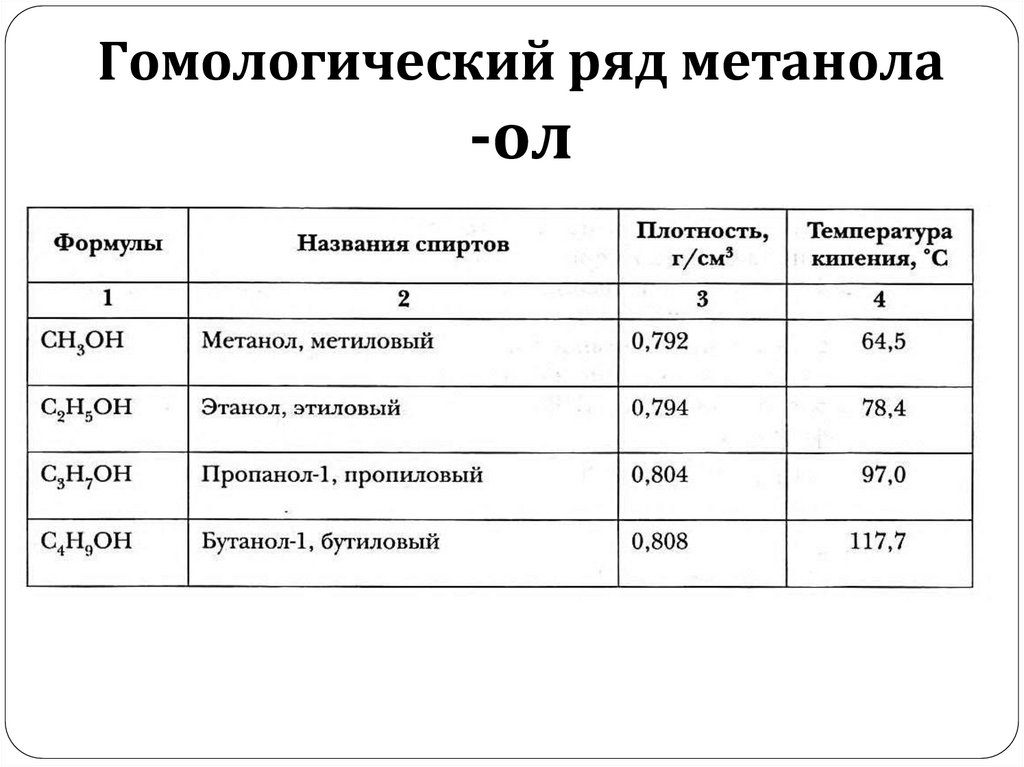
Гомологический ряд метанола-ол
5.
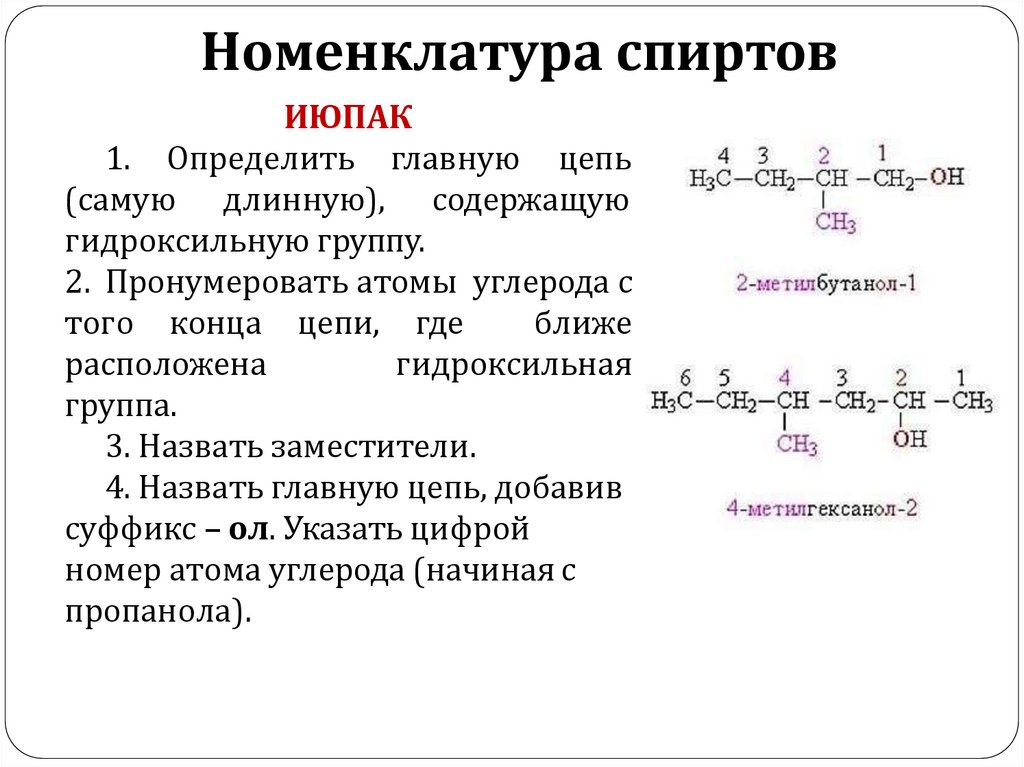
Номенклатура спиртовИЮПАК
1. Определить главную цепь
(самую длинную), содержащую
гидроксильную группу.
2. Пронумеровать атомы углерода с
того конца цепи, где
ближе
расположена
гидроксильная
группа.
3. Назвать заместители.
4. Назвать главную цепь, добавив
суффикс – ол. Указать цифрой
номер атома углерода (начиная с
пропанола).
6.
Изомерия спиртовI. Структурная изомерия
1. Изомерия углеродного скелета (начиная
с С4):
7.
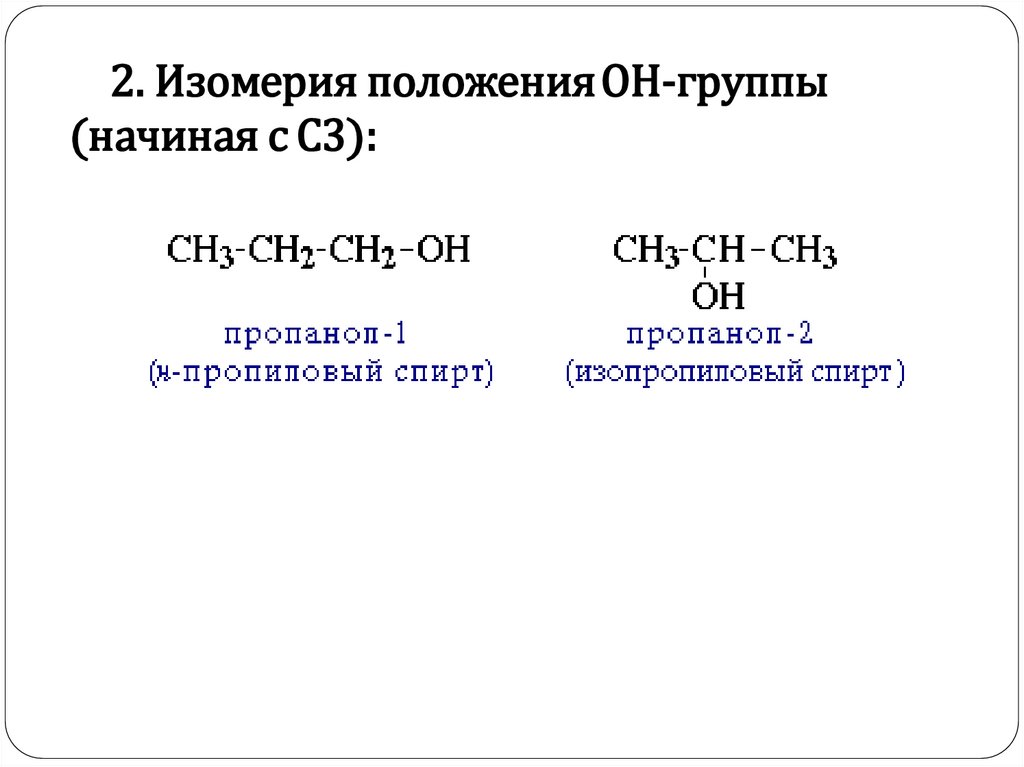
2. Изомерия положенияОН-группы(начиная с С3):
8.
3. Межклассовая изомерия с простымиэфирами:
этиловый спирт СН3CH2–OH
диметиловый эфир CH3–O–CH3
9.
Физические свойства спиртовВидеоопыт: Физические свойства спиртов
Почему первые представители
гомологического ряда не газы, а
жидкости?
10.
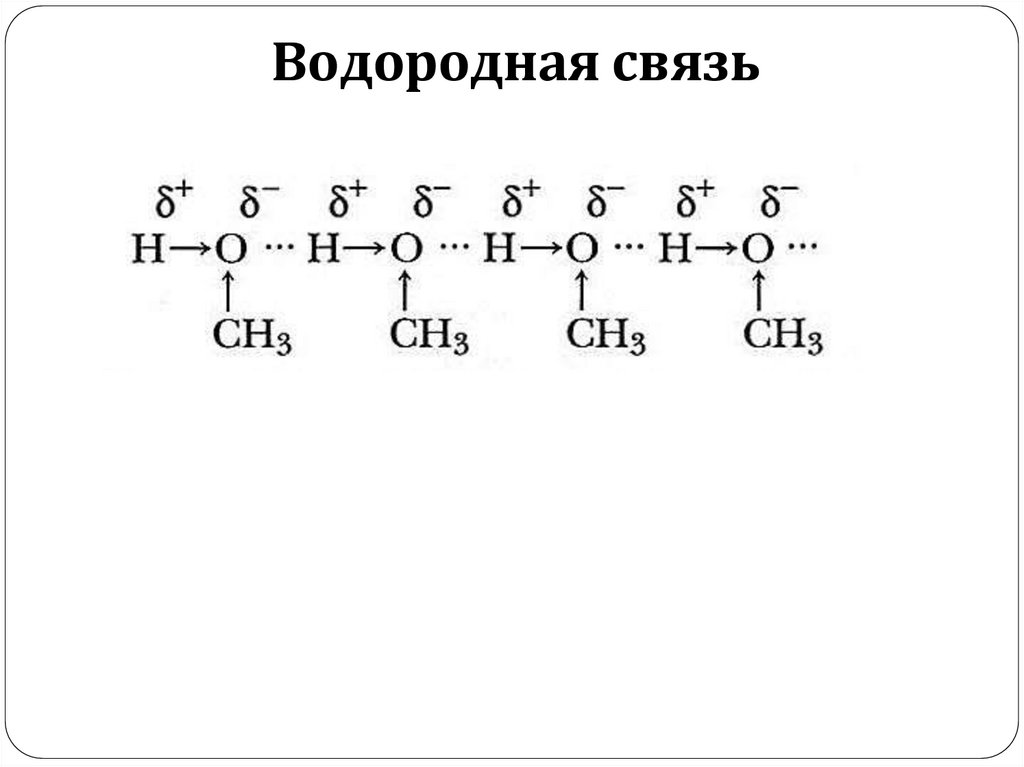
Водородная связь11.
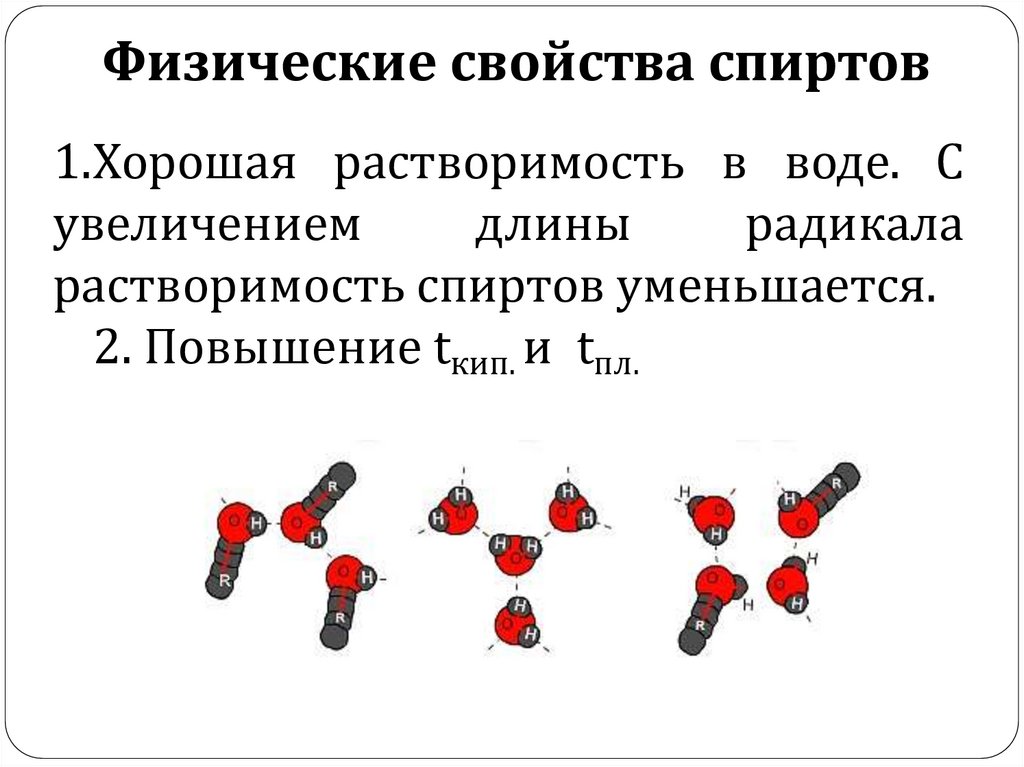
Физические свойства спиртов1.Хорошая растворимость в воде. С
увеличением
длины
радикала
растворимость спиртов уменьшается.
2. Повышение tкип. и tпл.
12.
Химические свойства спиртов1. Кислотные свойства спиртов (замещение
ат. Н в гидроксильной группе ):
2С2H5OH + 2Na 2С2H5ONa + H2
этилат натрия
Опыт. Взаимодействие этилового спирта с металлическим натрием
RONa - алкоголяты
13.
2. Взаимодействие сгалогеноводородами :
H2SO4 конц.
C2H5OH + HBr ⇄ C2H5Br + H2O
бромэтан
Опыт. Взаимодействие этилового спирта с бромоводородом
14.
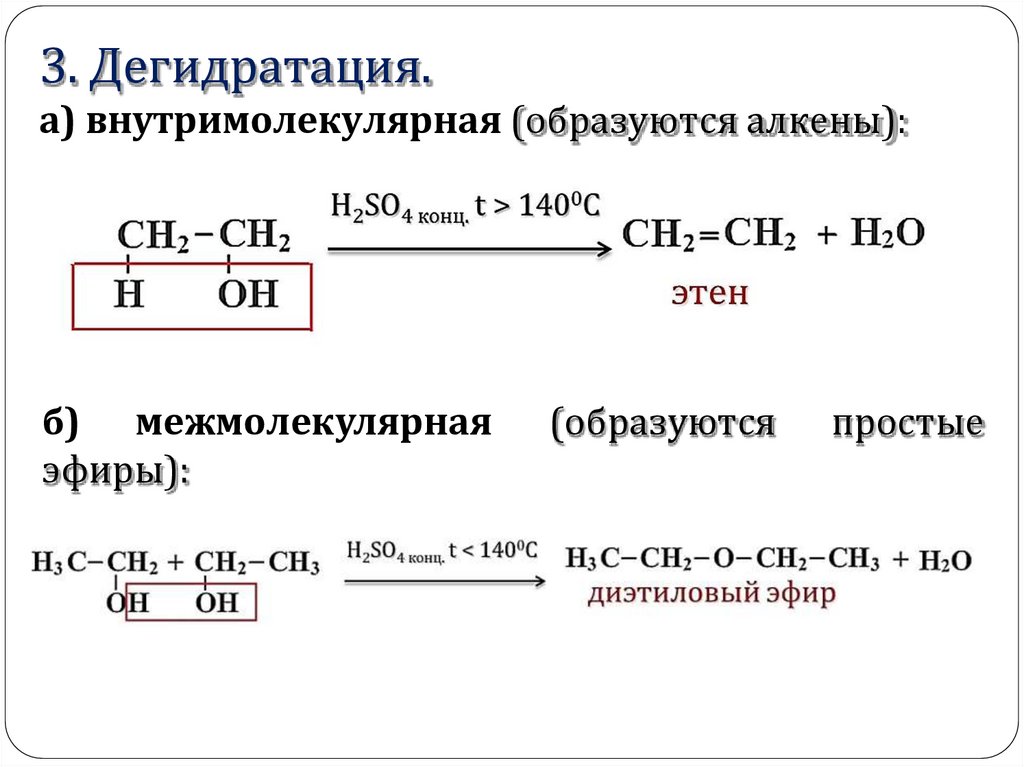
3. Дегидратация.а) внутримолекулярная (образуются алкены):
б) межмолекулярная
эфиры):
(образуются
простые
15.
4. Реакция этерификации (взаимодействиекарбоновых
кислот
со
спиртами,
приводящее к образованию сложных
эфиров):
16.
5. Реакции окисления.а) горение
С2H5ОH + 3O2 2СO2 + 3H2O +Q
Метанол и этанол горят голубоватым пламенем, с
увеличением массы углеводородного радикала – пламя
становится всё более коптящим.
Опыт. Горение спиртов
Благодаря высокой экзотермичности реакции горения
этанола, он считается перспективным и экологически
чистым заменителем бензинового топлива в двигателях
внутреннего сгорания. В лабораторной практике этанол
применяется как горючее для "спиртовок".
17.
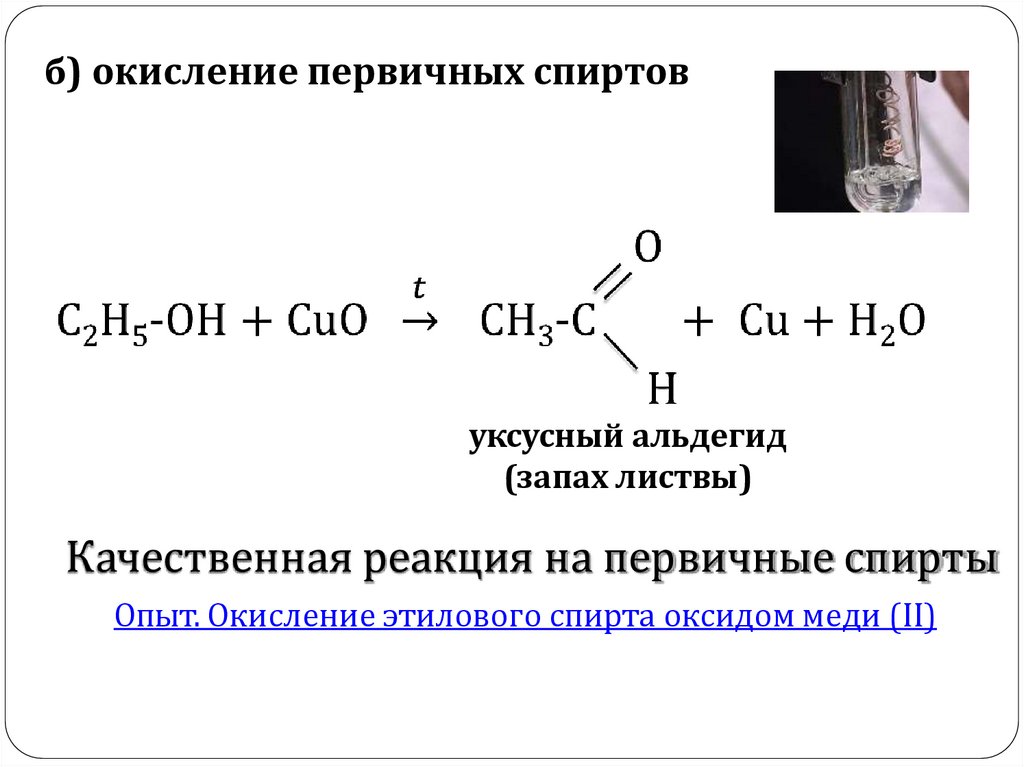
б) окисление первичных спиртовуксусный альдегид
(запах листвы)
Качественная реакция на первичные спирты
Опыт. Окисление этилового спирта оксидом меди (II)
18.
Лабораторный опыт№6.Свойства этилового спирта.
Цель: изучить свойства этилового спирта.
Ход опыта:
С правилами т.б. познакомился
1.Этанол имеет алкогольный (спиртовой) запах.
2. Этанол быстрее испаряется, чем вода.
3.Раскаленную медную проволоку опустим в
пробирку с этанолом. Запах листвы, появляется
медь.
СН3-СН2-ОН + СuO → CH3-CH=O + Cu + H2O
19.
Метанол(метиловый
спирт,
древесный спирт) — CH3OH, бесцветная
горючая жидкость со спиртовым запахом,
tкип= 64,50С, смешивается с водой в любых
соотношениях.
СИЛЬНЫЙ ЯД. 5-10 мл приводит к
слепоте, 30 мл – летальный исход от
паралича верхних дыхательных путей.
С воздухом в объёмных концентрациях
образует взрывоопасные смеси.
Используется
как
растворитель,
топливо для двигателей внутреннего
сгорания, повышает октановое число, в
органическом синтезе.
20.
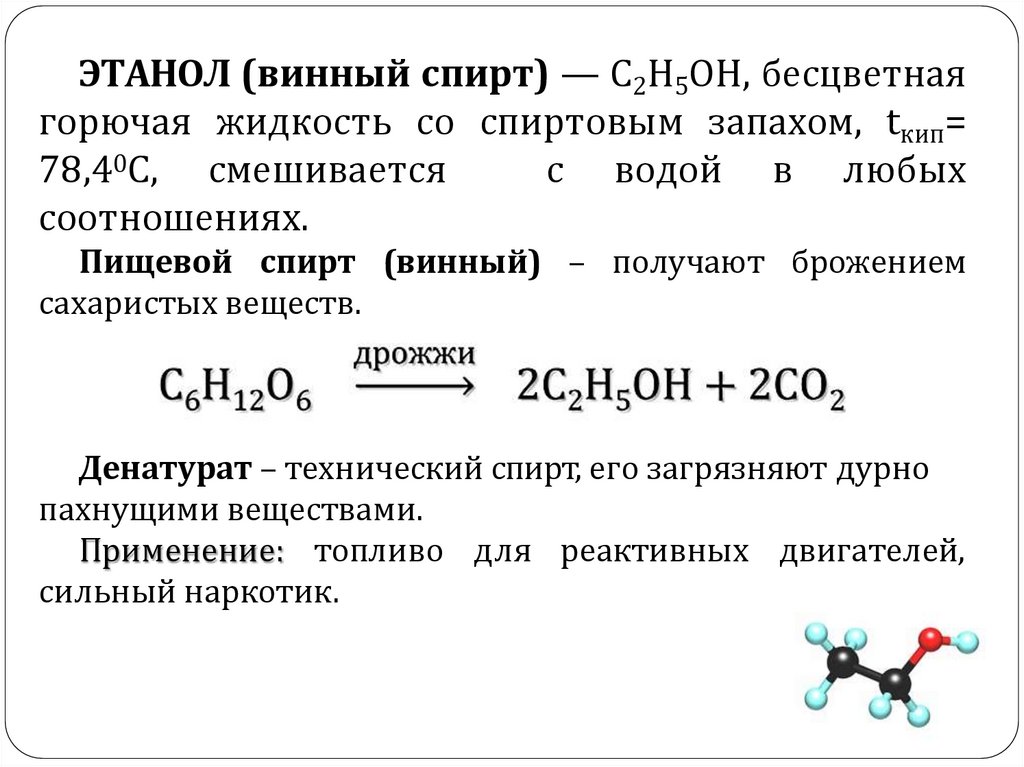
ЭТАНОЛ (винный спирт) — C2H5OH, бесцветнаягорючая жидкость со спиртовым запахом, tкип=
78,40С, смешивается
с водой в любых
соотношениях.
Пищевой спирт (винный) – получают брожением
сахаристых веществ.
Денатурат – технический спирт, его загрязняют дурно
пахнущими веществами.
Применение: топливо для реактивных двигателей,
сильный наркотик.
21.
1.Для
окисления
предельного
одноатомного спирта массой 3,7 г до
альдегида потребовалось 4,0 г оксида
меди(II).
Определите
молекулярную
формулу спирта. (Ответ: С4Н9ОН)
2. При взаимодействии предельного
одноатомного спирта массой 3,52 г с
избытком натрия выделилось 0,448 л
водорода. Определите молекулярную
формулу спирта. (Ответ: С5Н11ОН)












 chemistry
chemistry








