Similar presentations:
Теория электролитической диссоциации
1. Лекция №6. Теория электролитической диссоциации
2. 1. Истоки ТЭД
1.1. Физическая теория растворов1.2. Физико – химическая теория
растворов
3. 2. Факты, требующие объяснения
2.1. Электропроводность растворовсолей, щелочей и кислот.
4. Электропроводность
5. Электропроводность
6. Растворы солей, щелочей и кислот
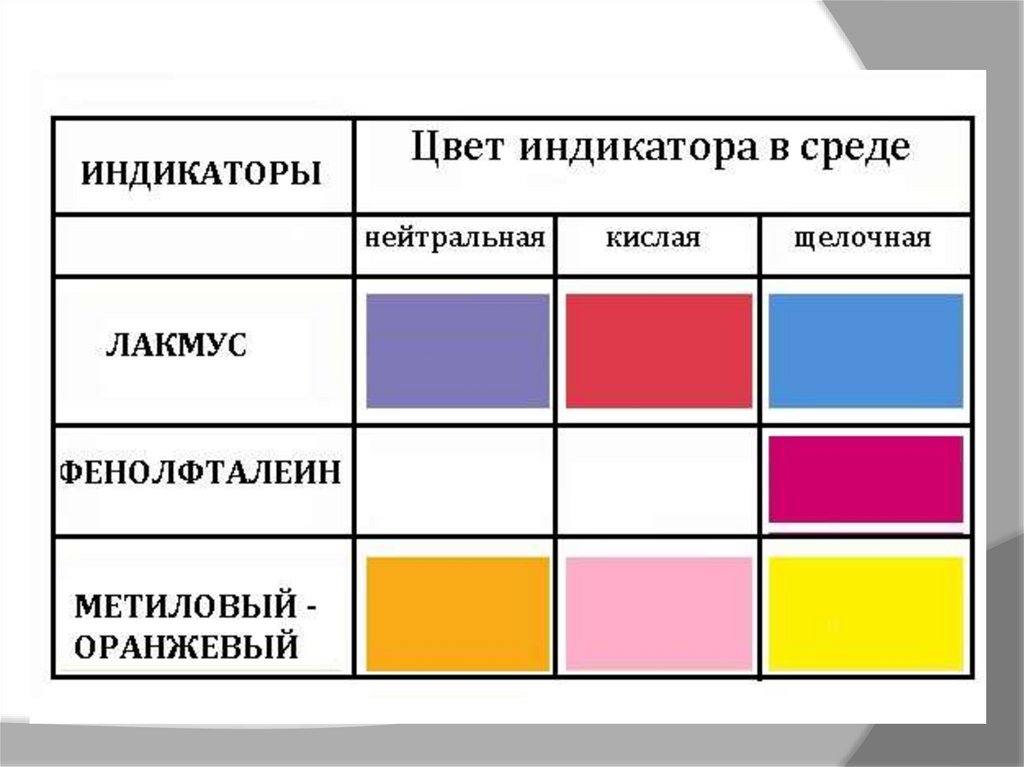
7. 2.2. Общие свойства щелочей и кислот
8.
9. Щелочь и фенолфталеин.
10. Кислота и лакмус.
11. Метиловый оранжевый.
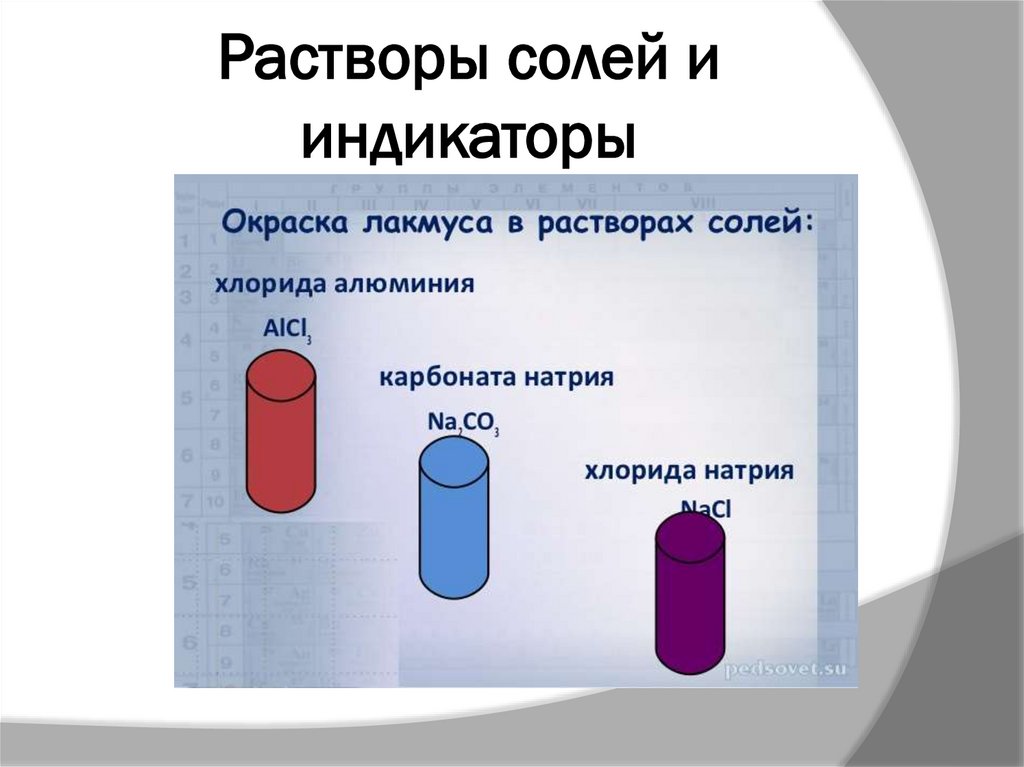
12. Растворы солей и индикаторы
13. 2.3. Почему одни реакции в растворах идут до конца, другие - нет?
14. Реакция между растворами сульфатом меди и гидроксида натрия.
15. Реакция между растворами карбоната натрия и соляной кислоты
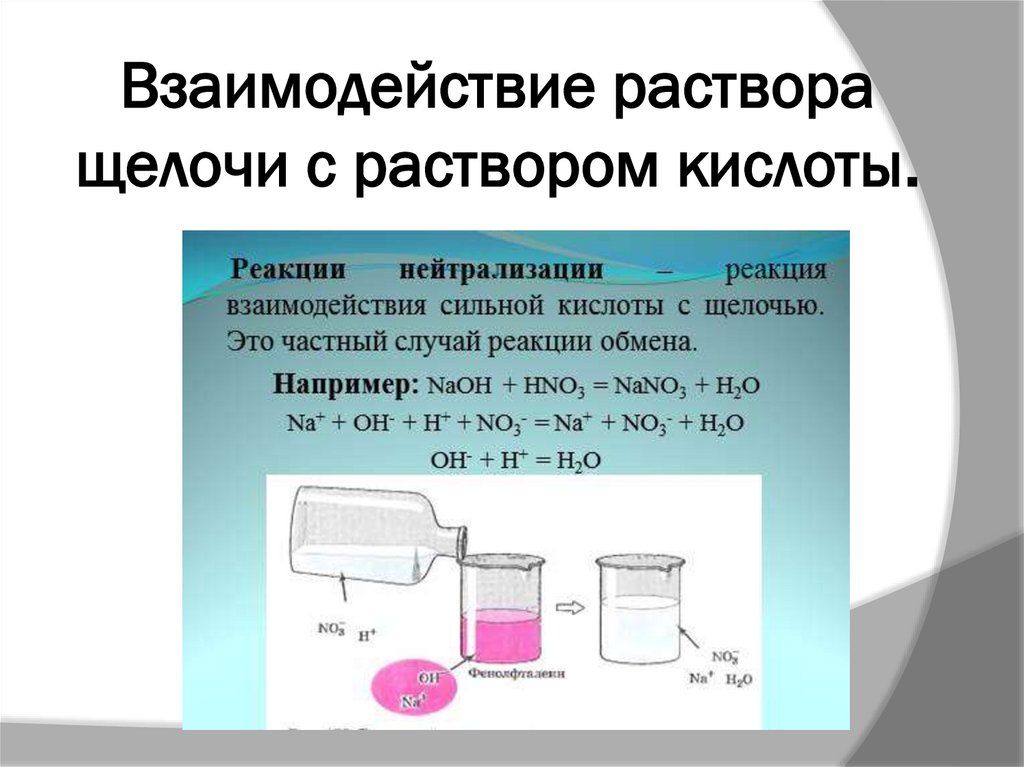
16. Взаимодействие раствора щелочи с раствором кислоты.
17. Взаимодействие раствора нитрата калия и хлорида натрия.
18.
19. 3. 1887 год. Шведский химик Сванте Аррениус создал ТЭД
20. 4. Положения ТЭД.
21. 4.1.Электролиты – вещества, которые в растворах и расплавах распадаются на ионы и проводят ток.
22. 4.2. Неэлектролиты – вещества, которые в растворах и расплавах не проводят ток.
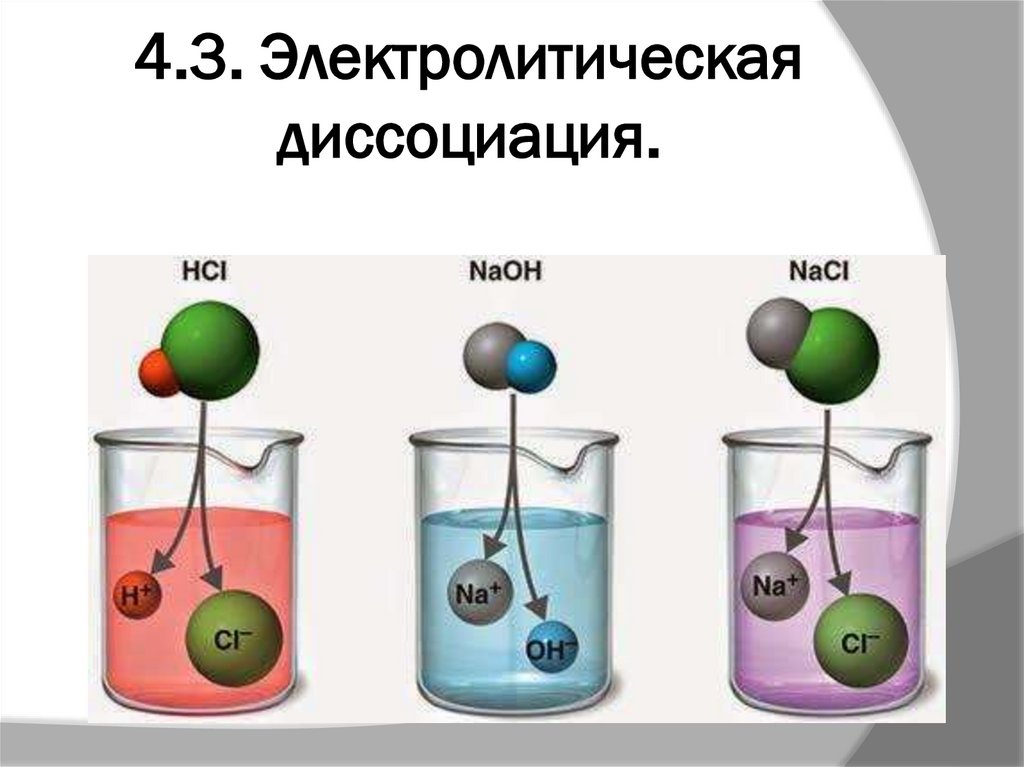
23. 4.3. Электролитическая диссоциация.
24. 4.4. Степень диссоциации. Сильные и слабые электролиты
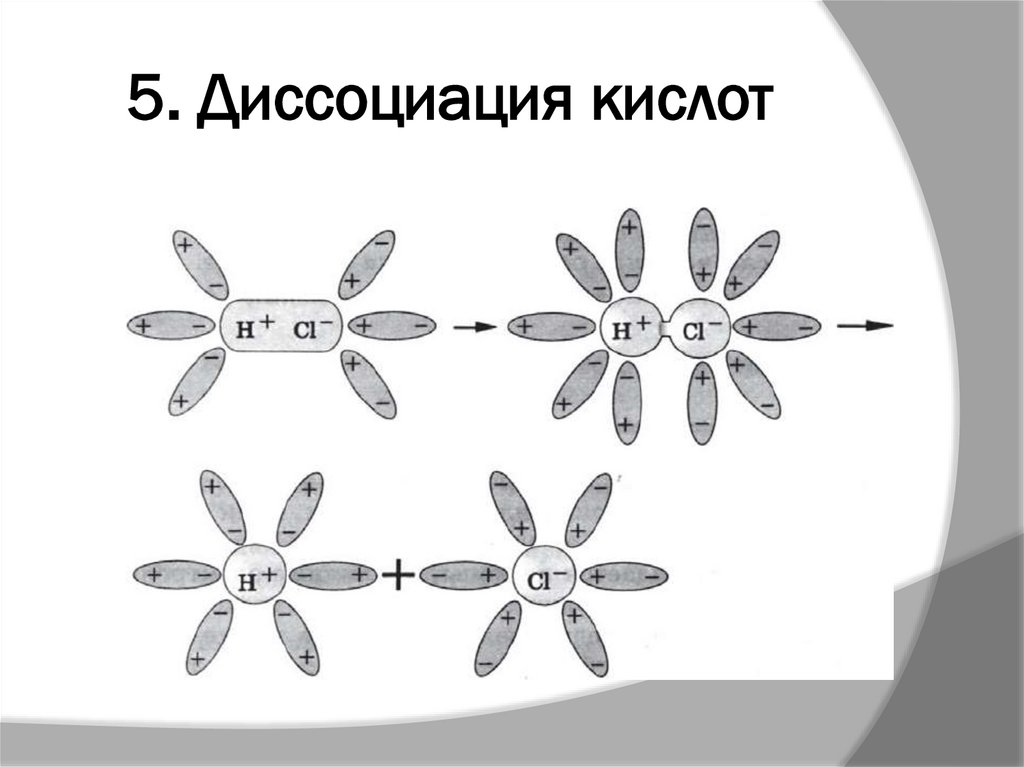
25. 5. Диссоциация кислот
26. 6. Диссоциация оснований
27. 7. Диссоциация солей.
28. 8. Недиссоциируют:
8.1. Нерастворимые в воде вещества8.2. Простые вещества
8.3. Оксиды.

























 chemistry
chemistry








