Similar presentations:
Физиология системы кровообращения ИГМА
1.
Физиология системыкровообращения
ИГМА
Кафедра нормальной физиологии
Доцент, к.м.н. А.А.Пермяков
2.
ФИЗИОЛОГИЯ КРОВООБРАЩЕНИЯ.ФИЗИОЛОГИЧЕСКИЕ СВОЙСТВА
СЕРДЕЧНОЙ МЫШЦЫ.
План лекции.
1. Кровообращение,
его
Функциональная
отделов
и
сущность.
характеристика
областей
системы
свойства
сердечной
кровообращения.
2. Физиологические
мышцы.
3. Проявления сердечной деятельности и
методы их исследования.
4. Понятие о сердечном цикле. Фазовый
анализ сердечного цикла.
3.
1. Внешние проявления работы сердца иметоды
исследования
сердечно–
сосудистой системы.
2. Регуляция работы сердца.
3. Функции
сосудистой
системы
и
основные принципы гемодинамики.
4. Функциональная
классификация
сосудистой системы.
5. Скорость кровотока в различных
участках сосудистой системы.
6. Артериальное давление и факторы,
определяющие его величину.
7. Давление
в
венах
и
факторы,
способствующие венозному возврату.
8. Пульс и его характеристика по основным
признакам.
9. Регуляция регионального и системного
кровообращения
4.
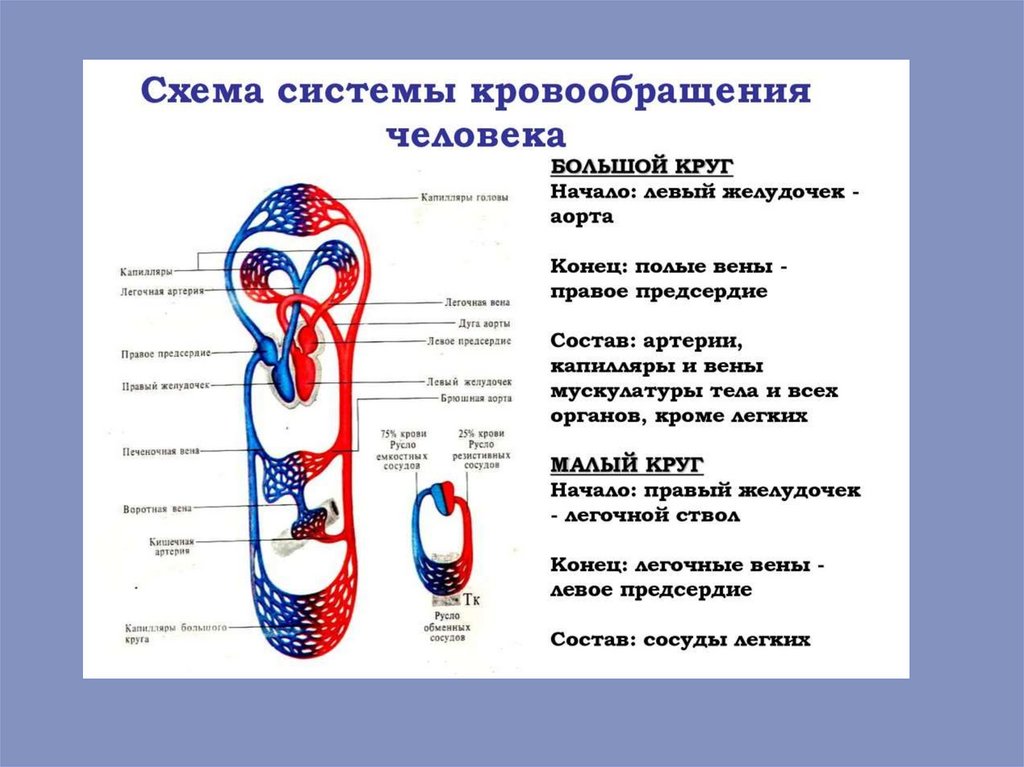
Система кровообращения – это замкнутая система, по которой осуществляетсяциркуляция крови. Система кровообращения человека состоит из четырех
камерного сердца и сосудов, которые формируют два круга кровообращения:
большого
(системного)
и
малого
(легочного).
Благодаря
постоянному
движению крови по сосудам, система кровообращения обеспечивает ряд
функций:
1. Транспорт питательных веществ и кислорода тканям и обеспечение, таким
образом, в них обмена веществ и энергии;
2. Транспорт от тканей продуктов метаболизма к органам, обеспечивающих
их экскрецию;
3. Транспорт биологически активных веществ, растворимых солей и
метаболитов, участвующих в механизмах гуморальной регуляции в
организме;
5.
4. Транспорт различных элементов иммуно-компетентной системы(специфических антител, фагоцитирующих клеток и др.) и
участие в
связи с этим в механизмах иммунологической защиты организма;
5.Участие в процессах терморегуляции;
6.Участие в механизмах гемостаза;
7.Участие в механизмах поддержания водно-электролитного баланса;
8.Участие в механизмах поддержания кислотно-щелочного равновесия (в
крови, циркулирующей по сосудам, находятся три буферные системы:
белковая, карбонатная, фосфатная).
6.
7.
8.
9.
10.
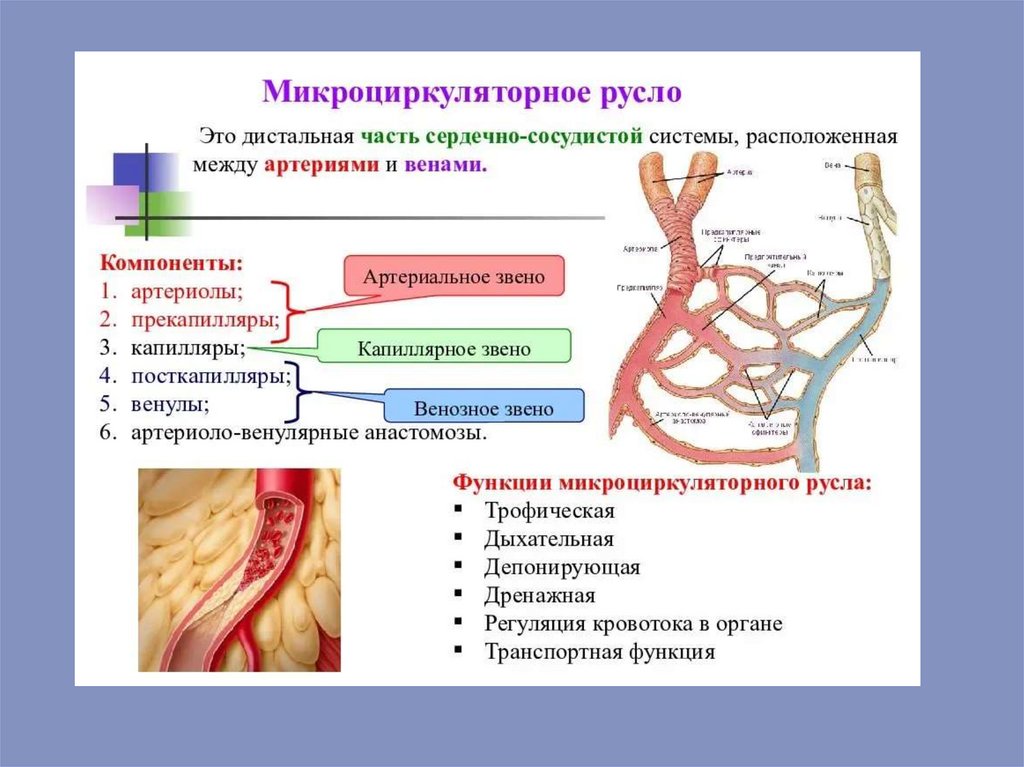
Область высокого давления характеризуется высокимиуровнями давления крови (в аорте и крупных артериях
давление составляет 120/70 мм. рт. ст.) и высокими
линейной и объемной скоростями движения крови по
сосудам. В этой зоне содержится лишь 15 – 20% всего
объема циркулирующей крови. Область транскапилярного
обмена характери-зуется относительно низкими значениями
давления крови: в прекапи-лярах давление составляет около
30 мм. рт. ст., а в посткапилярах – около 10-15 мм. рт. ст.. Это
сопровождается низкой скоростью движения крови по
капилярам и создает предпосылки для транскапилярного
обмена. В области транскапилярного обмена находится
около 5 – 10% всего объема циркулирующей крови. Наконец,
область большого объема характеризуется относительно
низким давлением крови, которое уменьшается по мере
приближения к сердцу, низкой скоростью кровотока и
большим объемом содержащейся крови (около 70-80%
объема циркулирующей крови).
11.
Более конкретную функциональную роль различным элементам системыкровообращения присваивает классификация, разработанная шведским ученым
Б.Фолковым в 70-х годах 20 столетия. В соответствии с этой классификацией
выделяют следующие звенья системы кровообращения:
1.
Сердце – биологический насос, ритмически выбрасывающий кровь в
сосудистое русло. Сердце во многом определяет систолический уровень
артериального давления;
2. Сосуды амортизаторы, обеспечивающие сглаживание пульсаций крови,
преобразование прерывистого тока крови в непрерывный. К этой группе
относят аорту и сосуды большого диаметра эластического и смешанного типа;
3.
Резистивные сосуды (сосуды сопротивления) – артерии малого диаметра.
Основная функция - стабилизация движения крови по сосудам, формирование
диастолического уровня артериального давления.
4.
Прекапилярные сфинктеры. Основное назначение – перераспределение
кровотока в тканях;
5.
Сосуды шунты. Также как и прекапилярные сфинктеры обеспечивают
перераспределение кровотока в тканях;
6.
Обменные сосуды (капиляры);
7.
Емкостные сосуды. К этой группе относят сосуды венозной системы.
Основная функция – обеспечение адекватного венозного возврата к сердцу.
12.
Автоматизм — свойство возбудимых образований выпол-нять ритмическуюдеятельность под влиянием импульсов, возни-кающих в них самих.
Возбудимость — способность возбудимых образований вос-принимать и отвечать
на стимулы специфической реакцией — возбуждением. Возбуждение — активный
физиологический процесс, прояв-ляющийся в изменении функционального
состояния возбудимых тканей (сокращение мышц, выделение секрета, проведение
воз-буждения по нерву).
Сократимость — способность мышечных
волокон укорачи-ваться или увеличивать
свое напряжение.
Проводимость — способность проводить
возбуждение от клетки к клетки без
затухания.
13.
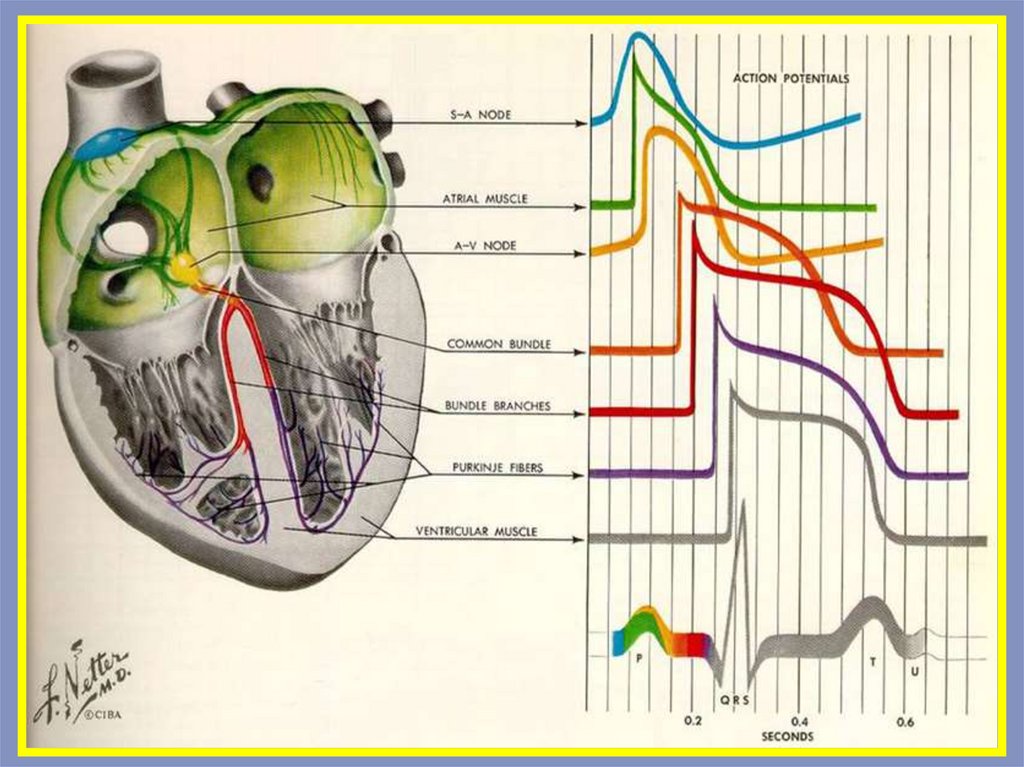
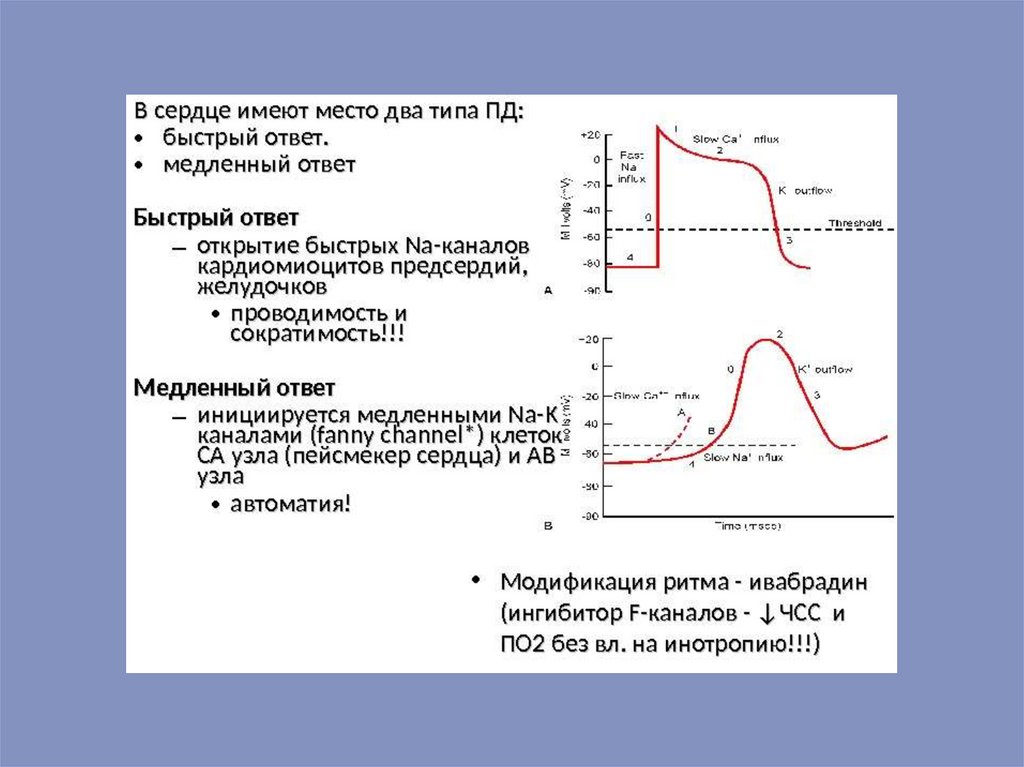
В результате исследований была доказана миогенная теория автоматизма, согласнокоторой структурной основой автоматизма являются атипичные пейсмекерные клетки (Рклетки).
Причинные теории объясняют механизм возникновения возбуждения в атипичных
клетках. Современная теория рассматривает природу автоматизма, исходя из специфики мембранного
потенциала покоя (МПП) и потенциала действия (ПД) Р-клеток. В этих клетках лучше
выражена проницаемость мембран для ионов на-трия, движущихся по медленным
натриевым каналам, а проницаемость для ионов калия снижена. Поэтому МПП Р-клеток
имеет низкую величину (60 мВ) и практически отсутствует. ПД начинается во время
диастолы медленной диастолической деполяризацией (МДД), которая обусловлена
вхождением ионов натрия в клетку по медленным каналам и в меньшей степени – ионов
кальция. Параллельно происходит снижение активности натрий – калиевого насоса, что
уменьшает градиент концентрации этих ионов снаружи и внутри пейсмекерных клеток,
облегчая деполяризацию мембраны. По некоторым данным, в формировании МДД также
участвуют ионы хлора. Когда МДД достигает критического уровня (40 мВ), открываются
быстрые натриевые и кальциевые каналы, происходит быстрая деполяризация –
возбуждение клеток Р. В ПД отсутствует натриевая инактивация, поэтому вместо пика
имеет место закругленная вершина (медленное вхождение ионов натрия и кальция на
фоне слабого выхода ионов калия из клетки). Его амплитуда составляет 100 мВ.
Реполяризация в ПД обусловлена преобладанием выхода калия из клетки и работой
мембранных ионных насосов. Чем быстрее скорость МДД Р – клеток синусного узла, тем
чаще он возбуждается и сокращается.
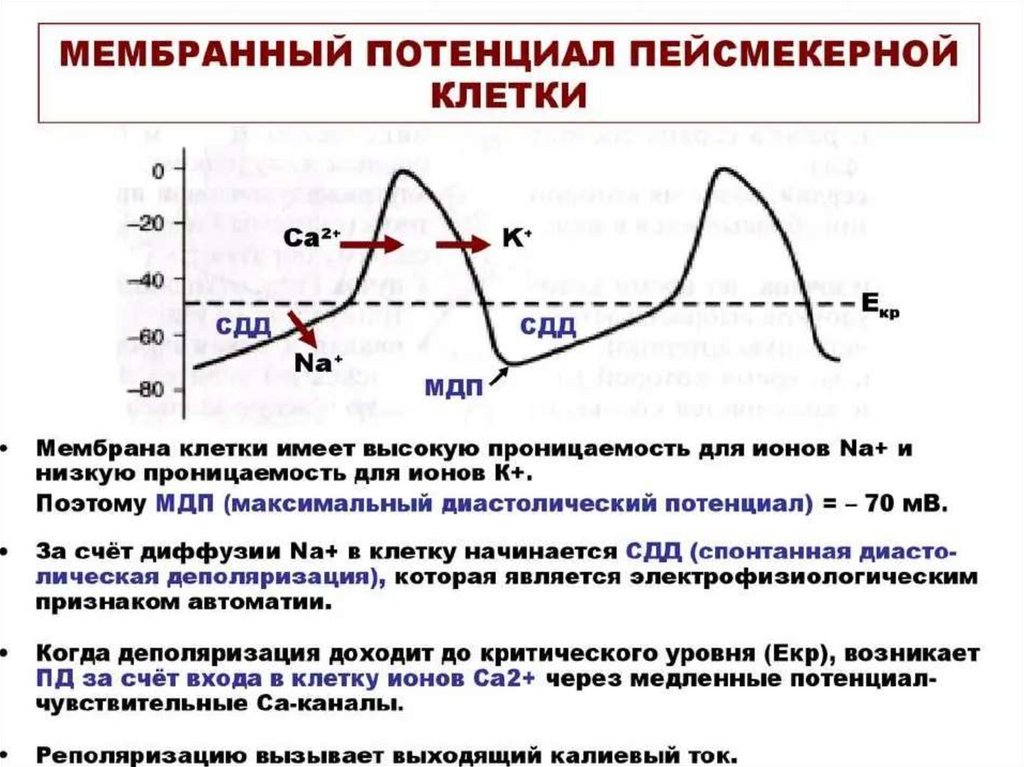
14.
Физиологической основой автоматизма сердечной мышцы является низкаяскорость ее аккомодации: при действии постепенно нарастающего по силе
раздражителя порог возбудимости у сердечной мышцы почти не изменяется. В
клетках рабочего миокарда предсердий и желудочков мембранный потенциал
покоя в интервалах между возбуждениями поддерживается на постоянном
уровне. В клетках же синоатриального узла мембранный потенциал покоя
нестабилен – в период диастолы происходит постепенное его уменьшение,
которое называется медленной диастолической деполяризацией (МДД). Она
является начальным компонентом потенциала действия пейсмекерных клеток.
При достижении МДД критического уровня деполяризации возникает
потенциал действия пейсмекерной клетки, который затем распространяется по
проводящей системе к миокарду предсердий и желудочков. После окончания
потенциала действия вновь развивается МДД. Ионный механизм МДД состоит в том,
что во время реполяризации
клеточная мембрана сохраняет относительно высокую натриевую
проницаемость. В результате проникновения внутрь клетки ионов натрия и
уменьшения скорости выхода из клетки ионов калия возникает МДД.
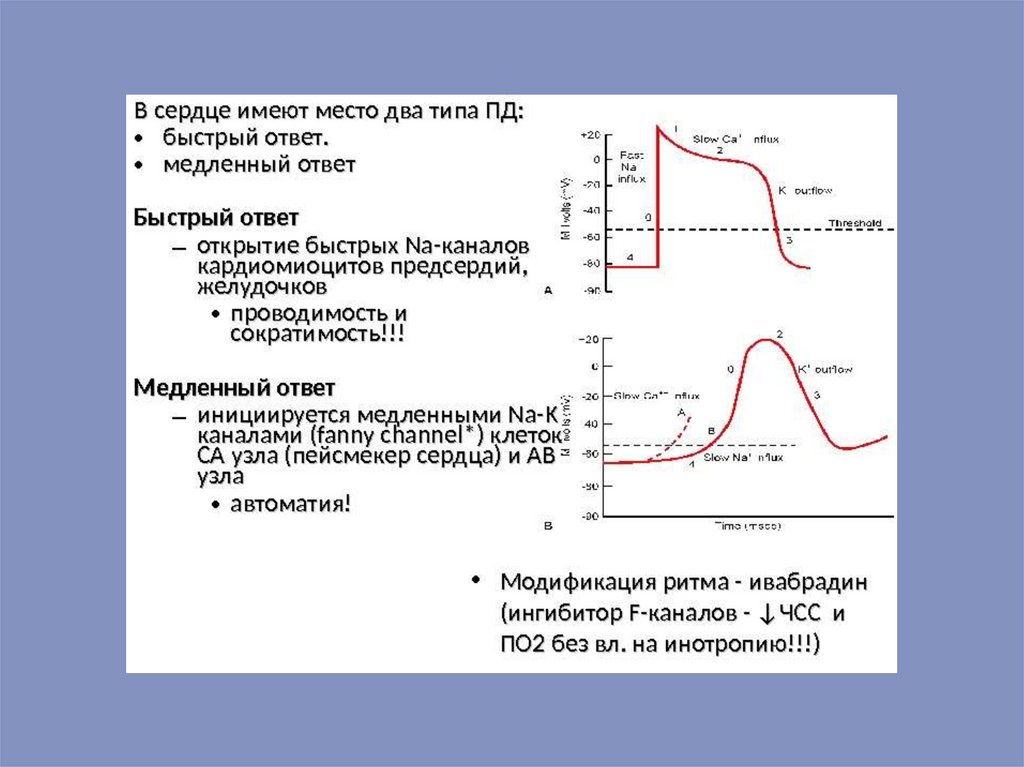
Уменьшение потенциала покоя до –40 мВ приводит к открытию медленныхнатрийкальциевых каналов, что приводит к возникновению быстрой
деполяризации. Реполяризация обеспечивается открытием калиевых каналов. В
отличие от клеток водителей ритма рабочие клетки миокарда в состоянии покоя
характеризуются очень низкой проницаемостью для ионов натрия, поэтому
сдвигов мембранного потенциала в них не возникает
15.
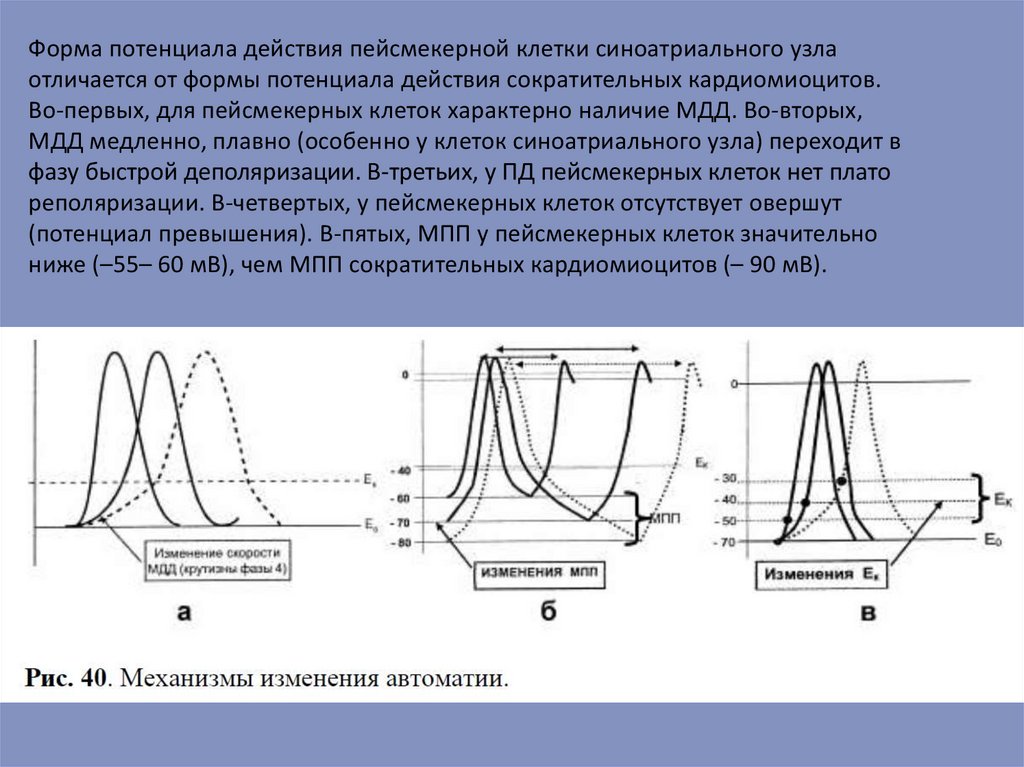
Форма потенциала действия пейсмекерной клетки синоатриального узлаотличается от формы потенциала действия сократительных кардиомиоцитов.
Во-первых, для пейсмекерных клеток характерно наличие МДД. Во-вторых,
МДД медленно, плавно (особенно у клеток синоатриального узла) переходит в
фазу быстрой деполяризации. В-третьих, у ПД пейсмекерных клеток нет плато
реполяризации. В-четвертых, у пейсмекерных клеток отсутствует овершут
(потенциал превышения). В-пятых, МПП у пейсмекерных клеток значительно
ниже (–55– 60 мВ), чем МПП сократительных кардиомиоцитов (– 90 мВ).
16.
17.
18.
19.
20.
21.
22.
23.
24.
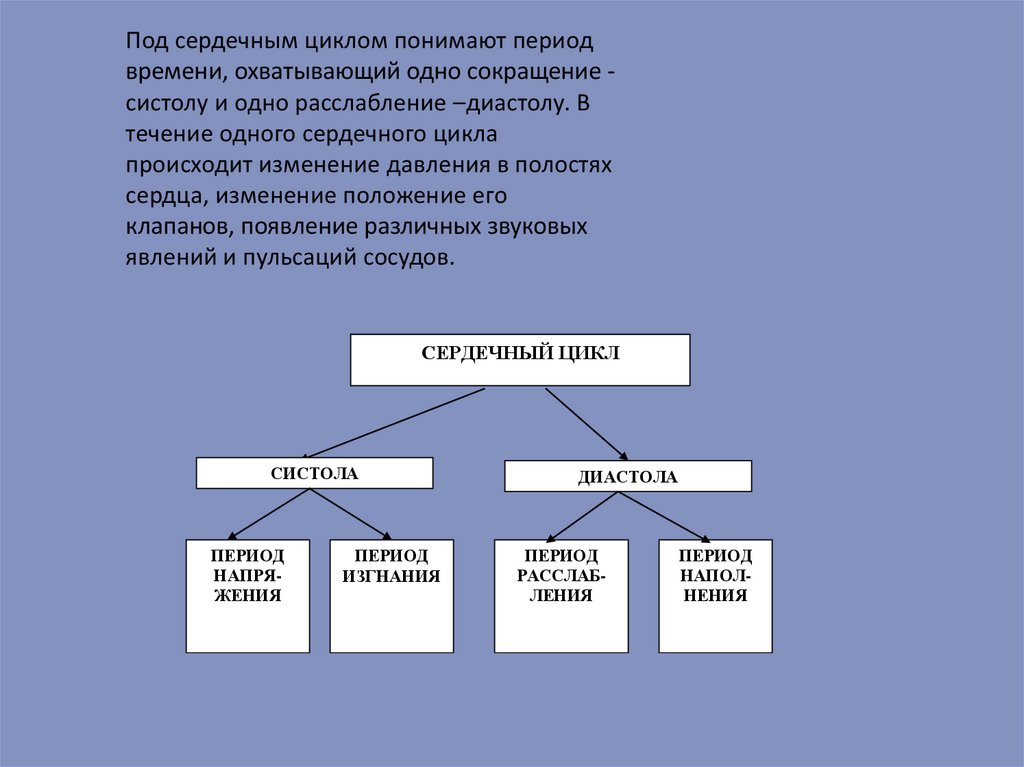
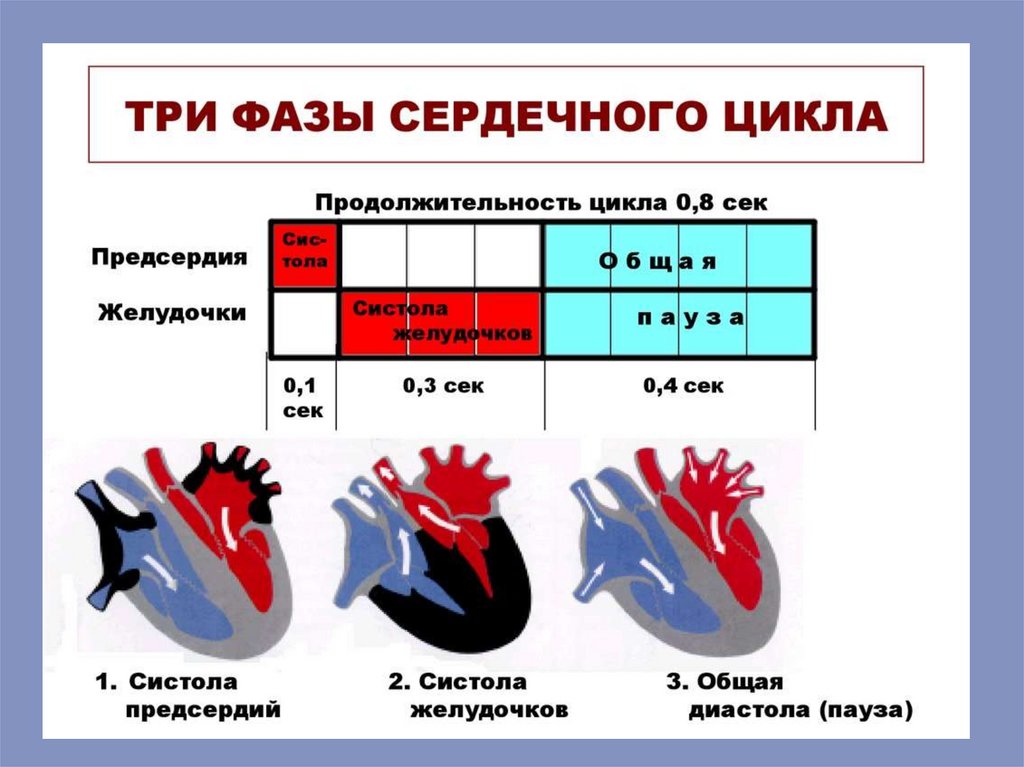
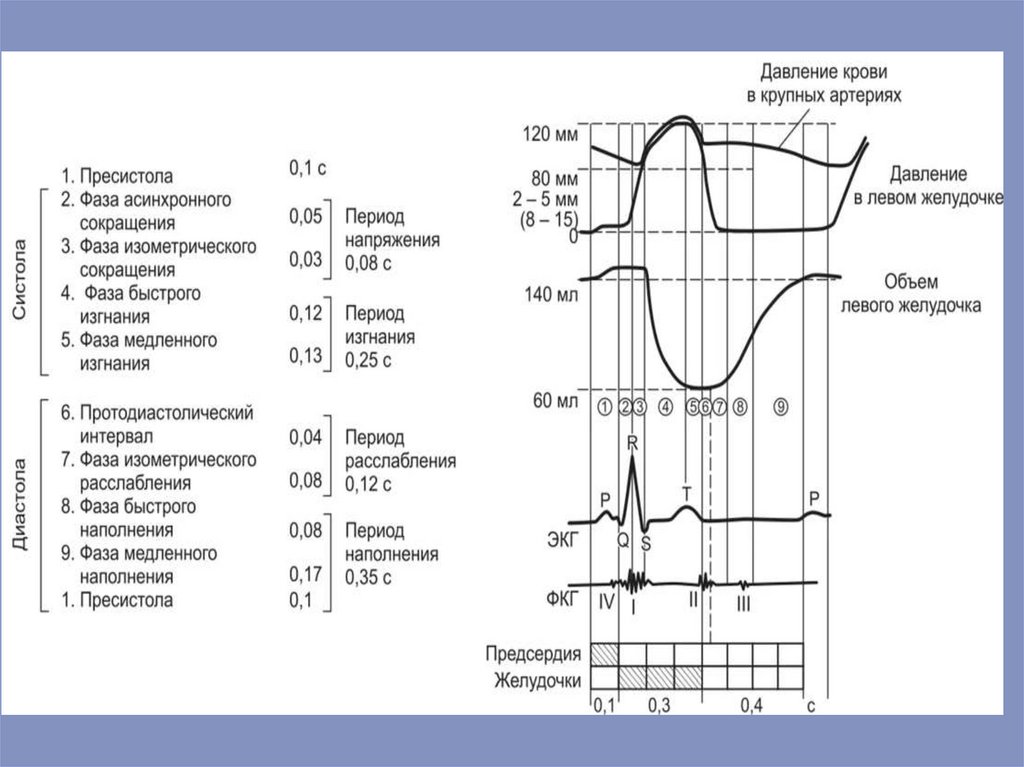
Под сердечным циклом понимают периодвремени, охватывающий одно сокращение систолу и одно расслабление –диастолу. В
течение одного сердечного цикла
происходит изменение давления в полостях
сердца, изменение положение его
клапанов, появление различных звуковых
явлений и пульсаций сосудов.
СЕРДЕЧНЫЙ ЦИКЛ
СИСТОЛА
ПЕРИОД
НАПРЯЖЕНИЯ
ПЕРИОД
ИЗГНАНИЯ
ДИАСТОЛА
ПЕРИОД
РАССЛАБЛЕНИЯ
ПЕРИОД
НАПОЛНЕНИЯ
25.
26.
27.
Временные параметры сердечного цикла:1. Систола желудочков — 0,33 с:
1.1. Период напряжения желудочков — 0,08
с:
а) фаза асинхронного сокращения — 0,05 с,
б) фаза изометрического сокращения —
0,03 с.
1.2. Период изгнания крови — 0,25 с:
а) фаза быстрого изгнания крови — 0,12 с,
б) фаза медленного изгнания крови — 0,13
с.
2. Диастола желудочков — 0,47 с:
2.1. Протодиастолический период — 0,04 с,
2.2. Период изометрического расслабления
— 0,08 с,
2.3. Период наполнения кровью — 0,35 с:
а) фаза быстрого наполнения — 0,08 с,
б) фаза медленного наполнения — 0,17 с,
в) фаза наполнения кровью, обусловленная
систолой предсердий — 0,1 с.
28.
29.
30.
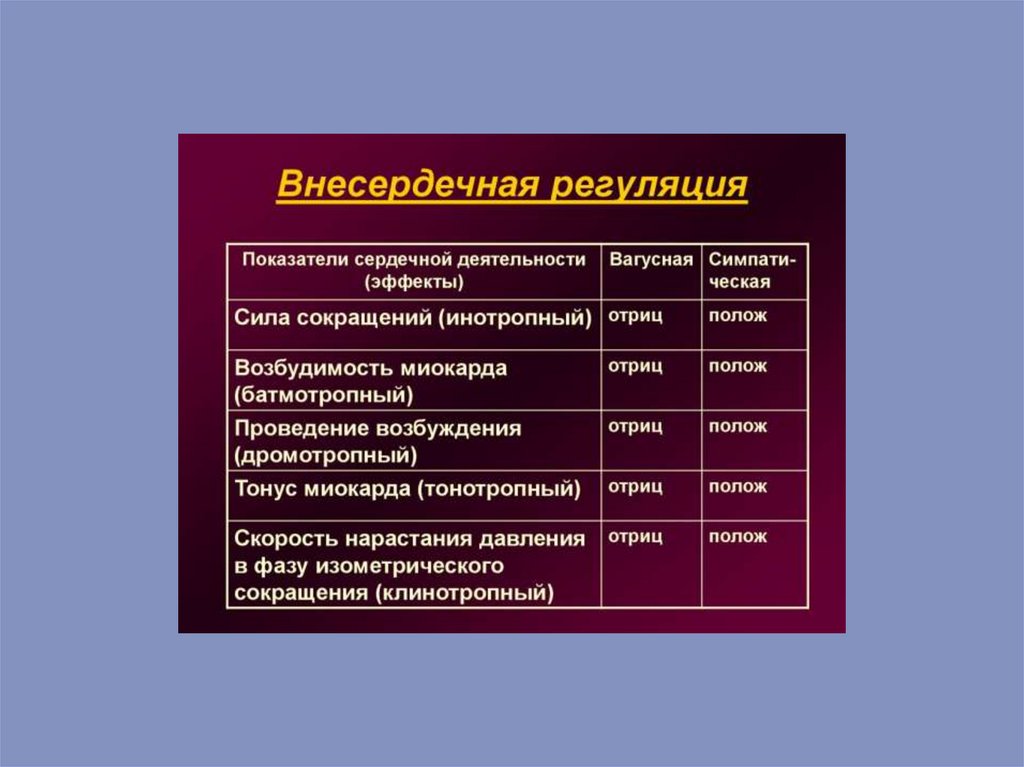
Регуляция деятельности сердцаРазличные факторы влияют на свойства сердечной мышцы (возбудимость,
проводимость, сократимость, автоматизм) и, следовательно, на основные
параметры деятельности сердца – частоту и силу сокращений.
Влияния на частоту сердечных сокращений называются хронотропными,
на силу сокращений – инотропными, на возбудимость – батмотропными, на
проводимость – дромотропными, на тонус сердечной мышцы –
тонотропнымивлияниями. Влияния, вызывающие увеличение этих показателей
называются
положительными, а уменьшение – отрицательными.
Принято различать несколько форм регуляции деятельности сердца:
кардиальную (представленную двумя ее видами – миогенным и нейрогенным) и
экстракардиальную регуляцию (нервную, гуморальную, рефлекторную).
31.
Внутриклеточная (миогенная) регуляция обеспечивает ра-венство притока крови ксердцу по венам и ее выброс в артерии, а также синтез различных белков в
соответствии с их разрушением во время работы миокарда. Кардиомиоциты способны
синтезировать различные белки за счет специальных ауторегуляторных механизмов.
Наиболее бы-стрый распад белков происходит в момент систолы, ресинтез
осуществляется за время диастолы. При повышенной активности миокарда в клетках
происходит синтез дополнительных сократи-тельных белков, появляется рабочая
(физиологическая) гипер-трофия миокарда. Механизм этот осуществляется внутри
сердца, и для его реализации не требуется влияние со стороны централь-ной нервной
системы. Внутриклеточные механизмы регуляции обеспечивают изме-нение
интенсивности деятельности миокарда в соответствии с притекающей к сердцу крови.
В сердечной мышце существует не-сколько миогенных механизмов, позволяющих
регулировать силу сокращений миокарда — гетерометрический и гомеометрический.
Гетерометрическая регуляция силы сокращений, или «закон сердца» Франка —
Старлинга: чем больше растягивается мышца желудочков во время фазы наполнения,
тем сильнее она будет со-кращаться во время систолы. Более сильное растяжение
миокарда во время диастолы соответствует усиленному притоку крови к сердцу. Во
время растяжения миофибрилл актиновые нити в большей степени выдвигаются из
промежутков между миозино-выми нитями, следовательно растет количество
резервных мости-ков, которые соединяют актиновые и миозиновые нити в момент
сокращения. Чем больше растянута каждая клетка во время диа-столы, тем больше она
укоротится во время систолы. Гомеомет-рическая регуляция: сила сердечных
сокращений может меняться при неизменной длине мышцы, чем чаще возникает
возбуждение в миокарде, тем сильнее сокращение («лестница» Боудича).
32.
Регуляция межклеточных взаимодействий. Межклеточная регуляция в сердечноймышце связана с наличием вставочных дис-ков — нексусов. Вставочные диски
выполняют механическуюфункцию, соединяя миофибриллы, обеспечивают транспорт
ве-ществ, переход возбуждения с клетки на клетку. При выпадении нексусов
нарушается синхронность сокращения кардиомиоцитов, одновременность
возбуждения отдельных клеток, что приводит к нарушению сердечного ритма. К
межклеточным взаимодействиям относят также взаимоотношения кардиомиоцитов с
соединитель-нотканными клетками. Последние поставляют для кардиомиоцитов
высокомолекулярные вещества, выполняют опорную функцию. Внутрисердечные
периферические рефлексы. Собственная нервная регуляция сердца осуществляется
метасимпатической нервной системой. В сердце имеются местные, периферические
рефлекторные дуги, которые представлены афферентными, эффе-рентными и
промежуточными нейронами, которые образуют реф-лекторную дугу. Эта дуга
замыкается не в ЦНС, а в интрамураль-ных ганглиях миокарда. Внутрисердечная
метасимпатическая нервная система регулирует ритм сердечных сокращений, скорость
предсердно-желудочкового проведения, реполяризацию кардио-миоцитов, скорость
диастолического расслабления. Местные реф-лексы необходимы для того, чтобы
сглаживать те изменения в дея-тельности сердца, которые возникают за счет
механизмов гетеро- и гомеометрической саморегуляции. Например, при умеренном
рас-тяжении правого предсердия происходит повышение силы сокра-щений левого
желудочка, а при чрезмерном растяжении правого предсердия сила сокращений
левого желудочка снижается. В естественных условиях внутрисердечная нервная
система не является автономной, она представляет собой низшее звено сложной
иерархии нервных механизмов, регулирующих деятель-ность сердца.
33.
34.
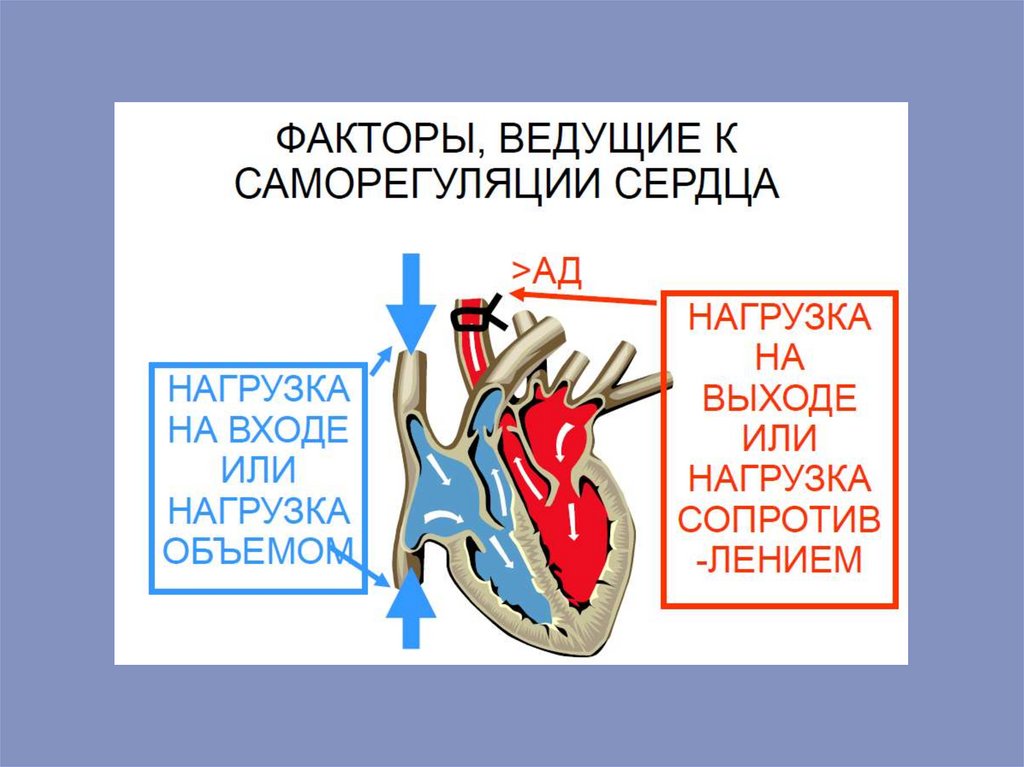
Гетерометрический механизм регуляцииВ основе гетерометрическогомеханизмалежит изменение исходных размеров длины волокон миокарда, которое
возникает при изменении величины притока венозной крови. Т.е. чем сильнее
растянуто сердце во время диастолы, тем оно сильнее сокращается во время
систолы.
Эта особенность сердечной мышцы установлена О.Франком и Е.Старлингом на
сердечно-мышечном препарате и получило название закона сердца ФранкаСтарлинга.
ЗАКОН СЕРДЦА ФРАНКА -СТАРЛИНГА
•СИЛА СОКРАЩЕНИЯ МИОКАРДА ПРОПОРЦИОНАЛЬНА СТЕПЕНИ
ЕГО КРОВЕНАПОЛНЕНИЯ В ДИАСТОЛУ.
или
•Чем больше растяжение миокарда в диастолу, тем сильнее его
сокращение в систолу
или
•ГЕТЕРОМЕТРИЧЕСКАЯ САМОРЕГУЛЯЦИЯ
35.
Отто Франк (21 июня1865 — 12 ноября 1944)
— немецкий врач и
физиолог, внесший
вклад
в физиологию сердца и
кардиологию .
Эрне́ст Ге́нри
Ста́рлинг (англ. Ernest Henry
Starling; 17
апреля 1866, Лондон — 2
мая 1927—
английский физиолог[
Глеб Васильевич фон
Анреп (во время жизни
в Великобритании и Егип
те — англ. Gleb
Vassilievitch von
Anrep[2]; 1889 — 1955) —
русский,
позднее британский физ
иолог, ученик
академика Ивана
Павлова. С 1920 года — в
эмиграции (сначала
в Великобритании, затем
в Египте).
36.
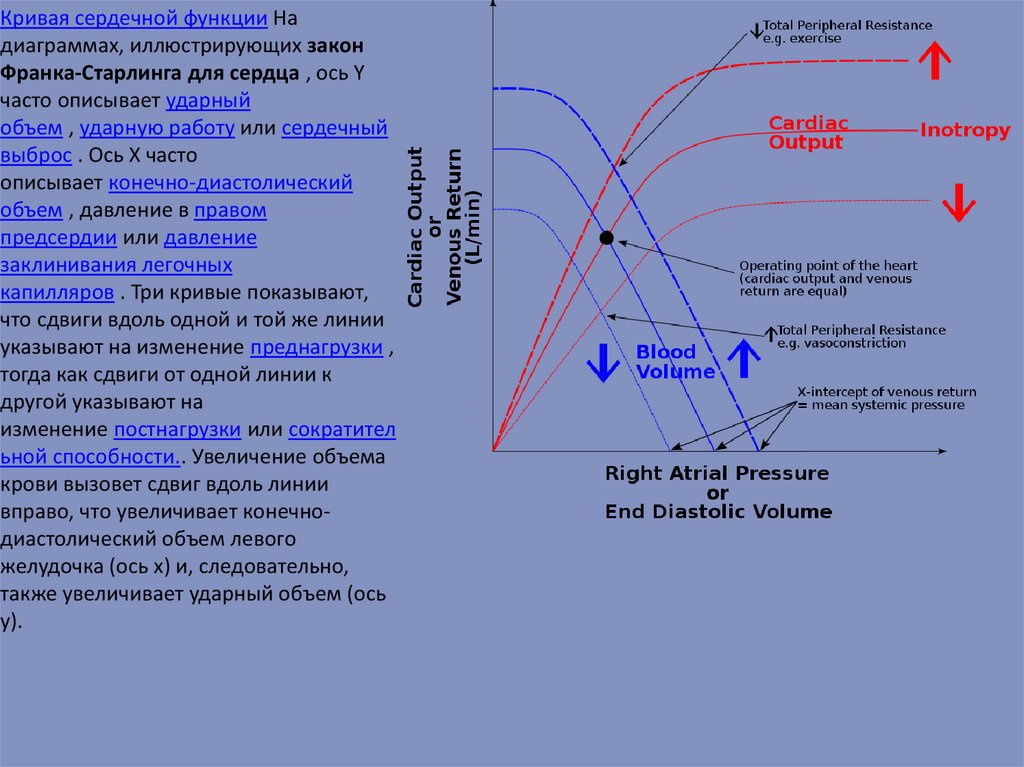
Кривая сердечной функции Надиаграммах, иллюстрирующих закон
Франка-Старлинга для сердца , ось Y
часто описывает ударный
объем , ударную работу или сердечный
выброс . Ось X часто
описывает конечно-диастолический
объем , давление в правом
предсердии или давление
заклинивания легочных
капилляров . Три кривые показывают,
что сдвиги вдоль одной и той же линии
указывают на изменение преднагрузки ,
тогда как сдвиги от одной линии к
другой указывают на
изменение постнагрузки или сократител
ьной способности.. Увеличение объема
крови вызовет сдвиг вдоль линии
вправо, что увеличивает конечнодиастолический объем левого
желудочка (ось x) и, следовательно,
также увеличивает ударный объем (ось
y).
37.
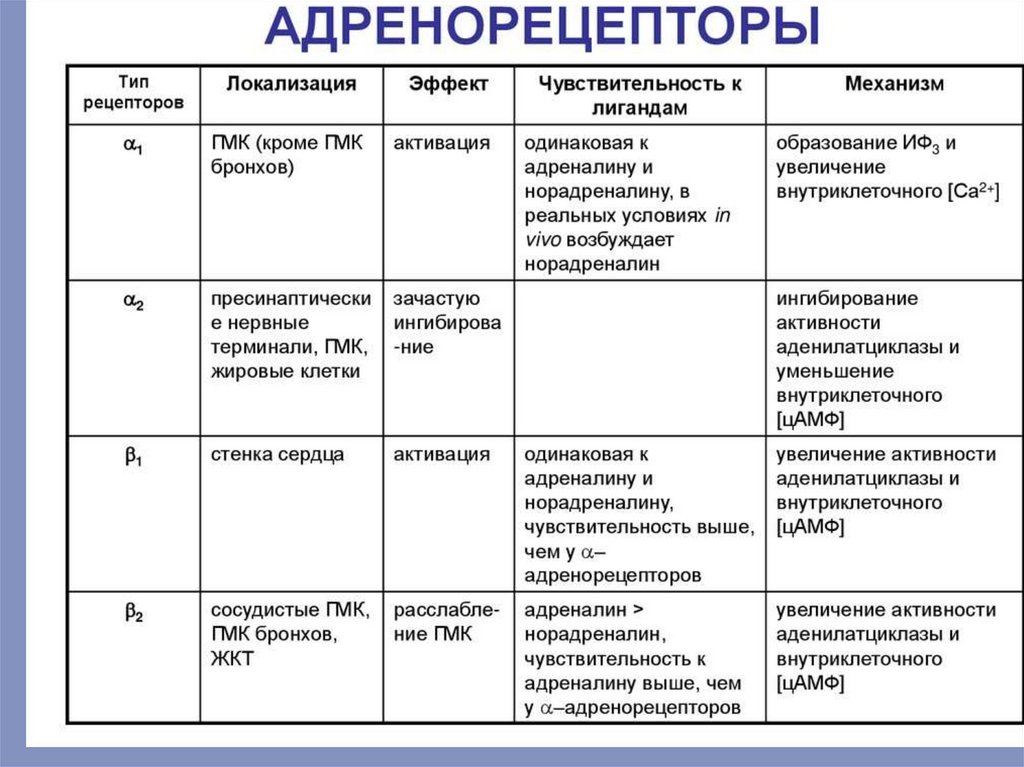
Гомеометрический механизм регуляции•Не связан с изменением длины саркомера и основан на непосредственном
действии биологически активных веществ (т.н. катехоламины) на метаболизм
мышечных волокон, выработку в них энергии. Адреналин и норадреналин
увеличивают вход Са2+ в клетку в момент развития ПД, вызывая тем самым усиления
сердечных сокращений.
ФЕНОМЕНЫ ГОМЕОМЕТРИЧЕСКОЙ САМОРЕГУЛЯЦИИ
•1. Хроноинотропная зависимость
(тахикардия, лестница Боудича)
•2. Эффект постнагрузки
(феномен Анрепа)
•3. Эффект катехоламинов (адреналина)
38.
39.
Миогенная авторегуляция включает в себя гетерометрический игомеометрический механизмы. Гетерометрический механизм опосредован
внутриклеточными взаимодействиями и связан с изменением
взаиморасположения актиновых и миозиновых нитей в миофибриллах
кардиомиоцитов при растяжении миокарда кровью, поступающей в полости
сердца. Растяжение миокардиоцитов приводит к увеличению количества
миозиновых мостиков, способных соединить миозиновые и актиновые нити во
время сокращения. Чем более растянут кардиомиоцит, тем на большую
величину он может укоротиться при сокращении, и тем более сильным будет
это сокращение (рис. 46). Этот вид регуляции был установлен на сердечнолегочном препарате и сформулирован в виде «закона сердца» или закона
Франка-Старлинга. Согласно этому закону, чем больше миокард растянут во
время диастолы, тем больше сила последующего сокращения.
40.
Гомеометрическая авторегуляция сердца связана с определеннымимежклеточными отношениями и не зависит от предсистолического его
растяжения. Большую роль в гомеометрической регуляции играют вставочные
диски – нексусы, через которые кардиомиоциты обмениваются ионами и
информацией. Реализуется данная форма регуляции в виде «эффекта Анрепа» –
увеличение силы сердечного сокращения при возрастании сопротивления в
магистральных сосудах.
Другим проявлением гомеометрической регуляции является так
называемая ритмоинотропная зависимость: изменение силы сердечных
сокращений при изменении частоты. Это явление обусловлено изменением
длительности потенциала действия кардиомиоцитов и, следовательно,
изменением количества экстрацеллюлярного кальция, входящего в
кардиомиоцит при развитии возбуждения
Внутрисердечные периферические рефлексы.
К внутриорганной регуляции деятельности сердца относятся так называемые
периферические рефлексы. Дуга этих рефлексов замыкается не в ЦНС, а в
интрамуральных ганглиях миокарда.
Внутрисердечные рефлексы, в отличие от гетеро- и гомеометрических видов регуляции,
существенно сглаживают и «смягчают» гемодинамические сдвиги, вызванные, в том
числе, и миогенной ауторегуляцией. Имеется в виду возможное резкое увеличение
энергии сердечного сокращения при гетерометрических и гомеометрических формах
ауторегуляции (например, при внезапном повышении венозного притока – в момент
струйного переливания крови или кровозаменителей или быстром повышении
артериального давления, связанного с какими- либо экстремальными ситуациями:
стресс, физическая нагрузка и т.д.).
41.
ВНУТРИСЕРДЕЧНЫЕ ПЕРИФЕРИЧЕСКИЕ РЕФЛЕКСЫ•В сердце имеются местные, периферические рефлекторные дуги,которые
представлены афферентными нейронами (клетки Догеля II порядка, эфферентными
нейронами (клетки Догеля I порядка) и промежуточными нейронами (клетками Догеля III
порядка), образующими рефлекторную дугу, начинающуюся с рецепторов (рецепторы
растяжения, хеморецепторы) и оканчивающуюся на миокардиоцитах, расположенных в
другом отделе сердца.
42.
Рефлекс Парина – урежение частоты сердечных сокращений, снижение артериальногодавления и расширение сосудов селезенки, при повышении давления в легочном стволе.
Рефлекс Китаева - это рефлекторный спазм легочных артериол в ответ на. повышение
давления в левом предсердии. В результате возникает «второй. (функциональный)
барьер», который первоначально играет защитную роль, предохраняя. легочные капилляры от
чрезмерного переполнения кровью.
Рефлекс Бейнбриджа и барорецепторный рефлекс контролируют частоту сердечных
сокращений. Барорецепторный рефлекс может корректировать изменение артериального давления
путем увеличения или уменьшения частоты сердечных сокращений. Напротив, рефлекс Бейнбриджа
реагирует на изменения объема крови. Рефлекс Бейнбриджа (или вазокардиальный рефлекс) —
увеличение силы и частоты сокращений сердца из-за увеличения центрального
венозного давления. Увеличенние объёма крови фиксируются барорецепторами.
Рефлекс Бецольда-Яриша (BJR) -рефлекторное расширение артериол большого круга
кровообращения в ответ на раздражение механо - и хеморецепторов, локализованных в
желудочках и предсердиях. В результате, возникает системная артериальная гипотония,
которая сопровождается брадикардией и временной остановкой дыхания (апноэ).
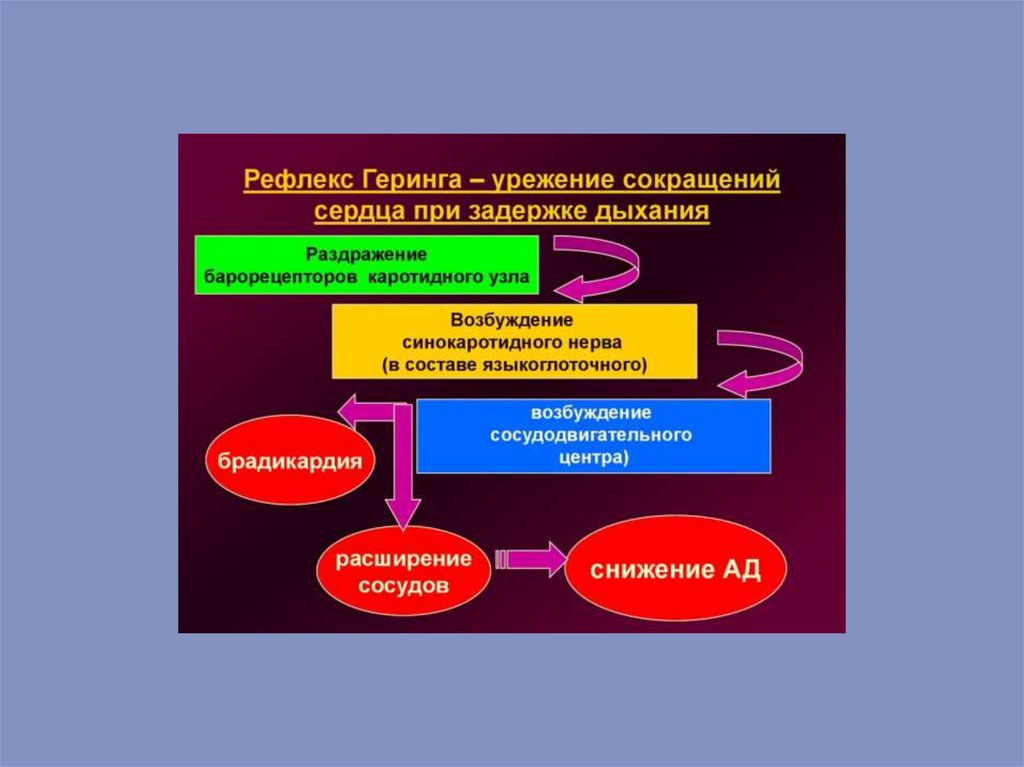
Геринга рефлекс (Н. Е. Hering, 1866—1948, нем. физиолог) — рефлекторное снижение
частоты сердечных сокращений при задержке дыхания на высоте глубокого вдоха.
Роль эфферентного звена в данном рефлексе играют блуждающие нервы. Г. р.
используется в клинике для определения возбудимости блуждающих нервов.
43.
44.
45.
46.
47.
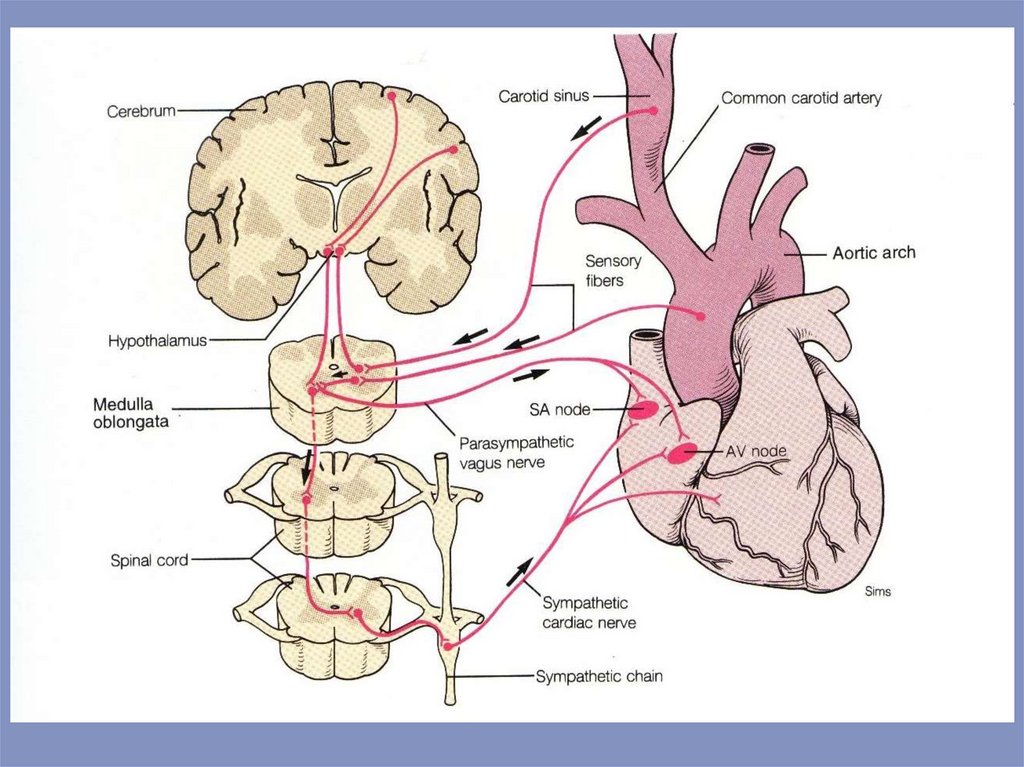
Экстракардиальные регуляторные механизмыСердечные центры продолговатогомозга и моста непосредственно управляют деятельностью сердца.
Это управление обеспечивается вегетативной иннервацией —передачей сигналов
по симпатическим и парасимпатическим нервам.Они изменяют
•частоту сокращений (хронотропноедействие),
•силу сокращений (инотропноедействие)
•скорость атриовентрикулярного проведения (дромотропноедействие).
•возбудимость сердечной мышцы (батмотропное действие)
•Передатчиками нервных влияний на сердце служат химические медиаторы —
•норадреналинв симпатической нервной системе и
•ацетилхолинв парасимпатической.
48.
49.
Примером условнорефлекторной регуляции работы сердца является предстартовое изменение ряда функцийорганизма, при этом усиливается не только работа сердца, а происходит повышение АД, гипервентиляция, повышение
активности ЦНС, вегетативной нервной системы, увеличение количества эритроцитов и гемоглобина, усиление функций
желез внутренней секреции. Подобные изменения функционального состояния проявляется у студентов и школьников во
время сдачи экзаменов.
50.
Гуморальная регуляция работы сердцаВещества, находящиеся в крови (гормоны, медиаторы, метаболиты и вещества пептидной природы) влияют на работу сердца.
Гормональная регуляция работы сердца, прежде всего, осуществляется катехоламинами (адреналином и норадреналином) —
гормонами мозгового вещества надпочечников). Катехоламины оказывают действие на сердце подобно симпатической нервной
системе, т.е. положительное хроно-, ино-, батмо-, дромотропное. Выделение этих гормонов значительно увеличивается при боли,
отрицательных эмоциях (гнев, ярость, страх), эмоциональном стрессе, физической нагрузке, гипоксии и т.д. Усиление работы
сердца, повышение АД и изменение других функциональных параметров организма при этом имеют адаптационноприспособительное значение.
Глюкокортикоиды увеличивают силу сокращения. Опосредованное влияние на сердце оказывают глюкагон и инсулин,
простагландины, усиливая его работу. Гормоны щитовидной железы — тироксин и трииодтиронин вызывают учащение и усиление
сокращений сердца.
Существенное влияние на силу и частоту сердечных сокращений оказывают ионы калия и кальция. Повышение содержания
калия в наружной среде (внеклеточный калий) приводит к снижению потенциала покоя (вследствие уменьшения градиента
концентрации калия) и к увеличению проницаемости возбудимых мембран для калия (как при действии ацетилхолина на миокард
предсердий). Увеличение концентрации калия вдвое приводит к незначительной деполяризации и очень слабому повышению
возбудимости и скорости проведения, что вызывает подавление гетеротопных очагов возбуждения. При дальнейшем увеличении
концентрации калия возбудимость, скорость проведения и длительность потенциала действия падают, в результате чего
уменьшается сила сокращения, синоатриальный узел перестает функционировать как водитель ритма сердца, что сопровождается
резко выраженной брадикардией и остановкой сердца в период диастолы.
Снижение концентрации внеклеточного калия приводит к повышению активности пейсмекера, активируются гетеротопные и
эктопические очаги возбуждения. Все это приводит к нарушению ритма сердца (экстрасистолия, мерцание и трепетание предсердий
и желудочков) и возможны очень тяжелые последствия вплоть до летального исхода из-за нарушения ритма сердца.
Увеличение содержания кальция во внеклеточной жидкости сопровождается увеличением силы и частоты сердечных
сокращений, а удаление кальция из внеклеточной жидкости (в эксперименте) вызывает прекращение сокращений сердца.
Деятельность сердца изменяется при изменении рН крови (слабый ацидоз усиливает, а выраженный ацидоз угнетает работу
сердца; алкалоз сопровождается увеличением силы сокращения сердца).
51.
52.
53.
54.
55.
56.
Внешние проявления сердечной деятельности[править | править код]Выделяются следующие группы проявлений:
Электрические — ЭКГ, вентрикулокардиография
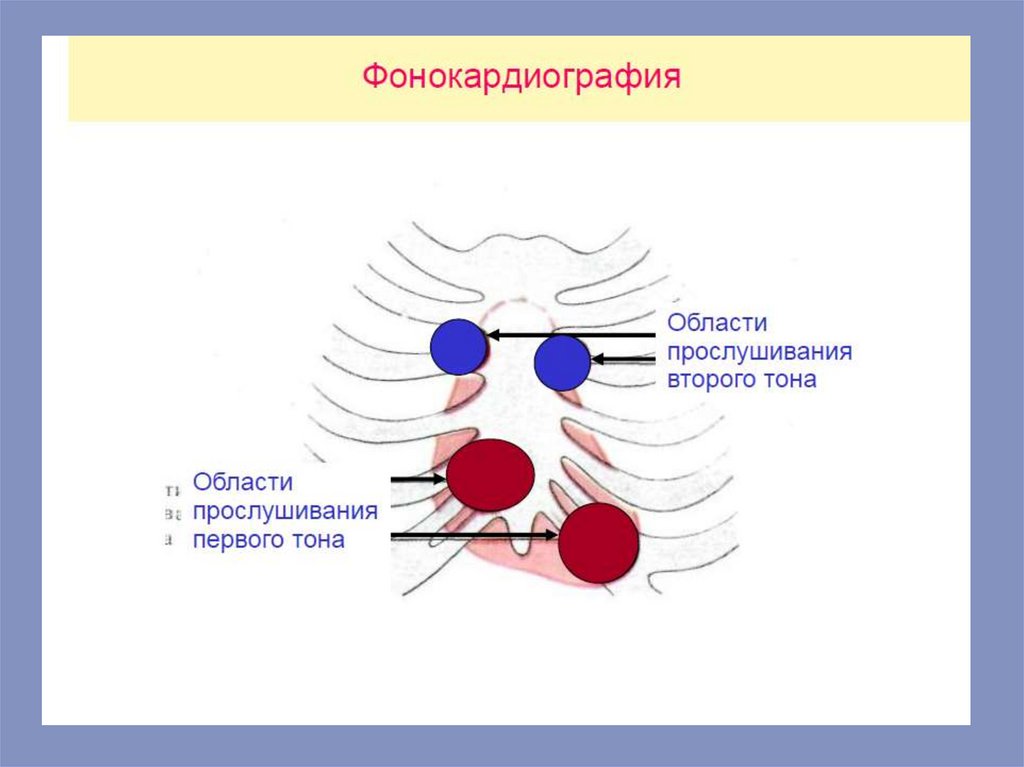
Звуковые — аускультация, фонокардиография
Механические:
Верхушечный толчок — пальпация, апекскардиография
Пульсовая волна — пальпация, сфигмография, флебография
Динамические эффекты —изменение центра тяжести грудной клетки в
сердечном цикле — динамокардиография
Баллистические эффекты — сотрясание тела в момент выброса крови из
сердца — баллистокардиография
Изменение размеров, положения и формы — УЗИ, рентгенокимография
57.
58.
59.
Авторство: Kalumet. selbst erstellt =Собственная работа, CC BY-SA 3.0,
https://commons.wikimedia.org/w/index.php?
curid=438140
60.
Авторство: Yundex-yandex. [1], CC BY-SA 4.0,https://commons.wikimedia.org/w/index.php?
curid=62170398
Электрическая ось сердца — проекция результирующего вектора возбуждения
желудочков во фронтальной плоскости (проекция на ось I стандартного
электрокардиографического отведения). Обычно она направлена вниз и вправо
(нормальные значения: 30°…70°), но может и выходить за эти пределы у высоких людей,
лиц с повышенной массой тела, детей (вертикальная ЭОС с углом 70°…90°, или
горизонтальная — с углом 0°…30°). Отклонение от нормы может означать как наличие
каких-либо патологий (аритмии, блокады, тромбоэмболия), так и нетипичное
расположение сердца (встречается крайне редко). Нормальная электрическая ось
называется нормограммой. Отклонения её от нормы влево или вправо —
соответственно левограммой или правограммой.
61.
Компьютерная модельработы сердца
Авторство: DrJanaOfficial.
Official Website, Support, CC BYSA 4.0,
https://commons.wikimedia.org
/w/index.php?curid=50477765
62.
63.
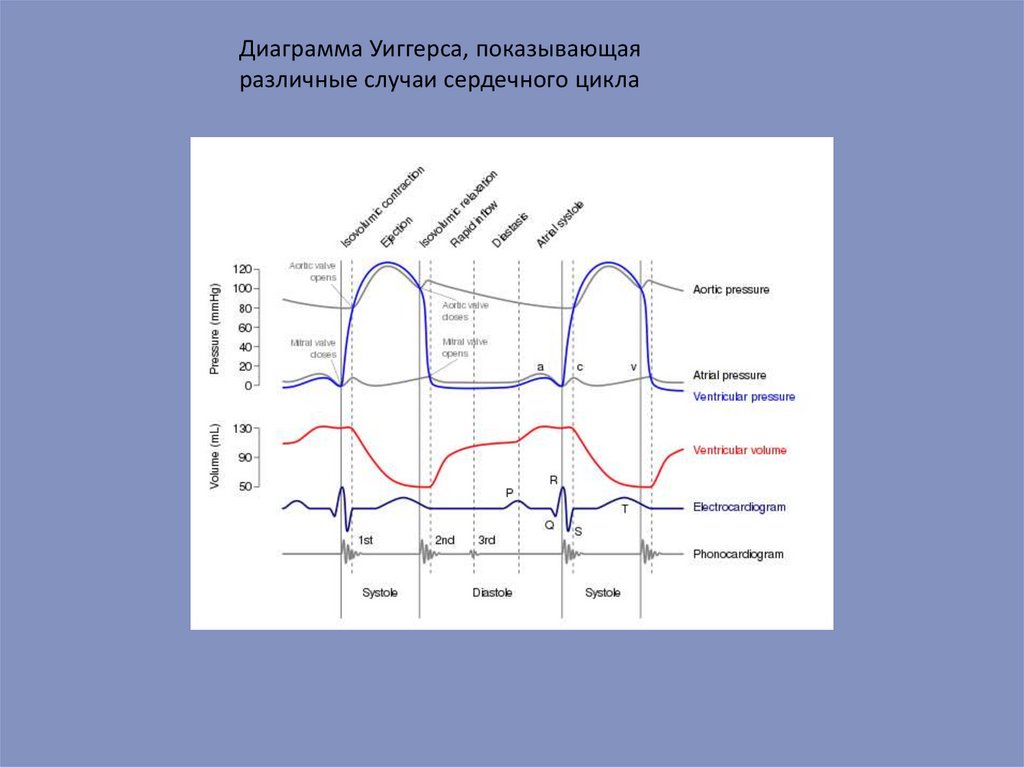
Диаграмма Уиггерса, показывающаяразличные случаи сердечного цикла
64.
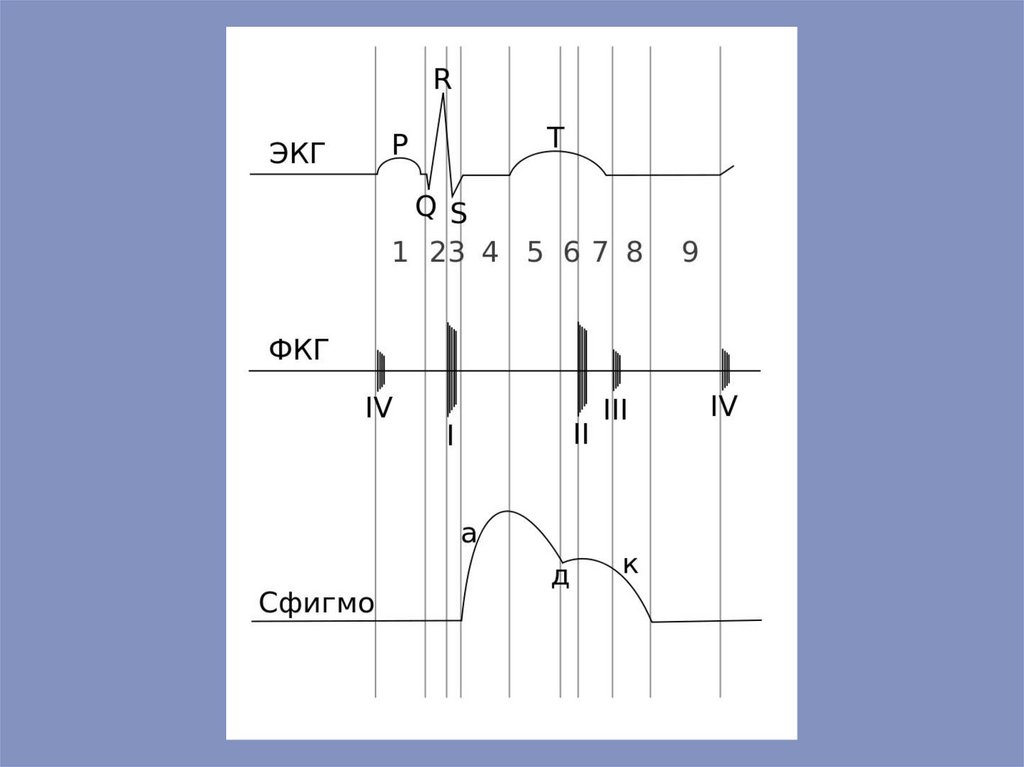
Верхушечный толчок — видимые колебания грудной клет-ки в области Vмежреберья слева от грудины. Возникает в ре-зультате изменения объема, формы и
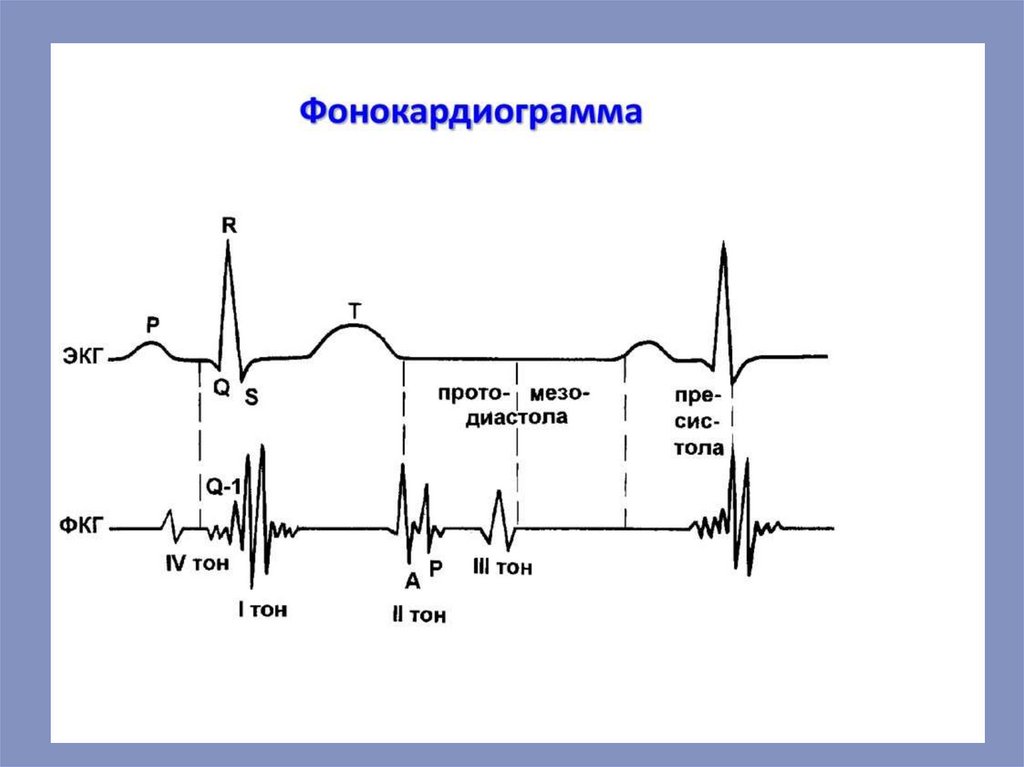
пространственного распо-ложения сердца в грудной полости. Тоны сердца. При
сокращении сердца возникают колебания звуковой частоты (15–400 Гц),
передающиеся на грудную клетку, где их можно выслушать ухом, стетоскопом или
зарегистриро-вать с помощью микрофона. Различают четыре тона: I и II тоны
называют облигатными, т. к. они выслушиваются постоянно, III и IV тоны относят к
факультативным, они не всегда выявляются. Первый тон (систолический) возникает
в результате закрытия предсердно-желудочковых клапанов, колебания их
сухожильных нитей и напряжения стенок желудочков. Второй тон (диастолический), более короткий, связан с закрытием полулунных клапа-нов. Третий тон
возникает в результате быстрого наполнения кровью желудочков и отражает
вибрацию их стенок. Четвертый тон возникает в момент систолы предсердий,
предшествует пер-вому тону и связан с выбросом крови из предсердий в
желудочки.
Электрокардиография (ЭКГ) — метод
графической реги-страции электрической
активности сердца при помощи электродов, помещаемых на различные участки
поверхности тела.
65.
ЭхоКГ с ЦДК66.
René-Théophile-Hyacinthe Laennec (1781 –1826) French physician and inventor of the
stethoscope.
67.
Лаэннек со стетоскопом осматривает пациента в присутствиистудентов. Картина Теобальда Шартрана
68.
4D Эхокардиограмма69.
70.
71.
Кафедра нормальной физиологииНа кафедре физиологии исследовали
взаимное влияние подкорковых структур
мозга и ноцицептивного раздражения на
гемодинамику, роль центральных
хемореактивных (адрен-, холин-,
серотонин-, ангиотензин-, опиатергичеких
структур мозга) в реализации ответных
реакций организма на боль. Показана
роль периферических звеньев
симпатоадреналовой системы и
адренергических механизмов мозга в
реализации исследуемых эффектов при
изолированном применении
ноцицептивного раздражения,
стимуляции подкорковых структур и их
сочетании. По этому фрагменту
исследований было защищено 6
кандидатских диссертаций (В.И.Стерхов,
1973, Н.Д.Лодыгина, 1975, Л.С.Исакова,
1977, В.И.Авдеев, 1983, А.А.Пермяков,
1987, Ю.Л.Петров, 1985).
Академик Г.Е.Данилов
72.
Кафедра нормальной физиологииВ 1973 г. В.И.Стерхов в кандидатской
диссертации «Рефлексы с
проприоцепторов на сердечнососудистую систему и дыхание при
локальных воздействиях на
гипоталамус» показал, что
проприоцептивные раздражения и
локальная электрическая стимуляция
заднего отдела гипоталамуса,
применяемые раздельно,
сопровождаются повышением
артериального давления, учащением
сердечных сокращений и усилением
дыхания, тогда как сочетание этих
воздействий ослабляет реакции со
стороны сердечно-сосудистой и
дыхательной систем.
Доцент В.И.Стерхов
73.
Кафедра нормальной физиологии – 75 лет ИГМА• 1975г. Н.Д.Лодыгина.
Кандидатская
диссертация.
«Изменение
артериального давления
и объёмной скорости
кровотока при
сочетании
ноцицептивного
раздражения и
стимуляции
ретикулярной
формации».
74.
Кафедра нормальной физиологии – 75 лет ИГМА• Аналогичное усиление прессорных ответов наблюдала Л.С.Исакова при
ноцицептивном раздражении на фоне электрической стимуляции миндалевидного
комплекса (кандидатская диссертация Ларисы Сергеевны «Изменение гемодинамики
при ноцицептивном раздражении, стимуляции миндалевидного комплекса и их
сочетании», 1977 г.). Показаны дифференцированные эффекты центральных и
периферических звеньев симпатоадреналовой системы в реализации
гемодинамических реакций при изолированном применении ноцицептивного
раздражения, стимуляции миндалевидного комплекса и их сочетании.
75.
Кафедра нормальной физиологииАналогичное усиление прессорных
ответов наблюдала Л.С.Исакова при
ноцицептивном раздражении на фоне
электрической стимуляции
миндалевидного комплекса
(кандидатская диссертация Ларисы
Сергеевны «Изменение гемодинамики
при ноцицептивном раздражении,
стимуляции миндалевидного
комплекса и их сочетании», 1977 г.).
Показаны дифференцированные
эффекты центральных и
периферических звеньев
симпатоадреналовой системы в
реализации гемодинамических
реакций при изолированном
применении ноцицептивного
раздражения, стимуляции
миндалевидного комплекса и их
сочетании.
Зав. кафедрой нормальной
физиологии, доктор мед.наук,
профессор Л.С.Исакова
76.
Кафедра нормальной физиологииВ.И.Авдеевым (1983) в диссертационной
работе “Изменения гемодинамики при
ноцицептивном раздражении, стимуляции
перегородки мозга и их сочетании”
показано, что электрическая стимуляция
латерального ядра перегородки мозга
вызывает угнетение гипертензивной
ноцицептивной реакции. Это происходит
главным образом за счет уменьшения
прироста периферического сосудистого
сопротивления.
Кандидат мед.наук В.И.Авдеев
77.
Кафедра нормальной физиологииВ следующей в кандидатской диссертации,
выполненной под руководством
Г.Е.Данилова (Петров Ю.Л. “Изменение
гемодинамики при сочетании
ноцицептивного раздражения с
воздействиями на ретикулярную формацию
продолговатого мозга”, 1985), изучен
характер взаимного влияния
ноцицептивного раздражения и стимуляции
мелкоклеточного ретикулярного ядра на
формирование гемодинамических реакций.
Установлено, что гипертензивная реакция в
ответ на ноцицептивное раздражение или
электростимуляцию мелкоклеточного
ретикулярного ядра изменяется
неодинаково при воздействиях на
некоторые периферические и центральные
звенья регуляции гемодинамики.
Кандидат мед.наук, доцент, директор
Ижевского мед.колледжа Ю.Л.Петров
78.
Кафедра нормальной физиологииА.А.Пермяковым (1987) в работе
“Изменение ноцицептивных
гемодинамических реакций при
воздействиях на гипоталамус” показано,
что совместное применение
ноцицептивного раздражения и
электрической стимуляции
вентромедиального ядра гипоталамуса
вызывает взаимное усиление
гипертензивных реакций. Обнаружены
механизмы (как периферические, так и
центральные), ограничивающие или,
напротив, усиливающие гипертензивную
реакцию болевого или центрального
происхождения.
Кандидат мед.наук А.А.Пермяков
(в молодости)
79.
80.
81.
82.
83.
84.
85.
86.
87.
88.
89.
90.
91.
92.
Гормоны гипоталамуса — важнейшие регуляторные гормоны,производимые гипоталамусом. Все гормоны гипоталамуса имеют пептидное
строение и делятся на 3 подкласса: рилизинг-гормоны стимулируют
секрецию гормонов передней доли гипофиза, статины тормозят
секрецию гормонов передней доли гипофиза, и гормоны задней доли гипофиза
традиционно называются гормонами задней доли гипофиза по месту их хранения и
высвобождения, хотя на самом деле производятся гипоталамусом.
93.
Гормоны передней доли гипофиза:Тропные, так как их органами-мишенями являются эндокринные железы.
Гипофизарные гормоны стимулируют определенную железу, а повышение
уровня в крови выделяемых ею гормонов подавляет секрецию гормона
гипофиза по принципу обратной связи.
Тиреотропный гормон (ТТГ) — главный регулятор биосинтеза и секреции
гормонов щитовидной железы.
Адренокортикотропный гормон (АКТГ) — стимулирует кору надпочечников.
Гонадотропные гормоны:
фолликулостимулирующий гормон (ФСГ) — способствует созреванию
фолликулов в яичниках, стимуляция пролиферации эндометрия, регуляция
стероидогенеза.
лютеинизирующий гормон (ЛГ) — вызывает овуляцию и образование жёлтого
тела, регуляция стероидогенеза.
Соматотропный гормон (СТГ) — важнейший стимулятор синтеза белка в клетках,
образования глюкозы и распада жиров, а также роста организма.
Лютеотропный гормон (пролактин) — регулирует лактацию, дифференцировку
различных тканей, ростовые и обменные процессы, инстинкты заботы о
потомстве.
94.
Задняя доля гипофиза (лат. pars posterior), или нейрогипо́ физ (лат. neurohypophysis),состоит из:
нервная доля. Образована клетками эпендимы (питуицитами) и окончаниями
аксонов нейросекреторных клеток паравентрикулярного и супраоптического ядер
гипоталамуса промежуточного мозга, в которых и синтезируются вазопрессин
(антидиуретический гормон) и окситоцин, транспортируемые по нервным волокнам,
составляющим гипоталамо-гипофизарный тракт, в нейрогипофиз. В задней доле
гипофиза эти гормоны депонируются и оттуда поступают в кровь.
воронка, infundibulum. Соединяет нервную долю со срединным возвышением.
Воронка гипофиза, соединяясь с воронкой гипоталамуса, образует ножку гипофиза.
Функционирование всех отделов гипофиза тесно связано с гипоталамусом. Это
положение распространяется не только на заднюю долю — «приемник» и депо
гипоталамических гормонов, но и на передний и средний отделы гипофиза, работа
которых контролируется гипоталамическими гипофизотропными гормонами —
рилизинг-гормонами[3].
Гормоны задней доли гипофиза:
аспаротоцин
вазопрессин (антидиуретический гормон, АДГ) (депонируется и секретируется)
вазотоцин
валитоцин
глумитоцин
изотоцин
мезотоцин
окситоцин (депонируется и секретируется)
95.
Вазопрессин выполняет в организме две функции:усиление реабсорбции воды в собирательных трубочках почек (это
антидиуретическая функция вазопрессина);
влияние на гладкую мускулатуру артериол.
Однако название «вазопрессин» не совсем соответствует свойству этого
гормона суживать сосуды. Дело в том, что в нормальных физиологических
концентрациях он сосудосуживающим эффектом не обладает. Сужение
сосудов может происходить при экзогенном внедрении гормона в больших
количествах или же при кровопотере, когда гипофиз интенсивно выделяет этот
гормон. При недостаточности нейрогипофиза развивается синдром
несахарного диабета, при котором с мочой в день может теряться
значительное количество воды (15 л/сутки), так как снижается её реабсорбция
в собирательных трубочках.
Окситоцин во время беременности не действует на матку, так как под
воздействием прогестерона, выделяемого жёлтым телом, она становится
нечувствительной к данному гормону. Окситоцин способствует сокращению
миоэпителиальных клеток, способствующих выделению молока из молочных
желез.
96.
Промежуточная (средняя) доляУ многих животных хорошо развита промежуточная доля гипофиза,
расположенная между передней и задней долями. По происхождению она
относится к аденогипофизу. У человека она представляет тонкую прослойку
клеток между передней и задней долями, довольно глубоко заходящую в
ножку гипофиза. Эти клетки синтезируют свои специфические гормоны —
меланоцитстимулирующие и ряд других.
Меланоцитстимулирующие гормоны (меланотропины, интермедины, МСГ,
меланокортины, melanocyte-stimulating hormones, MSH) — гормоны средней,
или промежуточной, доли гипофиза позвоночных животных и человека. По
химической природе — полипептиды.
Существует три основные разновидности
МСГ:
Альфа-меланоцитстимулирующий гормон(αМСГ)
Бета-меланоцитстимулирующий гормон (βМСГ)
Гамма-меланоцитстимулирующий гормон(γМСГ)
97.
98.
99.
100.
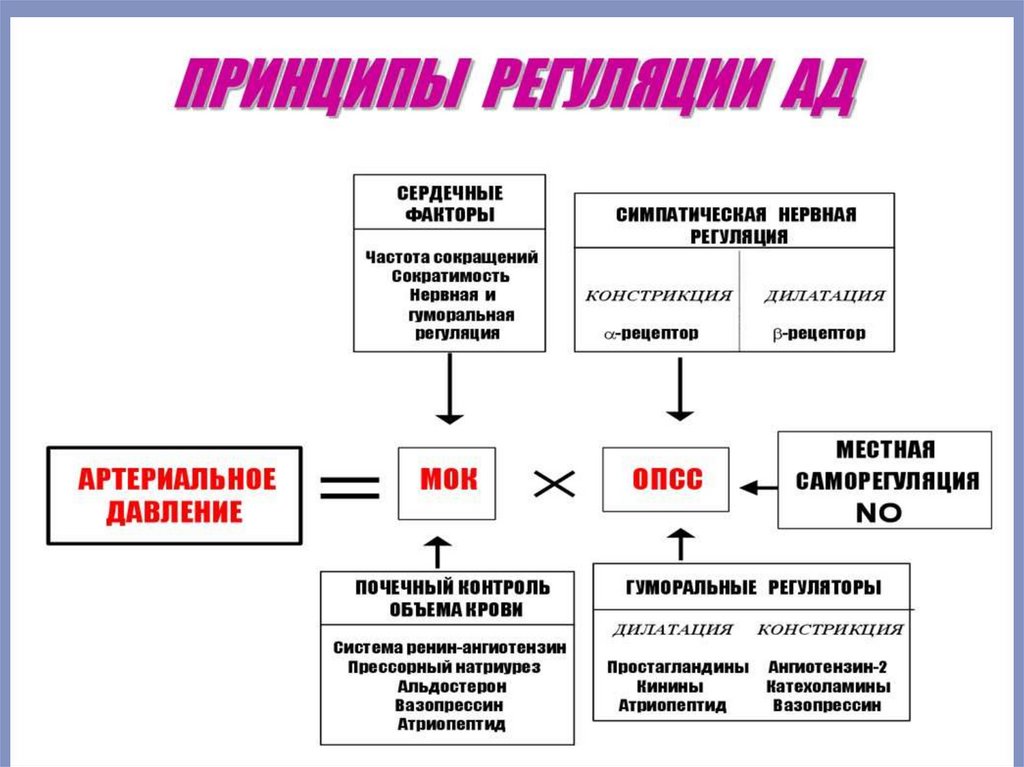
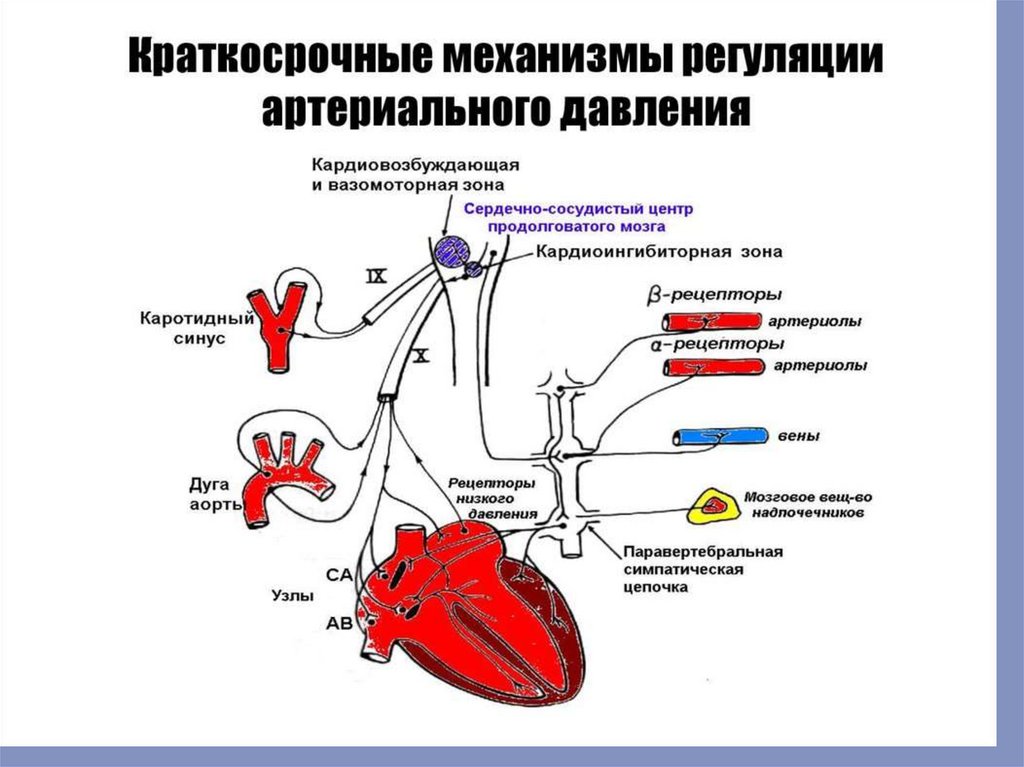
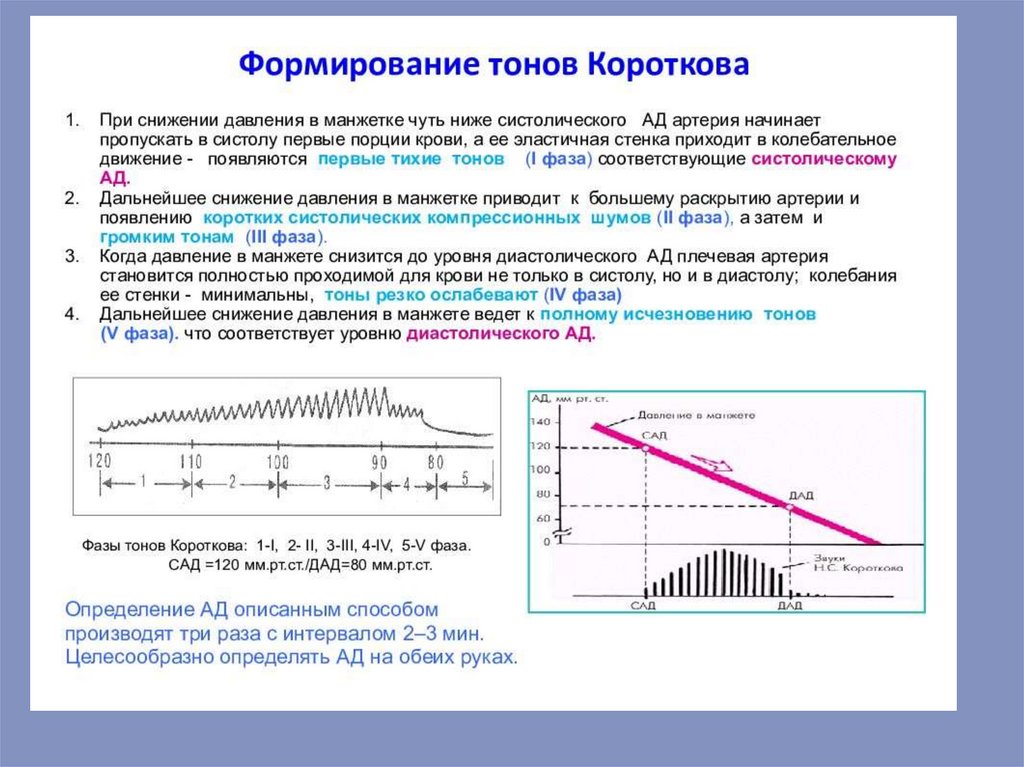
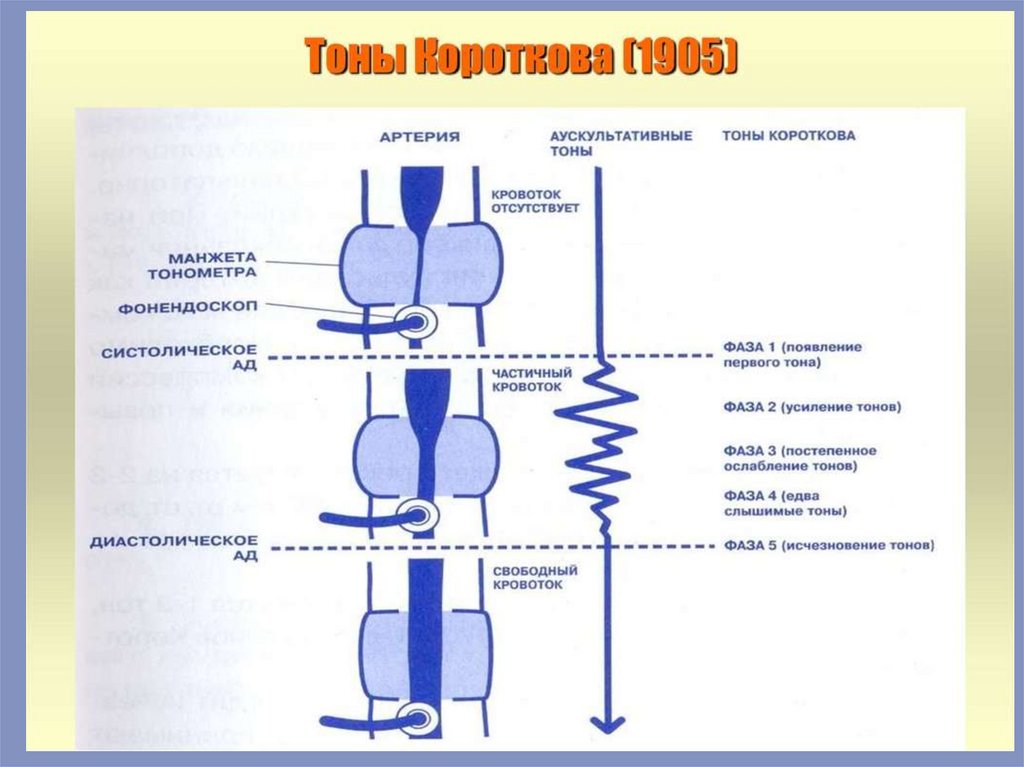
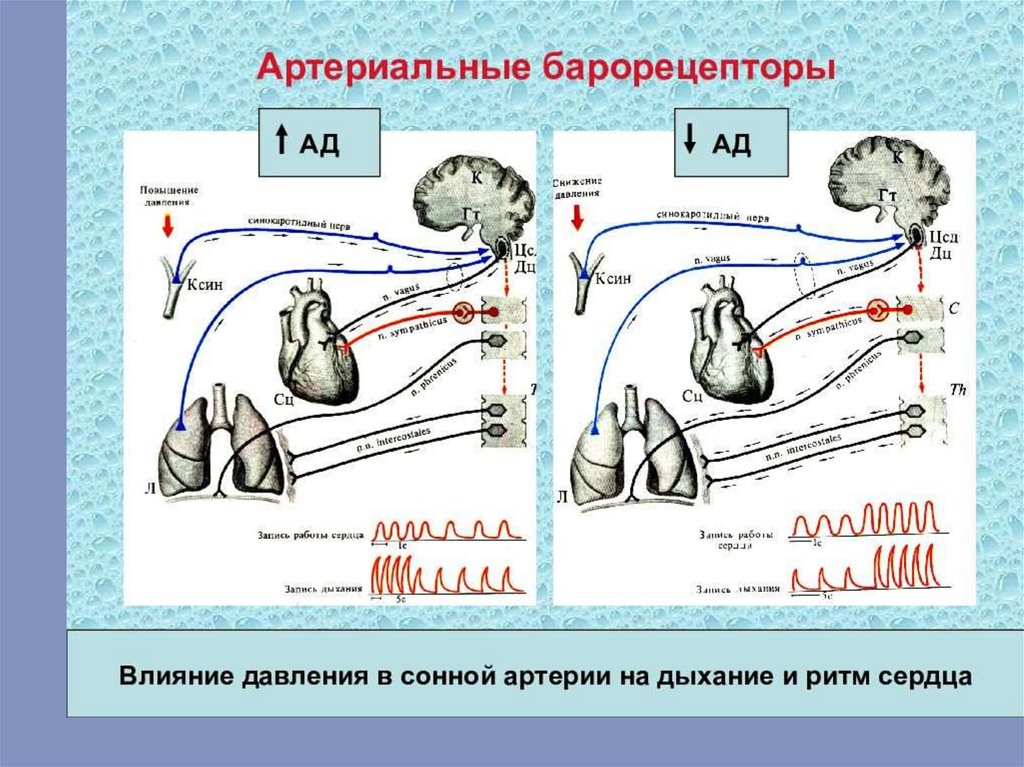
Барорецепторы можно разделить на две категории в зависимости от типакровеносного сосуда, в котором они расположены: артериальные барорецепторы
высокого давления и барорецепторы низкого давления (также известные как
сердечно-легочные [3] или объемные рецепторы [4] ).
Безусловно–рефлекторная регуляция деятельности сердца
Эта форма регуляции сердечной деятельности осуществляется при раздражении
различных рецепторов. Особое значение имеют рецепторы, расположенные в
некоторых участках сосудистой системы, получивших название «главных
сосудистых рефлексогенных зон». К основным рефлексогенным зонам относятся
начальный отдел аорты и каротидный синус, т.е. область разветвления общей
сонной артерии на наружную и внутреннюю. В этих сосудистых областях
располагаются барорецепторы (или прессорецепторы), а раздражителем для них
служит изменение артериального давления (АД). Барорецепторы можно
подразделить на 3 группы. Первую группу барорецепторов составляют рецепторы,
которые воспринимают ритмические колебания АД, связанные с систолой и
диастолой сердца, т.е. эти рецепторы возбуждаются ритмически. Вторая группа
рецепторов воспринимает постоянную, непрерывную нагрузку. Третья группа
барорецепторов воспринимает вибрационные колебания столба жидкости в
сосуде.
101.
давления — 90-100 мм рт.ст.; вибрацию создают вихревые движения крови.Отдельные барорецепторы, воспринимающие давление ниже 80 и выше 120 мм
рт.ст., в нормальных условиях практически не реагируют на изменение давления. Эти
барорецепторы настроены на возможные случаи снижения или повышения АД и
тогда они возбуждаются. При значительном и стабильном повышении АД, рецепторы
в норме возбуждающиеся при ритмических колебаниях давления (систола и
диастола) в пределах 80-120 мм рт.ст., перестают реагировать и посылать импульсы в
ЦНС. Если нет патологической гипертензии, то такое явление имеет положительное,
адаптивное значение, например при мышечной работе. Если в основе повышения АД
лежит патологический процесс (например, гипертоническая болезнь), то отсутствие
реакции со стороны «ритмическсих» барорецепторов оказывает отрицательное
влияние, т.к. рефлекс, ослабляющий работу сердца и понижающий АД не
проявляется.
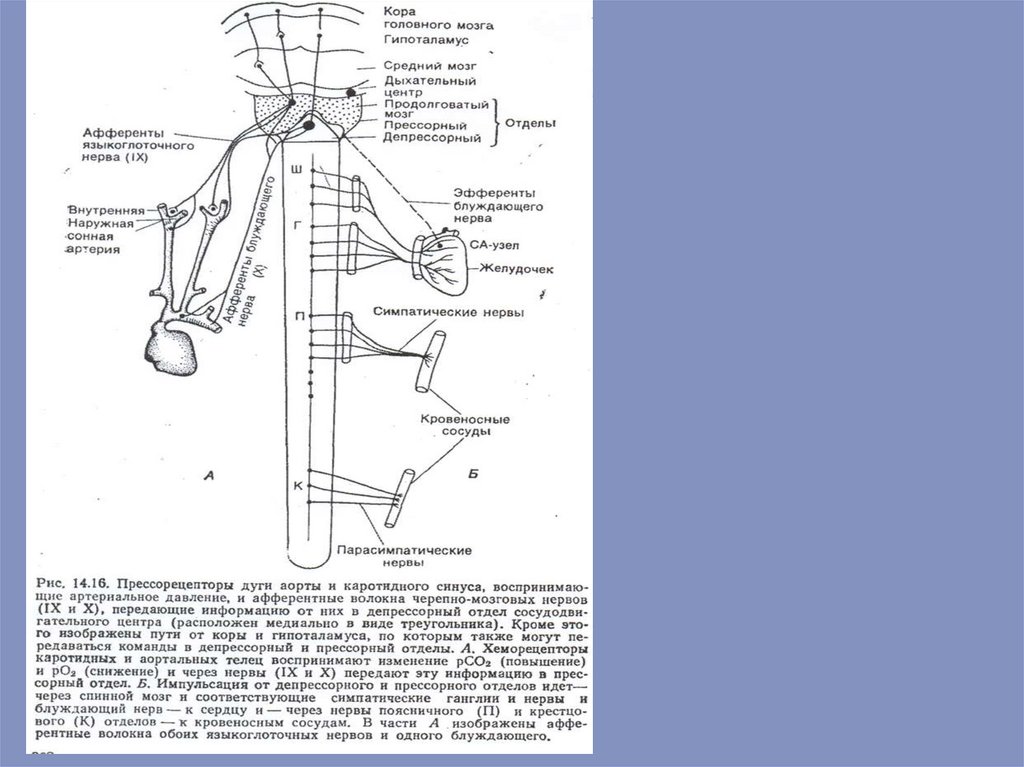
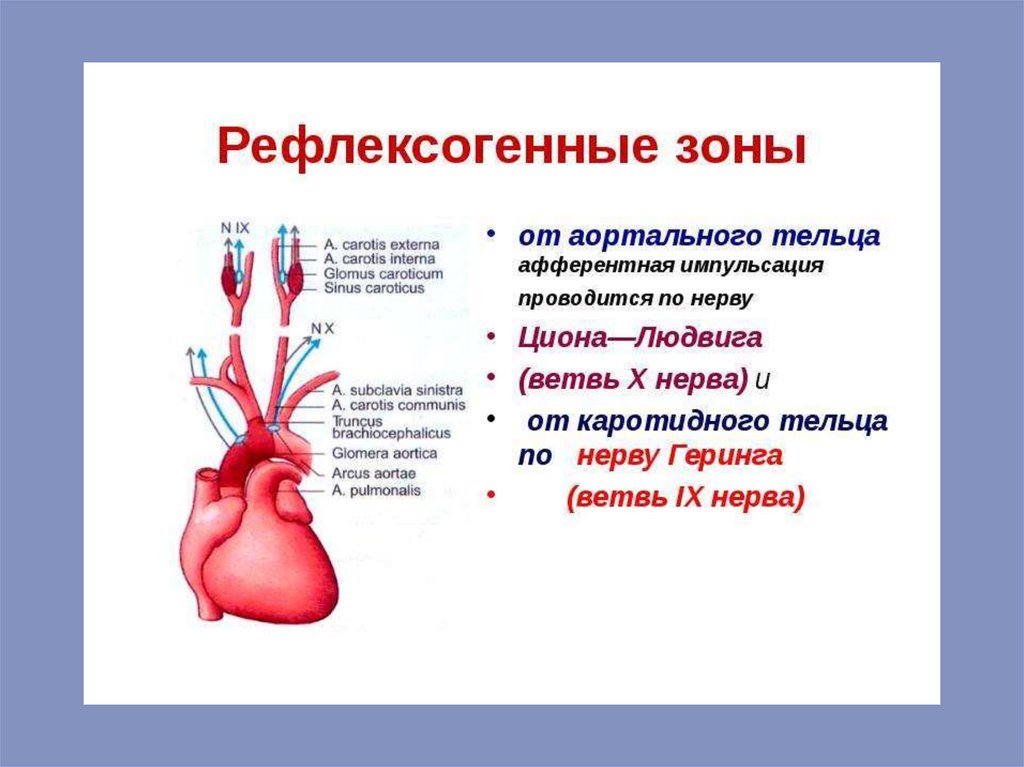
Афферентными нервами, проводящими возбуждение от рецепторов дуги аорты,
являются депрессорные нервы (нерв Циона-Людвига), а от каротидного синуса
импульсы передаются по синусному нерву (нерв Геринга). Возбуждение, которое
возникает в барорецепторах и указанных нервах при повышении давления в
сосудах, передается в продолговатый мозг, затем переключается на центр
блуждающего нерва и это сопровождается возникновением брадикардии
(вагусный эффект), расширением сосудов и снижением АД. При снижении АД и
уменьшении величины пульсовых колебаний, как правило, возникает тахикардия,
увеличение минутного объема крови и это приводит к восстановлению давления.
Но кроме сердечного компонента возникает при этом вазоконстрикторный
эффект, обусловленный возбуждением симпатических сосудосуживающих
нейронов.
102.
103.
104.
Илья Фаддеевич Цион,известный также под
именем Elie de Cyon (13 (25)
марта 1842, Тельши,
Ковенская губерния,
Российская империя — 5
ноября 1912, Париж,
Франция) — русский и
французский физиолог,
доктор медицинских наук,
профессор,
Карл Фри́ дрих Вильге́льм
Лю́ двиг (Carl Friedrich Wilhelm
Ludwig; 1816 — 1895) —
немецкий физиолог и педагог,
основатель Физиологического
института при Лейпцигском
университете. Противник витализма[5],
автор учебника по физиологии
человека и классических трудов
по иннервации кровеносных сосудов и
сердца. Открыл секреторные нервы
слюнных желёз, депрессорный нерв
(нерв Циона — Людвига)[5] и эффект
Людвига
Карл Эвальд
Константин
Ге́ринг (нем. Karl Ewald
Konstantin Hering; 5
августа 1834, Нойгерсдо
рф — 26
января 1918, Лейпциг)
— немецкий физиолог.
105.
106.
107.
108.
109.
110.
111.
112.
113.
114.
115.
116.
117.
118.
На сегодняшний день предложено считать термин «APUD-система»синонимом понятия «диффузная эндокринная система».
Составные части ДЭС — одиночные или небольшие скопления гормонпродуцирующих клеток, которые обладают механизмом APUDсистемы и располагаются в неэндокринных органах.
119.
120.
Если не можешь решить, спросисвое сердце: уж оно-то знает,
чего тебе на самом деле хочется.















































































 medicine
medicine