Similar presentations:
Непредельные углеводороды. Алкены. Алкадиены. Алкины
1.
Тема 3. Непредельныеуглеводороды. Алкены.
Алкадиены. Алкины.
Практическая работа № 1 «Получение этилена и изучение его
свойств»
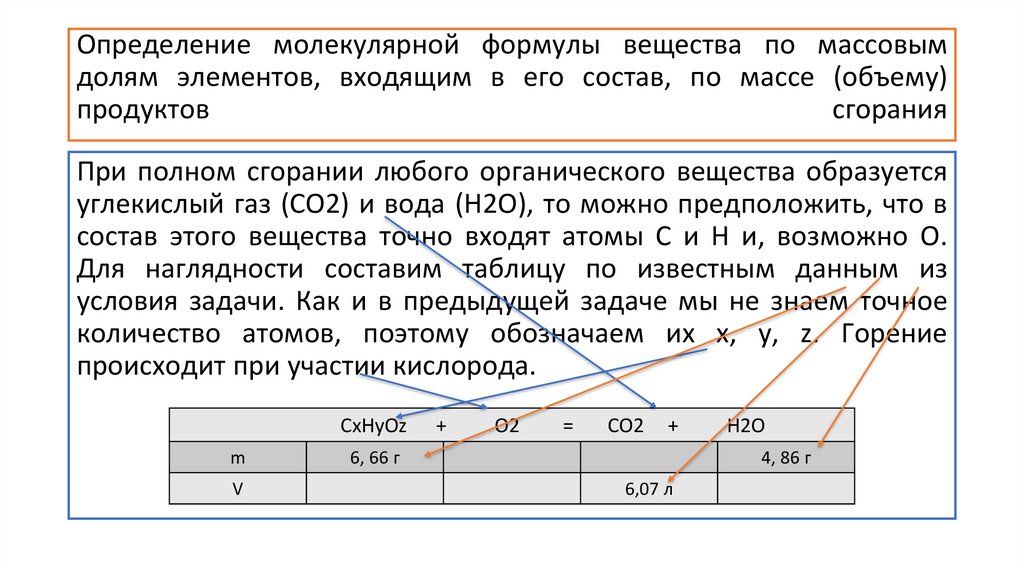
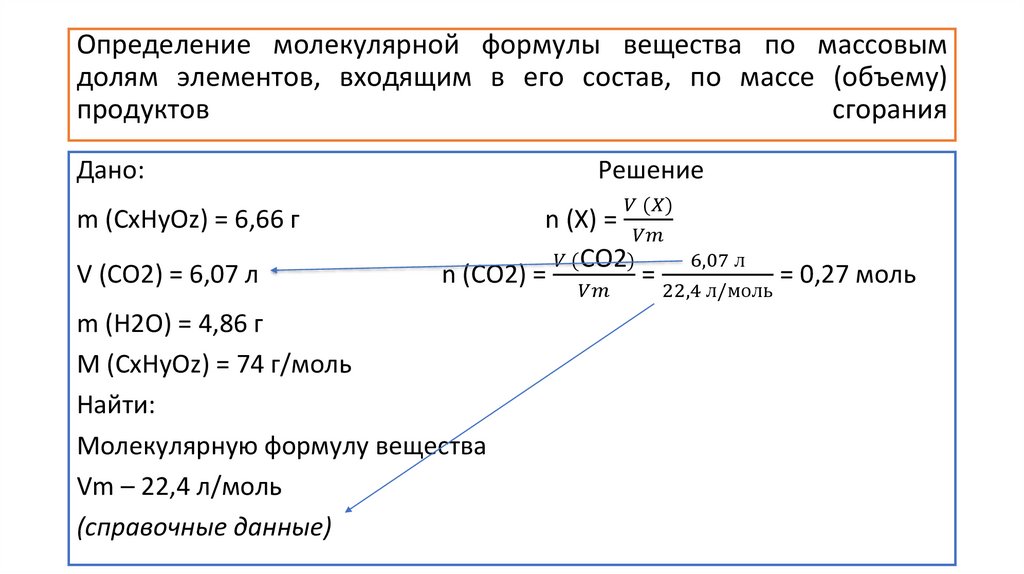
Определение молекулярной формулы вещества по массовым
долям элементов, входящим в его состав, по массе (объему)
продуктов сгорания
2.
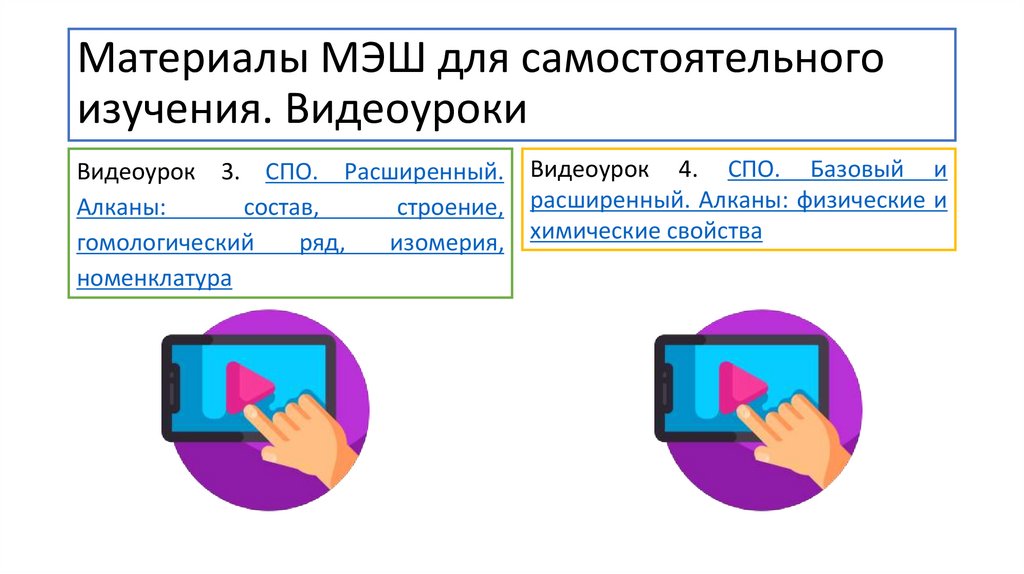
Материалы МЭШ для самостоятельногоизучения. Видеоуроки
Видеоурок 3. СПО. Расширенный.
Алканы:
состав,
строение,
гомологический
ряд,
изомерия,
номенклатура
Видеоурок 4. СПО. Базовый и
расширенный. Алканы: физические и
химические свойства
3.
Непредельные углеводороды. Алкены• Непредельные (ненасыщенные) углеводороды – углеводороды с
открытой цепью, в молекулах которых между атомами углерода
имеются двойные или тройные связи. К ним относятся алкены,
алкины и алкадиены.
• Алкены – углеводороды, молекулы которых содержат одну
двойную связь (σ- и π-связи). Атомы углерода С при двойной
связи находятся в состоянии sp2-гибридизации.
Общая формула CnH2n
4.
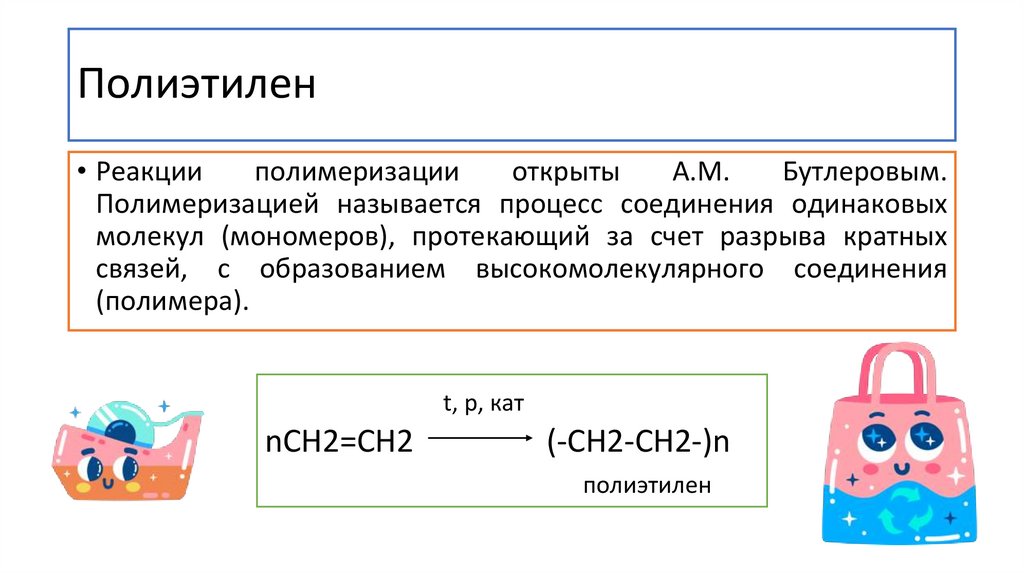
Полиэтилен• Реакции
полимеризации
открыты
А.М.
Бутлеровым.
Полимеризацией называется процесс соединения одинаковых
молекул (мономеров), протекающий за счет разрыва кратных
связей, с образованием высокомолекулярного соединения
(полимера).
t, p, кат
nCH2=CH2
(-CH2-CH2-)n
полиэтилен
5.
Практическая работа №1 «Получениеэтилена и изучение его свойств»
Цель: изучить получение этилена из этанола; его физические и
химические свойства.
Оборудование: колба Вюрца, капельная воронка, газоотводная
трубка, стакан, штатив, стеклянные трубочки, цилиндр, спички,
горелка.
Реактивы: этиловый спирт, серная кислота концентрированная,
бромная вода.
6.
Практическая работа №1 «Получениеэтилена и изучение его свойств»
Опыт № 1 «Получение этилена из этанола»
Опыт № 2 «Взаимодействие этилена с бромной
водой
7.
Практическая работа №1 «Получениеэтилена и изучение его свойств»
Ход работы
№
1
2
Опыт
Описание
Получение В стакан налили одну часть этилового
этилена из спирта и три части серной кислоты.
этанола
Серная
кислота
наливается
по
стеклянной трубочке и смесь постоянно
перемешивается. Полученный раствор
помещается в делительную воронку. Для
равномерного кипения в колбу Вюрца
помещаются
стеклянные
трубочки.
Смесь нагревается через рассекатель
газовой
горелкой.
Выделяющийся
этилен, собирают путем вытеснения
воды. Собранный этилен поджигают.
Наблюдения и уравнения реакций
Смесь нагревается, выделяется газ,
который вытесняет воду из цилиндра.
H2SO4, t
C2H5OH
C2H4 ↑ + H2O
этиловый
спирт
этилен
Горение этилена сопровождается ярким,
светящимся пламенем.
t
C2H4 + 3O2
2CO2 ↑ + 2H2O
8.
Практическая работа №1 «Получениеэтилена и изучение его свойств»
Вывод: вывод должен отражать цель ПР. В данной ПР целью
было 1) изучить получение этилена из этанола (опыт 1); 2) его
физические (опыт 1) и химические свойства (опыт 2).
В лабораторных условиях этилен можно получить путем
дегидратации этилового спирта, т.е. отщепления от него молекулы
воды. Этилен – бесцветный газ без запаха, нерастворимый в воде.
Химические свойства этилена обусловлены ….., поэтому для него
характерны реакции …..
9.
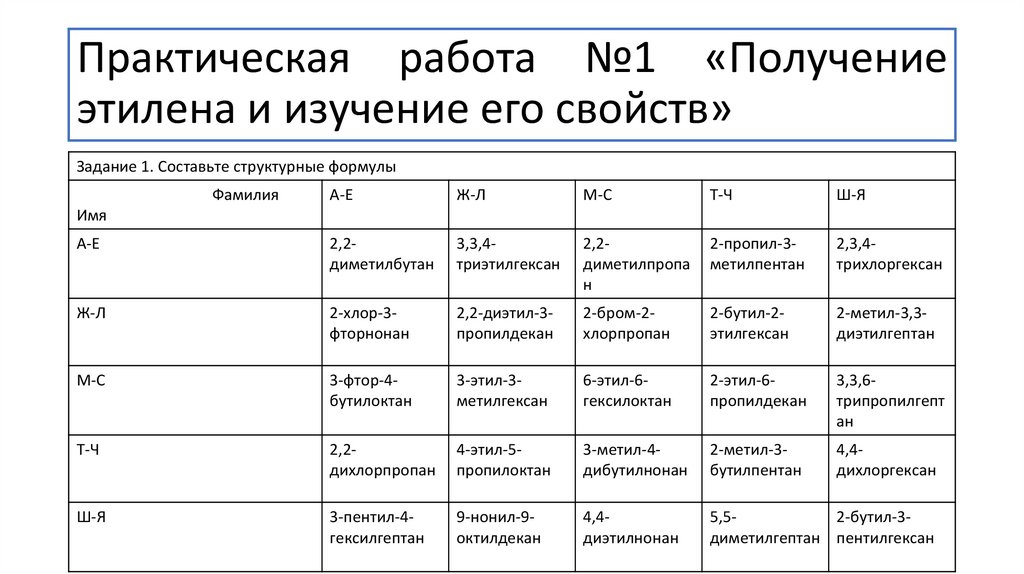
Практическая работа №1 «Получениеэтилена и изучение его свойств»
Задание 1. Составьте структурные формулы
Фамилия
А-Е
Ж-Л
М-С
Т-Ч
Ш-Я
А-Е
2,2диметилбутан
3,3,4триэтилгексан
2,2диметилпропа
н
2-пропил-3метилпентан
2,3,4трихлоргексан
Ж-Л
2-хлор-3фторнонан
2,2-диэтил-3пропилдекан
2-бром-2хлорпропан
2-бутил-2этилгексан
2-метил-3,3диэтилгептан
М-С
3-фтор-4бутилоктан
3-этил-3метилгексан
6-этил-6гексилоктан
2-этил-6пропилдекан
3,3,6трипропилгепт
ан
Т-Ч
2,2дихлорпропан
4-этил-5пропилоктан
3-метил-4дибутилнонан
2-метил-3бутилпентан
4,4дихлоргексан
Ш-Я
3-пентил-4гексилгептан
9-нонил-9октилдекан
4,4диэтилнонан
5,52-бутил-3диметилгептан пентилгексан
Имя
10.
Практическая работа №1 «Получениеэтилена и изучение его свойств»
Критерии оценивания (всего 20 баллов)
1. Описание опыта (5 баллов)
- Полное и четкое описание всех этапов опыта (5 баллов).
- Описание частично неполное или неясное (3-4 балла).
- Описание отсутствует или крайне неясное (0-2 балла).
- **Снятие баллов**: 1 балл за каждую пропущенную или неверно описанную стадию.
2. Наблюдения и уравнения (5 баллов)
- Все наблюдения записаны четко и логично; уравнения правильные (5 баллов).
- Наблюдения частично неполные или с незначительными ошибками; уравнения с незначительными
ошибками (3-4 балла).
- Наблюдения отсутствуют или уравнения неверные (0-2 балла).
- **Снятие баллов**: 1 балл за каждую неточность в наблюдениях или уравнениях.
11.
Практическая работа №1 «Получениеэтилена и изучение его свойств»
3. Вывод (5 баллов)
- Правильное дополнение пропущенных слов, логика вывода соблюдена (5 баллов).
- Пропущенные слова частично дополнены, логика вывода нарушена (3-4 балла).
- Вывод отсутствует или содержит серьезные ошибки (0-2 балла).
- **Снятие баллов**: 1 балл за каждое пропущенное слово или несуразность в выводе.
4. Дополнительное задание (5 баллов)
- Структурная формула алкана составлена правильно, соответствуют всем критериям (5
баллов).
- Формула неверно составлена, присутствуют 1-2 негрубые ошибки (3-4 балла).
- Формула отсутствует или неправильная, есть 1-2 грубые ошибки (0-2 балла).
- **Снятие баллов**: 1 балл за каждую ошибку в формуле.
12.
Практическая работа №1 «Получениеэтилена и изучение его свойств»
Перевод баллов в оценку
- 18-20 баллов: «5» (отлично)
- 15-17 баллов: «4» (хорошо)
- 12-14 баллов: «3» (удовлетворительно)
- 0-11 баллов: «2» (неудовлетворительно)
13.
Определение молекулярной формулы вещества по массовымдолям элементов, входящим в его состав, по массе (объему)
продуктов
сгорания
• Для нахождения молекулярной формулы вещества необходимо
определить соотношение числа атомов химических элементов в
искомой молекулярной формуле
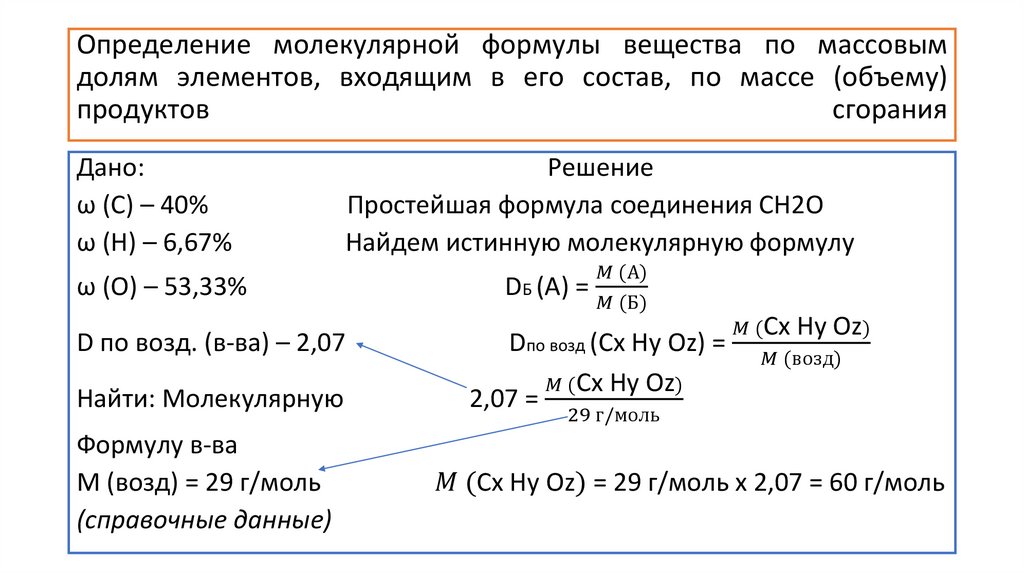
• Пример 1. Если известны массовые доли химических элементов,
входящих в состав данного вещества.
Определите молекулярную формулу органического вещества, если
известно, что массовая доля углерода в нем составляет 40%,
водорода 6,67%, кислорода 53,33%, а относительная плотность
вещества по воздуху 2,07.
14.
Определение молекулярной формулы вещества по массовымдолям элементов, входящим в его состав, по массе (объему)
продуктов
сгорания
При решении данной задачи используются следующие формулы:

































 chemistry
chemistry








