Similar presentations:
Виды химических связей
1.
2.
Под химической связью понимаются электрическиесилы притяжения, удерживающие частицы друг около
друга. Частицами могут быть атомы, ионы, молекулы.
3.
Причина образования химической связи — стремлениеатомов посредством взаимодействия с другими атомами
достичь более устойчивого состояния.
Электроотрицательность (ЭО) – способность
притягивать электроны.
Если атомы обладают одинаковой ЭО, возникает
ковалентная неполярная связь;
Если атомы обладают ЭО разной, но не резко отличаются,
разность в ЭО < 1,7 – возникает ковалентная полярная
связь;
Если атомы обладают ЭО разной, резко отличаются,
разность в ЭО > 1,7 – возникает ионная связь.
4.
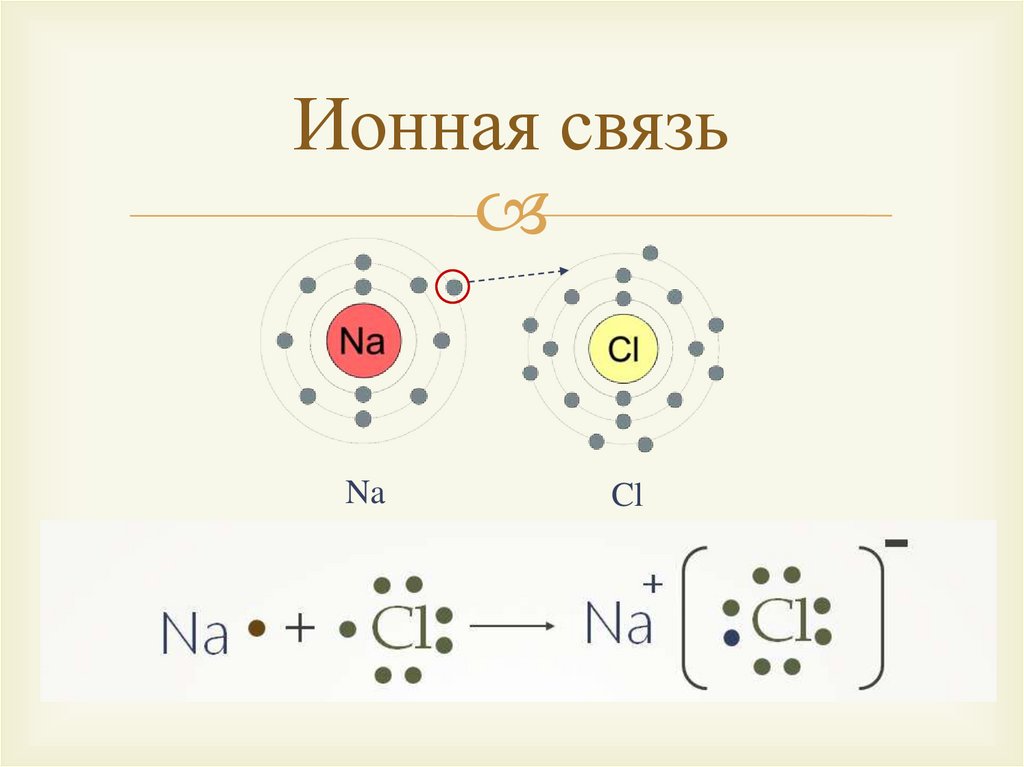
Ионная связьNa
Cl
5.
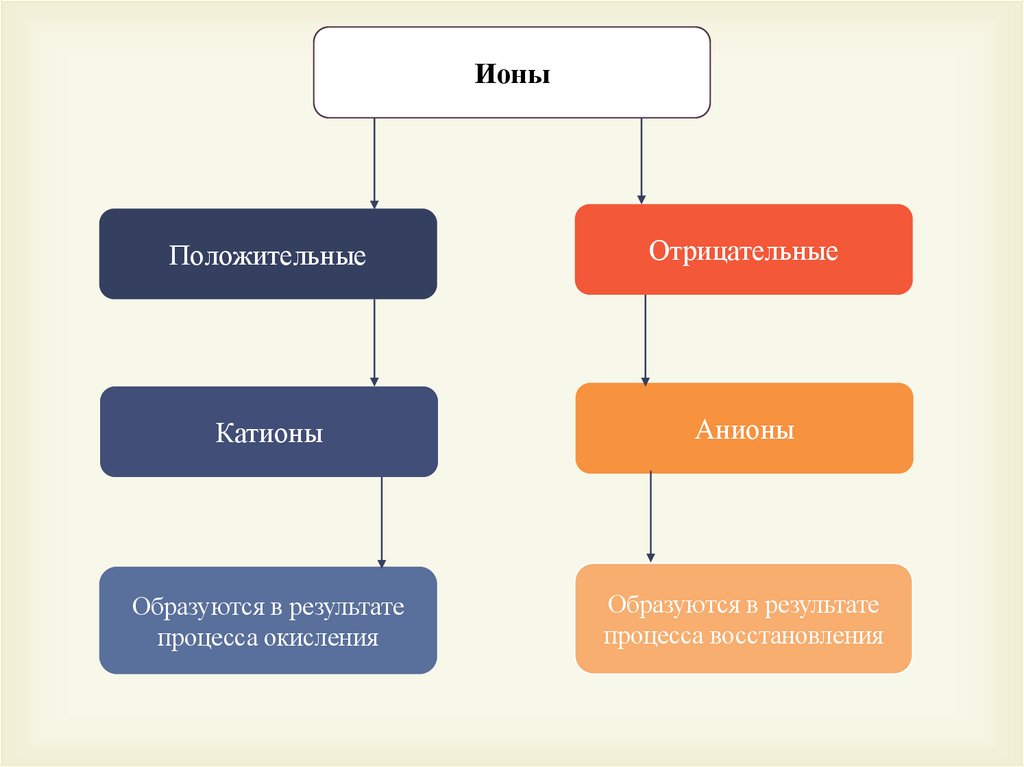
ИоныПоложительные
Отрицательные
Катионы
Анионы
Образуются в результате
процесса окисления
Образуются в результате
процесса восстановления
6.
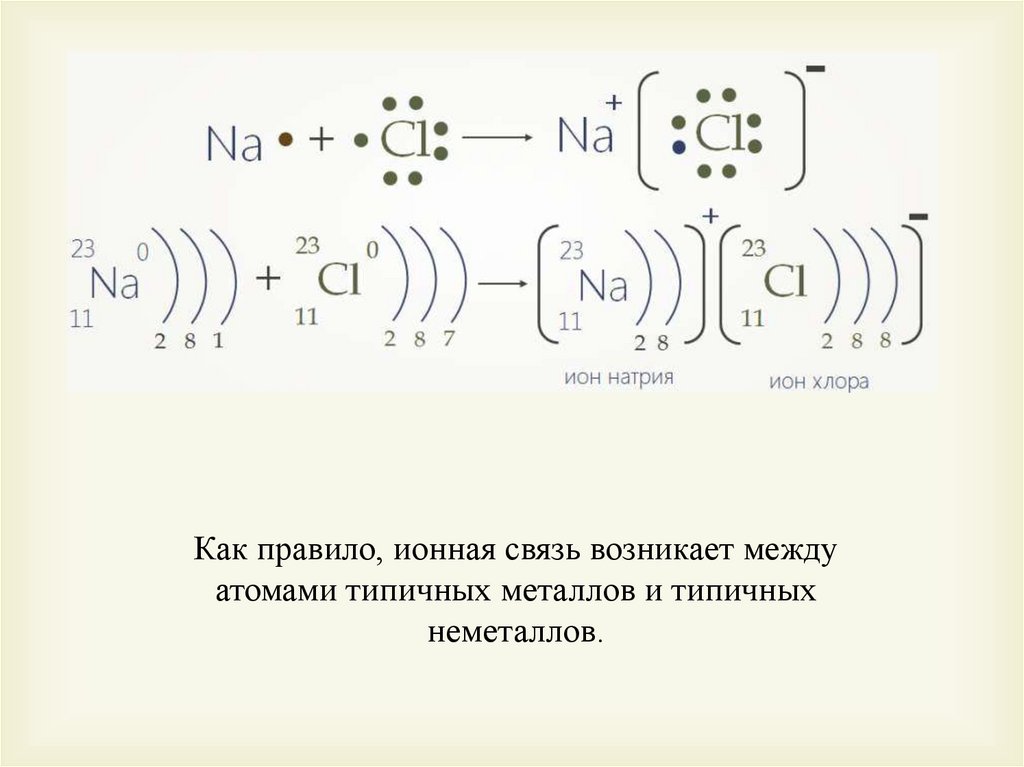
Как правило, ионная связь возникает междуатомами типичных металлов и типичных
неметаллов.
7.
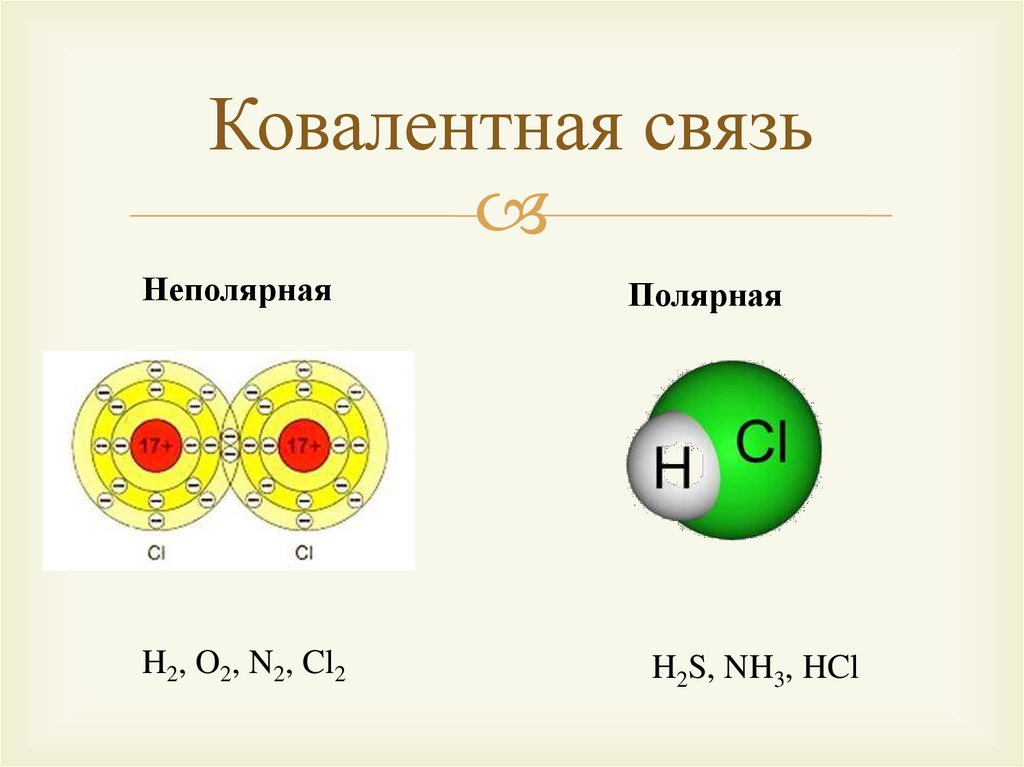
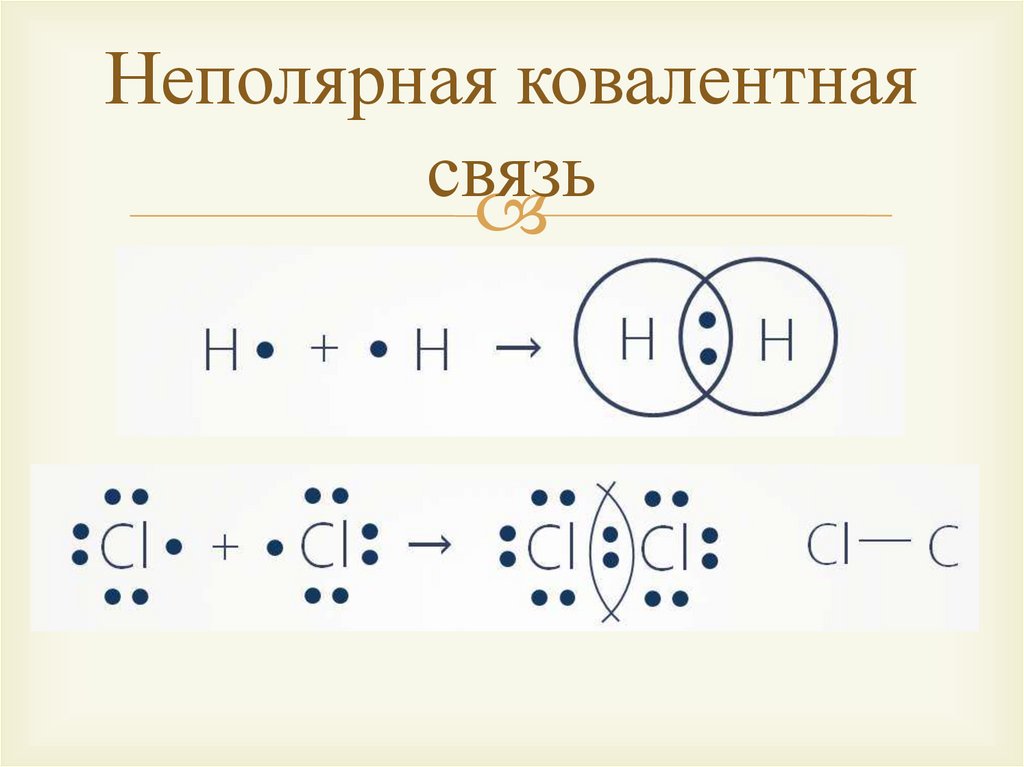
Ковалентная связьНеполярная
H2, O2, N2, Cl2
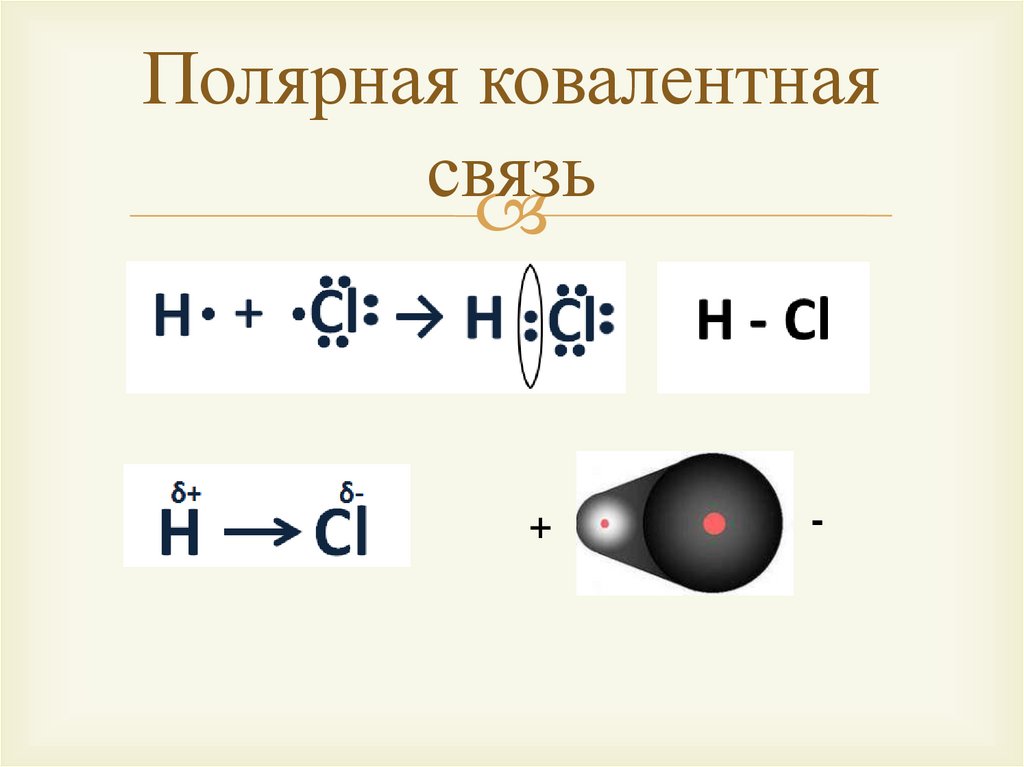
Полярная
H2S, NH3, HCl
8.
Неполярная ковалентнаясвязь
9.
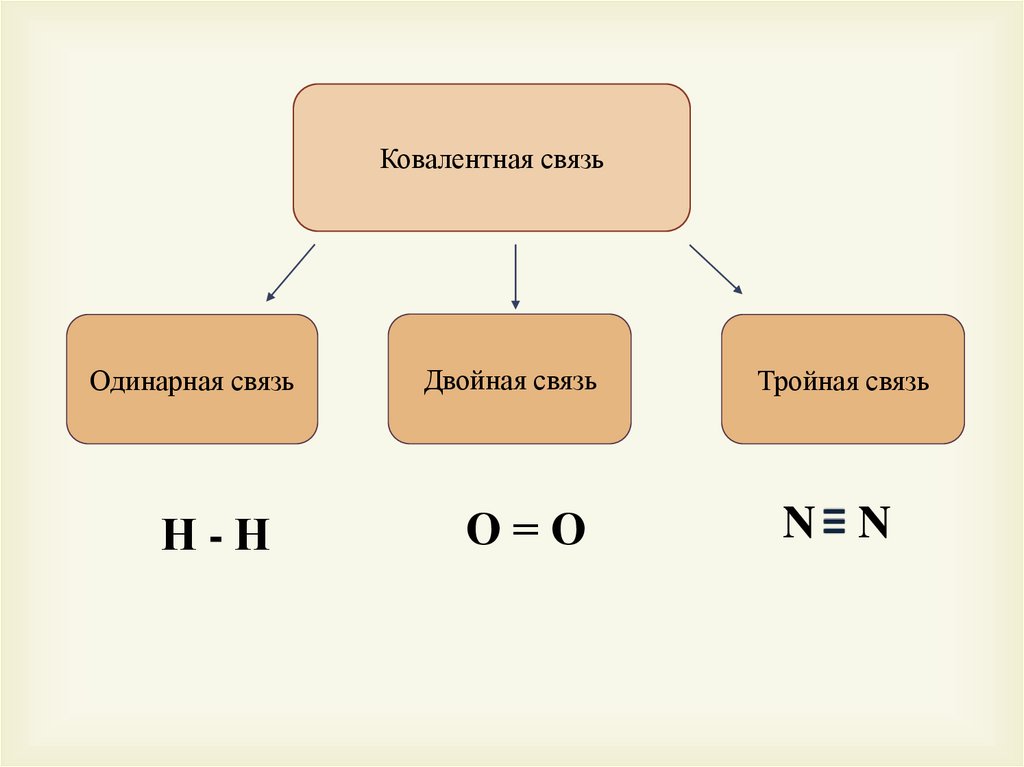
Ковалентная связьОдинарная связь
Н-Н
Двойная связь
Тройная связь
О=О
N N
10.
Полярная ковалентнаясвязь
+
-
11.
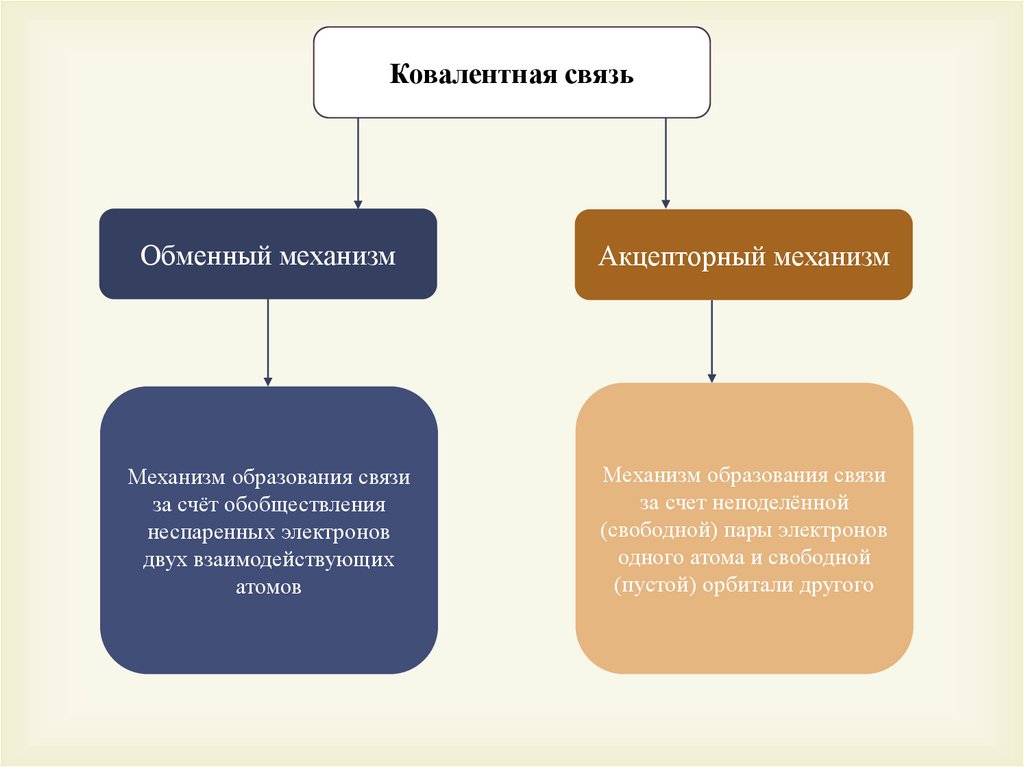
Ковалентная связьОбменный механизм
Акцепторный механизм
Механизм образования связи
за счёт обобществления
неспаренных электронов
двух взаимодействующих
атомов
Механизм образования связи
за счет неподелённой
(свободной) пары электронов
одного атома и свободной
(пустой) орбитали другого
12.
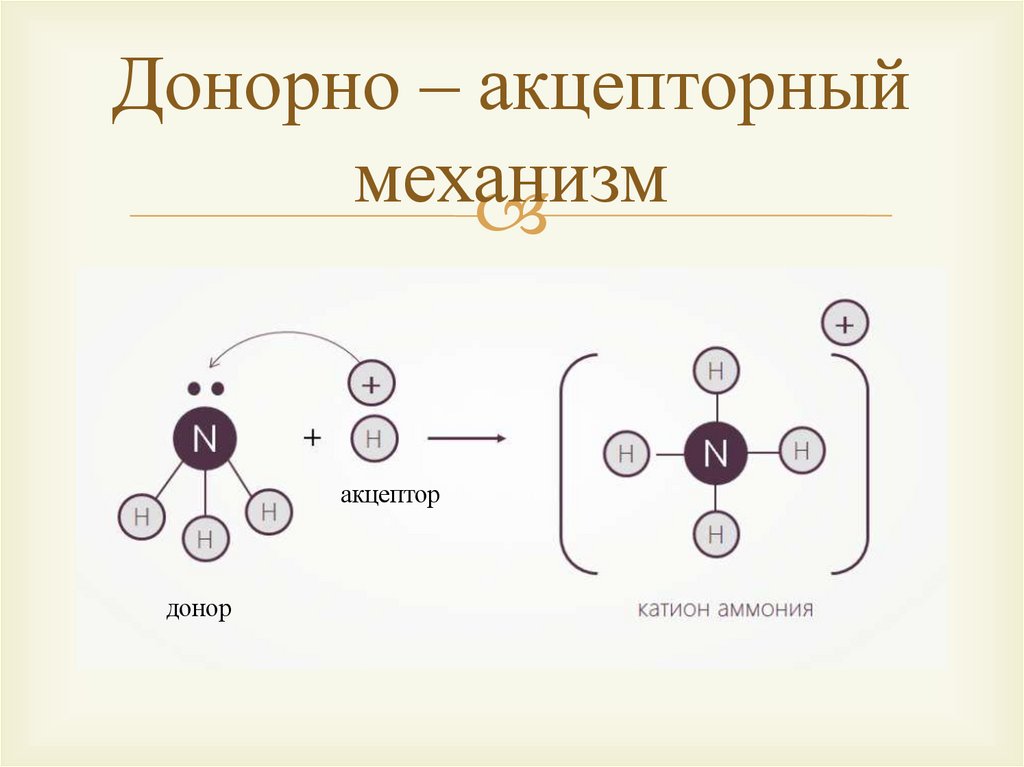
Донорно – акцепторныймеханизм
акцептор
донор
13.
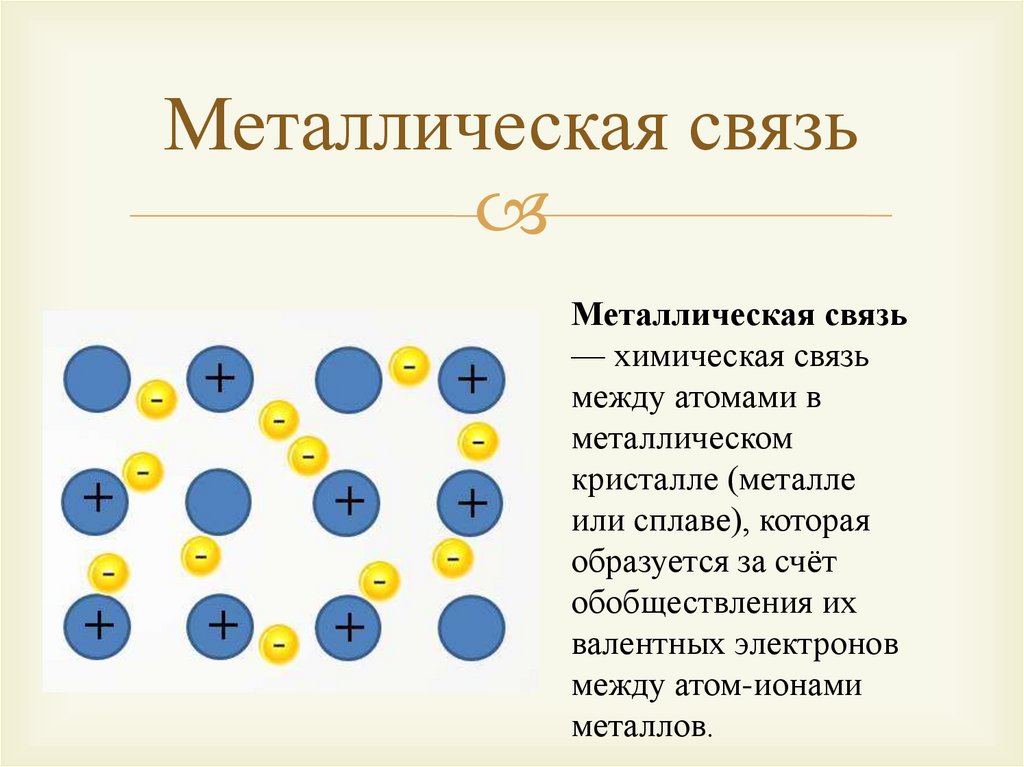
Металлическая связьМеталлическая связь
— химическая связь
между атомами в
металлическом
кристалле (металле
или сплаве), которая
образуется за счёт
обобществления их
валентных электронов
между атом-ионами
металлов.
14.
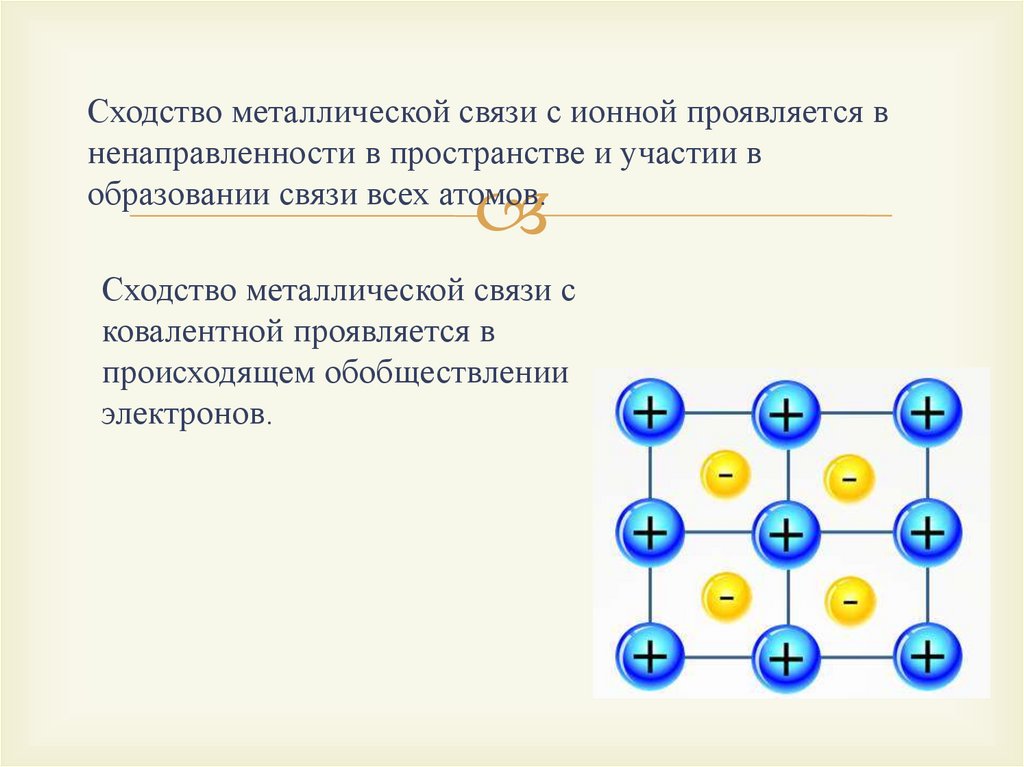
Сходство металлической связи с ионной проявляется вненаправленности в пространстве и участии в
образовании связи всех атомов.
Сходство металлической связи с
ковалентной проявляется в
происходящем обобществлении
электронов.
15.
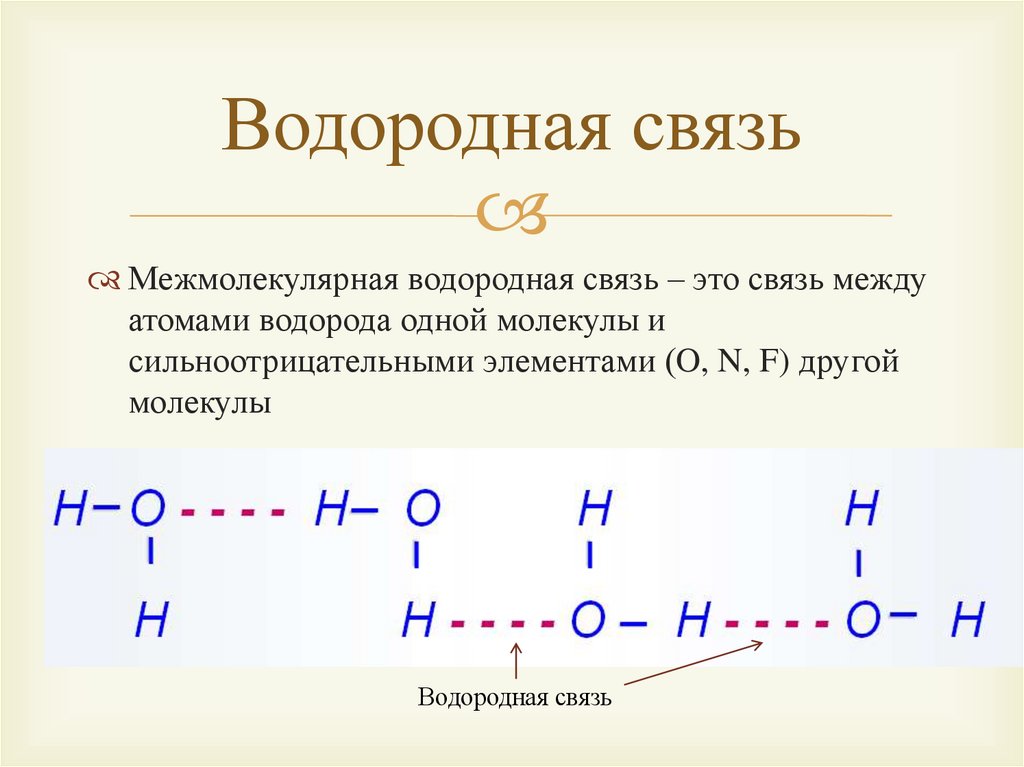
Водородная связьМежмолекулярная водородная связь – это связь между
атомами водорода одной молекулы и
сильноотрицательными элементами (O, N, F) другой
молекулы
Водородная связь
16.
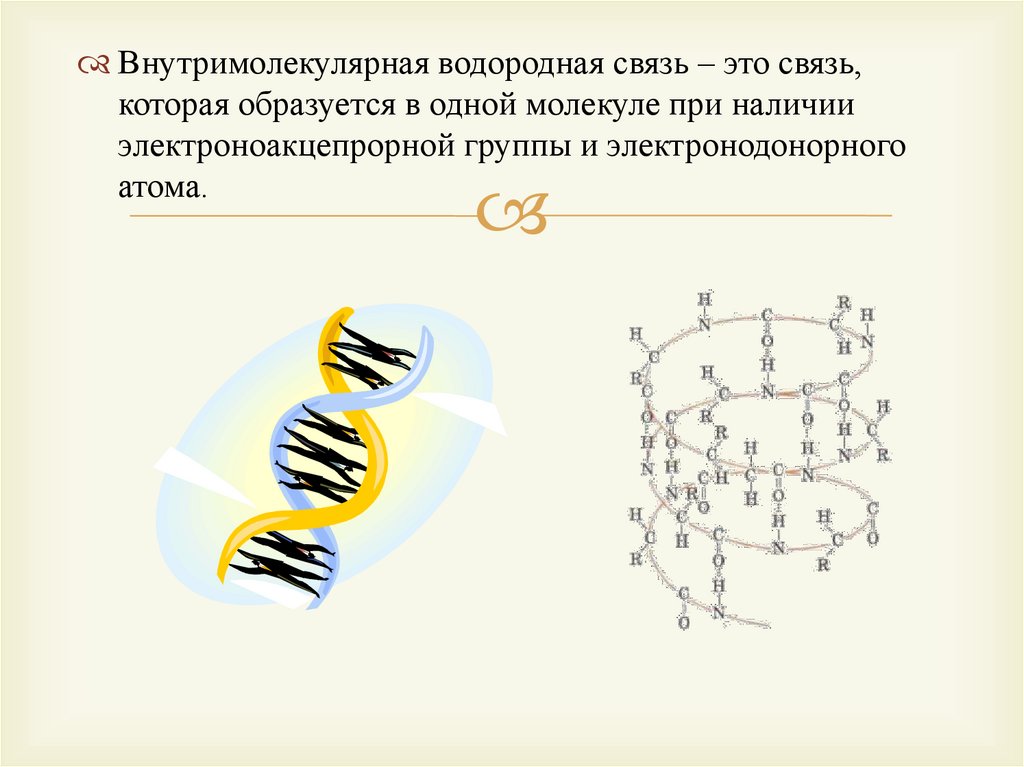
Внутримолекулярная водородная связь – это связь,которая образуется в одной молекуле при наличии
электроноакцепрорной группы и электронодонорного
атома.



 chemistry
chemistry








