Similar presentations:
Электролитическая диссоциация
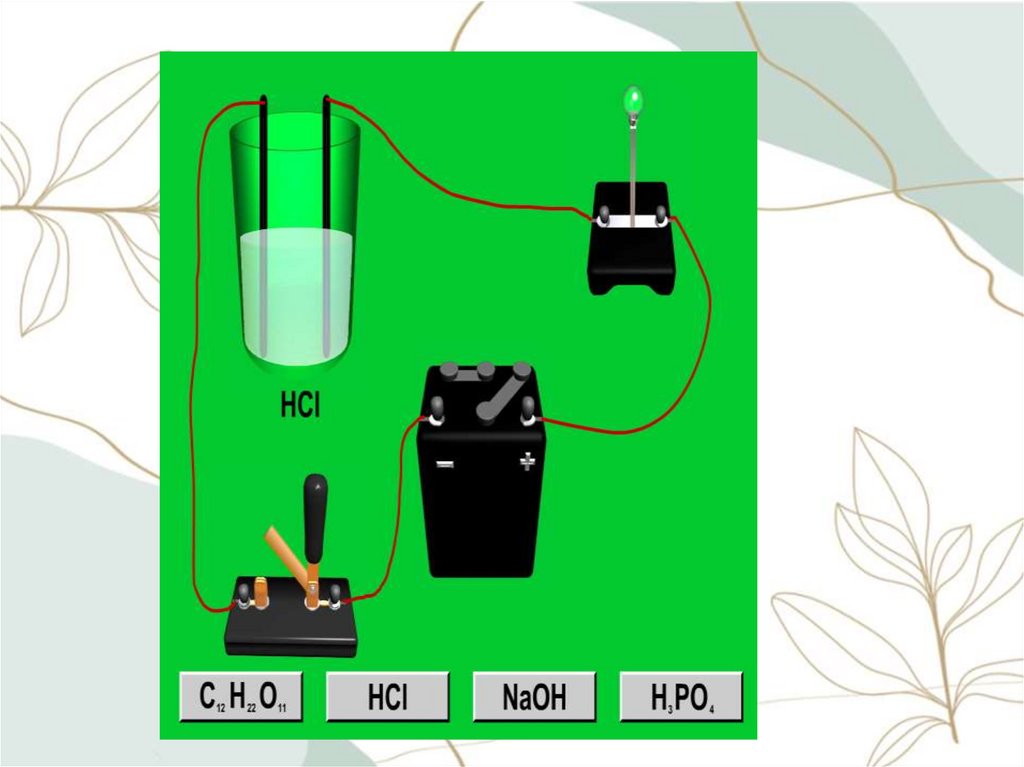
1. Электролитическая диссоциация
2.
3.
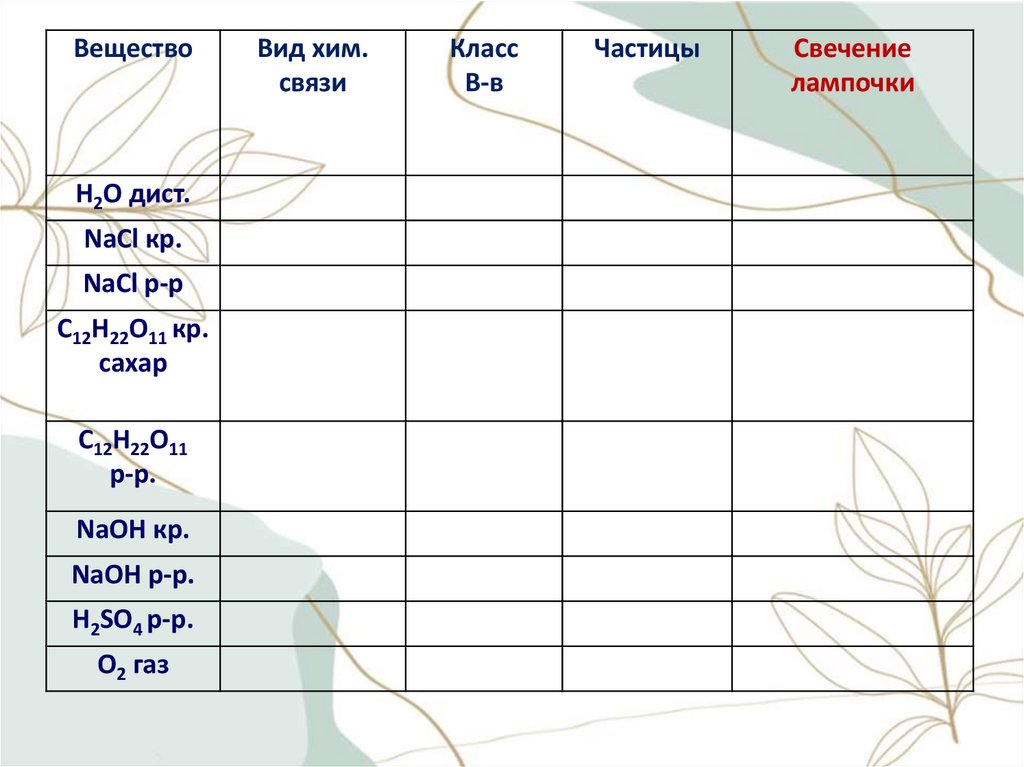
ВеществоН2О дист.
NaCl кр.
NaCl р-р
C12H22O11 кр.
сахар
C12H22O11
р-р.
NaOH кр.
NaOH р-р.
H2SO4 р-р.
O2 газ
Вид хим.
связи
Класс
В-в
Частицы
Свечение
лампочки
4.
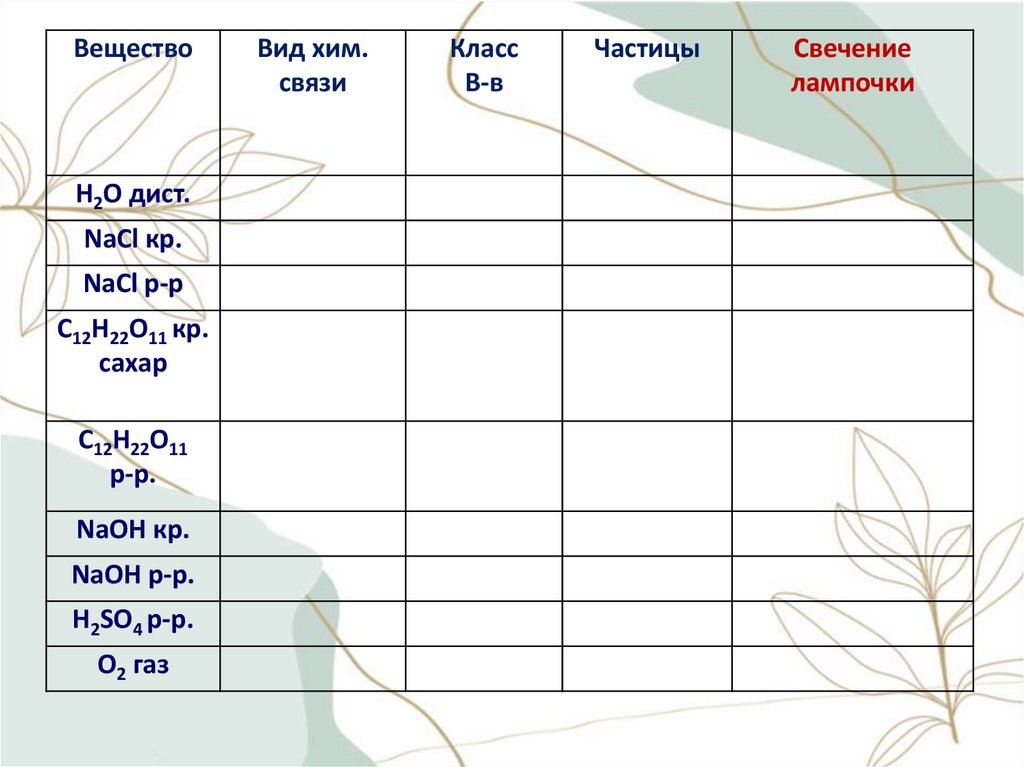
ВеществоН2О дист.
NaCl кр.
NaCl р-р
C12H22O11 кр.
сахар
C12H22O11
р-р.
NaOH кр.
NaOH р-р.
H2SO4 р-р.
O2 газ
Вид хим.
связи
Класс
В-в
Частицы
Свечение
лампочки
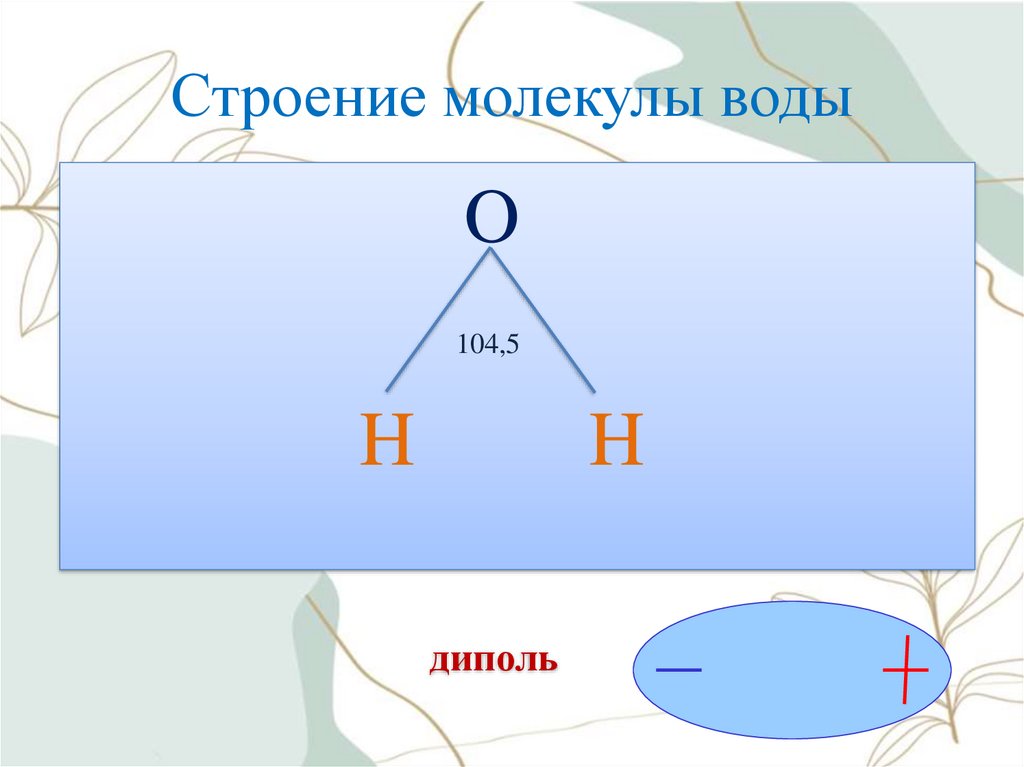
5. Строение молекулы воды
O104,5
H
H
диполь
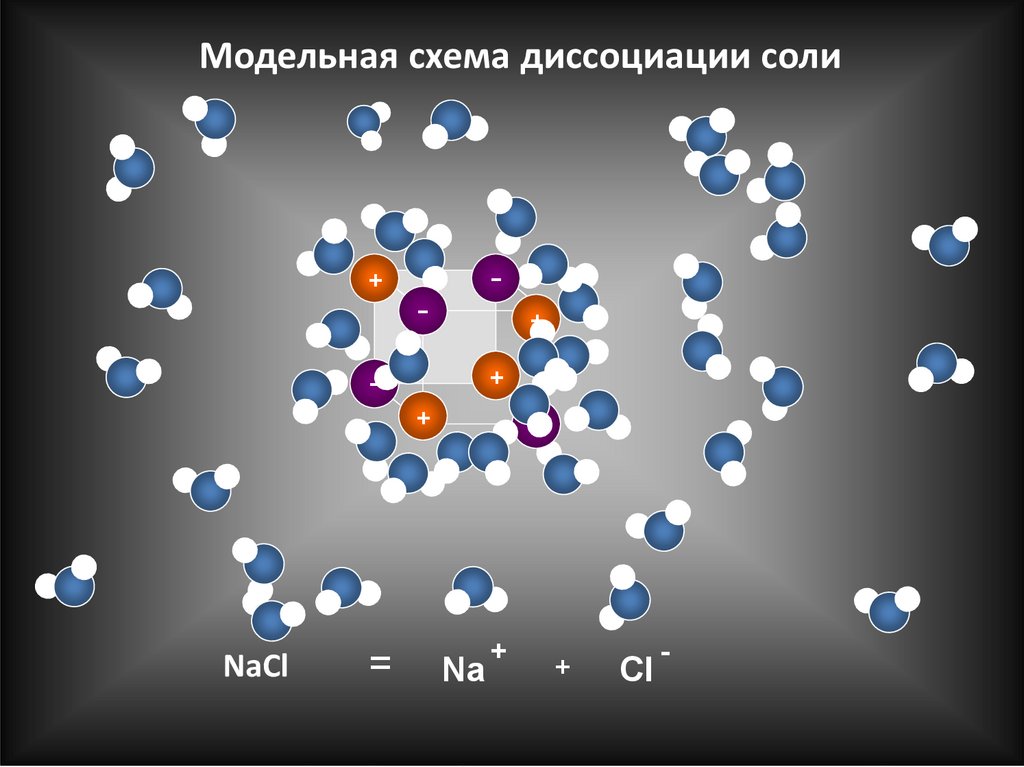
6. Модельная схема диссоциации соли
-+
-
+
+
+
NaCl
=
-
Na
+
+
Cl
-
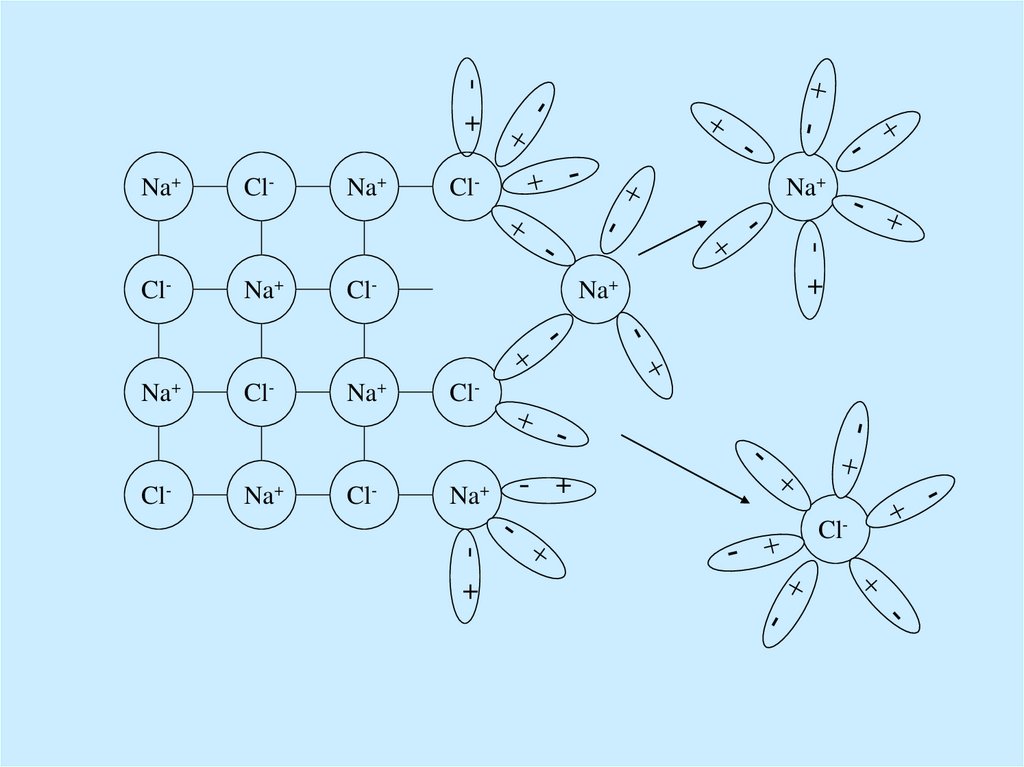
7.
+ Cl-Na+
Cl-
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
Cl-
Na+
Cl-
Na+
Na+
Na+
+ -
Na+
+ -
+ -
Cl-
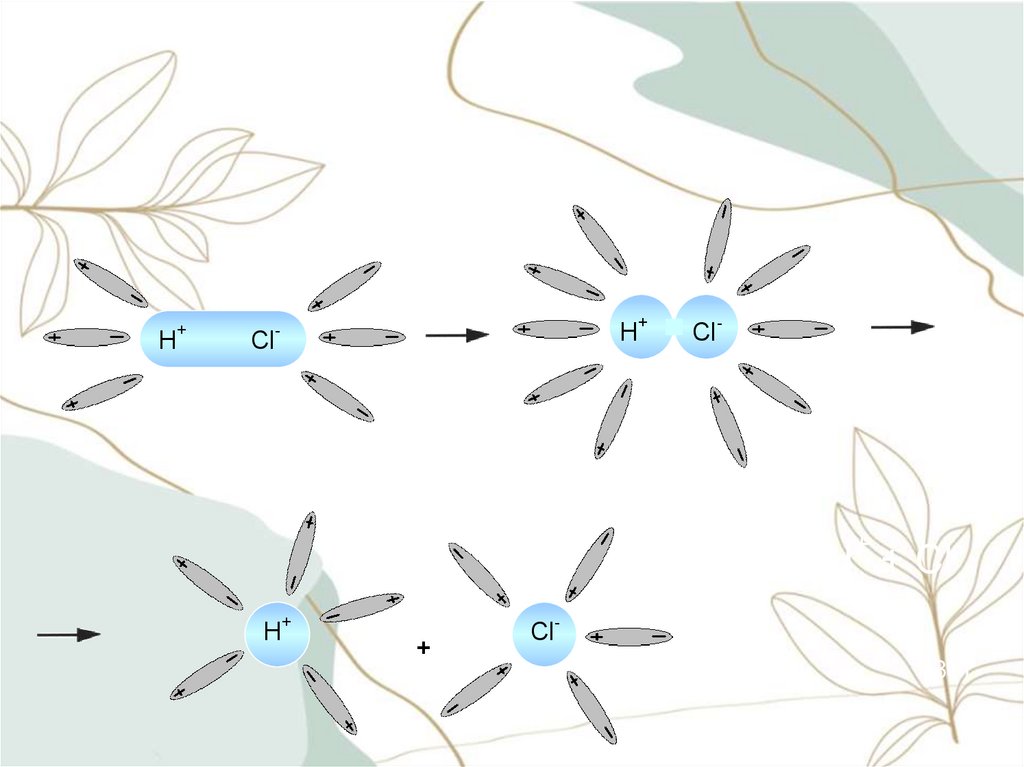
8.
+H
H+
-
Cl
Cl-
+
HCl H + Cl
H+
+
-
Cl(3б)
9. Последовательность процессов, происходящих при электролитической диссоциации:
Ориентация молекул – диполей воды околоионов;
Гидратация (взаимодействие) молекул
воды с противоположно заряженными
ионами поверхностного слоя кристалла;
Диссоциация (распад) кристалла
электролита на гидратированные ионы
10.
11.
12. Электролитическая диссоциация – процесс распада электролита на ионы при растворении его в воде или расплавлении.
13.
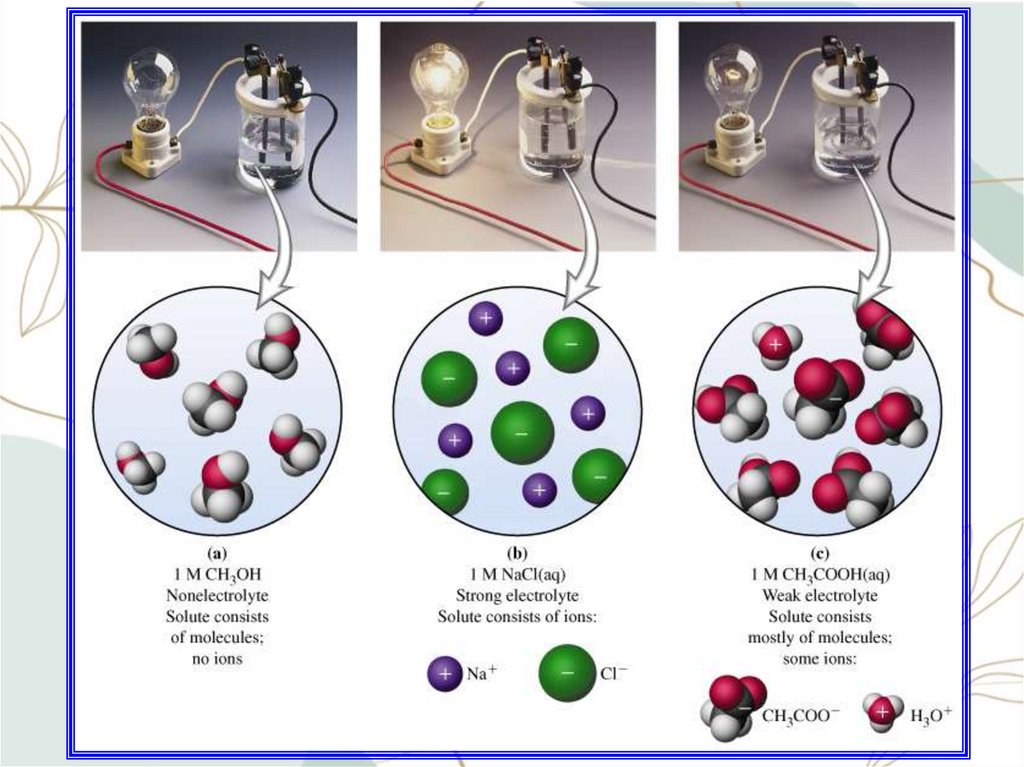
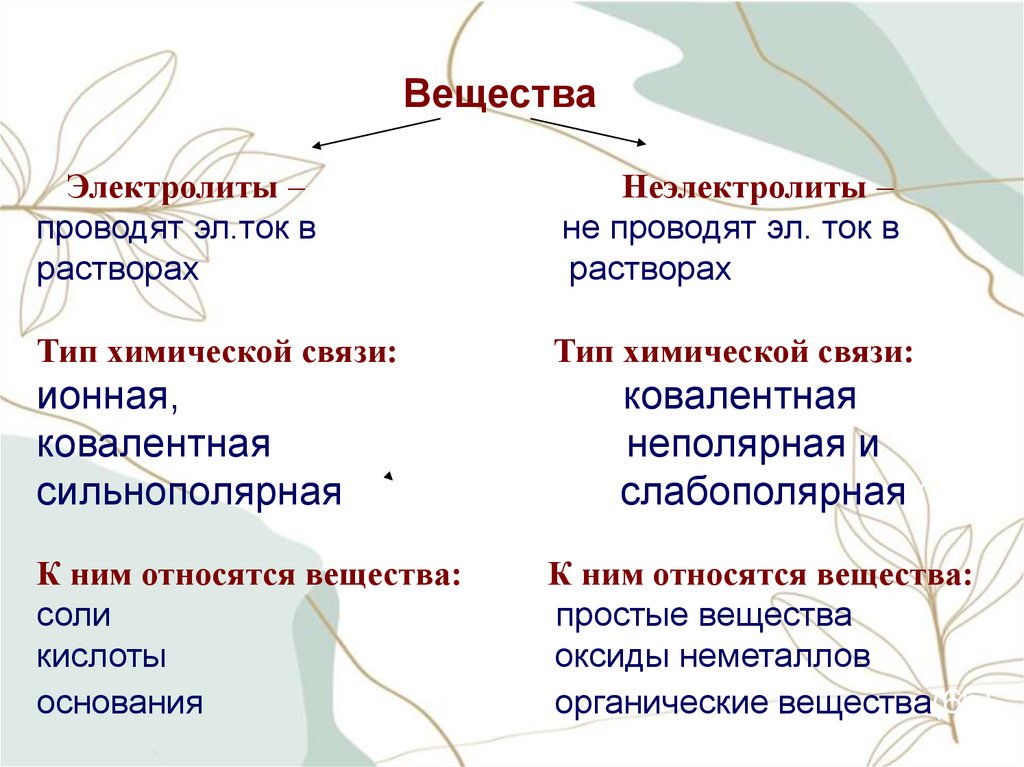
ВеществаЭлектролиты –
проводят эл.ток в
растворах
Неэлектролиты –
не проводят эл. ток в
растворах
(1б)
Тип химической связи:
Тип химической связи:
ионная,
ковалентная
сильнополярная
К ним относятся вещества:
соли
кислоты
основания
ковалентная
неполярная и
слабополярная (4б)
К ним относятся вещества:
простые вещества
оксиды неметаллов
органические вещества(6б)
14.
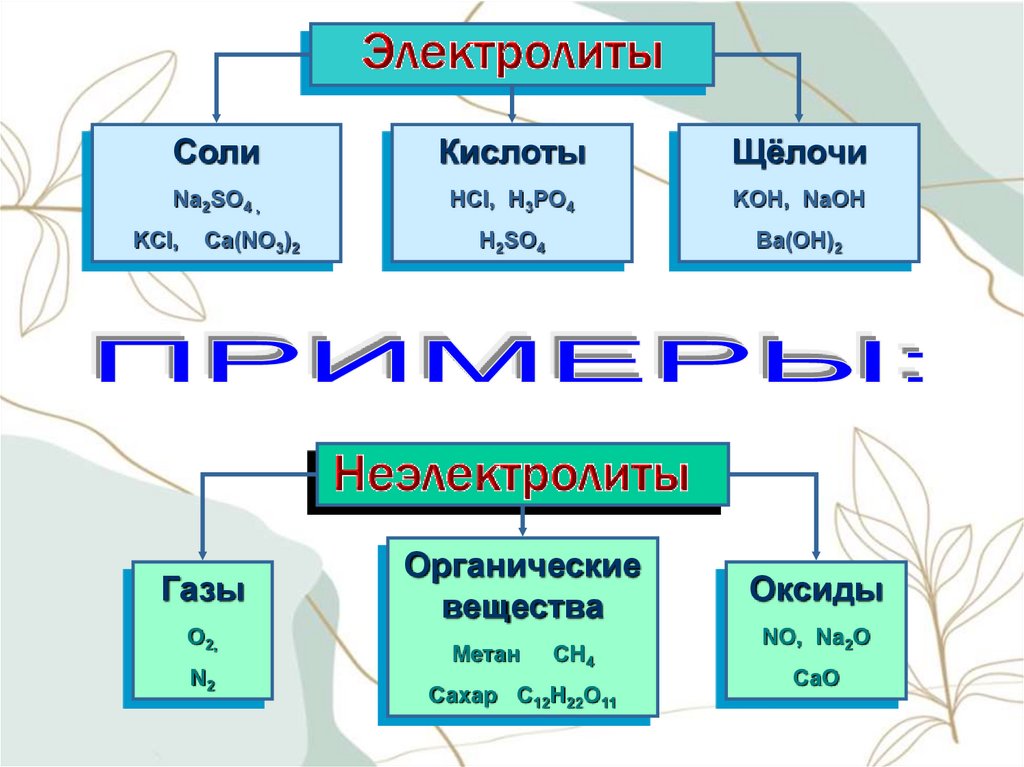
CолиКислоты
Щёлочи
Na2SO4 ,
HCl, H3PO4
KOH, NaOH
H2SO4
Ba(OH)2
KCl,
Ca(NO3)2
Газы
O2,
N2
Органические
вещества
Метан
CH4
Сахар C12H22O11
Оксиды
NO, Na2O
CaO
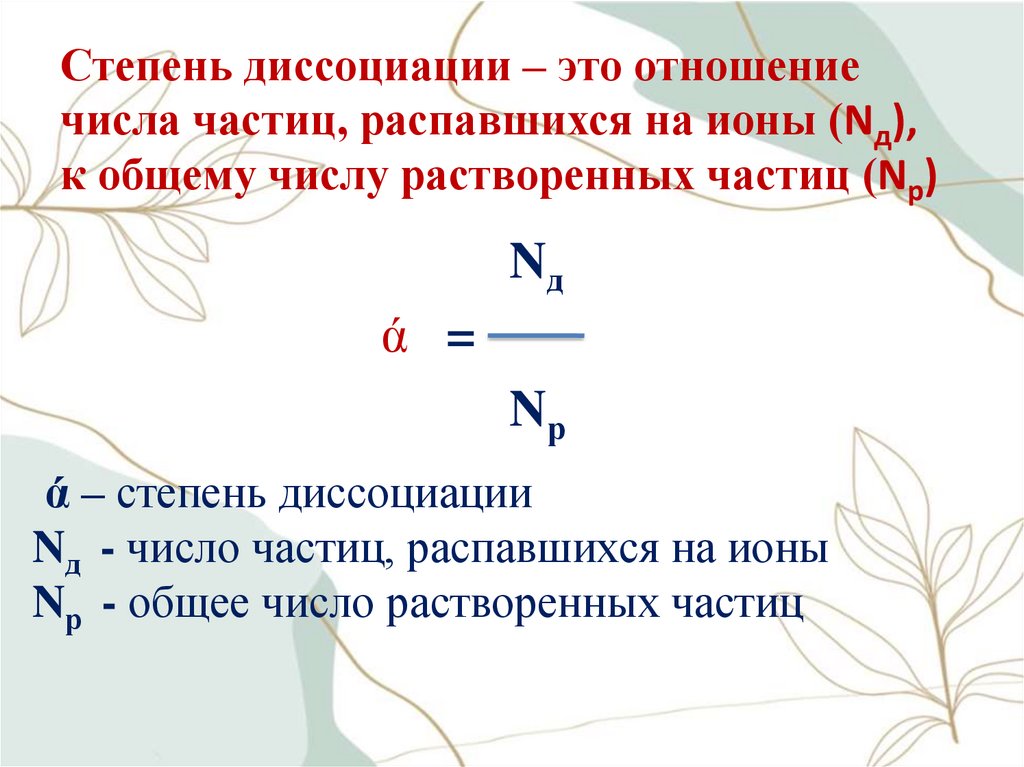
15. Степень диссоциации – это отношение числа частиц, распавшихся на ионы (Nд), к общему числу растворенных частиц (Nр)
Nдά =
Nр
ά – степень диссоциации
Nд - число частиц, распавшихся на ионы
Nр - общее число растворенных частиц
16.
Легче всего диссоциируют вещества сионной и ковалентной полярной связью:
Кислоты : HCl, H2SO4, HF, HNO3
Основания: NaOH, Ba(OH)2, KOH
Соли : NaCl, CuSO4, KNO3
17. Степень диссоциации выражают в долях или процентах.
При ά = 0 диссоциация отсутствуетПри ά = 1 или 100% электролит
полностью распадается на ионы
По степени электролитической
диссоциации электролиты делят
сильные
слабые
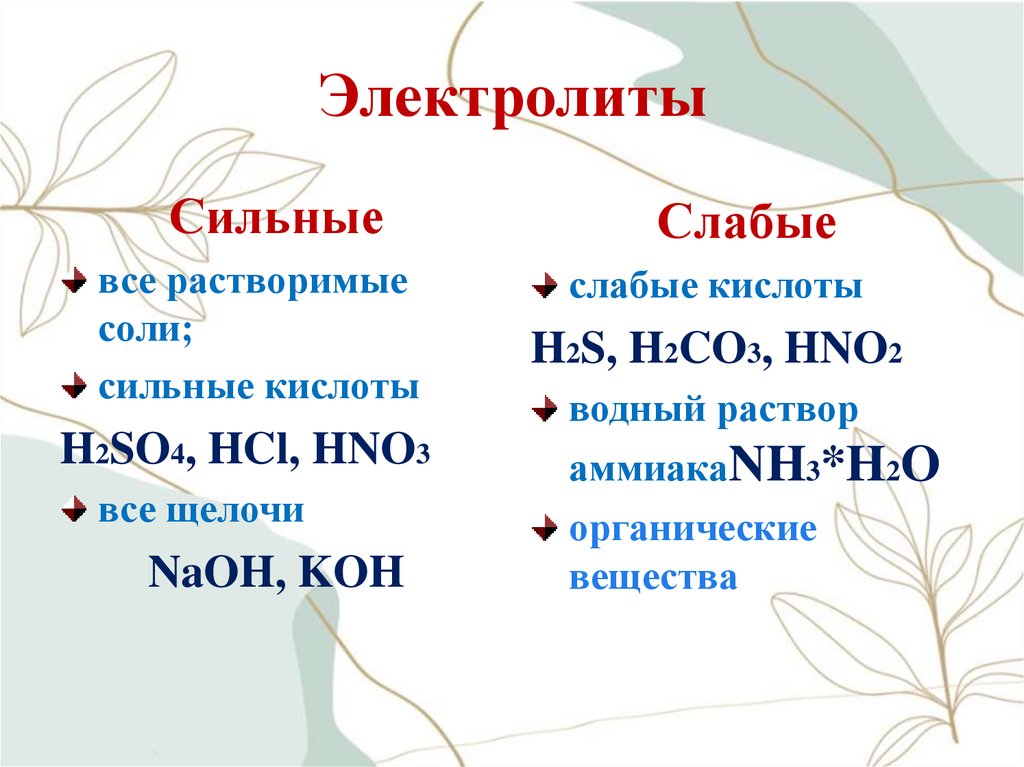
18. Электролиты
Сильныевсе растворимые
соли;
сильные кислоты
H2SO4, HCl, HNO3
все щелочи
NaOH, KOH
Слабые
слабые кислоты
H2S, H2CO3, HNO2
водный раствор
аммиакаNH3*H2O
органические
вещества
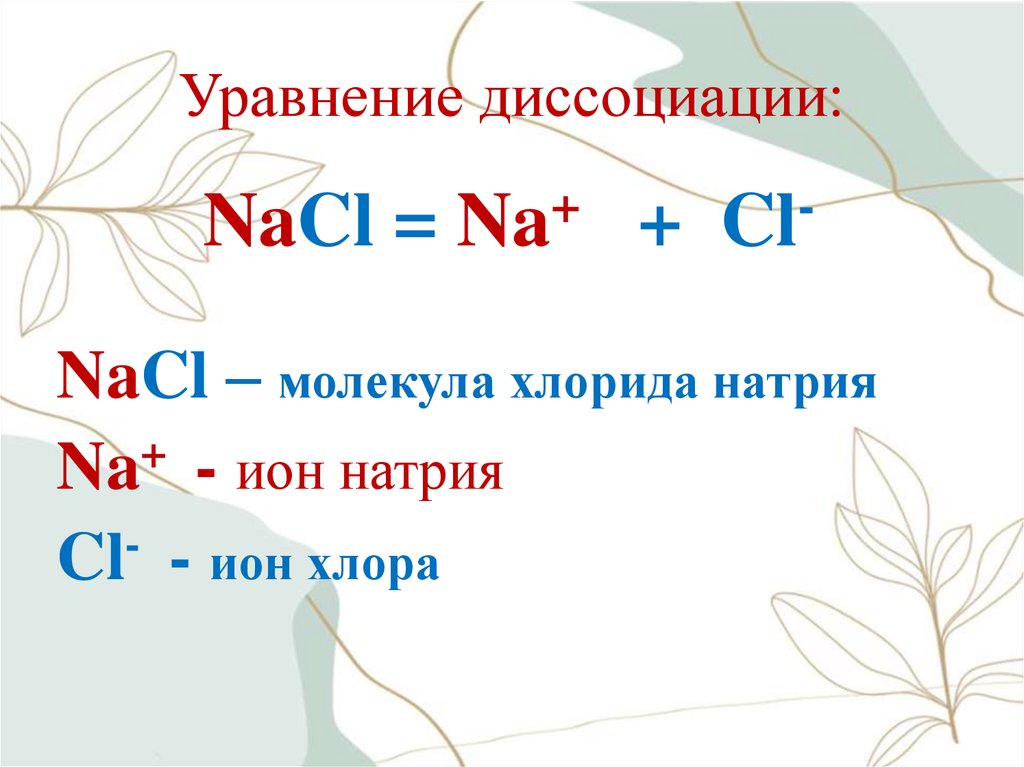
19. Уравнение диссоциации:
NaCl =+
Na
+
Cl
NaCl – молекула хлорида натрия
Na+ - ион натрия
Cl- - ион хлора
20. Почему растворы электролитов проводят электрический ток?
Сванте Аррениус(1859-1927)
Создал теорию
электролитической
диссоциации. За
исследования в
области
электролитов был
удостоен
Нобелевской
премии в 1903 г.
21. Причину диссоциации объяснили
• И.А. Каблуков,• В.А. Кистяковский ─ при
растворении электролита
происходит химическое
взаимодействие
растворенного вещества с
водой, которое приводит к
образованию гидратов, а
затем они диссоциируют на
ионы. В растворах находятся
не свободные, а
гидратированные ионы
(4б)
22.
Условия протекания реакции ионногообмена
• Образуется или растворяется
осадок;
• Выделяется газ;
• Образуется малодиссоциирующее
вещество (например Н2О)









 chemistry
chemistry








