Similar presentations:
Спирты (алкоголи)
1.
Спирты2.
Спирты (алкоголи)– производные углеводородов, в молекулах которых один
или несколько атомов замещены на соответствующее число
гидроксильных групп (–ОН)
Шаблоны презентаций с сайта presentation-creation.ru
3.
4.
I.Классификация спиртовПо типу углеводо─
родного радикала
Предельные
Непредельные
СН3 – СН – СН3
СН2 = СН – СН2 – ОН
Ароматические
|
OH
пропанол-2
(изопропиловый спирт)
пропен-2-ол-1
(аллиловый спирт)
Шаблоны презентаций с сайта presentation-creation.ru
СН2 – ОН
5.
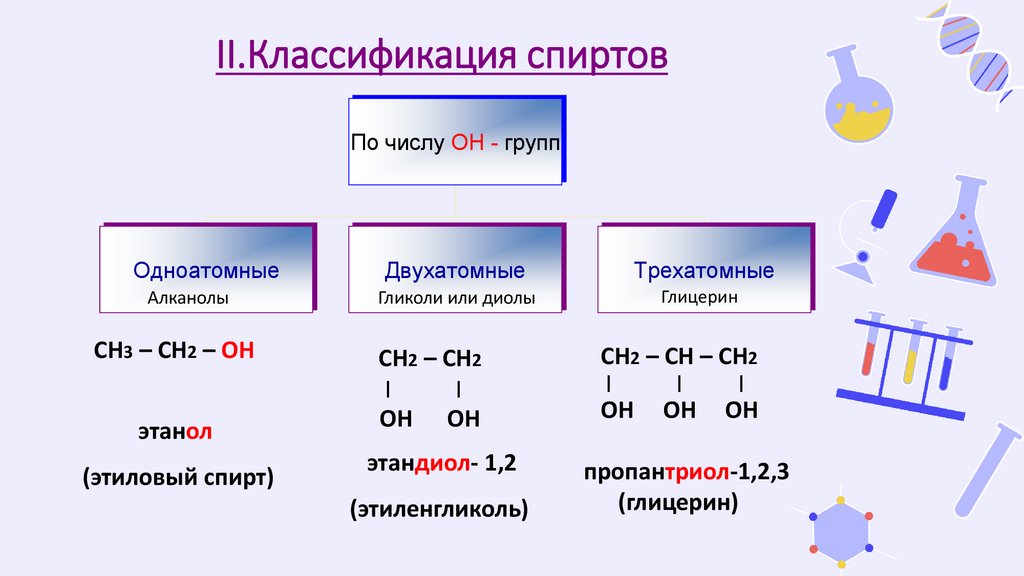
II.Классификация спиртовПо числу ОН - групп
Одноатомные
Алканолы
СН3 – СН2 – OH
этанол
(этиловый спирт)
Двухатомные
Трехатомные
Гликоли или диолы
Глицерин
СН2 – СН2
СН2 – СН – СН2
|
|
|
|
|
ОН
ОН
ОН
ОН
ОН
этандиол- 1,2
(этиленгликоль)
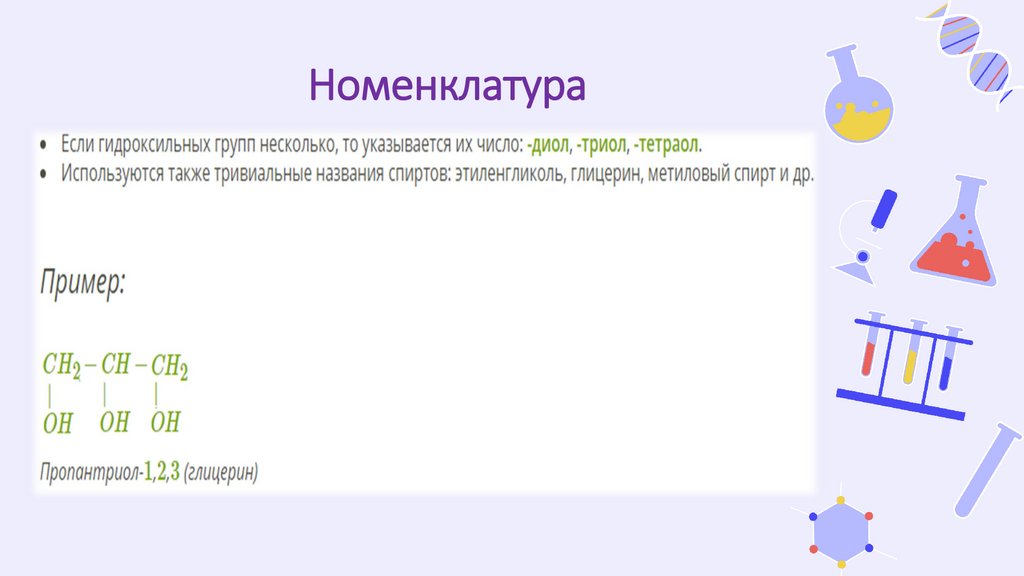
пропантриол-1,2,3
(глицерин)
6.
III.Классификация спиртовПо типу атома С,
связанного с гр. -ОН
Первичные
Вторичные
СН3–СН–СН2 –ОН
|
СН3
СН3–СН–СН2–СН3
2-метилпропанол-1
(изобутиловый спирт)
Третичные
СН3
|
|
ОН
СН3 – С – СН3
бутанол-2
(вторичный бутиловый
спирт)
|
ОН
2-метилпропанол-2
(третичный бутиловый
спирт)
7.
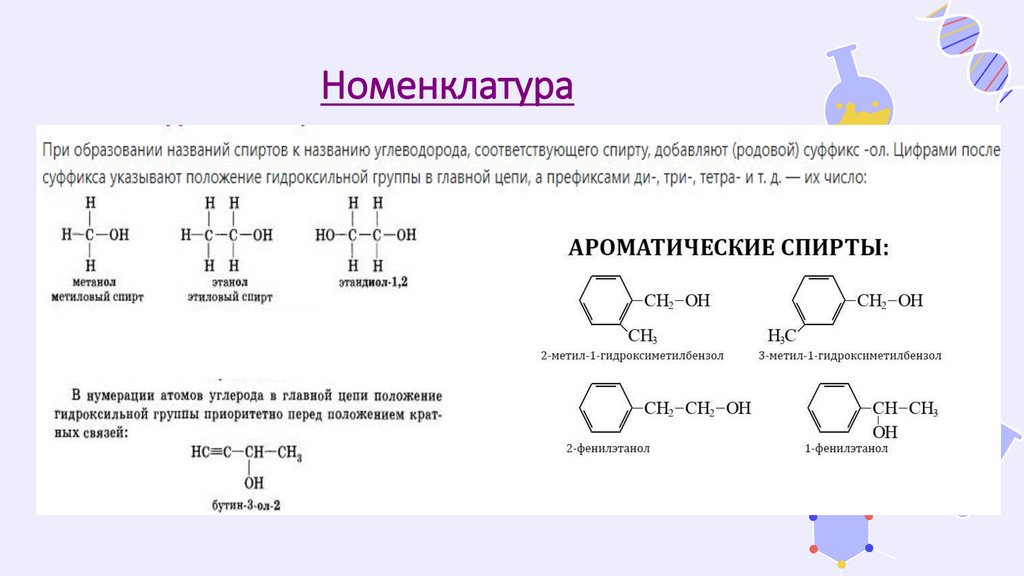
Номенклатура8.
Номенклатура9.
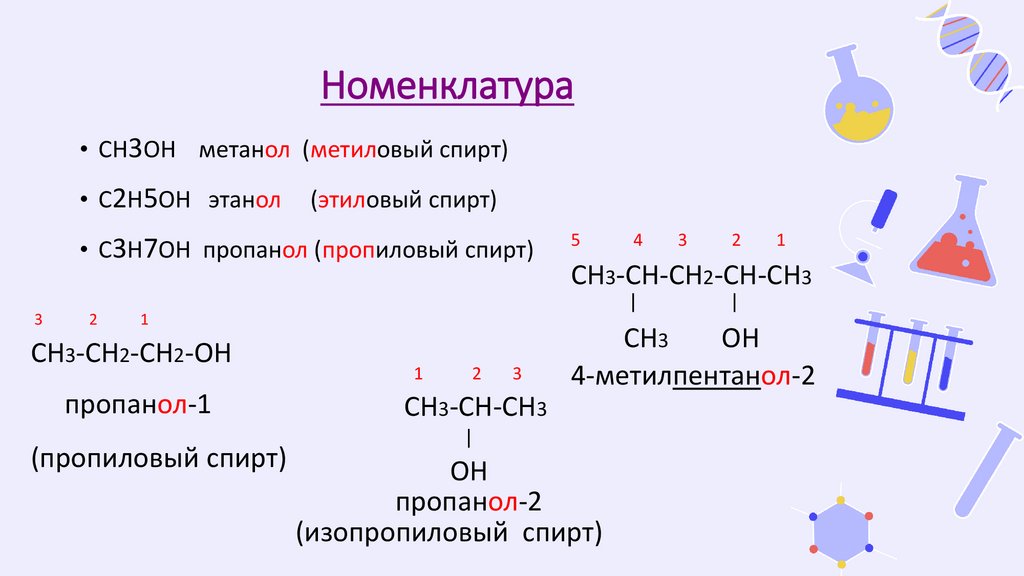
Номенклатура• СН3ОН метанол (метиловый спирт)
• С2Н5ОН этанол
(этиловый спирт)
• С3Н7ОН пропанол (пропиловый спирт)
3
2
пропанол-1
(пропиловый спирт)
4
1
2
3
3
2
1
СН3-СН-СН2-СН-СН3
|
1
СН3-СН2-СН2-ОН
5
|
CH3
ОН
4-метилпентанол-2
СН3-СН-СН3
|
ОН
пропанол-2
(изопропиловый спирт)
10.
Номенклатура11.
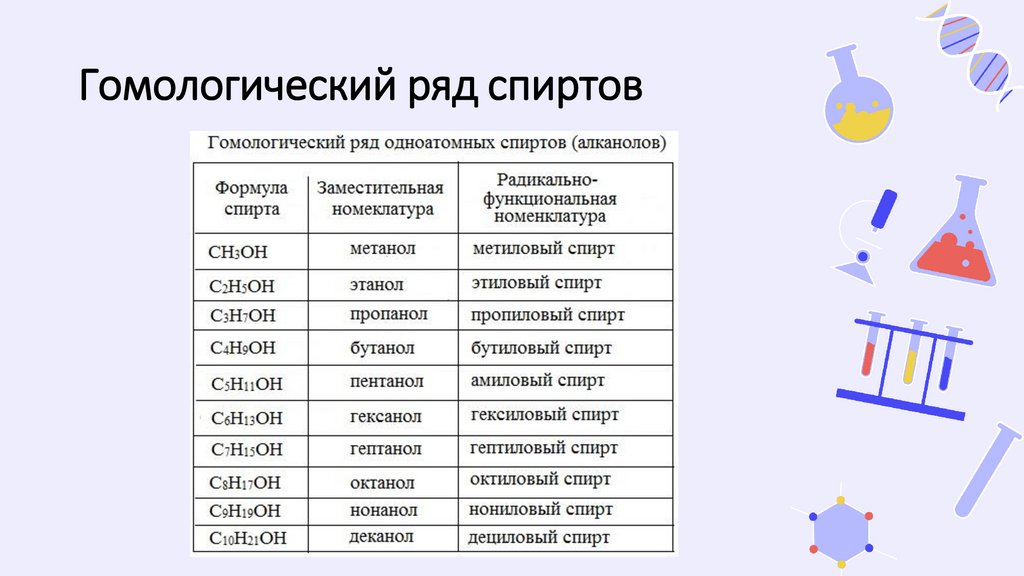
Гомологический ряд спиртов12.
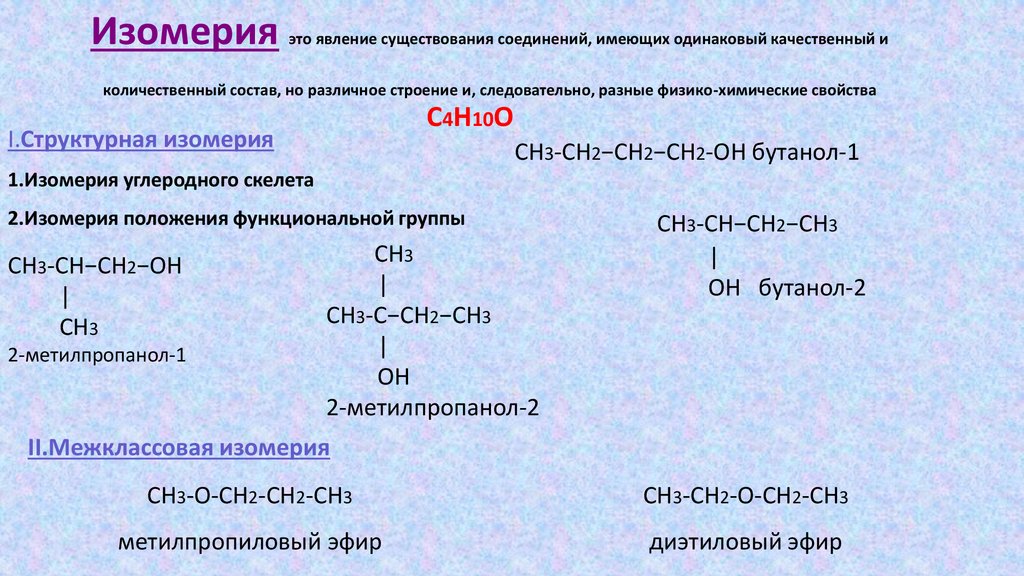
Изомерияэто явление существования соединений, имеющих одинаковый качественный и
количественный состав, но различное строение и, следовательно, разные физико-химические свойства
С4Н10О
I.Структурная изомерия
СН3-СН2−СН2−СН2-ОН бутанол-1
1.Изомерия углеродного скелета
2.Изомерия положения функциональной группы
СН3-СН−СН2−ОН
|
СН3
2-метилпропанол-1
CH3
|
СН3-С−СН2−СН3
|
OH
2-метилпропанол-2
СН3-СН−СН2−СН3
|
OH бутанол-2
II.Межклассовая изомерия
СН3-О-СН2-СН2-СН3
СН3-СН2-О-СН2-СН3
метилпропиловый эфир
диэтиловый эфир
13.
Получение13
14.
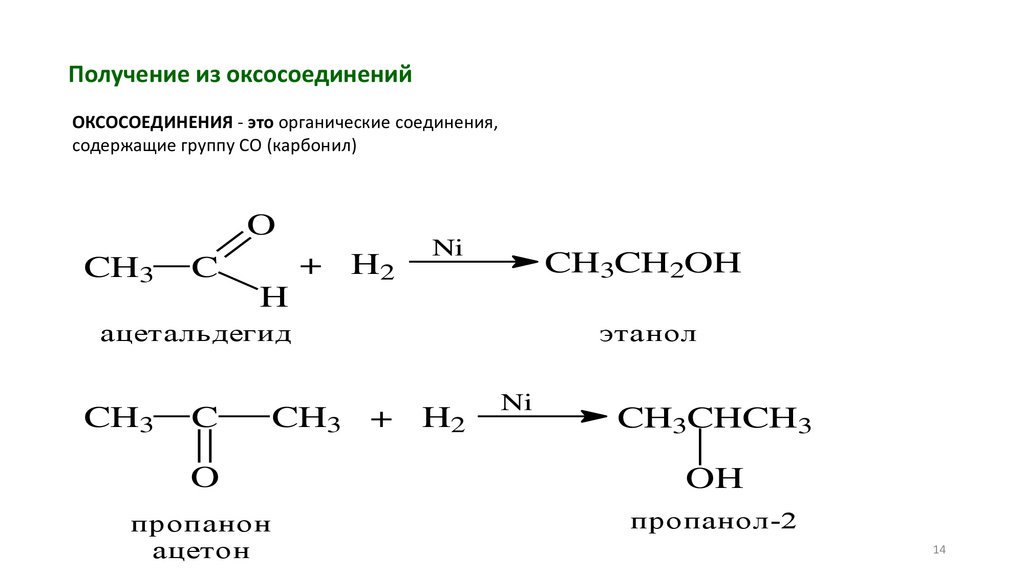
Получение из оксосоединенийОКСОСОЕДИНЕНИЯ - это органические соединения,
содержащие группу СО (карбонил)
O
CH3
+ H2
C
Ni
CH3CH2OH
H
ацетальдегид
CH3
C
CH3 + H2
этанол
Ni
CH3CHCH3
O
OH
пропанон
ацетон
пропанол-2
14
15.
Физические свойстваАгрегатное состояние
01
предельные одноатомные спирты от С1 до С12 – жидкости
высшие спирты – мазеобразные вещества
от С21 и выше – твердые вещества
02
Плотность
Легче воды
Температура кипения
03
• t кип. спиртов увеличивается с увеличением молекулярной массы
Растворимость в воде
04
С увеличением молекулярной массы снижается.
Метиловый, этиловый и пропиловый спирты хорошо растворимы.
05
Горючесть
Шаблоны презентаций с сайта presentation-creation.ru
16.
Химические свойства (одноатомных спиртов)Взаимодействие со щелочными металлами:
2С2Н5ОН + 2Na → 2C2H5ONa + H2.
Взаимодействие со щелочами:
С2H5OH + NaOH ⇄ C2H5ONa + H2O
Дегидратация спиртов (реакция с отщеплением молекул воды):
При температуре 140°C и в присутствии серной кислоты происходит внутримолекулярная
дегидратация. В результате реакции получается алкен.
При температуре < 140°C и в присутствии серной кислоты происходит межмолекулярная
дегидратация. В результате образуется простой эфир.
17.
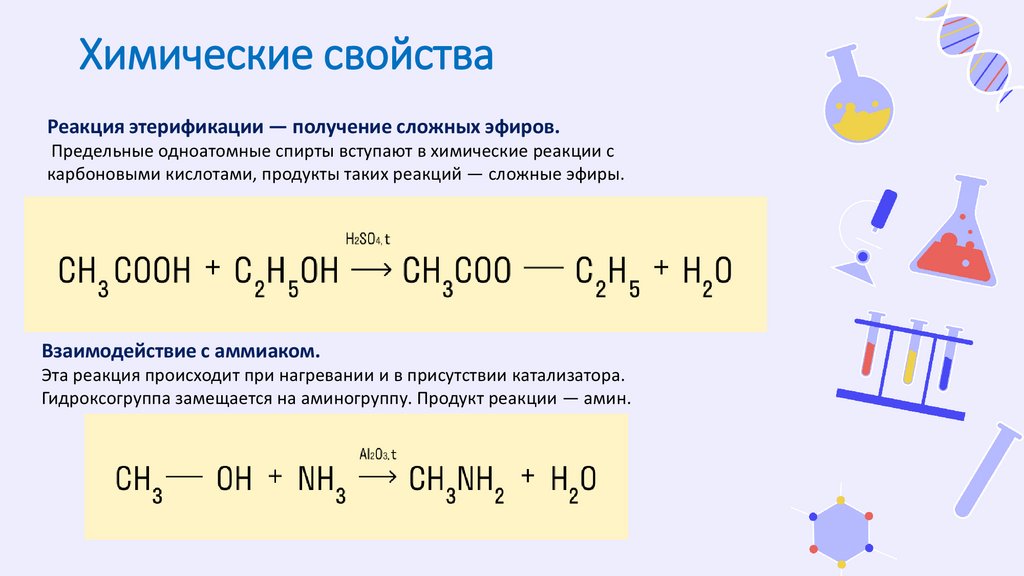
Химические свойстваРеакция этерификации — получение сложных эфиров.
Предельные одноатомные спирты вступают в химические реакции с
карбоновыми кислотами, продукты таких реакций — сложные эфиры.
Взаимодействие с аммиаком.
Эта реакция происходит при нагревании и в присутствии катализатора.
Гидроксогруппа замещается на аминогруппу. Продукт реакции — амин.
18.
Химические свойстваОкисление:
1.Горение спиртов:
C2H5OH + 3O2 → 2CO2 + 3H2O
2Жидкофазное окисление с применением хромовой смеси
K2Cr2O7 + H2SO4:
3C2H5OH + K2Cr2O7 + 4H2SO4 → 3CH3COOH + K2SO4 +
Cr2(SO4)3 + H2O
3.Окисление оксидом меди (II) при нагревании:
CH3—CH2—OH + CuO → CH3—CHO + Cu + H2O
19.
Химические свойства (многоатомныхспиртов)
Многоатомные спирты сходны с одноатомными, но имеют
особенности: проявляют более сильные кислотные свойства
и вступают в специфические реакции.
1. Многоатомные спирты взаимодействуют с щелочными
металлами
2. Взаимодействие со свежеосажденным гидроксидом меди
(II)Это качественная реакция на многоатомные спирты
3. Окисление йодной кислотой и ее солями
4. Образование эфиров с азотной кислотой
20.
Нахождение в природе• Метиловый спирт в небольшом
количестве содержится в некоторых
растениях, например: борщевике
• Этиловый спирт — естественный
продукт спиртового брожения
органических продуктов,
содержащих углеводы, часто
образующийся в прокисших ягодах
и фруктах без всякого участия
человека.
• Кроме того, этанол является
естественным метаболитом и
содержится в тканях и крови
животных и человека.
21.
Применение22.
Вред алкоголя!!!23.
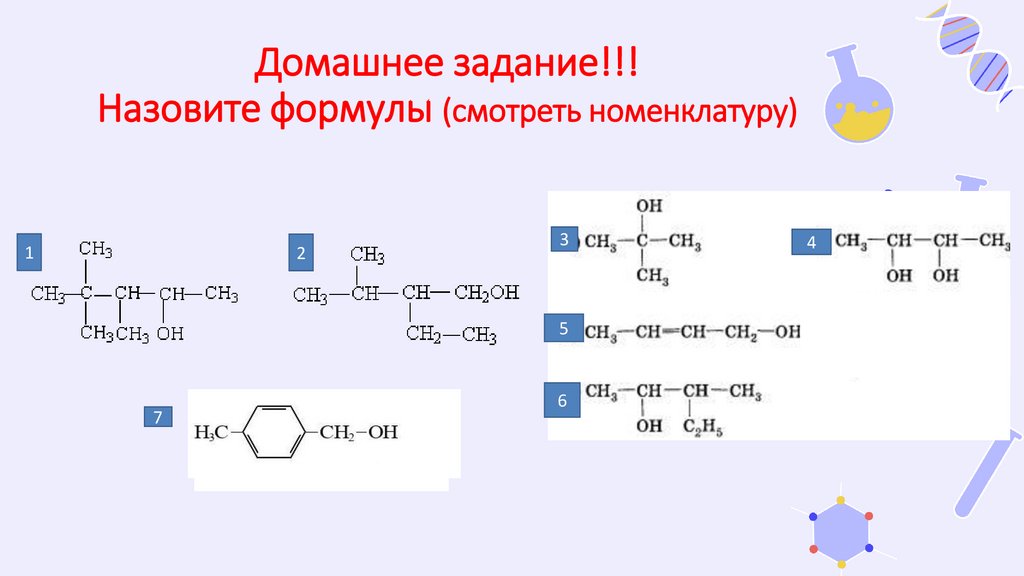
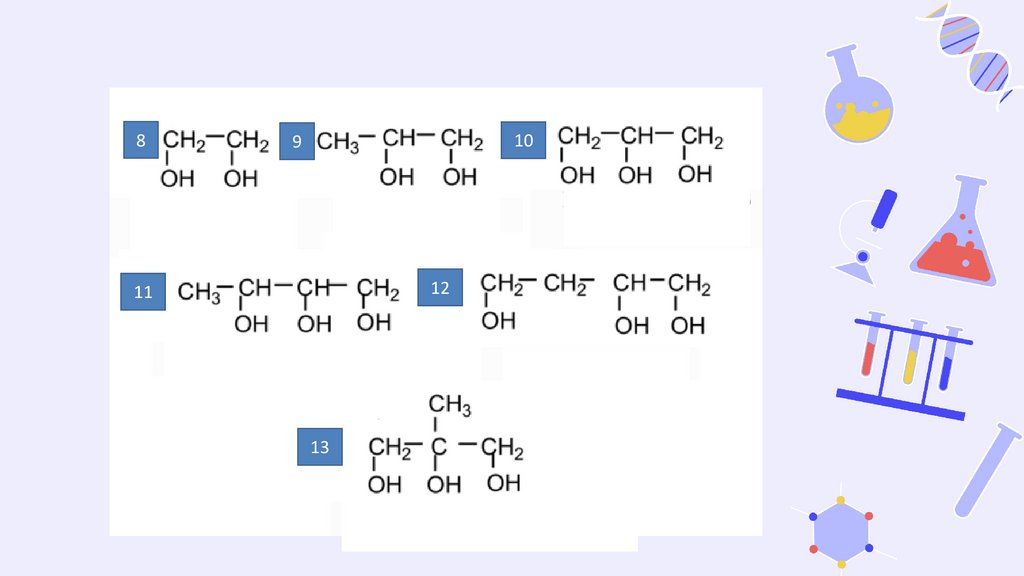
Домашнее задание!!!Назовите формулы (смотреть номенклатуру)
1
2
7
3
4
5
13
6
24.
810
9
12
11
13













 chemistry
chemistry








