Similar presentations:
Растворы. Виды
1.
РастворыПреподаватель Юридического колледжа
Валентина Владимировна Киреева
2.
РЕМОНТРастворы - это гомогенные системы,
состоящие из растворителя,
растворимого вещества и продуктов их
взаимодействия
Жидкие: водные и
неводные
Газообразные
Твердые
3.
РЕМОНТРастворитель - это компонент,
- агрегатное состояние которого
не изменяется при растворении,
- взятый в большем объеме, если
вещества находятся в
одном агрегатном состоянии
Состав стекла:
75% оксид кремния
(SiO2)
25% примеси (оксиды
натрия, железа,
алюминия, красители и
т.д.)
4.
РЕМОНТРастворимость
- способность данного вещества
растворяться в данном растворителе
при данных условиях.
Растворимость зависит от
природы растворителя и растворенного
вещества.
5.
РЕМОНТуменьшится в 4 раза
увеличится в 2 раза
6.
РЕМОНТРастворимость
газов
в
жидкостях
увеличивается с повышением давления и
понижением температуры.
Закон У. Генри: растворимость газа
при постоянной температуре прямо
пропорциональна
его давлению над
жидкостью.
7.
РЕМОНТРастворимость жидкостей
увеличивается с повышением
температуры.
Неограниченное растворение:
вода + спирт;
Ограниченное растворение:
вода + диэтиловый эфир.
Практическая
нерастворимость: вода + масло.
8.
РЕМОНТРастворимость твердых веществ в
жидкостях зависит от типа связи в их
кристаллических решетках. Например,
вещества с атомными решетками практически
не растворимы в воде. Вещества с ионной
решеткой, как правило, хорошо растворимы в
воде. Растворимость твердых
веществ также зависит от
степени их измельчения и
в большинстве случает от
температуры
9.
РЕМОНТПо растворимости в воде твердые
вещества делят на 3 группы:
1. Р - хорошо растворимые в воде (>10 г вещества
в 100 г воды).
2. М - малорастворимые в воде (от 0, 01 до 10 г
вещества в 100 г воды).
3. Н - практически нерастворимые в воде (< 0, 01 г
в 100 г воды)
10.
РЕМОНТТеории растворения
В. Оствальд и С. Аррениус
Физическая теория: растворы смеси,
образовавшиеся
в
результате
дробления
растворимого вещества в среде
растворителя без химического
воздействия между ними.
11.
РЕМОНТД.И. Менделеев
Химическая теория:
Растворение -химическое
взаимодействие частиц
растворяемого вещества и
молекул растворителя с
образованием молекулярных
комплексов - сольватов.
12.
РЕМОНТИ.А. Каблуков и В.А. Кистяковский
объединили
представления
Оствальда,
Аррениуса и Менделеева, заложив основу
современной теории растворов.
Растворение – физико-химический процесс, в
котором
наряду
с
образованием
механической смеси веществ идет процесс
взаимодействия
частиц
растворенного
вещества с растворителем с образованием
молекулярных комплексов - сольватов.
13.
РЕМОНТЭтапы растворения:
1. Разрушение кристаллической решетки.
2. Сольватация – процесс взаимодействия
молекул растворителя и растворяемого
вещества (в водных растворах - гидратация).
3. Диффузия – самопроизвольное выравнивание
концентрации.
14.
РЕМОНТТепловые эффекты при растворении
На разрушение структуры растворяемого вещества
затрачивается
энергия,
а
взаимодействие
частиц
растворенного вещества с частицами растворителя
(сольватация) идет с выделением теплоты.
Таким образом, процесс растворения может быть
экзотермическим или эндотермическим, в зависимости от
соотношения этих тепловых эффектов.
Например, при растворении серной кислоты
наблюдается сильное разогревание раствора, а при
растворении нитрата калия – сильное охлаждение раствора
(эндотермический процесс).
15.
РЕМОНТКонцентрация раствора –
это содержание вещества в определенной массе или объеме
раствора.
Типы растворов
1.Насыщенный – вещество при данной температуре больше не
растворяется.
2. Ненасыщенный – вещество еще растворяется.
3. Пересыщенный - уже нельзя растворить данное вещество (его
избыток выпадает в осадок).
Понятия разбавленный и концентрированный растворы
определяют соотношение между количествами растворенного
вещества и растворителя.
Разбавленные растворы – это растворы, содержащие небольшие
количества растворенного вещества по сравнению с
количеством растворителя.
Концентрированные – с большим содержанием растворенного
вещества.
16.
РЕМОНТСпособы
выражения концентрации
растворов
Существуют различные способы численного
выражения состава растворов: массовая
доля растворенного вещества, молярность,
титр и др.
17.
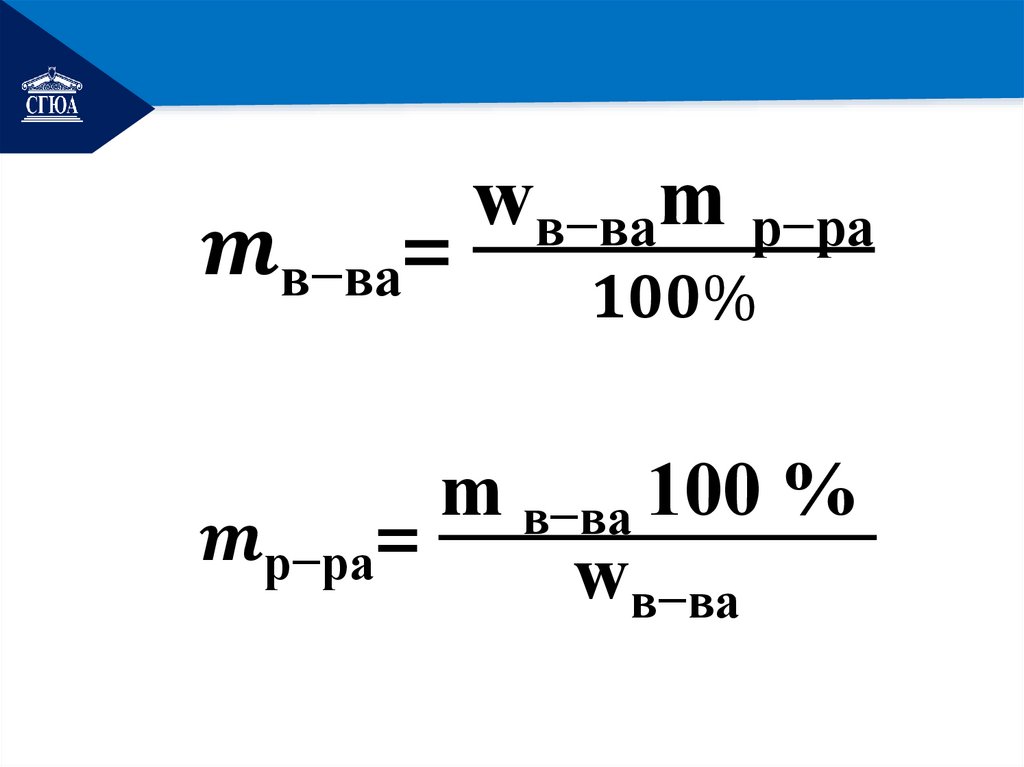
РЕМОНТ1. Массовая доля растворенного вещества
в растворе – отношение массы вещества
к массе раствора ( доли единицы/
проценты).































 chemistry
chemistry








