Similar presentations:
Щелочные металлы
1. Щелочные металлы
Душак О.М. Железногорск2.
Душак О.М. Железногорск3. 1) строение атома
Щелочные металлы напоследнем энергетическом
уровне имеют по одному
электрону, который легко
отдают, приобретая при
этом положительную
степень окисления.
Являются только
восстановителями. С
увеличением заряда ядра
атома у них увеличиваются
металлические свойства,
увеличивается радиус атома.
Душак О.М. Железногорск
4. Работа с ПСХЭ :
проанализировать какменяются восстановительные
свойства металлов в группе
сверху - вниз, в периоде слева направо.
Душак О.М. Железногорск
5. Вопрос №1:
На схеме изображенаэлектронная
конфигурация атома:
а) лития;
б) натрия;
в) хлора;
г) калия.
Душак О.М. Железногорск
6. Вопрос №2
Способность отдавать электроныусиливается в ряду:
• а) натрий – магний – алюминий;
• б) литий – натрий – калий;
• а) барий – кальций – магний;
• г) калий – натрий – литий.
Душак О.М. Железногорск
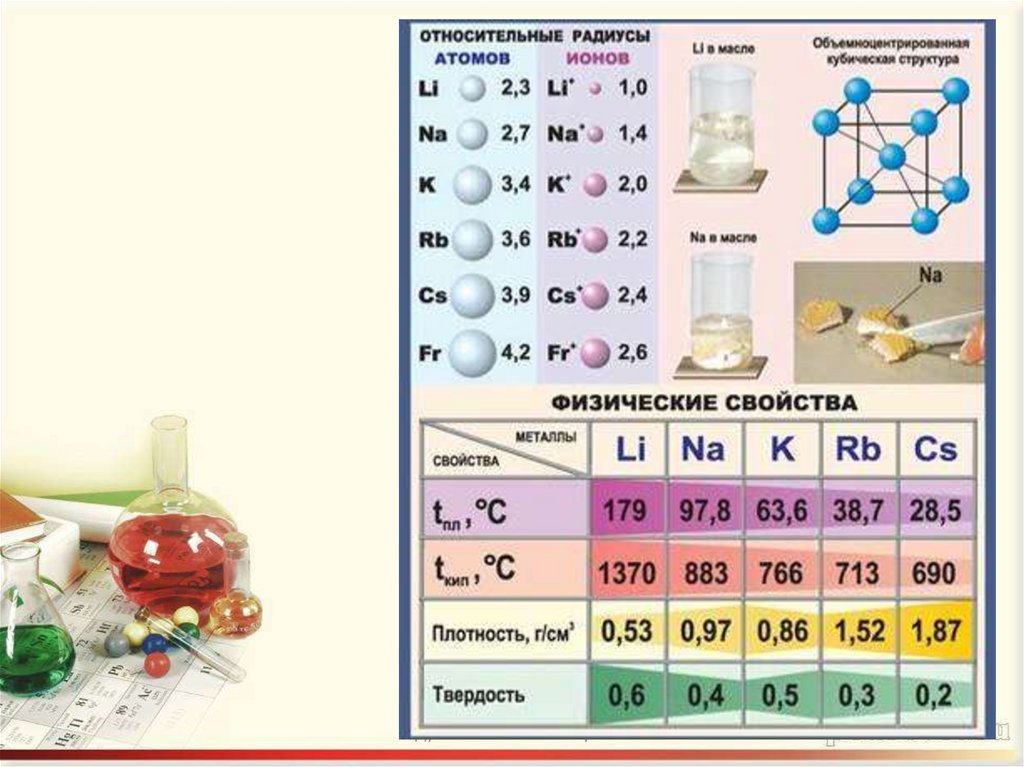
7. 2) физические свойства
• Металлы серебристо-белогоцвета, режутся ножом, легкие и
мягкие, легкоплавкие,
плотность возрастает, а
температура плавления
уменьшается от Li к Cs.
• При горении металлы
окрашивают пламя в
характерные цвета. Fr –
радиоактивный металл, его
свойства изучены
недостаточно, поэтому его не
включают в характеристику.
Душак О.М. Железногорск
8.
Душак О.М. Железногорск9. 3) химические свойства и техника безопасности при работе с активными металлами
• Из-за высокой химической активностищелочных металлов по отношению к воде,
кислороду, азоту их хранят под слоем
керосина. Чтобы провести реакцию со
щелочным металлом, кусочек нужного
размера аккуратно отрезают скальпелем
под слоем керосина, в атмосфере аргона
тщательно очищают поверхность металла
от продуктов его взаимодействия с
воздухом и только потом помещают
образец в реакционный сосуд.
Душак О.М. Железногорск
10. 3) химические свойства и техника безопасности при работе с активными металлами
• Щелочные металлывзаимодействуют с простыми
веществами: при
взаимодействии с O2 только Li
дает оксид, другие металлы –
пероксиды. Щелочные металлы
взаимодействуют со сложными
веществами: при растворении в
воде выделяется газ- водород.
Душак О.М. Железногорск
11. Например, химические свойства лития:
4Li+O2=2 Li 2O
2Na+ O2 = Na2 O2
2Li+ H2 = 2 Li H
2Li + Cl2 = 2Li Cl
2Li + S = Li 2S
6Li + N2= 2 Li3 N
2Li + 2H2 O = 2LiOH + H2↑
Душак О.М. Железногорск
12. 4. Качественное определение щелочных металлов.
• Поскольку потенциалы ионизации щелочныхметаллов невелики, то при нагревании
металла или его соединений в пламени атом
ионизируется, окрашивая пламя в
определённый цвет:
• Окраска пламени щелочными металлами
Li
Na
K
Rb
Cs
Карминно-красный
Жёлтый
Фиолетовый
Беловато-розовый
Фиолетово-красный
Душак О.М. Железногорск
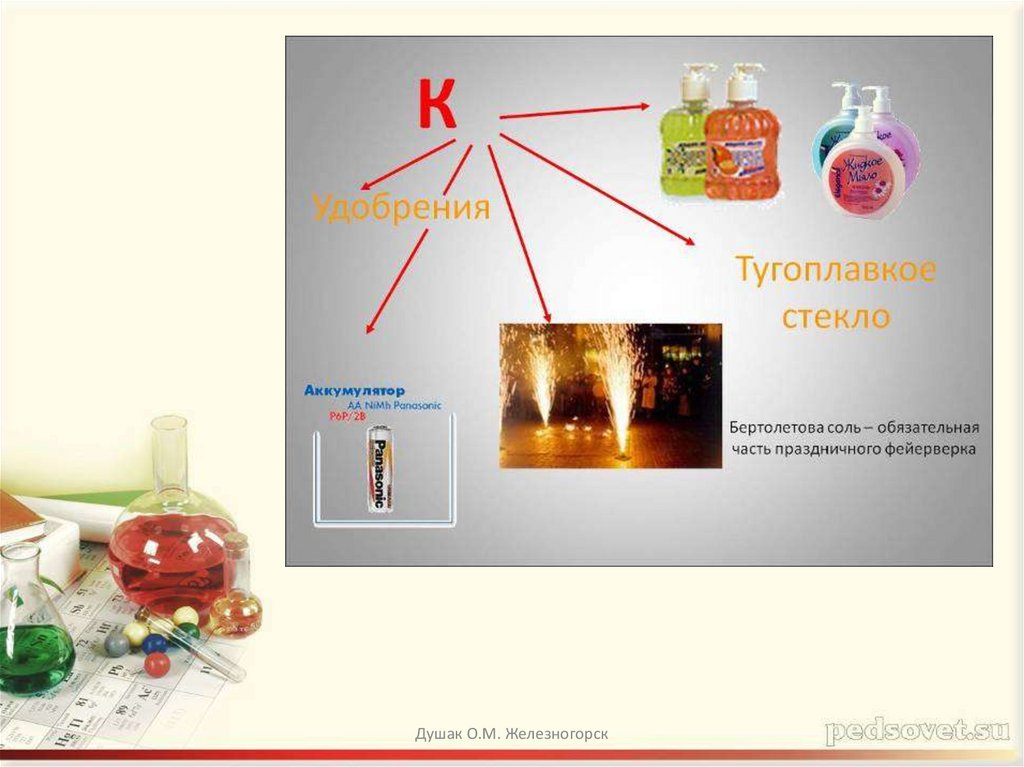
13. 5) применение
• Li используется для получения трития(ракетное топливо), как добавка к
сталям (придает твердость);
• Na и K используются в атомных
реакторах, в органических синтезах;
• Cs и Rb – получение фотоэлементов,
преобразование солнечного света в
электрическую энергию.
Душак О.М. Железногорск













 chemistry
chemistry








