Similar presentations:
Взаимосвязь между тишами связей, видами кристаллических решеток и свойствами веществ
1.
2.
Цели урока:- Объяснять зависимость
свойств веществ от типа
решетки
3.
Актуализация знаний1.Что такое электроотрицательность?
2.Назовите основные виды химической
связи?
3.Что представляет собой ковалентная
связь?
4.Назовите виды ковалентной связи?
5. Какая разница в образовании связи
между атомами в молекулах Н2 и Н2O?
6. Что представляет собой ионная связь?
7. Что такое ионы? Какие виды бывают?
4.
Прием «Чистая доска»Какой тип связи существует между
атомами в каждом отдельном соединении,
обоснуйте свой ответ
NaI, HCL, O2, CaF2, N2
5.
Состояниевещества
Твердое
Жидкое
Газообразное
6.
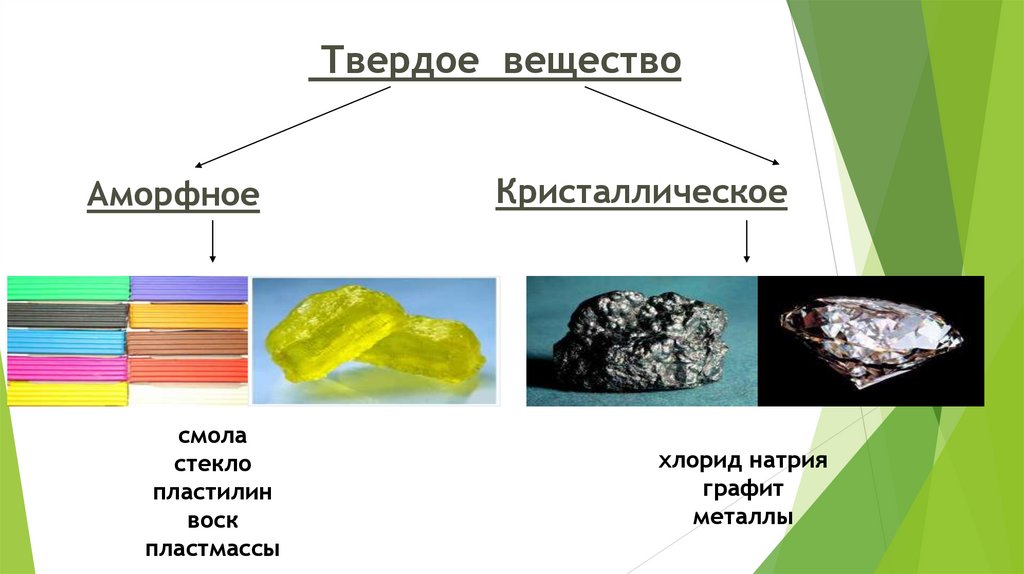
Твердое веществоАморфное
смола
стекло
пластилин
воск
пластмассы
Кристаллическое
хлорид натрия
графит
металлы
7.
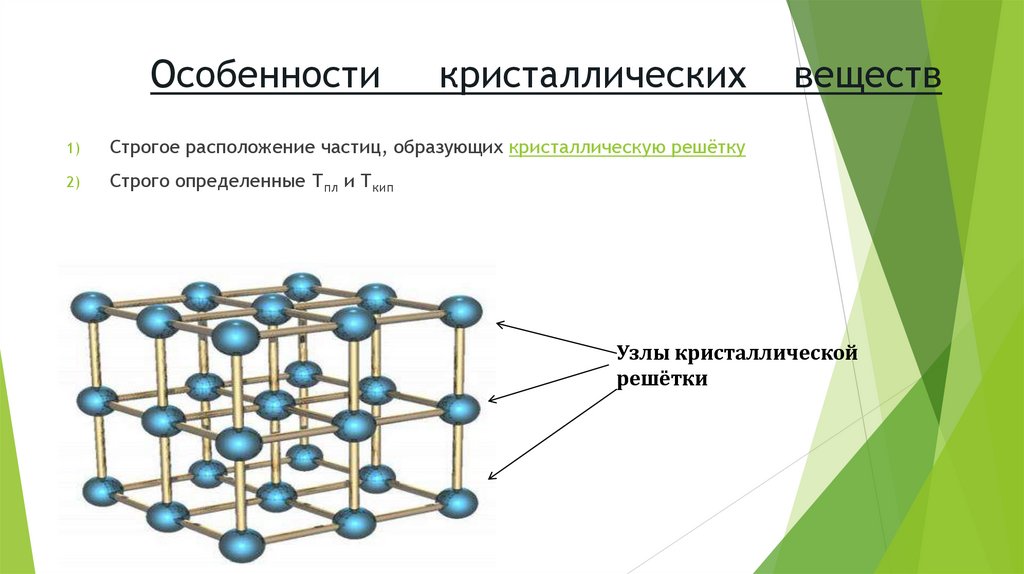
Особенностикристаллических
1)
Строгое расположение частиц, образующих кристаллическую решётку
2)
Строго определенные Тпл и Ткип
веществ
Узлы кристаллической
решётки
8.
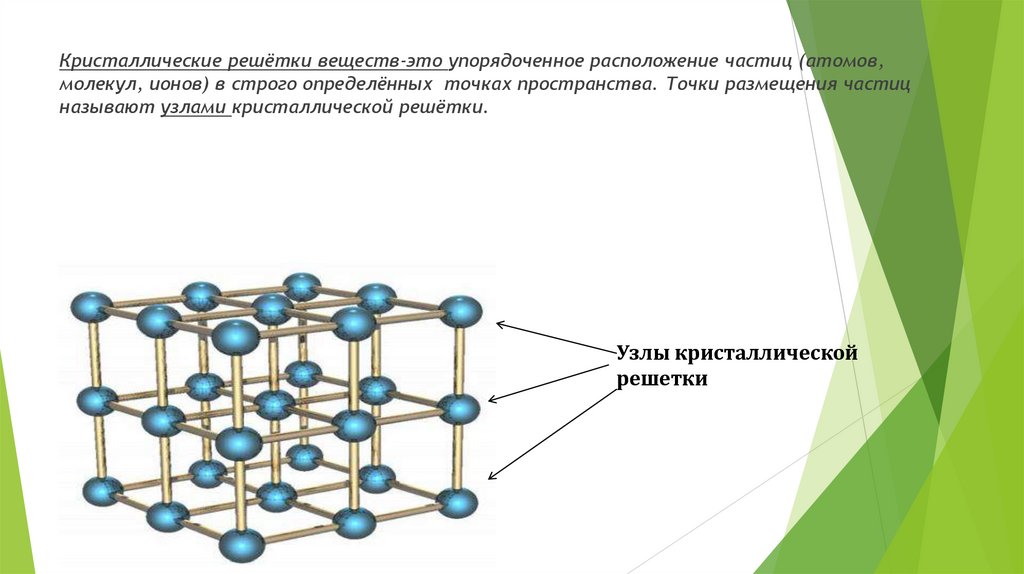
Кристаллические решётки веществ-это упорядоченное расположение частиц (атомов,молекул, ионов) в строго определённых точках пространства. Точки размещения частиц
называют узлами кристаллической решётки.
Узлы кристаллической
решетки
9.
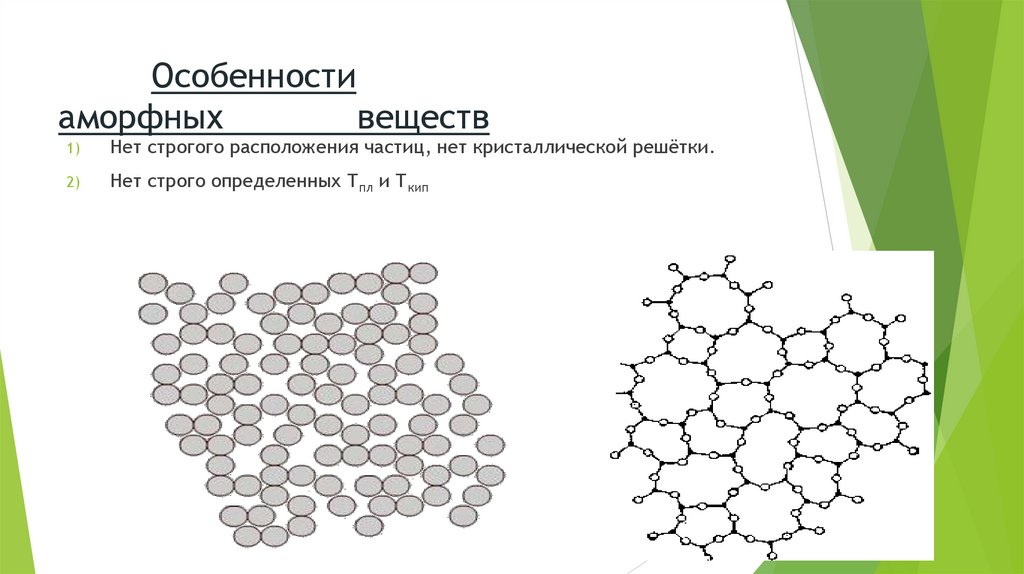
Особенностиаморфных
веществ
1)
Нет строгого расположения частиц, нет кристаллической решётки.
2)
Нет строго определенных Тпл и Ткип
10.
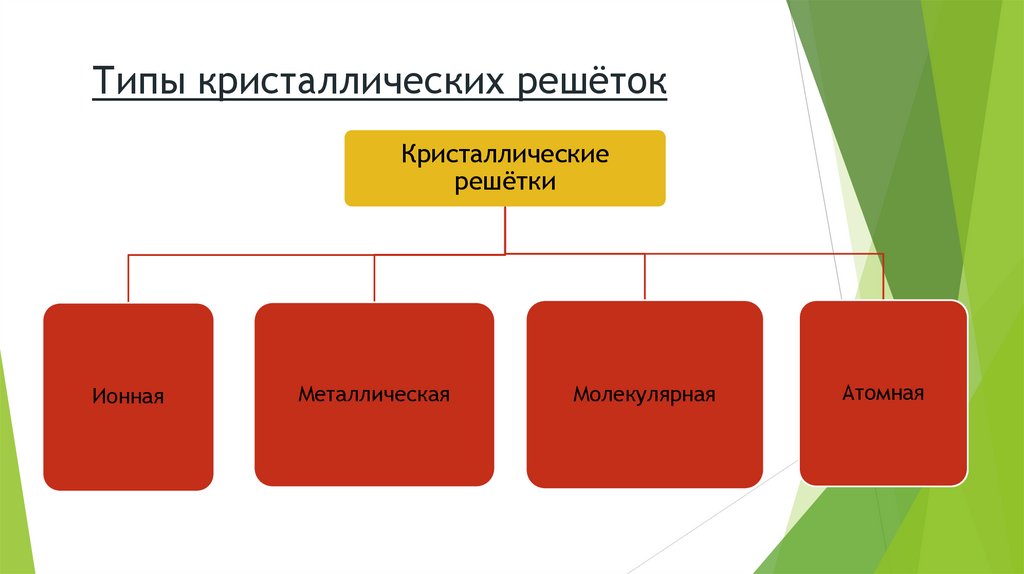
Типы кристаллических решётокКристаллические
решётки
Ионная
Металлическая
Молекулярная
Атомная
11.
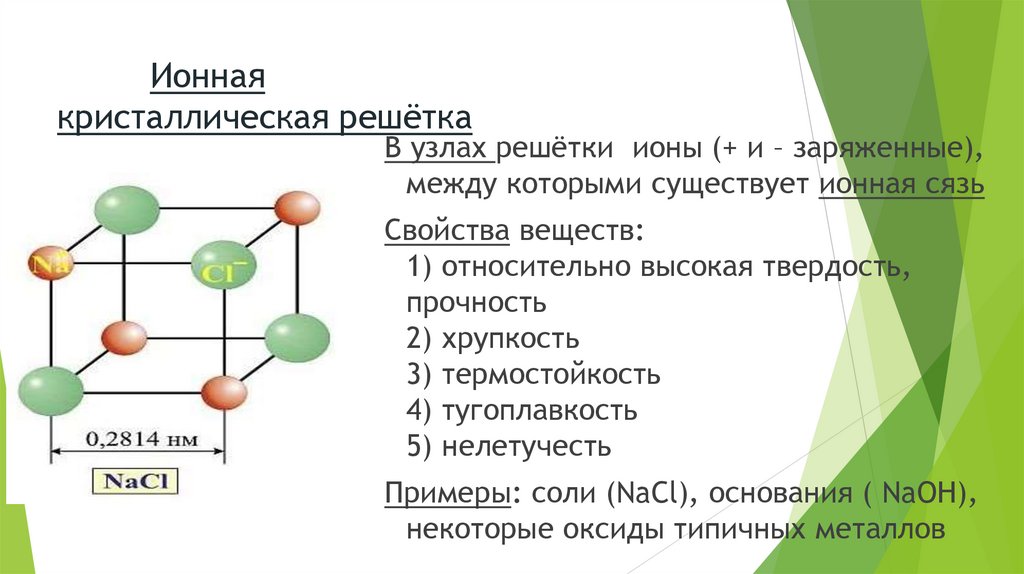
Ионнаякристаллическая решётка
В узлах решётки ионы (+ и – заряженные),
между которыми существует ионная сязь
Свойства веществ:
1) относительно высокая твердость,
прочность
2) хрупкость
3) термостойкость
4) тугоплавкость
5) нелетучесть
Примеры: соли (NaCl), основания ( NaOH),
некоторые оксиды типичных металлов
12.
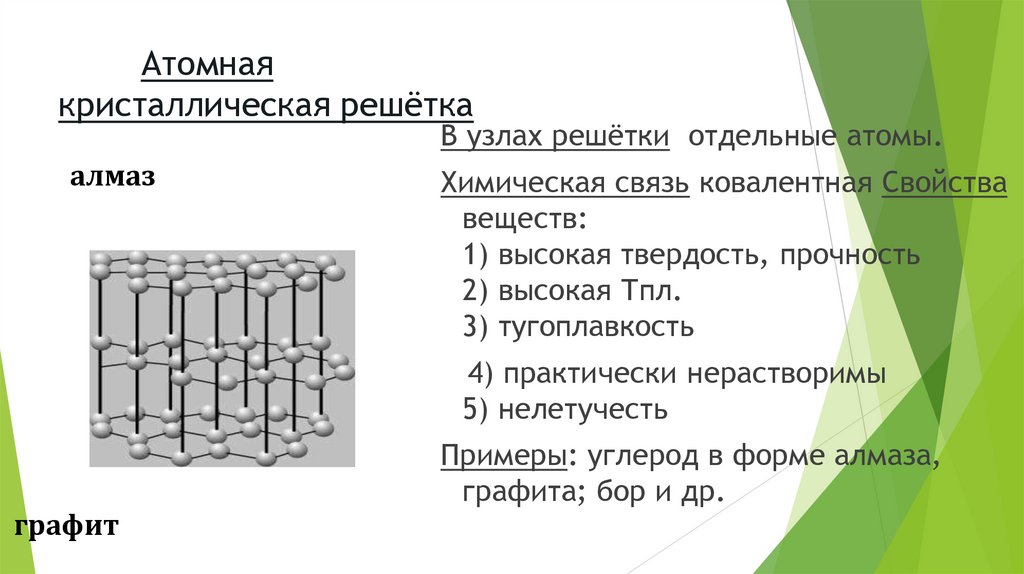
Атомнаякристаллическая решётка
В узлах решётки отдельные атомы.
алмаз
Химическая связь ковалентная Свойства
веществ:
1) высокая твердость, прочность
2) высокая Тпл.
3) тугоплавкость
4) практически нерастворимы
5) нелетучесть
графит
Примеры: углерод в форме алмаза,
графита; бор и др.
13.
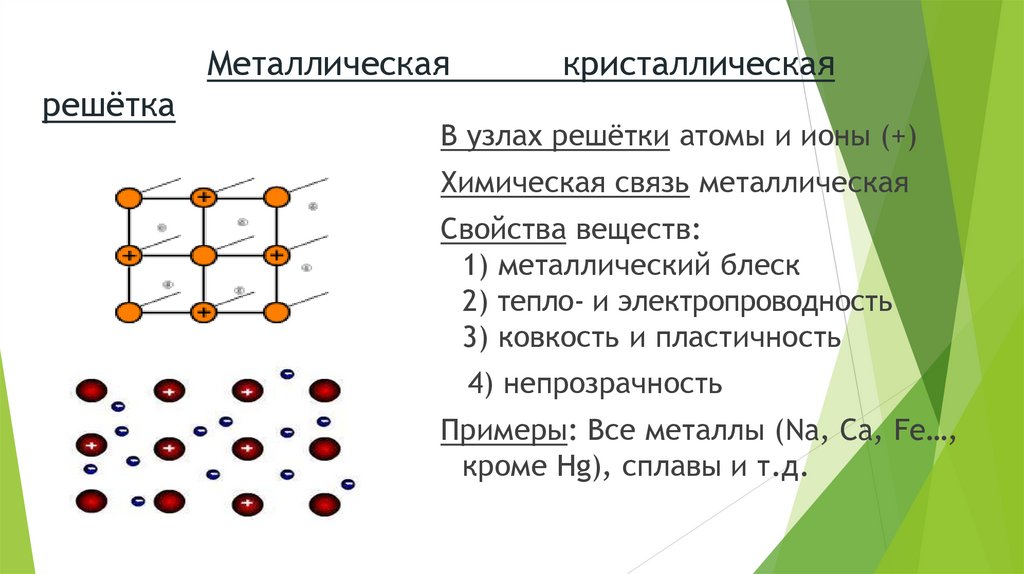
Металлическаярешётка
кристаллическая
В узлах решётки атомы и ионы (+)
Химическая связь металлическая
Свойства веществ:
1) металлический блеск
2) тепло- и электропроводность
3) ковкость и пластичность
4) непрозрачность
Примеры: Все металлы (Na, Ca, Fe…,
кроме Hg), сплавы и т.д.
14.
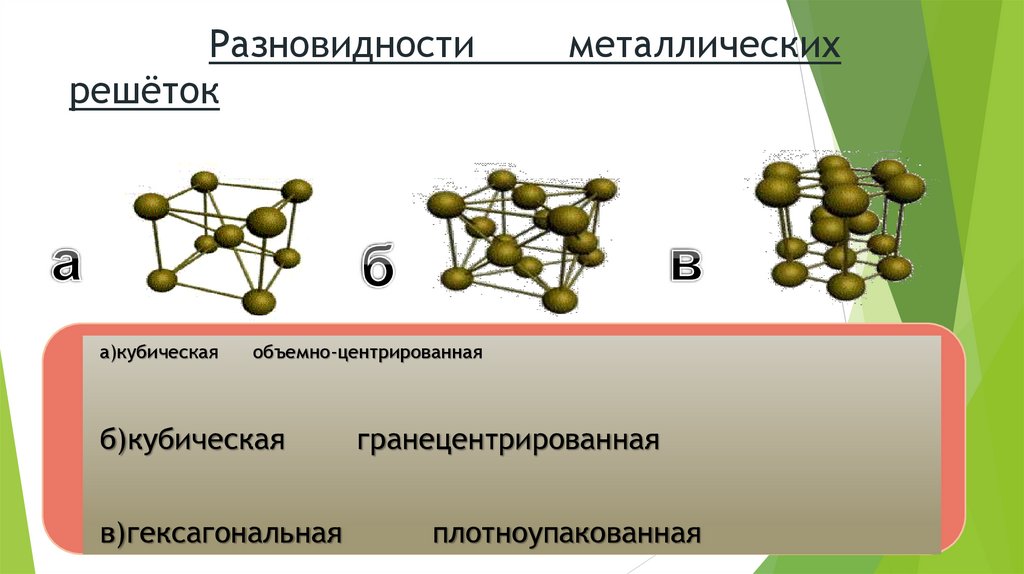
Разновидностирешёток
а)кубическая
металлических
объемно-центрированная
б)кубическая
в)гексагональная
гранецентрированная
плотноупакованная
15.
ВеществаМолекулярного
строения:
состоят из молекул
Немолекулярного
строения:
состоят из атомов
и ионов
16.
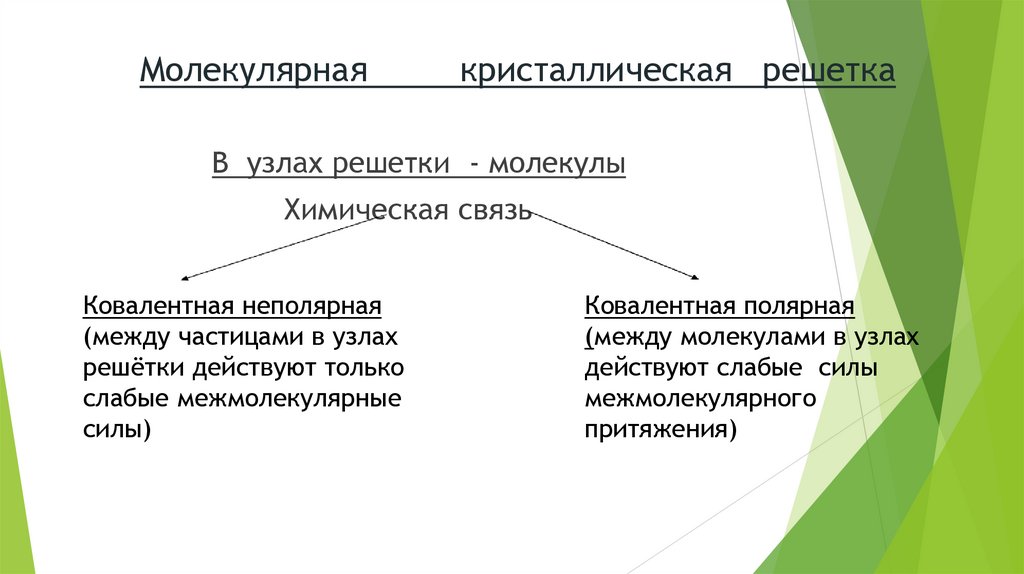
Молекулярнаякристаллическая решетка
В узлах решетки - молекулы
Химическая связь
Ковалентная неполярная
(между частицами в узлах
решётки действуют только
слабые межмолекулярные
силы)
Ковалентная полярная
(между молекулами в узлах
действуют слабые силы
межмолекулярного
притяжения)
17.
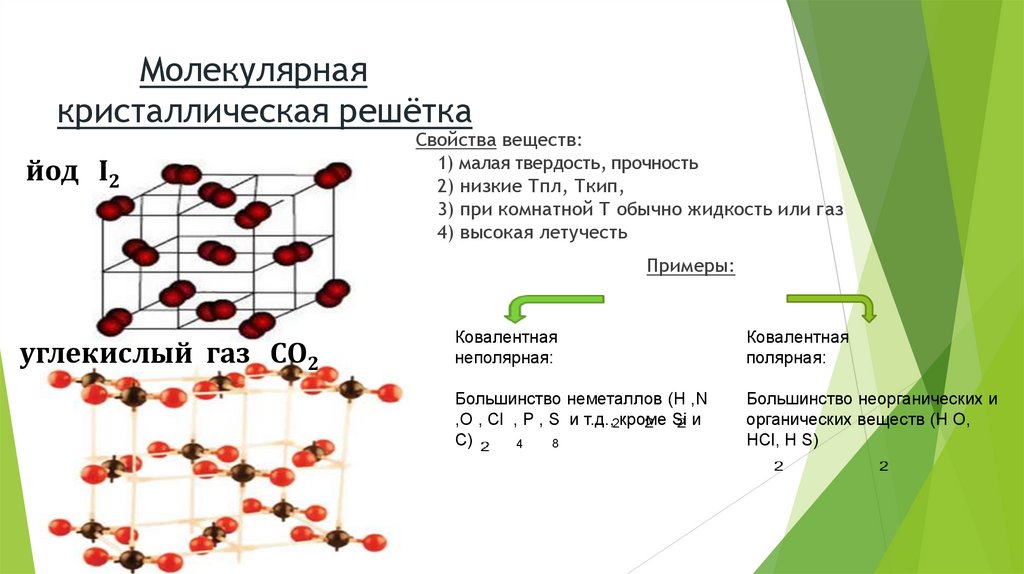
Молекулярнаякристаллическая решётка
йод I2
Свойства веществ:
1) малая твердость, прочность
2) низкие Тпл, Ткип,
3) при комнатной Т обычно жидкость или газ
4) высокая летучесть
Примеры:
углекислый газ СО2
Ковалентная
неполярная:
Ковалентная
полярная:
Большинство неметаллов (H ,N
,O , Cl , P , S и т.д.,2кроме Si и
C)
8
4
Большинство неорганических и
органических веществ (H O,
HCl, H S)
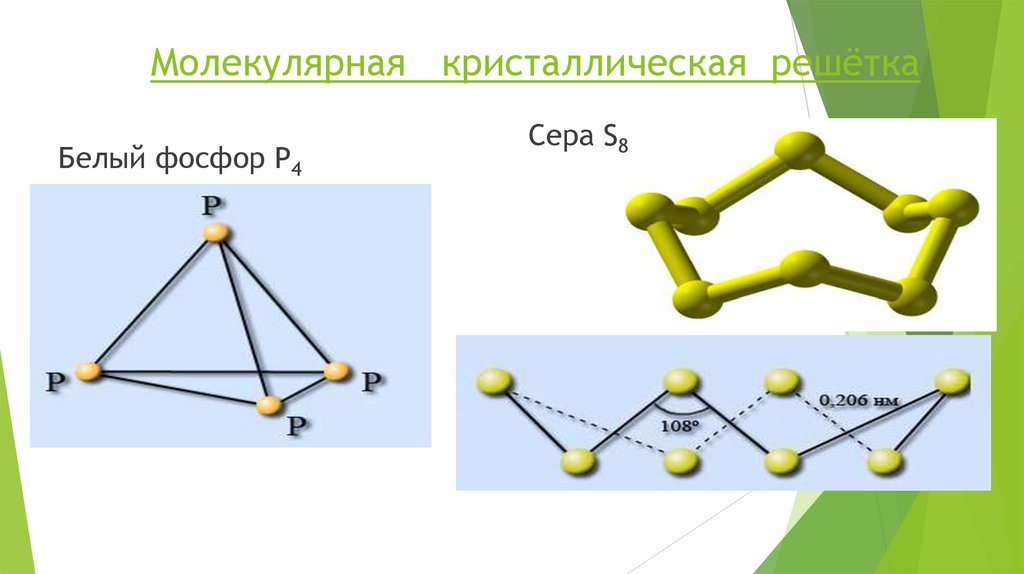
18.
Молекулярная кристаллическая решёткаБелый фосфор Р4
Сера S8
19.
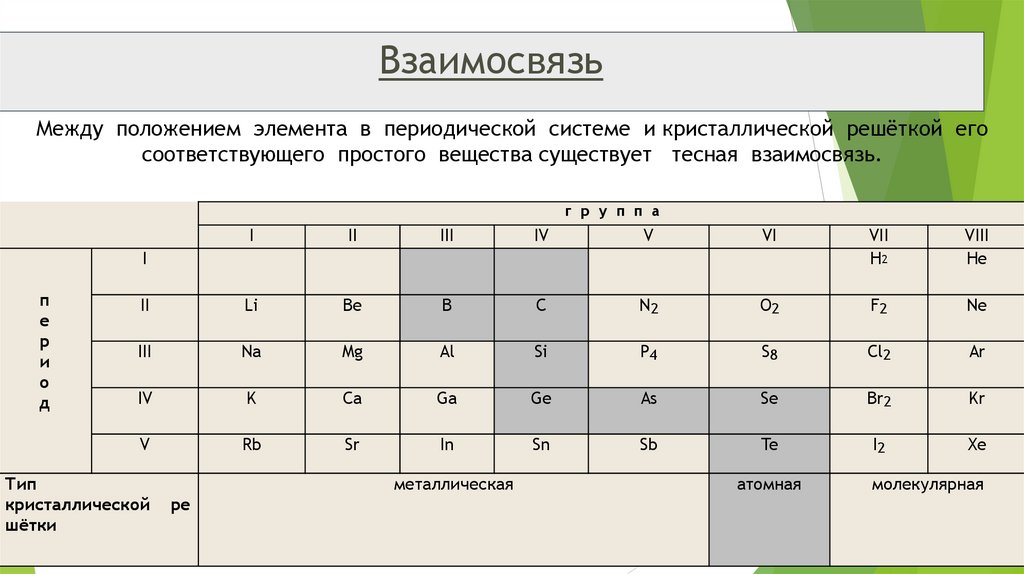
ВзаимосвязьМежду положением элемента в периодической системе и кристаллической решёткой его
соответствующего простого вещества существует тесная взаимосвязь.
г р у п п а
I
II
III
IV
V
VI
VII
H2
VIII
He
II
Li
Be
B
C
N2
O2
F2
Ne
III
Na
Mg
Al
Si
P4
S8
Cl2
Ar
IV
K
Ca
Ga
Ge
As
Se
Br2
Kr
V
Rb
Sr
In
Sn
Sb
Te
I2
Xe
I
п
е
р
и
о
д
Тип
кристаллической
шётки
металлическая
ре
атомная
молекулярная
20.
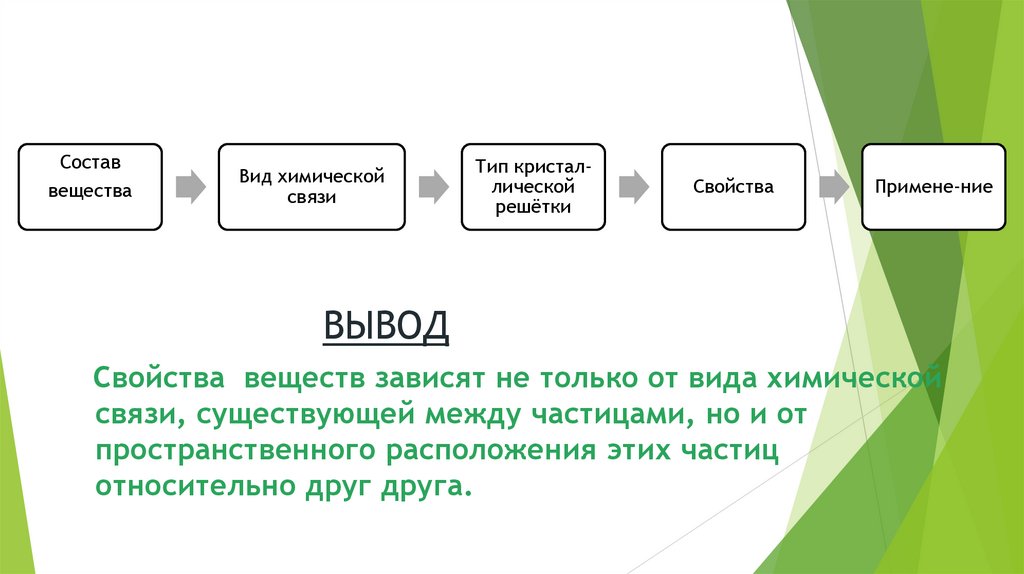
Составвещества
Вид химической
связи
Тип кристаллической
решётки
Свойства
Примене-ние
ВЫВОД
Свойства веществ зависят не только от вида химической
связи, существующей между частицами, но и от
пространственного расположения этих частиц
относительно друг друга.
21.
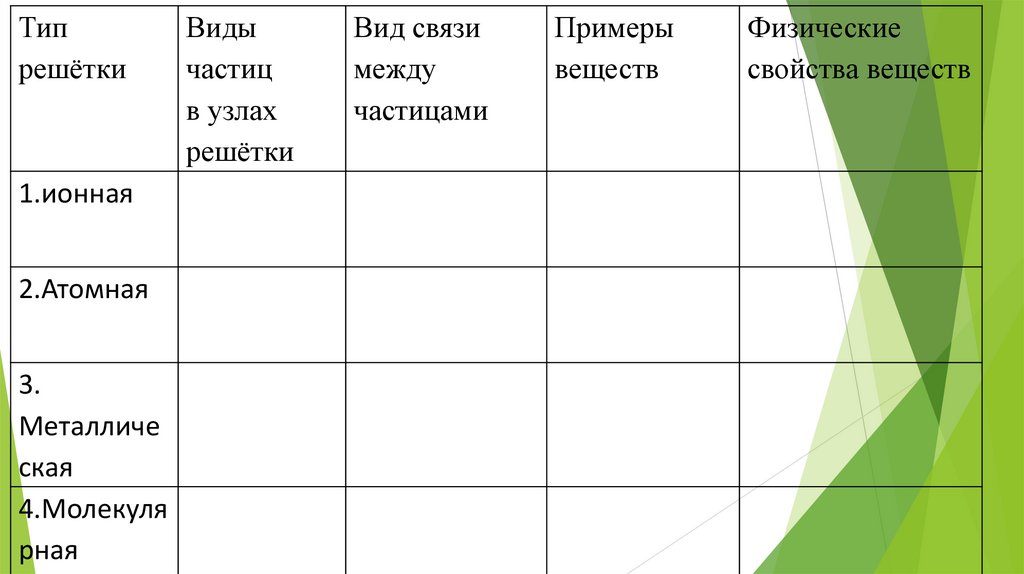
Типрешётки
1.ионная
2.Атомная
3.
Металличе
ская
4.Молекуля
рная
Виды
частиц
в узлах
решётки
Вид связи
между
частицами
Примеры
веществ
Физические
свойства веществ
22.
Опишите соединение NaF:А)тип связи
Б)тип решетки
В) свойства вещества (не менее 3)
2.Приведите пример соединения с ковалентной связью:
Укажите 2 его свойства:
23.
1 - заданиеa) Ковалентная связь – это
b) Объясните и распишите механизм
образования химической связи в следующих
соединениях и назовите ее : F 2 ; NH3
c) Дайте определение значению
электроотрицательности
d) Расположите элементы в порядке
возрастания электроотрицательности : Cu Cl
Au I As Ba Li
24.
2 - заданиеa) Ионы – это
b) Ионная связь – это
c) Распределите на катионы и анионы следующие
ионы :
N- Br- H+ Cu+ O2- Ra2+ Ga+3
d) Распишите механизм образование ионной связи на
примере молекулы Li2O







 chemistry
chemistry








