Similar presentations:
Вода в атмосфере. Часть 1
1.
ВОДА В АТМОСФЕРЕЧасть 1
2.
В атмосфере постоянно находится около 10 000 миллиардов тонн воды в видепара. Это означает, что над каждым гектаром земной
поверхности в воздухе содержится в среднем более 200 тонн воды
В облаках 12 000 м3 воды
3.
Вода на Земле находится в постоянном движении, она все времярасходуется и восстанавливается в процессе кругооборота на земном шаре
• ОБЩИЙ ОБЪЕМ ВОДЫ на ЗЕМЛЕ: 1,4 – 1,5 млрд км3,
• Из них суша дает 90 млн км3, остальное - моря и океаны.
• Суша дает : подземные воды – 60 млн км3,
ледники – 29 млн км3
озера
- 0,75 млн км3
реки - 0,012 млн км3
• В результате процесса испарения – моря и океаны дают 1/300 часть от вего содержания
воды, 1/10 часть этой воды конденсируется и выпадает в виде осадков 5*1014 тонн
• В каждый момент времени в атмосфере находится1,3*1013 тонн, т.е.осадков
выпадает в 40 раз больше одновременного содержания воды в атмосфере,
т.е. • . КРУГОВОРОТ ВОДЫ в АТМОСФЕРЕ 365дн*40 = 9 суток
4.
Физико-химические свойства воды1. Плотность всех веществ уменьшается при росте их температуры,
плотность воды имеет максимум (0,9999 г/см3 ) при температуре 4
град., снижение и рост температуры приводит к понижению
плотности воды.
2.Если бы в воде были упакованы однородно, то температура
кипения равнялась 63,5 град., но в воде образуются различные
ассоциации молекул, поэтому температура кипения – 100 град.
3 Вязкость воды снижается при повышения давления, в других
веществах при росте давления вязкость растет. (Поэтому подземные
воды подвижны).
Имеется 36 изотопов воды, что приводит к изменению физических
свойств воды. Так тяжелая вода D2 O Т кип = 101,42град, Т зам =3,8
град
Под словом ВОДА физики понимают абсолютно чистое вещество,
однако такой воды нет, т.к. в любой воде есть примеси и и вода
постоянно диссоциируется на Н и ОН.
Коэффициент σ
называется коэффициентом поверхностного натяжения ( σ > 0 ). Таким
Образом, коэффициент поверхностного натяжения равен работе,
необходимой для увеличения площади поверхности жидкости при
постоянной температуре на единицу поверхности . ( Дж/м2 ) или в ньютонах
на метр ( 1 Н/м = 1 Дж/м2 ).
5.
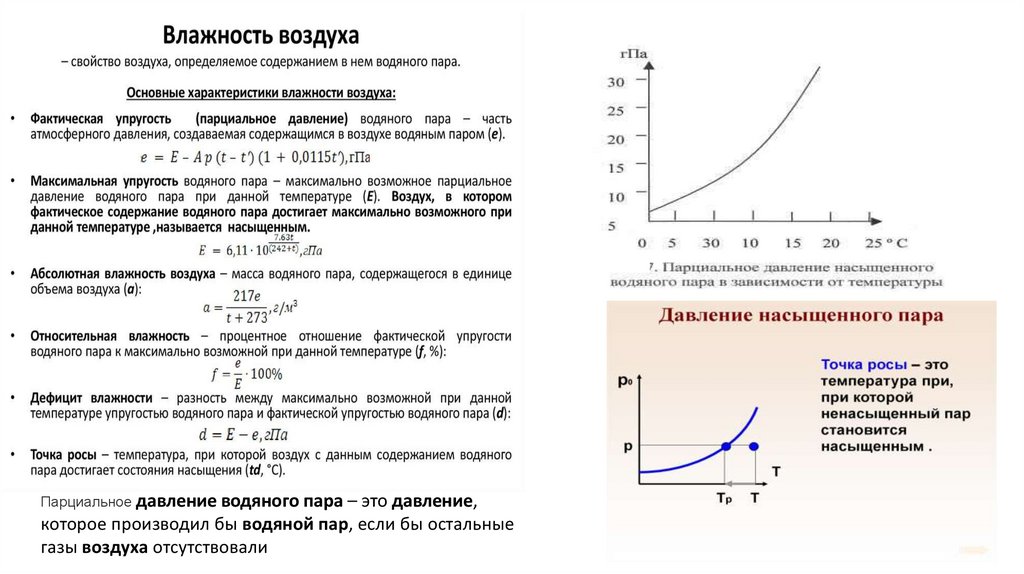
Парциальное давление водяного пара – это давление,которое производил бы водяной пар, если бы остальные
газы воздуха отсутствовали
6.
7.
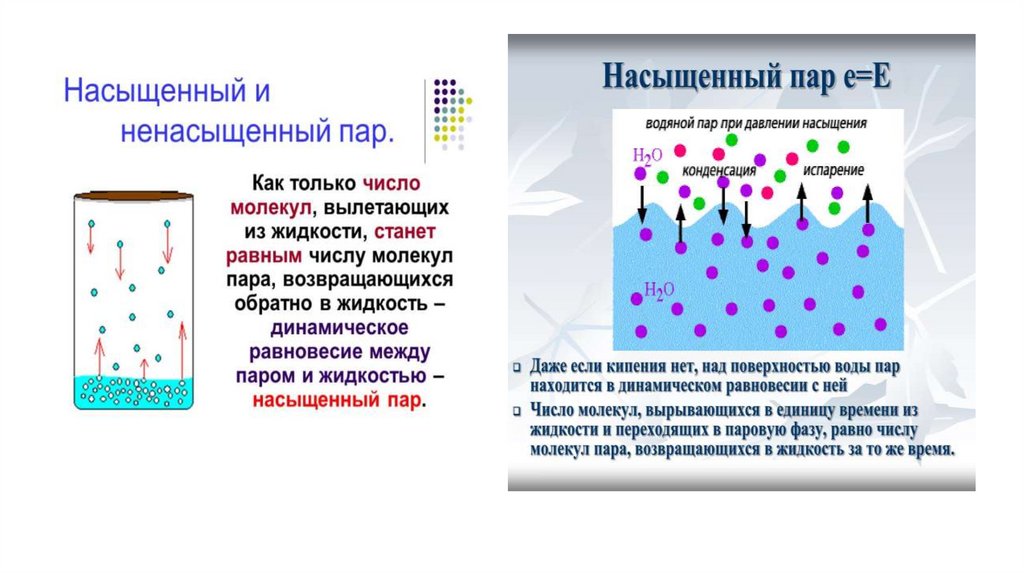
Давлением насыщенного пара Е , гПа, называется наибольшее содержаниеводяного пара над данной поверхностью и данной температуре, при котором наступает
динамическое равновесие между фазовыми переходами воды.
• ОСНОВНЫЕ ПОНЯТИЯ :
• ФАЗА – В термодинамике – физически однородное тело или совокупность нескольких тождественных по
состоянию тел, находящихся в тождественных равновесных состояниях
• РАВНОВЕСИЕ ФАЗ – Установившееся состояние системы с несколькими фазами, при котором переход вещества
из одной фазы в другую уравновешивается обратным переходом. Таким образом, если равновесие существует,
то в любой точке межфазовой границы нормальные к ней потоки равны.
• ПРИМЕР равновесия фаз: при Т = const, e стремится к Е и наступает равновесие
• ПРАВИЛО фаз Гиббса, 1868г. - Для описания равновесия фаз предложил формулу:
• F = K – n +2, где F – число степеней свободы, K - число компонент, n – число фаз
• При К =1.(вода),
a) n = 1, ( одна фаза) F =2, т.е. могут меняться 2 параметра (е и Т).
b) n =2, ( две фазы), F = 1, т.е. есть одна независимая переменная ( или е или Т )и мы имеем линию равновесия
фаз : F = f (T)
c) n = 3, F = 0, (точка).
8.
При отрицательных температурах давление насыщенного водяного пара над поверхностью ледяныхкристаллов меньше, чем над поверхностью переохлажденных капель (при одинаковом их размере)
(При температуре = -10 °С над переохлажденной водой давление насыщенного водяного пара 2,85 гПа, а
надо льдом 2,60 гПа.
9.
• Поскольку давление создается двигающимися молекулами, то значение давленияпрямо пропорционально числу молекул в единице объема (в 1 м3 ) и скорости их
перемещения, то есть температуре. Следовательно, парциальное давление
водяного пара может быть выражено через концентрацию молекул водяного пара:
• e= N П ⋅ k ⋅T , (1)
• где e − парциальное давление водяного пара, гПа; N П − концентрация молекул
водяного пара, м-3; k − постоянная Больцмана, 1.38 10− 23⋅ Дж/К;
T − температура,
• При условии равновесия между водяным паром и водой, то есть когда за некоторый
интервал времени с поверхности воды отрывается такое же количество молекул,
сколько и конденсируется, концентрация молекул водяного пара называется
равновесной N ПВ , а создаваемое молекулами давление – давлением насыщения
водяного пара над поверхностью воды EП
• EПВ = N ПВ ⋅ k ⋅T . (2)
• Или, равновесная концентрация молекул водяного пара может быть рассчитана по
давлению насыщения:
N ПВ = Епв/kT
10.
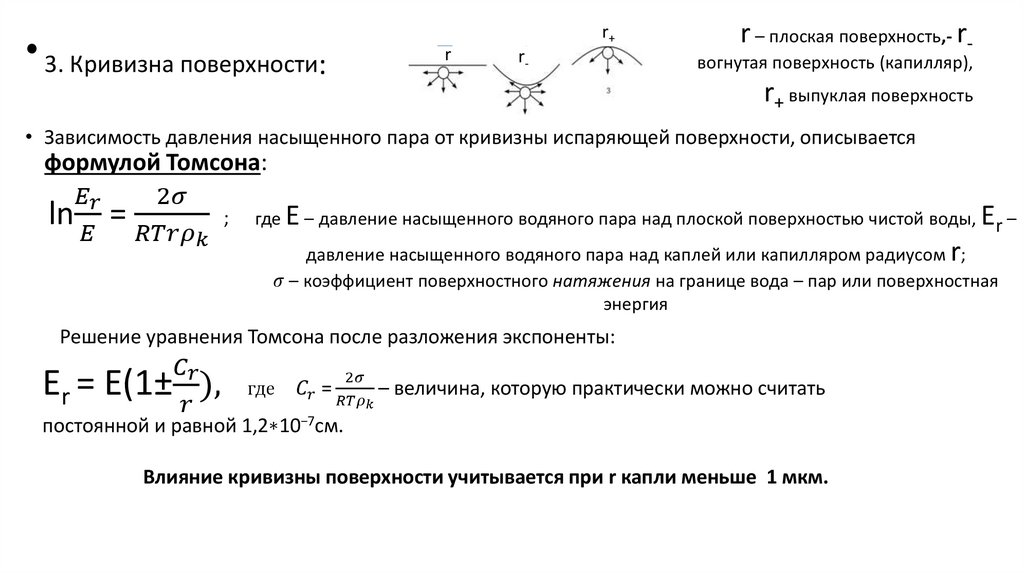
ФАКТОРЫ, ВЛИЯЮЩИЕ на ДАВЛЕНИЕ НАСЫЩЕННОГО ПАРА• 1. Температура:















 geography
geography








