Similar presentations:
Уравнение Менделеева-Клапейрона
1. Эпиграф Успех не станет разыскивать тебя. Ты сам должен его искать.
У. Брайан2. PV=(m/M)*RT
Уравнение Менделеева-КлапейронаPV=(m/M)*RT
3. Изо – (постоянный)
Процессв
газах
ἴσος «равный»
и χώρος
«место»
ἴσος
«одинако
вый»
и βάρος
«тяжесть»
Барос
(давление,
тяжесть)
Хорос
(место,
объем)
ἴσος
«равный»
и θέρμη
«жар»
Термо
(жар,
температура)
4. Изо – (постоянный)
Изобарныйизопроцессы
Изохорный
Изотермический
5. Изопроцессы в газах
Урок изучениянового
материала
Изопроцессы в газах
10 класс
учитель: Брянцева С.А.
6. Цель:
установить зависимость междудвумя макроскопическими
параметрами газа при
неизменном третьем.
7. Изопроцесс -
Изопроцесс процесс, при котором один измакроскопических параметров
состояния данной массы газа
остается постоянным.
V, p, Т
8. Изотермический процесс -
Изотермическийпроцесс ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ
МАССЫ ГАЗА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ.
Т = const
m = const
9. Изобарный процесс -
Изобарный процесс ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙМАССЫ ГАЗА ПРИ ПОСТОЯННОМ ДАВЛЕНИИ.
P = const
m = const
10. Изохорный процесс -
Изохорный процесс ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙМАССЫ ГАЗА ПРИ ПОСТОЯННОМ ОБЪЕМЕ.
V = const
m = const
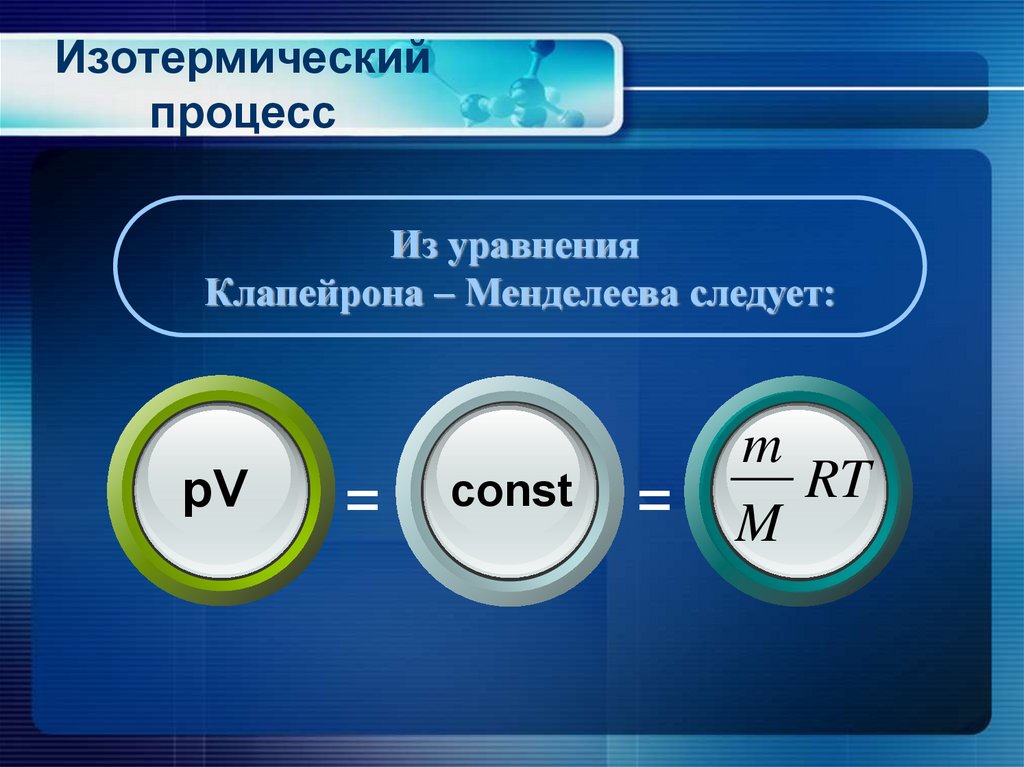
11. Изотермический процесс
Из уравненияКлапейрона – Менделеева следует:
pV
=
const
=
m
RT
M
12. Закон Бойля – Мариотта.
Закон экспериментально получен в:• 1662 г. Р. Бойлем;
• 1676 г. Э. Мариоттом.
T - const
Р. Бойль
Для газа данной массы при постоянной
температуре произведение давления газа
на его объем постоянно:
p1V1 = p2V2
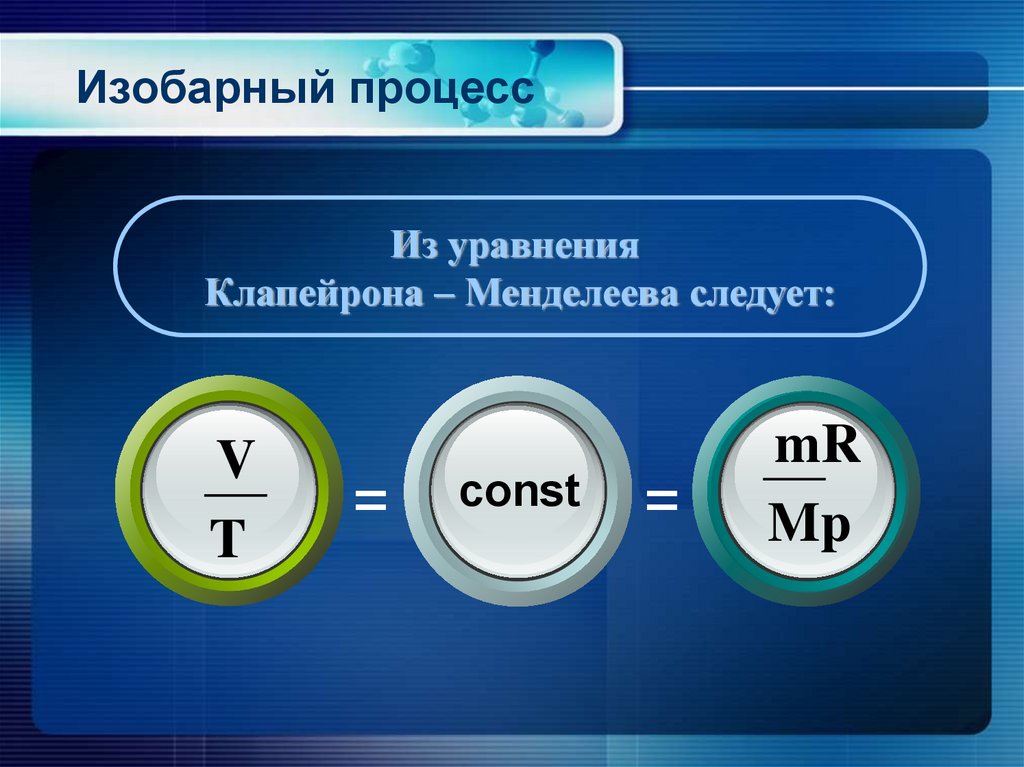
13. Изобарный процесс
Из уравненияКлапейрона – Менделеева следует:
V
T
=
const
=
mR
Mp
14. Закон Гей-Люссака.
Закон экспериментальнополучен в 1802 г.
p - const
Для газа данной массы при постоянном
давлении отношение объема газа к его
термодинамической температуре
постоянно:
V1 / T1 = V2 / T2
ГЕЙ-ЛЮССАК
Жозеф Луи
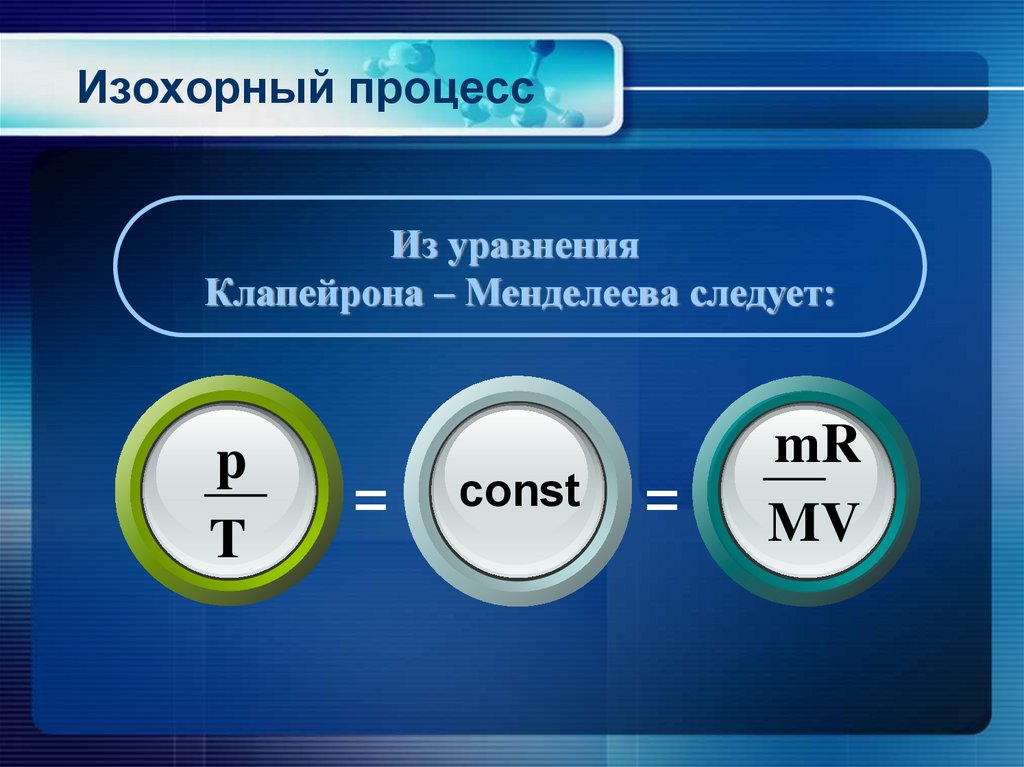
15. Изохорный процесс
Из уравненияКлапейрона – Менделеева следует:
p
T
=
const
=
mR
MV
16. Закон Шарля.
Закон экспериментальнополучен в 1787 г.
V - const
Для газа данной массы при постоянном
объеме отношение давления газа к его
термодинамической температуре
постоянно:
p1 / T1 = p2 / T2
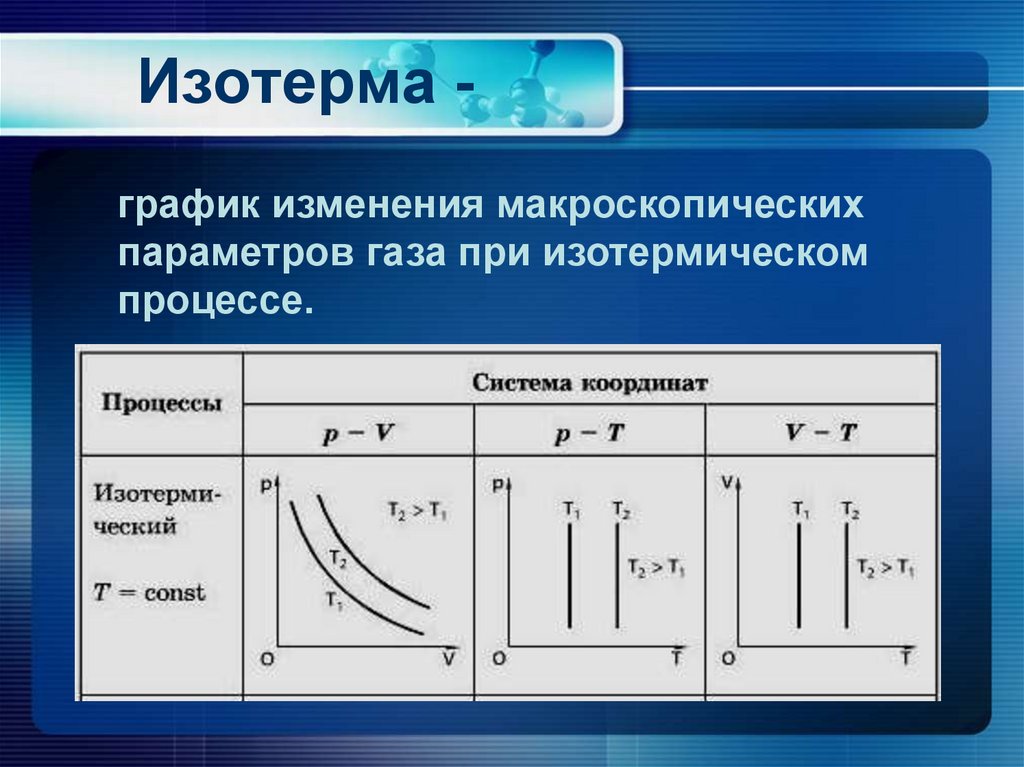
17. Изотерма -
Изотерма график изменения макроскопическихпараметров газа при изотермическом
процессе.
18. Изобара –
график изменения макроскопическихпараметров газа при изобарном
процессе.
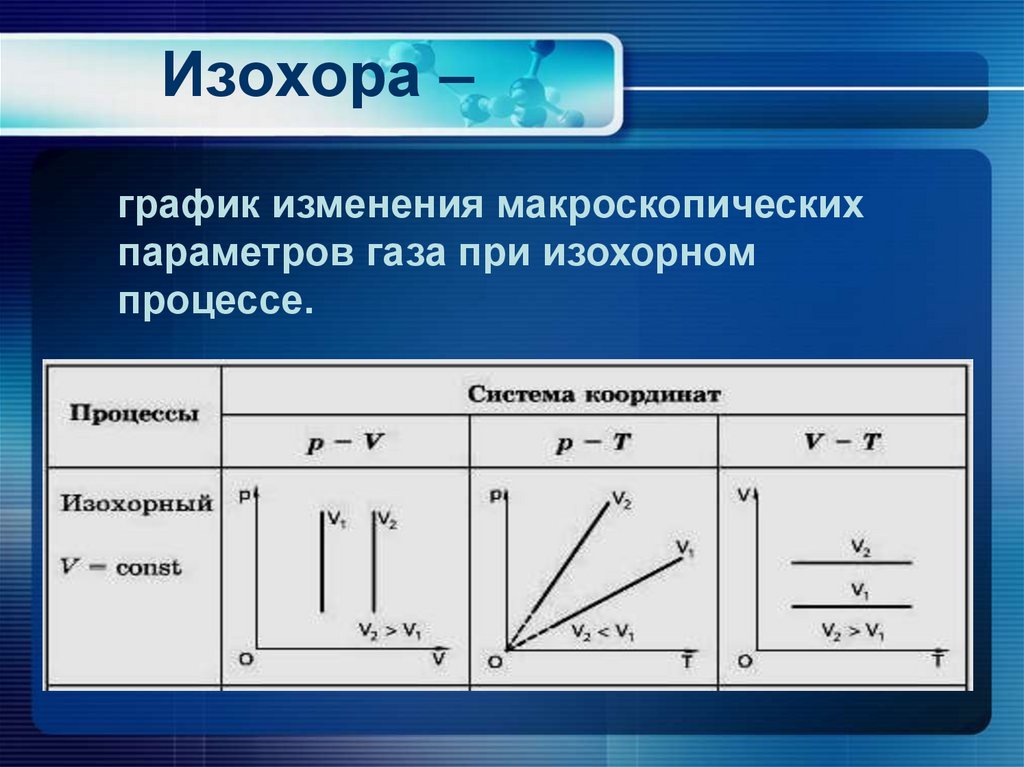
19. Изохора –
график изменения макроскопическихпараметров газа при изохорном
процессе.














 physics
physics








