Similar presentations:
Термохимия. Закон Гесса
1.
ТЕРМОХИМИЯЗАКОН ГЕССА
е
2.
ТЕРМОХИМИЯ исследует термические эффекты,сопутствующие химическим процессам.
Результаты термохимических расчетов принято относить к 1
моль вещества.
Экзотермическая реакция – тепло выделяется (Δ H˂0 ),
эндотермическая реакция – тепло поглощается (Δ H ˃0 ).
Теплота (энтальпия) образования – количество теплоты,
которое выделяется при образовании 1 моль соединения из
простых веществ.
Теплота (энтальпия) сгорания – количество теплоты,
которое выделяется при сгорании 1 моль вещества.
ЗАКОН ЛАВУАЗЬЕ-ЛАПЛАСА:
Если
при
образовании
какого-либо
соединения
выделяется некоторое количество теплоты, то при
разложении этого соединения до исходных реагентов в
тех же условиях такое же количество теплоты
поглощается.
3.
ЗАКОН ГЕССАТЕПЛОВОЙ ЭФФЕКТ РЕАКЦИИ ЗАВИСИТ ТОЛЬКО
ОТ НАЧАЛЬНОГО И КОНЕЧНОГО СОСТОЯНИЯ
ВЕЩЕСТВ И НЕ ЗАВИСИТ ОТ ПРОМЕЖУТОЧНОЙ
СТАДИИ ПРОЦЕССА.
(Герман Иванович ГЕСС, 1840 г.)
(при условии, что (1) единственная работа, совершаемая
системой это работа расширения и (2) – р и V-const)
СЛЕДСТВИЯ
1. Энтальпия образования соединения из исходных
веществ не зависит от способа получения этого
соединения.
2. Теплота (энтальпия) разложения вещества до
одинаковых продуктов равна и противоположна по знаку
теплоте (энтальпии) образования его из этих продуктов.
4.
3. Тепловой эффект реакции равен алгебраическойсумме энтальпий образования реагентов из простых
веществ, т.е. сумме энтальпий образования продуктов
реакции за вычетом суммы энтальпий образования
исходных веществ:
ΔН = Ʃ(ΔНобр)прод - Ʃ(ΔНобр)исх
5.
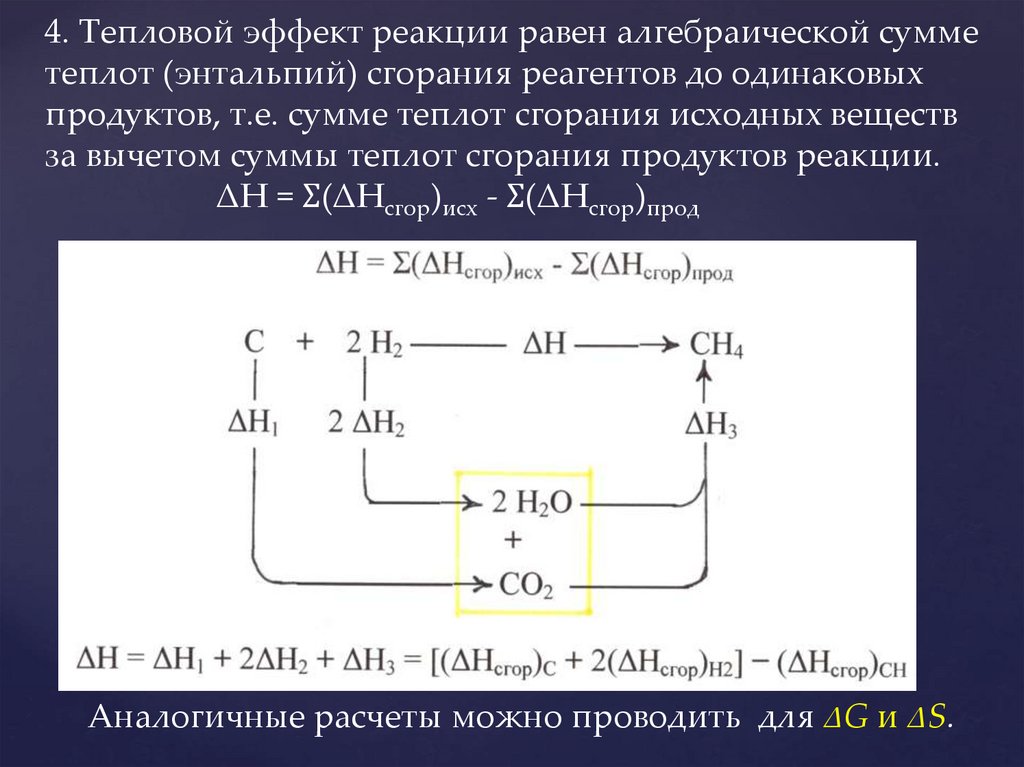
4. Тепловой эффект реакции равен алгебраической сумметеплот (энтальпий) сгорания реагентов до одинаковых
продуктов, т.е. сумме теплот сгорания исходных веществ
за вычетом суммы теплот сгорания продуктов реакции.
ΔН = Ʃ(ΔНсгор)исх - Ʃ(ΔНсгор)прод
Аналогичные расчеты можно проводить для ΔG и ΔS.




 chemistry
chemistry