Similar presentations:
Вода
1.
Автор презентации:Мишина и
Малютина Кати
21группа
2.
Воде была дана волшебная власть статьсоком жизни на Земле.
Леонардо да Винчи
3.
Вода в природеФизические
свойства воды
Химические свойства
воды
Круговорот воды
Применение воды
Тест
4.
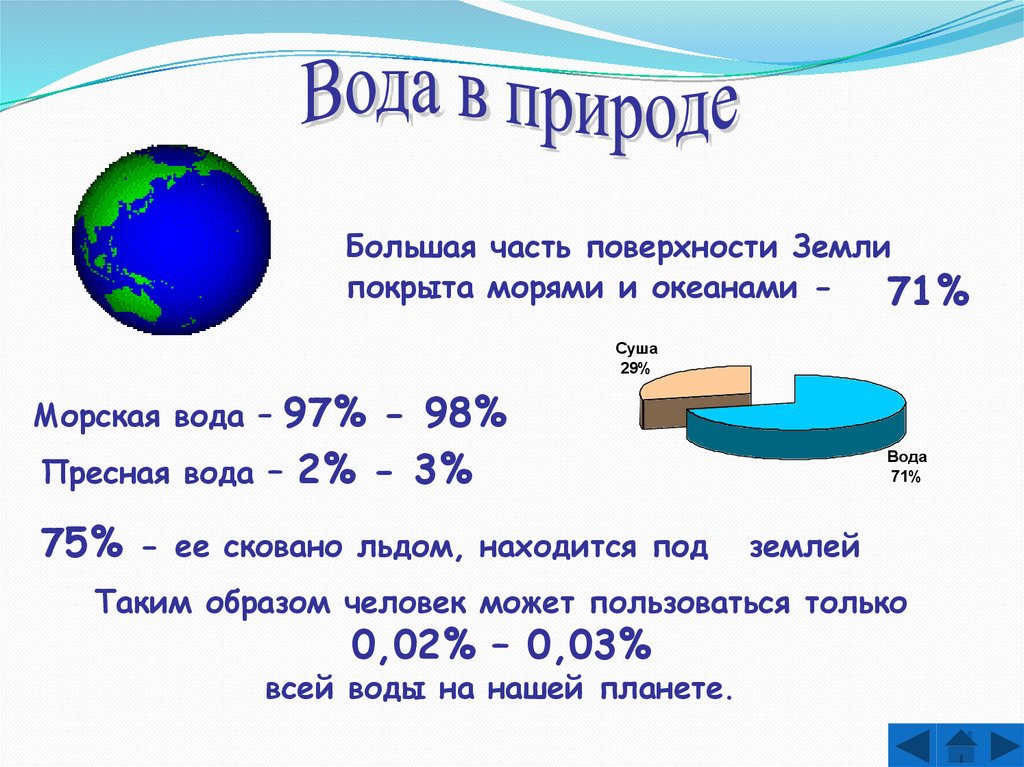
Большая часть поверхности Землипокрыта морями и океанами 71%
Суша
29%
97% - 98%
– 2% - 3%
Морская вода –
Пресная вода
75% -
ее сковано льдом, находится под
Вода
71%
землей
Таким образом человек может пользоваться только
0,02% – 0,03%
всей воды на нашей планете.
5.
Вода – единственное вещество в природе, которое в земныхусловиях существует во всех трех агрегатных состояниях:
жидком (вода), твердом (лед), газообразном (пар).
Пар
Жидкость
Лед
6.
Кровь человека на75%
Кости на 28%
90% состоит из воды
Мышцы на
Стекловидное тело глаза на
99%
7.
Обезвоживание организмана 12 – 15 % приводит к
нарушению обмена веществ,
А потеря до 25 % воды –
к гибели организма
Без воды человек может прожить
3 дня,
в то время, как без пищи
30 – 50 дней
8.
Лёд плавает на поверхностиводоёма,
(льда) = 0,92 г/см3, max
(воды) при +4°С = 1г/см3
При замерзании воды
происходит расширение
объёма.
Самая большая теплоемкость (
в 3100 раз больше, чем у
воздуха, в 4 раза больше, чем у горных пород)
Молекулы
взаимодействуют
между собой с
образованием
водородных связей.
9.
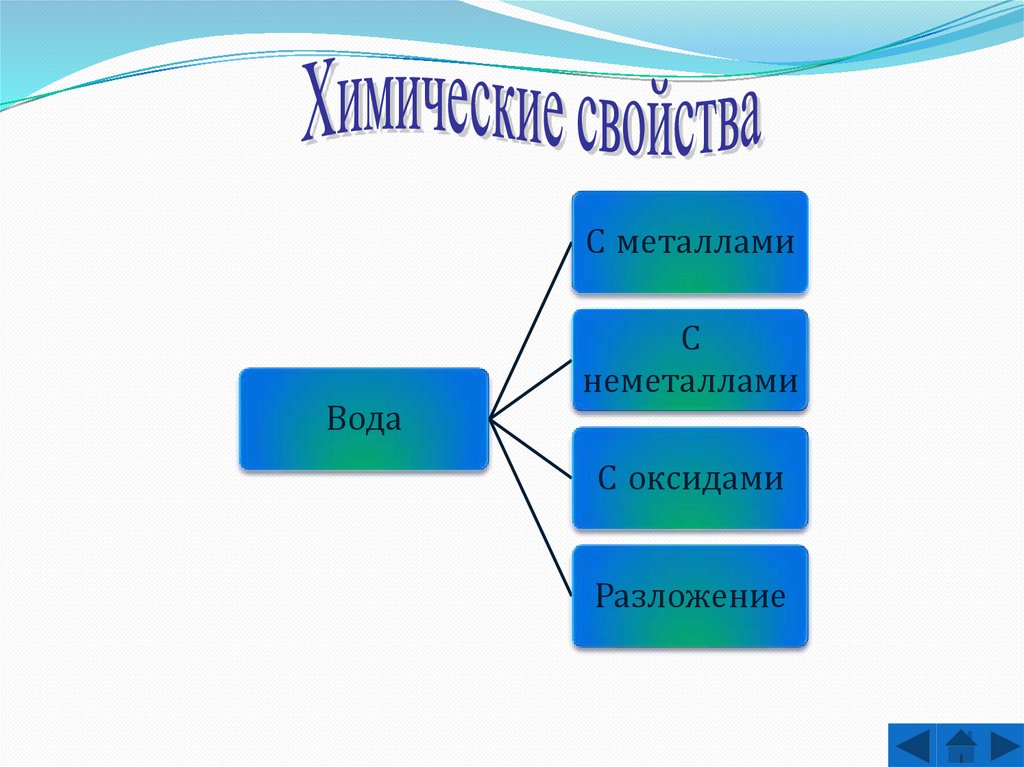
С металламиВода
С
неметаллами
С оксидами
Разложение
10.
При взаимодействии воды с активными металламиобразуется щелочь и водород:
2Na + 2H2О= H2 + 2NaOH (бурно)
2K + 2H2О = H2 + 2KOH (бурно)
При взаимодействии воды с менее активными
металлами образуется оксид и водород:
3Fe + 4H2О = 4H2 + Fe3О4 (только при нагревании)
11.
Вода взаимодействует с некоторыми неметаллами;получающиеся продукты взаимодействия очень
разнообразны:
C + H2О = H2 + CO (при сильном нагревании)
Cl2 + H2О = HClO + HCl
Под действием постоянного электрического тока
или высокой температуры вода разлагается на
кислород и водород:
2Н2О = 2Н2 + О2
12.
Некоторые оксиды металлов могут вступать в реакциисоединения с водой, в результате этой реакции
образуется щелочь:
СаО + Н2О = Са(ОН)2
Na2O + H2O =2 NaOH
Некоторые кислотные оксиды вступают в реакции
соединения с водой, в результате образуются кислоты:
SO3 + H2O = H2SO4
CO2 + H2O = H2CO3
13.
Вода постоянно испаряетсяс поверхности наземных
водоемов, листьев
растений Так возникает
водяной пар, который,
конденсируясь, ставновится
облаками.
Атмосферная вода
попадает на землю в
виде осадков.
Но не нужно думать, что круговорот – это панацея от исчерпания
доступных запасов пресной воды. Все же он происходит
медленно.
Берегите воду!
14.
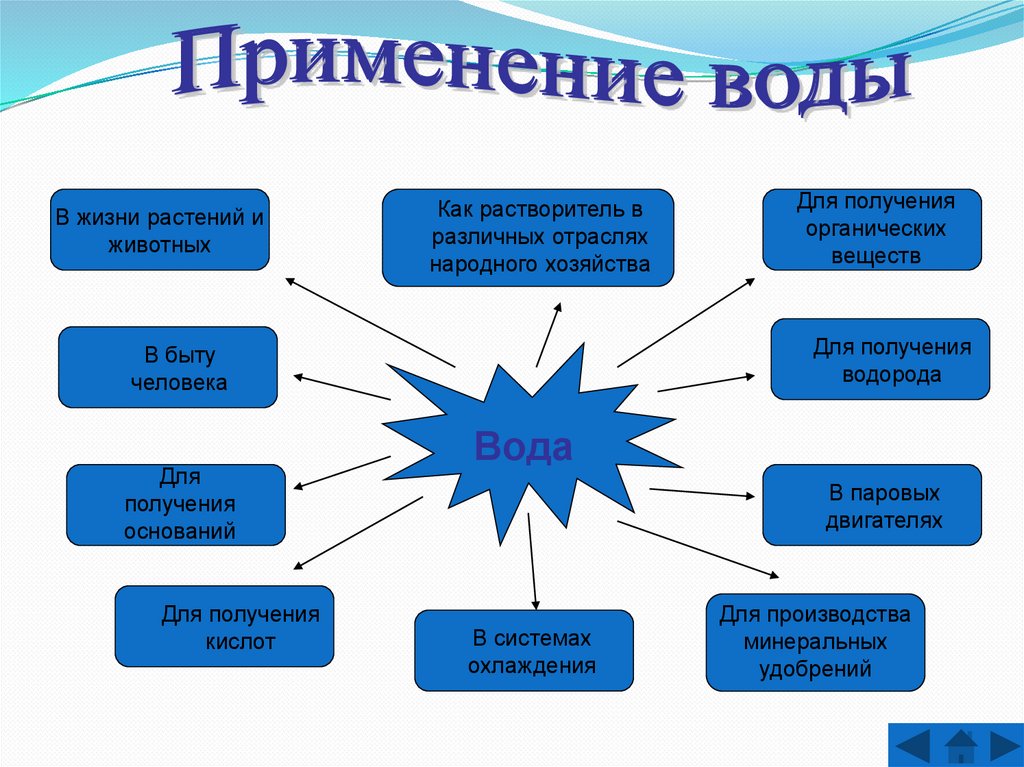
В жизни растений иживотных
Как растворитель в
различных отраслях
народного хозяйства
Для получения
водорода
В быту
человека
Для
получения
оснований
Для получения
кислот
Для получения
органических
веществ
Вода
В паровых
двигателях
В системах
охлаждения
Для производства
минеральных
удобрений
15.
Вода необходима всем живым организмам:растениям, животным и человеку.
Без воды нет жизни.
Вода – одно из самых главных богатств
Земли.
16.
17.
« Вода – у тебя нет ни цвета, ни вкуса, низапаха, тебя невозможно описать, тобою
наслаждаются, не ведая, что ты такое.
Нельзя сказать, что ты необходима для жизни:
ты – сама жизнь!»
Антуан Сент – Экзюпери
18.
19.
+ Вопрос 1 + Вопрос 2 + Вопрос 3 + Вопрос 4 -Выберите
формулу
оксида,
ссводой
которым
Выберите
формулу
оксида,
которым
Агрегатное
состояние
воды
Наиболее
энергично
с
Формула
Между
Больше
молекулами
продукта
всего
примесей
реакции
воды
При
комнатной
температуре
водород
Только
при
нагревании
Наталья
Валерьевна
вода
Ушакова
взаимодействует
с образованием
Вид
связи
в
молекуле
воды
выделяется,
если
с
водой
реагирует
при
обычных
условиях
реагирует
оксида
содержится
образуется
серы
(IV)
всвязь
воде
с водой
реагирует
с водой
щелочи
кислоты
+ Вопрос 5 + Вопрос 6 + Вопрос 7 -
А
А
А
+ Вопрос 8 -
+ Вопрос 9 + Вопрос 10 -
ВВВ
В
оксид
водородная
водородная
дождевой
Кальций
кальций
фосфора
P
SiO
H22O
S25
(V)
жидкость
ковалентная
кальций
H
железо
речной
Na
SO
газообразное
2CO
2O
24
полярная
Б
Б
ГГГ
ковалентная
твердое
оксид
морской
магний
золото
BaO
CO
SOкалия
3
2
неполярная
оксид
оксид
родниковой
ионная
H
калий
ионная
CaO
SO
натрия
бария
возможны
2SO
3 3 все
















 chemistry
chemistry








