Similar presentations:
Раздел 2. Органическая химия. Тема 2.1. Теоретические основы органической химии
1.
Раздел 2.Органическая химия
Лекция
Тема 2.1.Теоретические
основы органической химии
2.
Состав органических веществОрганические вещества отличаются от неорганических
тем, что в их состав обязательно входит углерод
В настоящее время к органическим веществам относят и
такие, которые не имеют прямого отношения к живым и
растительным объектам. Более того, некоторые из них,
полученные человеком с помощью синтеза, просто не могут
существовать в живых организмах. Однако единственным
критерием всех органических соединений является
наличие в них одного или нескольких углеродных атомов.
Существуют простые вещества, которые также содержат углерод (СО, С02, соли угольной
кислоты и др.). Но эти соединения не обладают свойствами органических соединений.
3.
Состав органических веществКроме углерода органические вещества:
–почти всегда содержат водород,
–довольно часто — кислород и азот,
–несколько реже — галогены, серу, фосфор и многие
другие элементы.
Таким образом, органическая химия изучает
соединения углерода со многими элементами.
Атом углерода в органических соединениях
всегда четырехвалентен.
4.
УглеводородыЕсли в состав молекулы органического вещества входят атомы только
углерода и водорода, то такие вещества называются углеводородами. В
зависимости от количества связей между соседними атомами углерода,
различают следующие классы углеводородов:
а) насыщенные углеводороды. В молекулах данных органических веществ
все связи между углеродными атомами одинарные ( -связи), а все
остальные связи заняты (насыщены) атомам водорода (также только связи). Этот класс также называется алканами. Примером может служить
молекула метана СН4;
б) ненасыщенные углеводороды могут содержать в составе молекулы
кратные связи: двойные (алкены) СН2=СН2 этен, две двойные (алкадиены)
СН2=СН-СН=СН2 бутадиен или тройную связь (алкины) СН=СН этин;
в) ароматические углеводороды — это соединения, молекулы которых
содержат устойчивые циклические группы атомов (бензольные ядра) с
особым характером химических связей. Представителем данного класса
является бензол С6Н6.
5.
Функциональные группыУникальность атома углерода, как уже отмечалось, — это его
способность образовывать устойчивые связи с другими элементами,
причем самого широкого спектра от металлов до неметаллов.
Если связанные с атомом углерода атомы или
группы атомов определяют химические свойства
образуемых органических соединений, то такие группы
атомов называют функциональными группами (табл. 1).
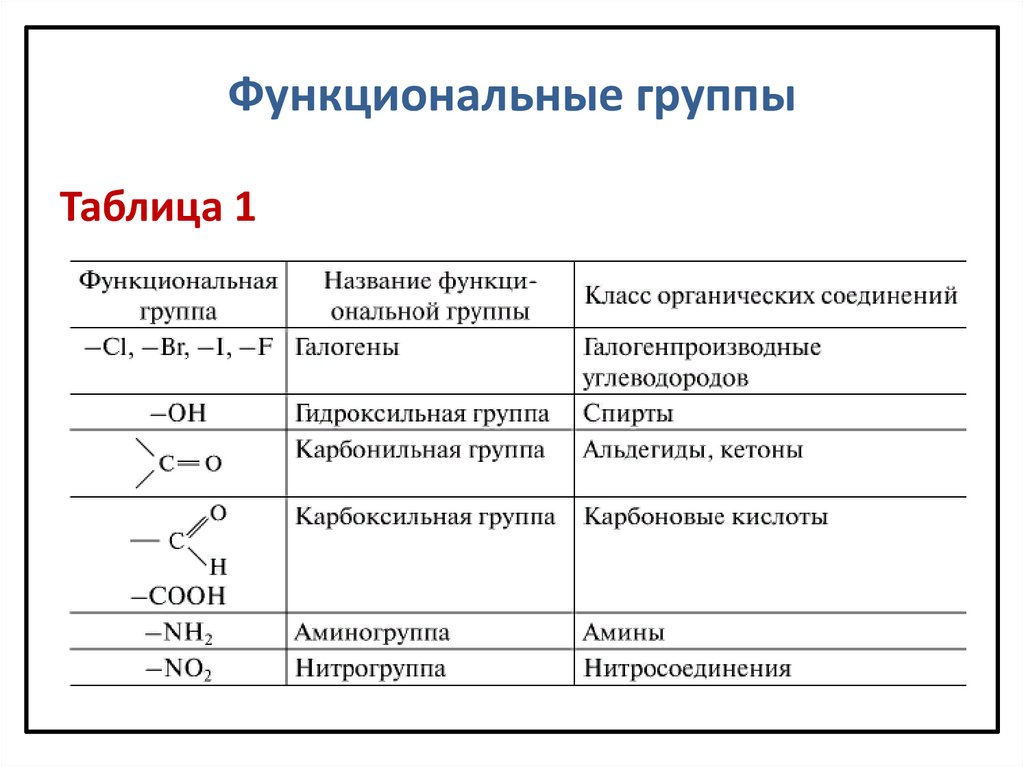
В таблице приведены примеры функциональных групп и названия
классов органических соединений, к которым относятся органические вещества,
молекулы которых содержат данные группы (чертой показано число связей,
образуемых данной группой с углеродным скелетом).
6.
Функциональные группыТаблица 1
7.
Гомологический рядГруппа органических соединений, имеющих одинаковое
строение молекулы (содержащих в составе молекулы
одинаковую функциональную группу, или одинаковое
количество кратных связей), но отличающиеся друг от друга
числом углеродных атомов в скелете, называются
гомологическим радом.
Каждый последующий член гомологического ряда
отличается от предыдущего на гомологическую разность
— СН2
8.
Теория А.М.БутлероваA.M. Бутлеров (1828—1886)
разработал теорию
химического строения
органических соединений,
объясняющую особые
свойства органических
соединений и позволяющую
прогнозировать получение
новых органических
соединений
9.
Теория А.М.Бутлерова1) атомы в молекулах соединены друг с другом химическими
связями в соответствии с их валентностью;
2) атомы в молекулах органических веществ соединяются между
собой в определенной последовательности, что обусловливает
химическое строение молекулы;
3) свойства органических соединений зависят не только от числа и
природы входящих в их состав атомов, но и от химического
строения молекул;
4)
в молекулах существует взаимное влияние атомов как
связанных, так и непосредственно друг с другом не связанных;
5) химическое строение вещества можно определить в результате
изучения его химических превращений и, наоборот, по
строению вещества можно характеризовать его свойства.
10.
Формулы строения органическихсоединений
Важным следствием теории строении был вывод о том, что каждое
органическое соединение должно иметь одну химическую формулу,
отражающую ее строение. Для изображения строения органических соединений
используются формулы строения, называемые также структурными формулами.
В структурных формулах органических соединений каждая химическая связь
обозначается чертой между химическими символами связываемых атомов.
Например, для метилового спирта можно представить единственно возможную
последовательность связей с учетом валентности связываемых атомов в виде
следующей формулы:
11.
ИзомерыОдному и тому же составу могут соответствовать два различных органических
соединения, отличающихся строением, т.е. последовательностью связи атомов.
Такими соединениями будут этиловый спирт (жидкое вещество) и диметиловый
эфир (газообразное вещество), отличающиеся физическими и химическими
свойствами.
Пример показывает проявление действия одного из основных положений теории
строения, а именно зависимости свойств веществ не только от состава, но и от
строения молекул. С другой стороны — этот пример показывает сущность
свойственного органическим соединениям важнейшего явления — изомерии (от
греч. isos — равный), т.е. возможности существования нескольких различных
веществ, обладающих различными свойствами, но имеющих при этом один и тот
же состав и одинаковую молекулярную массу.
12.
ИзомерыИзомеры — это вещества, которые имеют одинаковую
молекулярную формулу, но различное химическое строение,
а поэтому обладают разными свойствами.
Изомерия — одно из наиболее своеобразных проявлений
специфики и особенности органической химии.
13.
Изомеры (примеры)Структурная изомерия
Изомерия положения
Пространственная
изомерия












 chemistry
chemistry








