Similar presentations:
Аміни. Анілін
1.
Аміни. Анілін2.
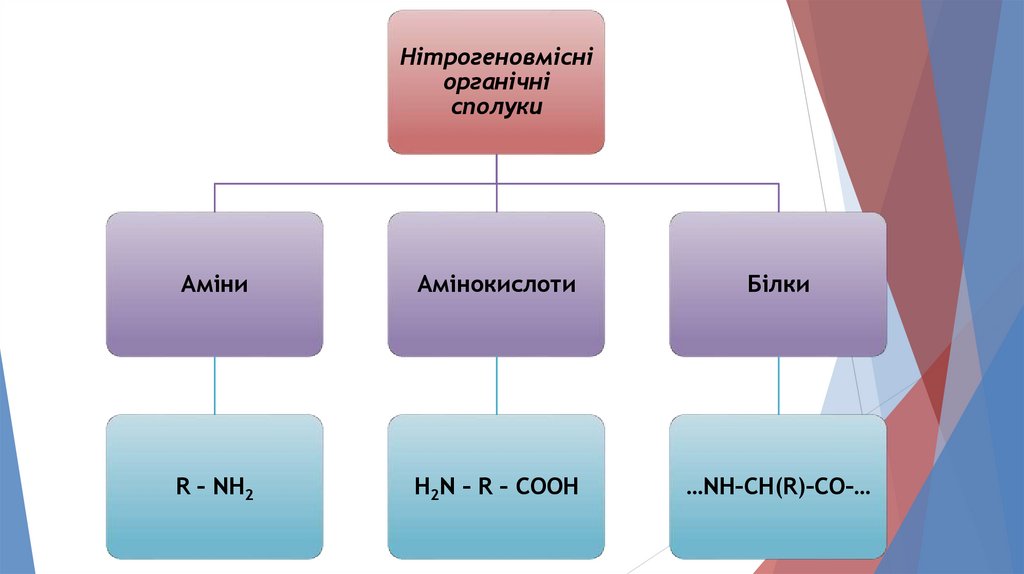
Нітрогеновмісніорганічні
сполуки
Аміни
Амінокислоти
Білки
R – NH2
H2N – R – COOH
…NH–CH(R)–CO–…
3.
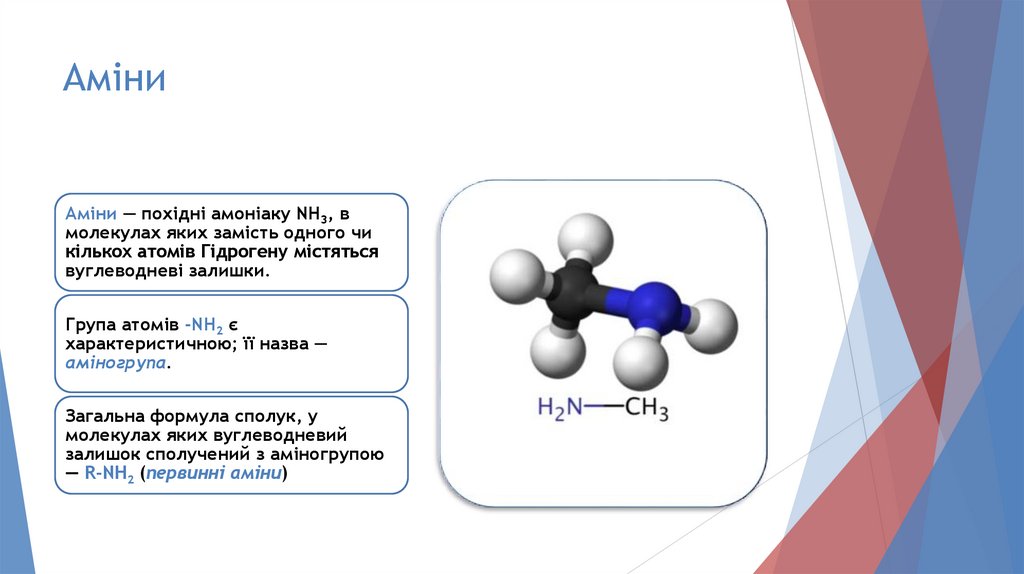
АміниАміни — похідні амоніаку NH3, в
молекулах яких замість одного чи
кількох атомів Гідрогену містяться
вуглеводневі залишки.
Група атомів -NH2 є
характеристичною; її назва —
аміногрупа.
Загальна формула сполук, у
молекулах яких вуглеводневий
залишок сполучений з аміногрупою
— R-ΝΗ2 (первинні аміни)
4.
Класифікація амінівЗалежно від
будови
вуглеводневих
залишків аміни
насичені
ароматичні
5.
Насичені аміниУ молекулі насиченого аміну аміногрупа сполучена із залишком
молекули алкану.
Загальна формула таких речовин — CnH2n+1NH2.
У молекулах амінів, зокрема метиламіну, як і в молекулі амоніаку
NH3, атом Нітрогену сполучений із трьома іншими атомами простим
ковалентним зв’язком.
Зв’язок реалізується за участю неспарених електронів зовнішнього
енергетичного рівня атома Нітрогену:
6.
Номенклатура амінівСистематична назва насиченого аміну
складається із двох частин — назви
відповідного алкану і слова амін:
CH3NH2 — метанамін, C2H5NH2 —
етанамін.
У назвах інших насичених амінів
указують номер атома Карбону, з яким
сполучена аміногрупа. Для цього
обирають найдовший карбоновий
ланцюг (до нього має бути приєднана
група -NH2) і нумерують атоми. Атому
Карбону, сполученому з аміногрупою,
надають найменший номер і записують
його перед словом амін:
3-етил-4-метилгексан-1-амін
7.
ЗавданняНазвіть амін, формула якого:
4-етил-5,6-диметилоктан-2-амін
Складіть формулу 4,5-диметил-3-пропілоктан-2-аміну
8.
Фізичні властивостіЗа звичайних умов
метанамін, етанамін і
деякі інші аміни є газами,
решта — рідини або тверді
речовини.
Газоподібні та рідкі аміни
мають різкий неприємний
запах.
Аміни з невеликими
відносними
молекулярними масами
добре розчиняються у
воді.
Температури кипіння
амінів вищі, ніж
відповідних вуглеводнів.
Це пояснюється здатністю
молекул амінів утворювати
водневі зв’язки.
9.
Хімічні властивості•Реакції з кислотами.
Хімічні
Аміни - органічні
властивості
основи
насичених
первинних •Реакції з водою
амінів
•Реакції окиснення
10.
11.
Реакції з кислотамиПід час взаємодії амінів з кислотами утворюються
солі — йонні сполуки:
CH3NH2 + HCl → [CH3NH3]Cl
метанамін
метанамоній хлорид
CH3NH2 + H+ → [CH3NH3]+
катіон метанамонію
Аміни - органічні основи
12.
Реакції з водоюПід час розчинення у воді
насичені аміни частково реагують
з нею:
Реакції окиснення
Аміни горять на повітрі й здатні
утворювати з ним вибухові
суміші.
13.
Застосування та фізіологічна дія амінівАміни
використовують у
виробництві
полімерів,
синтетичних
волокон, барвників,
лікарських
препаратів.
Багато амінів є
токсичними
речовинами.
Наприклад,
метиламін
подразнює слизові
оболонки.
Спричиняє
порушення дихання,
негативно діє на
нервову систему і
внутрішні органи.
14.
АнілінНайпростішим ароматичним аміном є анілін, або феніламін C6H5NH2.
Це — безбарвна рідина з характерним запахом, яка розчиняється у
спирті, бензені, але малорозчинна у воді.
15.
16.
17.
Хімічні властивості анілінуРеакції за участю аміногрупи
Реакція заміщення атомів Гідрогену в
бензеновому кільці
Реакції окиснення
18.
Реакції з за участю аміногрупиВзаємодія із сильними кислотами
з утворенням солей, які є
йонними сполуками, розчинними
у воді:
Реакції заміщення (за бензеновим кільцем)
Взаємодія з бромною
водою, внаслідок чого
утворюється білий,
іноді ледь жовтуватий
осад
19.
Реакції окисненняАнілін горить кіптявим полум’ям. На відміну від
бензену він легко окиснюється на повітрі,
перетворюючись на різні сполуки.
При додаванні хлорного вапна або хлорної води
(це розчин хлору у воді) до водного розчину
аніліну виникає фіалкове забарвлення, властиве
продуктам окиснення аміну. У такий спосіб можна
виявити навіть незначну кількість аніліну.
20.
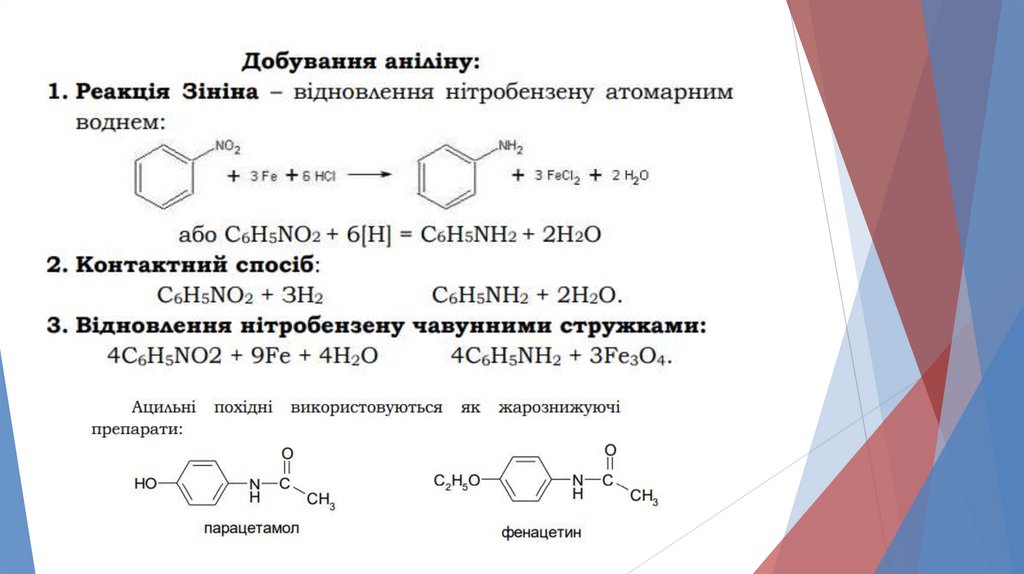
Застосування анілінуАнілін у промисловості
добувають відновленням
нітробензену
C6H5NO2 воднем за 250—350
°С та наявності
каталізатора.
Анілін є вихідною
речовиною у виробництві
багатьох його похідних —
барвників, деяких
лікарських препаратів,
полімерів, пестицидів.
Анілін — отруйна речовина.
Потрапляючи в навколишнє
середовище, він завдає
шкоди рослинам,
тваринам.
Цей амін, а також його
похідні подразнюють
слизові оболонки,
пригнічують дихання,
негативно діють на кров,
внутрішні органи, нервову
систему людини.
















 chemistry
chemistry








