Similar presentations:
Прогноз отложения сульфатов
1.
Прогноз отложения сульфатов2.
Расчет концентраций ионов• Степень насыщенности вод карбонатными и сульфатными солями
рассчитывается по уравнениям, учитывающим термобарические условия (Р-Т
условия) и химический состав вод.
• В этих уравнениях содержания компонентов выражаются в г-ион/кг, а также
учитывается ионная сила раствора.
• Результаты химических анализов, выраженные в мг/л или мг-экв/л, дополняются
расчетом молярной (грамм-ионной) формы содержания ионов Са2+ HCO3-, SO42-.
m=(C∙M1)/(1000∙M),
где m – молярная (грамм-ионная) масса;
С – эквивалентная концентрация (мг-экв/дм3 или мг-экв/кг);
М1 – эквивалент элемента;
М – молекулярная масса иона.
3.
Пример расчета концентрации Са2+1) содержание Са2+ = 53,92 мг-экв/кг.
mСа= (53,92∙20,04)/(1000∙40,08)=0,027 г-ион/кг
2) содержание Са2+ = 496 мг/кг.
mСа= 496/(1000∙40,08)=0,012 г-ион/кг
• Аналогично ведется расчет для остальных ионов
4.
Ионная сила раствораПрисутствие в растворе других ионов, даже не участвующих в данной химической
реакции, влияет на химическое равновесие. Это влияние учитывают с помощью
параметра, который называется «ионная сила раствора»
Ионная сила раствора - мера интенсивности электрического поля создаваемого ионами
в растворе; При увеличении ионной силы коэффициенты активности ионов снижаются,
при этом чем больше заряд иона, тем больше это уменьшение.
Расчет ионной силы воды потребуется при вычислении прогнозной оценки выпадения
солей в условиях разных температур и давлений.
Рассчитываем по формуле:
C 2 C 3 C
1
2
3
2 1000
где ΣС1, ΣС2, ΣС3 - сумма концентраций одно-, двух- и трехвалентных ионов, (мгэкв/кг).
5.
Прогноз выпадения сульфатовпо методу Дж. Е. Оддо и М.Б. Томсона, 1998
Насыщенность воды сульфатами кальция (СаSО4 – ангидрит, СаSО4 ∙2Н2О – гипс ), стронция
(SrSO4) и бария (BaSO4) определяется по индексу насыщения – SI:
SI lg
[ Kt 2 ][ An
2
]
K
где [Kt 2+] x [An 2-] - произведение г-ионных концентраций солеобразующих катиона и аниона,
K - константа произведения растворимости при равновесном состоянии, которую в
зависимости от термобарических условий и ионной силы раствора (µ) предлагается
определять по соотношению:
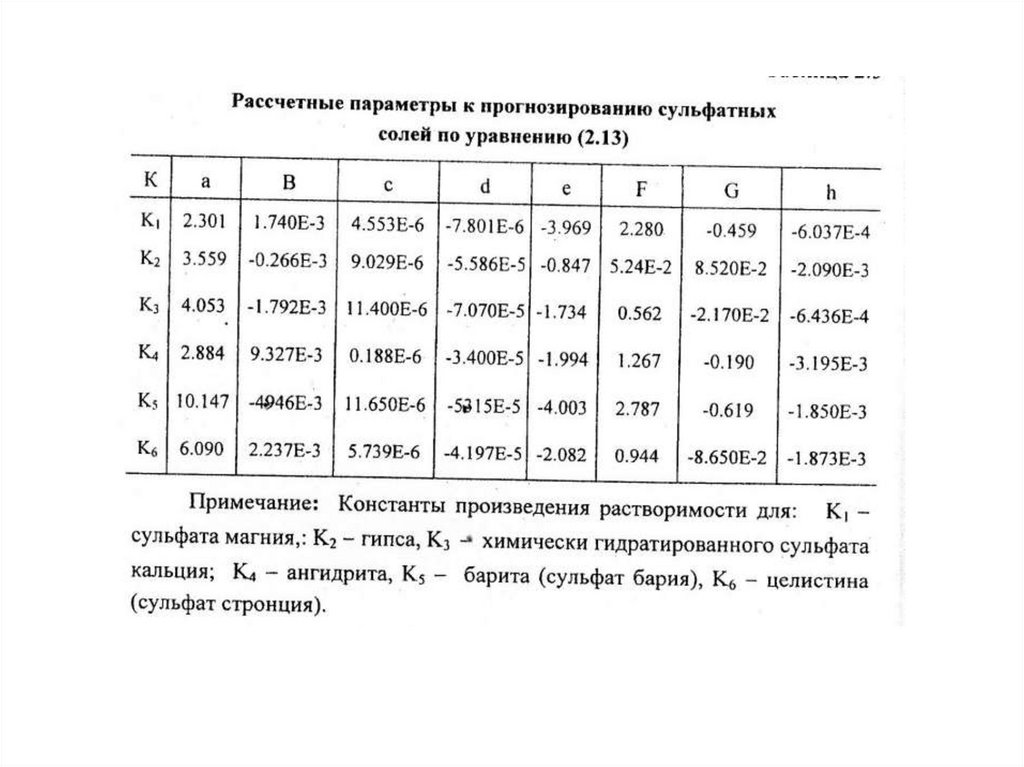
• -lg(K)= a+bT+cT2+dP+eµ0.5+fµ+gµ1.5+hTµ0.5
где, µ - ионная сила раствора; Т - температура ° F (в градусах Фаренгейта); Р - давление, psi,
a, b, c, d, e, f, g, h - эмпирические коэффициенты (из специальных таблиц)
При SI < 0 нет угрозы выпадения сульфата
При SI >0 есть угроза выпадения сульфата
6.
Расчет содержания ионов, значения температурыи формы выделения сульфата в смеси вод
При прогнозе солеотложения аналитическими методами составляется смесь
пластовой и закачиваемой воды с шагом 10%
Содержание отдельных ионов в смеси вод рассчитывается просто по
механическим пропорциям смешения, так же как значение температуры
Температурные диапазоны образования сульфатно-кальциевых отложений
для различных модификаций солей различны: до 50оС выпадает гипс, а после
60оС – ангидрит. Это надо учитывать в расчете
Давление (Р) меняется не в соответствии с пропорциями смешения, а по
достаточно сложной зависимости, которую в аналитическом прогнозе учесть
невозможно, поэтому пользуются ориентировочными показателями.
В учебном задании брать просто значение пластового давления
7.
8.
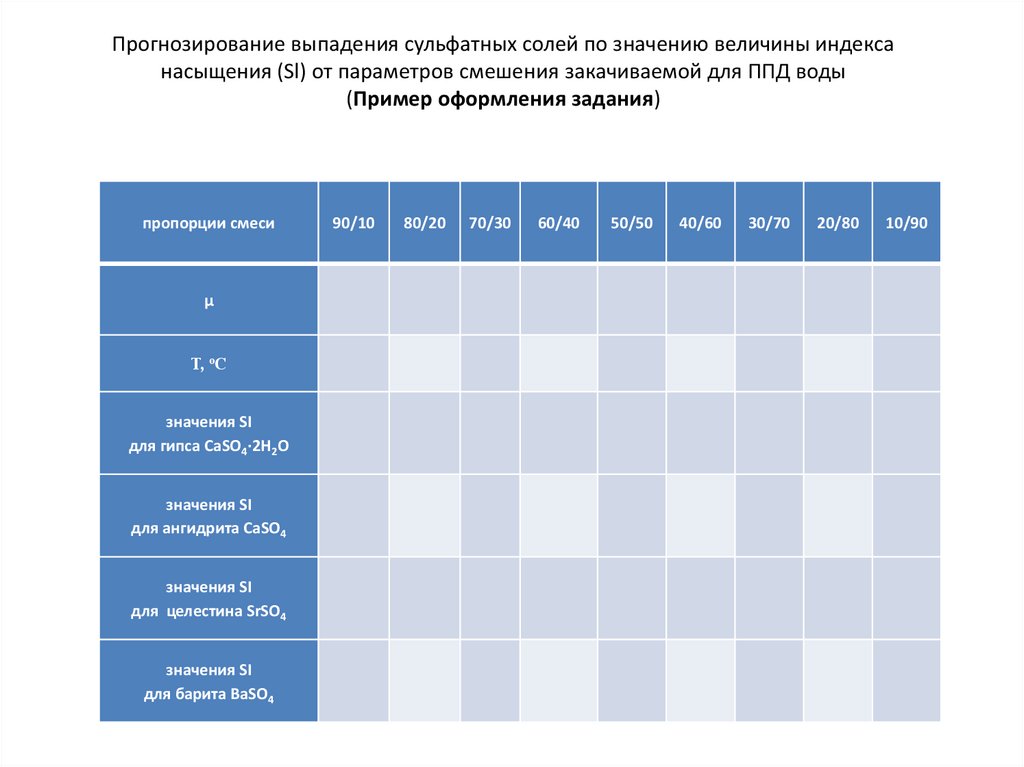
Прогнозирование выпадения сульфатных солей по значению величины индексанасыщения (Sl) от параметров смешения закачиваемой для ППД воды
(Пример оформления задания)
пропорции смеси
μ
Т, оС
значения SI
для гипса CaSO4∙2H2O
значения SI
для ангидрита CaSO4
значения SI
для целестина SrSO4
значения SI
для барита BaSO4
90/10
80/20
70/30
60/40
50/50
40/60
30/70
20/80
10/90






 chemistry
chemistry








