Similar presentations:
Основания
1.
Основания.2. План изучения темы:
1. Состав, названия иопределение оснований.
2. Классификация оснований.
3. Физические свойства
оснований.
4. Химические свойства
оснований.
3.
Основания– это сложные вещества,
состоящие из атома
металла и одной или
нескольких
гидроксогрупп.
4. Состав оснований: Назовите составные части оснований.
СО гидроксогруппы (ОН) – 1Количество гидроксогрупп определяется СО металла,
образующего основание.
Ме(ОН)х
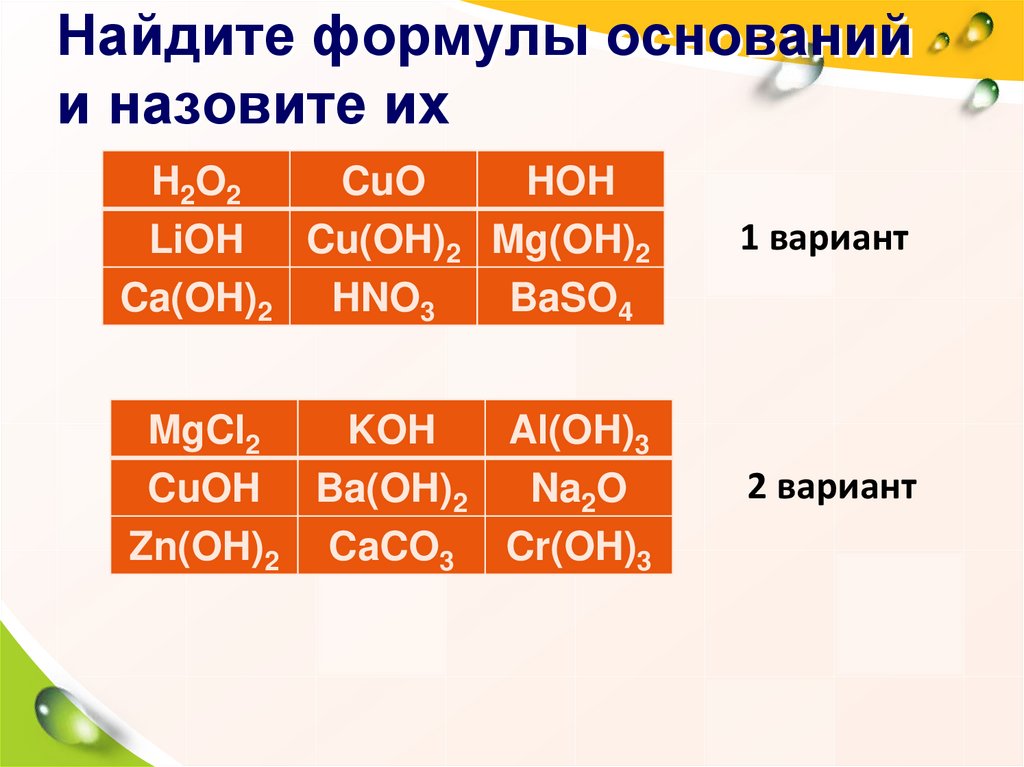
5. Найдите формулы оснований и назовите их
H2O2CuO
HOH
LiOH
Cu(OH)2 Mg(OH)2
Ca(OH)2 HNO3
BaSO4
1 вариант
MgCl2
KOH
Al(OH)3
CuOH Ba(OH)2
Na2O
Zn(OH)2 CaCO3 Cr(OH)3
2 вариант
6. Выберите формулы оснований. Назовите их.
НСl, NaOH, Na2O,Ca(OH)2, H2SO4,
P2O5, Fe(OH)3, MgO,
Cи(OH)2
7. Основания
NaOH – гидроксид натрияCa(OH)2 – гидроксид кальция
Fe(OH)3 – гидроксид железа (III)
Cи(OH)2 – гидроксид меди (III)
Найдите ошибку!
8.
Классификация9. Классификация оснований
1. По растворимости в водеОснования
РАСТВОРИМЫЕ
(ЩЕЛОЧИ)
НЕРАСТВОРИМЫЕ
СЛАБЫЕ
Исключение –
Mg(OH)2 – гидроксид
магния
СИЛЬНЫЕ
Исключение NH4OH –
гидроксид аммония
2. По силе
10. Классификация оснований
РастворимыеНерастворимые
(щелочи)
NaOH
KOH
Ba(OH)2
LiOH
Cu(OH)2
Al(OH)3
Ni(OH)2
Fe(OH)2
Fe(OH)3
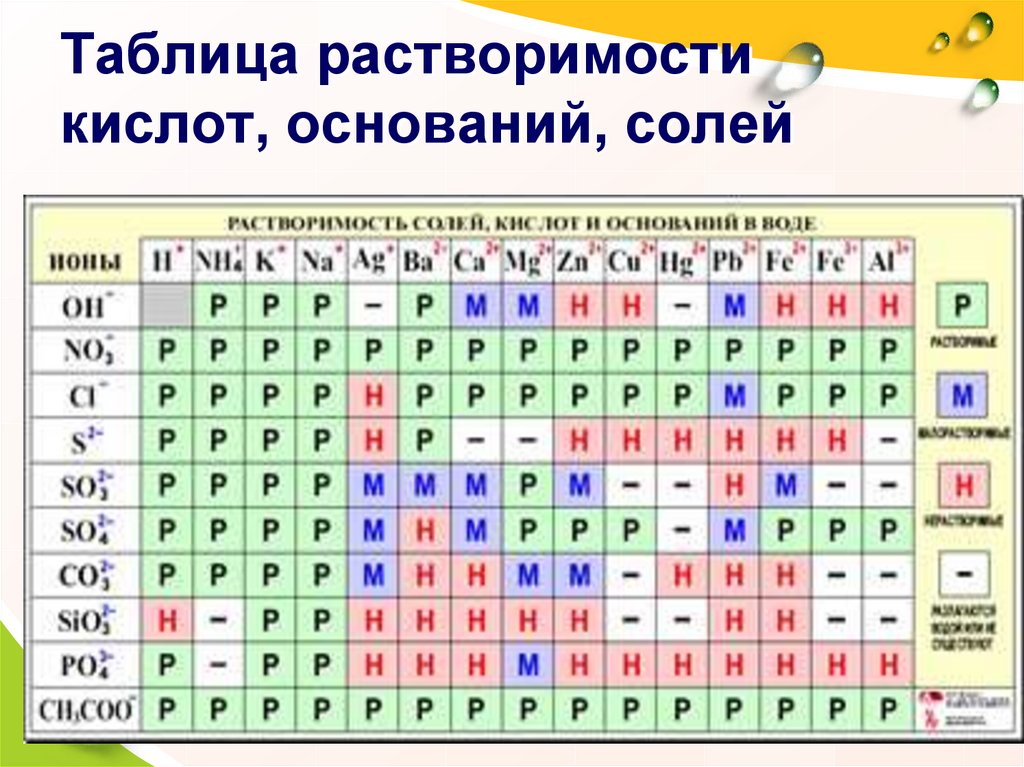
11. Таблица растворимости кислот, оснований, солей
12. По какому признаку основания разделены на группы?
?NaOH
KOH
LiOH
СsOH
?
Cu(OH)2
Ba(OH)2
Pb(OH)2
Fe(OH)2
?
Al(OH)3
Fe(OH)3
13. Классификация оснований
3.По кислотности (числу гидроксидионов ОН-)Основания
Однокислотные
MeOH
Двухкислотные
Me(OH)2
Трехкислотные
Me(OH)3
Найдите формулы оснований и разделите их по
группам:
NaOHHClCuOHFeCl2Ba(OH)2CO2Mg(OH)2Na2SAl(OH)3
Cu(OH)2SCaONa2SO4LiOHHNO3Cr(OH)3
14. Классификация оснований по числу гидроксогрупп.
ОснованияОднокислотные NaOH, KOH
Двухкислотные
Pb(OH)2, Fe(OH)2
Трехкислотные
Al(OH)3
15.
Физическиесвойства
16. Физические свойства оснований
Агрегатное состояние:Все твердые вещества
• Цвет :
Белого – КОН,
Голубого - Cu(OH)2
Красно-бурого - Fe(OH)3
КОН
Cu(OH)2
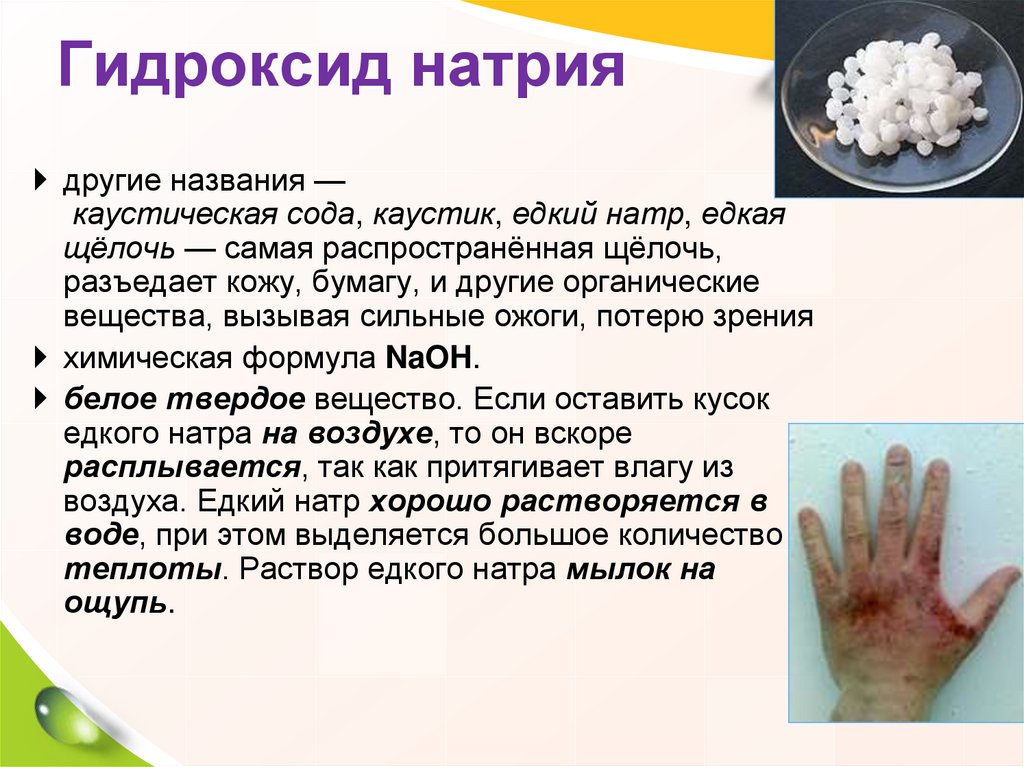
17. Гидроксид натрия
другие названия —каустическая сода, каустик, едкий натр, едкая
щёлочь — самая распространённая щёлочь,
разъедает кожу, бумагу, и другие органические
вещества, вызывая сильные ожоги, потерю зрения
химическая формула NaOH.
белое твердое вещество. Если оставить кусок
едкого натра на воздухе, то он вскоре
расплывается, так как притягивает влагу из
воздуха. Едкий натр хорошо растворяется в
воде, при этом выделяется большое количество
теплоты. Раствор едкого натра мылок на
ощупь.
18. Едкий натр применяется во множестве отраслей промышленности и для бытовых нужд:
Едкий натр применяется во множествеотраслей промышленности и для бытовых
нужд:
в целлюлозно-бумажной промышленности в
производстве бумаги, картона, искусственных волокон,
древесно-волоконных плит
Для омыления жиров при производстве мыла, шампуня и
других моющих средств
В химических отраслях промышленности
В гражданской обороне для
нейтрализации отравляющих веществ
19.
Химическиесвойства
20. Химические свойства нерастворимых оснований.
1). Разлагаются принагревании.
2). Взаимодействуют с
кислотами (реакция
нейтрализации).
21. Химические свойства щелочей.
1). Изменяют окраскуиндикаторов.
Взаимодействуют с:
2). кислотами (реакция
нейтрализации),
3). кислотными оксидами,
4). солями.
22.
23.
ПРАВИЛА БЕЗОПАСНОСТИЕдкое вещество—щелочь!
Разрушает и раздражает
кожу, слизистые оболочки.
Попавшие на кожу капли раствора
щелочи немедленно смойте
сильной струей холодной воды, а
затем обработайте поврежденную
поверхность 1% раствором
уксусной кислоты.
24.
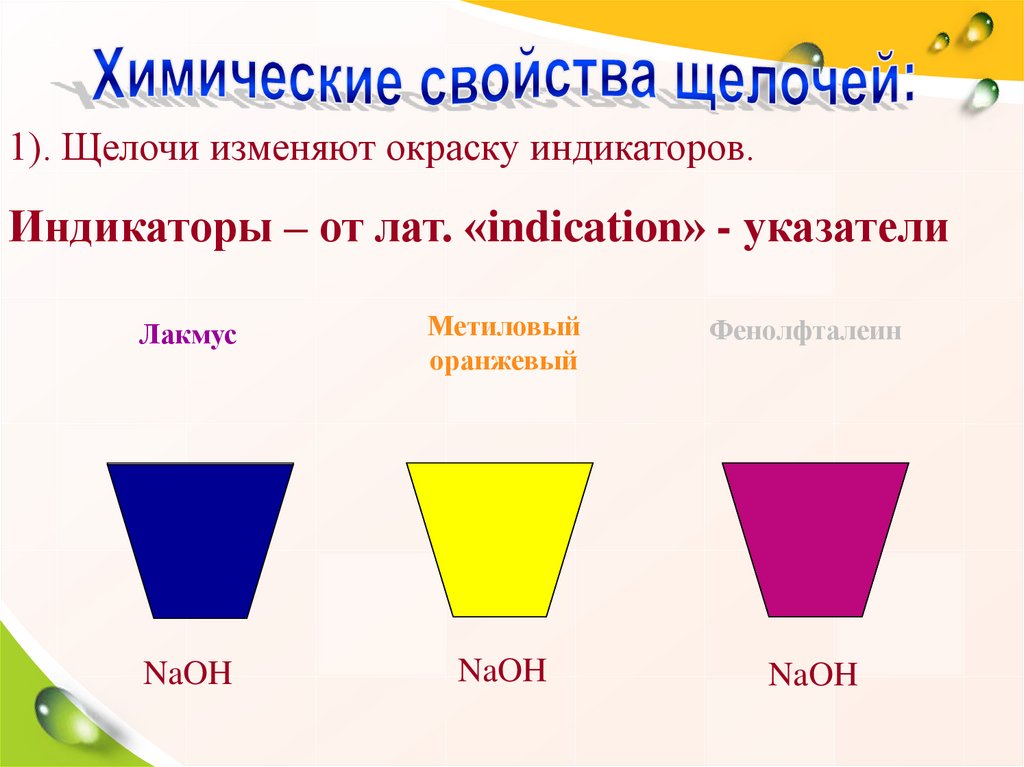
1). Щелочи изменяют окраску индикаторов.Индикаторы – от лат. «indication» - указатели
Лакмус
Метиловый
оранжевый
Фенолфталеин
NaOH
NaOH
NaOH
25.
2. Щелочь + кислота :Ва(ОН)2 + 2НСl = ВаСl2 + 2Н2О
хлорид бария
26.
3. Щелочь + кислотный оксид:В ходе реакции образуется соль и вода
Для написания реакции необходимо знать,
какая кислота соответствует кислотному оксиду.
27.
28. Условия протекания реакции: 1). исходные вещества должны быть растворимыми 2). образование осадка
4. Щелочь + соль =Условия протекания реакции:
1). исходные вещества должны быть
растворимыми
2). образование осадка
29.
Д/З § 31,выполнить задания со
слайдов
L/O/G/O
30. Выполните задание. Допишите уравнения реакций. Назовите вещества.
1). NaOH + H2SO4 =2). NaOH + SO3 =
3). NaOH + CuSO4 =
4). NaOH + фенолфталеин =
t
5). Mg(OH)2 =
6). КOH + HNO3 =
7). KOH + N2O5 =
8). KOH + Cu(NO3)2 =
9). KOH + лакмус =
t
10). Pb(OH)2 =


























 chemistry
chemistry








