Similar presentations:
Организация и проведение производственного контроля за соблюдением санитарных правил
1. Требования к организации производственного контроля на коммунальных объектах.
2. Правовые основы
• №52-ФЗ «О санитарноэпидемиологическом благополучиинаселения» ст.32
3. Ст. 32 Производственный контроль
Ст. 32 Производственный контроль• 1. Производственный контроль, в том числе проведение
лабораторных исследований и испытаний, за соблюдением
санитарно-эпидемиологических требований и выполнением
санитарно-противоэпидемических
(профилактических)
мероприятий
в
процессе
производства,
хранения,
транспортировки и реализации продукции, выполнения работ
и оказания услуг, а также условиями труда осуществляется
индивидуальными предпринимателями и юридическими
лицами в целях обеспечения безопасности и (или)
безвредности для человека и среды обитания таких
продукции, работ и услуг.
4. Ст. 32 Производственный контроль
• 2. Производственный контроль осуществляется впорядке, установленном техническими регламентами
или применяемыми до дня вступления в силу
соответствующих технических регламентов санитарными
правилами, а также стандартами безопасности труда,
если иное не предусмотрено федеральным законом
• 3. Лица, осуществляющие производственный контроль,
несут ответственность за своевременность, полноту и
достоверность его осуществления.
5. Правовые основы
• СП 1.1.1058-01 (ред. изм и доп №1 от27.03.2007 «Организация и проведение
производственного
контроля
за
соблюдением санитарных правил и
выполнением
санитарнопротивоэпидемических
(профилактических) мероприятий»
6. СП 2.1.3678-20 "Санитарно-эпидемиологические требования к эксплуатации помещений, зданий, сооружений, оборудования и
СП 2.1.3678-20 "Санитарно-эпидемиологические требования кэксплуатации помещений, зданий, сооружений, оборудования
и транспорта, а также условиям деятельности хозяйствующих
субъектов, осуществляющих продажу товаров, выполнение
работ или оказание услуг"
• хозяйствующий субъект в соответствии с осуществляемой им
деятельностью по предоставлению услуг населению должен
осуществлять производственный контроль за соблюдением
санитарных правил и гигиенических нормативов, санитарнопротивоэпидемические (профилактические) мероприятия, с
проведением лабораторных исследований и измерений с
привлечением испытательных лабораторных центров,
аккредитованных в национальной системе аккредитации в
соответствии с законодательством Российской Федерации
(п.2.1)
7. СП 2.2.3670-20 «Санитарно-эпидемиологические требования к условиям труда»
• юридические лица и индивидуальные предпринимателиобязаны осуществлять производственный контроль за
условиями труда; разрабатывать и проводить санитарнопротивоэпидемические (профилактические) мероприятия,
предусмотренные санитарными правилами (п.1.4).
• По результатам проведения производственного контроля и
специальной оценки условий труда хозяйствующим субъектом
должен быть разработан и выполняться в установленные им
сроки перечень мероприятий по улучшению условий труда,
направленных на снижение рисков для здоровья человека в
части профессиональных заболеваний, заболеваний
(отравлений) и инфекционных заболеваний, связанных с
условиями труда (п.1.7).
8. СанПиН 2.3/2.4.3590-20 «Санитарно-эпидемиологические требования к предприятиям общественного питания населения»
СанПиН 2.3/2.4.3590-20 «Санитарноэпидемиологические требования к предприятиямобщественного питания населения»
• предприятия общественного питания должны
проводить производственный контроль, основанный
на принципах ХАССП в соответствии с порядком и
периодичностью (включая организационные
мероприятия, лабораторные исследования и
испытания), установленные предприятием
общественного питания (п.2.1).
9.
• 2.1. КОММУНАЛЬНАЯ ГИГИЕНА• МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
• ПО
ОБЕСПЕЧЕНИЮ
САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКИХ
ТРЕБОВАНИЙ
• К ЭКСПЛУАТАЦИИ ПОМЕЩЕНИЙ, ЗДАНИЙ, СООРУЖЕНИЙ,
ОБОРУДОВАНИЯ
• И ТРАНСПОРТА, А ТАКЖЕ УСЛОВИЯМ ДЕЯТЕЛЬНОСТИ
ХОЗЯЙСТВУЮЩИХ
• СУБЪЕКТОВ, ОСУЩЕСТВЛЯЮЩИХ ПРОДАЖУ ТОВАРОВ,
ВЫПОЛНЕНИЕ
• РАБОТ ИЛИ ОКАЗАНИЕ УСЛУГ
• МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
• МР 2.1.0247-21
10. МР 2.1.0247-21
• 2.2.2. Порядок проведения производственногоконтроля, в том числе местоположение точек контроля,
перечень исследуемых параметров, веществ,
периодичность контроля определяется хозяйствующим
субъектом с учетом осуществляемого им вида
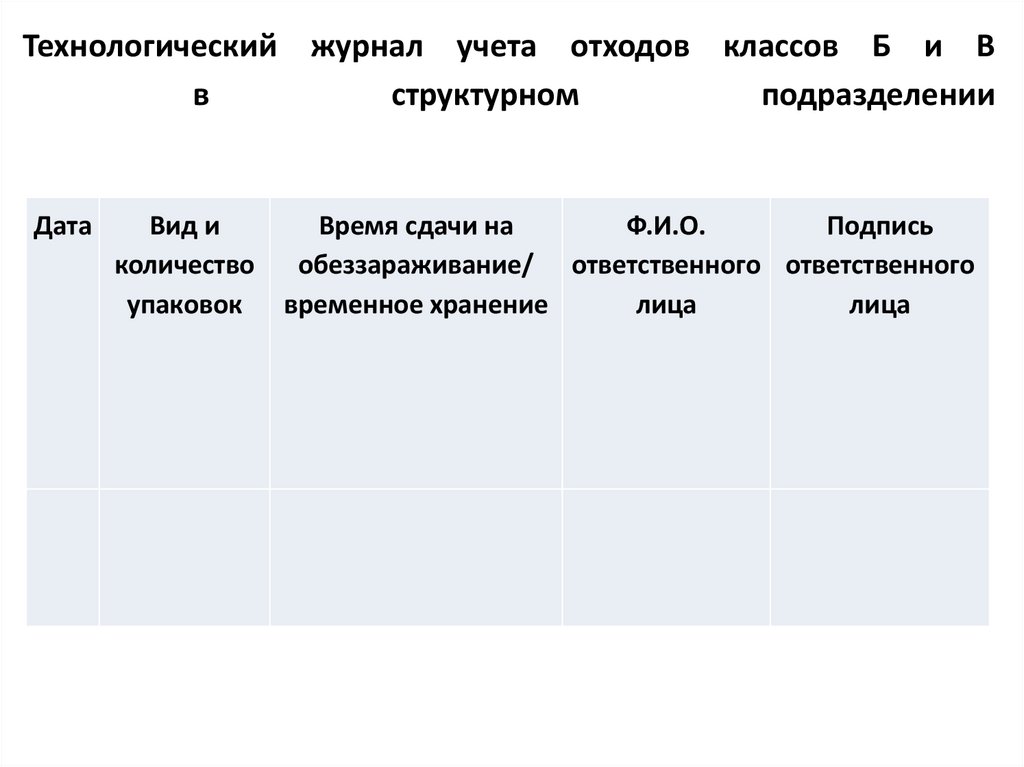
деятельности и связанных с ним возможных
негативных последствий для сотрудников, посетителей
и лиц, находящихся/проживающих в зоне влияния
данного объекта (за исключением тех видов
деятельности, для которых порядок осуществления
производственного контроля регламентирован
конкретными санитарно-эпидемиологическими
требованиями (бассейны, объекты водоснабжения и
др.).
11.
• 2.2.4. Программа производственного контроля разрабатывается сучетом специфики вида деятельности объектов, для каждого из
которых имеются свои "критические точки контроля": для
объектов, связанных с выделением загрязняющих веществ лабораторные исследования качества атмосферного воздуха, для
салонов красоты - оценка качества обработки инструментария,
для объектов торговли - наличие и достоверность документов,
подтверждающих качество и безопасность продукции, и т.д.
Кроме того, объектом производственного контроля для всех
перечисленных видов объектов будет являться контроль за
сроками
прохождения
медицинских
осмотров,
профилактической вакцинации и гигиенической аттестации,
визуальный контроль за соблюдением требований санитарных
правил и норм на объекте, в том числе на предмет
заселенности объекта населенными и грызунами. Перечень
"критических точек контроля" этим не ограничивается и
полностью зависит от характеристик объекта и осуществляемого
12.
• Необходимость прохождения периодическихмедицинских осмотров и
иммунопрофилактики и гигиенической
аттестации работниками регламентирована
СанПиН 3.3686-21 "Санитарноэпидемиологические требования по
профилактике инфекционных болезней"), а
также ст. 34, 35 и 36 Федерального закона от
30.03.1999 N 52-ФЗ "О санитарноэпидемиологическом благополучии
населения".
13.
Порядок прохождения медицинских осмотров определяетсяприказом Минздрава от 28.01.2021 N 29н "Об утверждении Порядка
проведения обязательных предварительных и периодических
медицинских осмотров работников, предусмотренных частью
четвертой статьи 213 Трудового кодекса Российской Федерации,
перечня медицинских противопоказаний к осуществлению работ с
вредными и (или) опасными производственными факторами, а
также работам, при выполнении которых проводятся обязательные
предварительные и периодические медицинские осмотры" и
совместным приказом Минтруда России и Минздрава России от
31.12.2020 N 988н/1420н "Об утверждении перечня вредных и (или)
опасных производственных факторов и работ, при выполнении
которых проводятся обязательные предварительные медицинские
осмотры при поступлении на работу и периодические медицинские
осмотры"
14.
• Порядок проведения иммунопрофилактикирегламентируется - Федеральным законом
от 17.09.1998 N 157-ФЗ "Об
иммунопрофилактике инфекционных
болезней", национальным и
региональными календарями прививок.
15.
• Требования к прохождению гигиеническойаттестации отдельных категорий
работников установлены приказом
Минздрава России от 29.06.2000 N 229 "О
профессиональной гигиенической
подготовке и аттестации должностных лиц
и работников организаций".
16.
• Ответственность за непрохождениемедицинских осмотров, профилактической
вакцинации, гигиенической аттестации, так
же, как за невыполнение иных санитарнопротивоэпидемических мероприятий,
предусмотрена ст. 6.3 Кодекса Российской
Федерации об административных
правонарушениях.
17.
• Разработаннаяпрограмма
(план)
производственного
контроля
утверждается
руководителем организации, индивидуальным
предпринимателем либо уполномоченными в
установленном порядке лицами.
• Мероприятия по проведению производственного
контроля осуществляются юридическими лицами и
индивидуальными
предпринимателями.
Ответственность за своевременность организации,
полноту
и
достоверность
осуществляемого
производственного контроля несут юридические
лица, индивидуальные предприниматели.
18.
• Юридические лица и индивидуальныепредприниматели представляют
информацию о результатах
производственного контроля по запросам
органов, уполномоченных осуществлять
государственный санитарноэпидемиологический надзор.
19.
• Отсутствие программы производственного контроляявляется административным правонарушением
подпадающим под статью 6.3 КоАП РФ КоАП РФ «
Нарушение законодательства в области обеспечения
санитарно-эпидемиологического благополучия
населения», в соответствии с которой
нарушение законодательства в области обеспечения
санитарно-эпидемиологического благополучия
населения, выразившееся в нарушении действующих
санитарных правил и гигиенических нормативов,
невыполнении санитарно-гигиенических и
противоэпидемических мероприятий, -
20.
• влечет предупреждение или наложениеадминистративного штрафа на граждан в
размере от ста до пятисот рублей; на
должностных лиц - от пятисот до одной
тысячи рублей; на лиц, осуществляющих
предпринимательскую деятельность без
образования юридического лица, - от пятисот
до одной тысячи рублей или
административное приостановление
деятельности на срок до девяноста суток; на
юридических лиц - от десяти тысяч до
двадцати тысяч рублей или административное
приостановление деятельности на срок до
21.
• Юридическое лицо, индивидуальныйпредприниматель при выявлении
нарушений санитарных правил должен
принять меры, направленные на
устранение выявленных нарушений и
недопущение их возникновения, в том
числе:
• - приостановить либо прекратить свою
деятельность или работу отдельных цехов,
участков, эксплуатацию зданий,
сооружений, оборудования, транспорта,
выполнение отдельных видов работ и
оказание услуг;
22.
• - прекратить использование в производстве сырья,материалов, не соответствующих установленным
требованиям и не обеспечивающих выпуск
продукции, безопасной (безвредной) для человека,
снять с реализации продукцию, не соответствующую
санитарным правилам и представляющую опасность
для человека, и принять меры по применению
(использованию) такой продукции в целях,
исключающих причинение вреда человеку, или ее
уничтожению;
• - информировать орган, уполномоченный на осуществление
государственного санитарно-эпидемиологического надзора о
мерах, принятых по устранению нарушений санитарных
правил;
• - принять другие меры, предусмотренные действующим
23. Цель
• производственногоконтроля
обеспечение
безопасности
и
(или)
безвредности для человека и среды
обитания вредного влияния объектов
производственного
контроля
путем
должного
выполнения
санитарных
правил, санитарно-противоэпидемических
24. Требования к программе (плану) производственного контроля
• Перечень официально изданных санитарныхправил, методов и методик контроля
факторов среды обитания в соответствии с
осуществляемой деятельностью;
• Перечень должностных лиц (работников),
на которых возложены функции по
осуществлению производственного
контроля;
25.
• Перечень химических веществ,биологических, физических и иных факторов,
а также объектов производственного
контроля, представляющих потенциальную
опасность для человека и среды его обитания
(контрольных критических точек), в
отношении которых необходима организация
лабораторных исследований и испытаний, с
указанием точек, в которых осуществляется
отбор проб (проводятся лабораторные
исследования и испытания), и периодичности
отбора проб (проведения лабораторных
исследований и испытаний) ;
26.
• Перечень должностей работников,подлежащих медицинским осмотрам,
профессиональной гигиенической
подготовке и аттестации;
• Перечень осуществляемых юридическим
лицом, индивидуальным предпринимателем
работ и услуг, выпускаемой продукции, а
также видов деятельности, представляющих
потенциальную опасность для человека и
подлежащих санитарно-эпидемиологической
оценке, сертификации, лицензированию;
27.
• Мероприятия, предусматривающиеобоснование безопасности для человека и
окружающей среды продукции и технологии
ее производства, критериев безопасности и
(или) безвредности факторов
производственной и окружающей среды и
разработка методов контроля, в том числе
при хранении, транспортировке, реализации
и утилизации продукции, а также
безопасности процесса выполнения работ,
оказания услуг;
28.
• Перечень форм учета и отчетности, установленнойдействующим законодательством по вопросам,
связанным с осуществлением производственного
контроля;
• Перечень возможных аварийных ситуаций,
связанных с остановкой производства, нарушениями
технологических процессов, иных создающих угрозу
санитарно-эпидемиологическому благополучию
населения ситуаций, при возникновении которых
осуществляется информирование населения,
органов местного самоуправления, органов,
уполномоченных осуществлять государственный
санитарно-эпидемиологический надзор;
29.
• Другие мероприятия, проведение которыхнеобходимо для осуществления эффективного
контроля за соблюдением санитарных правил и
гигиенических нормативов, выполнением санитарнопротивоэпидемических (профилактических)
мероприятий. Перечень указанных мероприятий
определяется степенью потенциальной опасности для
человека деятельности (выполняемой работы,
оказываемой услуги), осуществляемой на объекте
производственного контроля, мощностью объекта,
возможными негативными последствиями нарушений
санитарных правил.
30. Производственный контроль осуществляется с применением лабораторных исследований, испытаний на следующих категориях объектов:
• а) промышленные предприятия (объекты):рабочие места, производственные помещения,
производственные площадки (территория),
граница санитарно-защитной зоны, сырье для
изготовления продукции, полуфабрикаты,
новые виды продукции производственнотехнического назначения, продукция пищевого
назначения, новые технологические процессы
отходы производства и потребления (сбор,
использование, обезвреживание,
транспортировка, хранение, переработка и
захоронение отходов).
31.
• б) водные объекты, используемые в целяхпитьевого и хозяйственно-бытового
водоснабжения и рекреационных целей,
расположенные в черте городских и сельских
поселений.
• Лабораторный контроль осуществляется за
соответствием питьевой воды требованиям
санитарных правил, а также за соответствием
водного объекта санитарным правилам и
безопасностью для здоровья человека
условий его использования.
32.
• При осуществлении фармацевтической имедицинской деятельности с целью
профилактики
инфекционных
заболеваний,
в
том
числе
внутрибольничных,
следует
предусматривать
контроль
за
соблюдением
санитарнопротивоэпидемических
требований,
дезинфекционных и стерилизационных
мероприятий;
33.
• При осуществлении деятельности, связанной свыпуском всех видов производственных,
хозяйственно-бытовых
и
поверхностных
сточных вод с территорий населенных мест,
производственных и иных объектов, следует
предусматривать лабораторный контроль за
работой очистных сооружений, составом
сбрасываемых сточных вод;
34.
• в) объекты водоснабжения (эксплуатацияцентрализованных, нецентрализованных,
домовых распределительных, автономных
систем
питьевого
водоснабжения
населения,
системы
питьевого
водоснабжения
на
транспортных
средствах);
35.
• г) общественные здания и сооружения: лечебнопрофилактические, стоматологические, клиники,кабинеты и иные здания и сооружения, в которых
осуществляется
фармацевтическая
и/или
медицинская деятельность.
• При
осуществлении
фармацевтической
и
медицинской деятельности с целью профилактики
инфекционных заболеваний, в том числе
внутрибольничных, следует предусматривать
контроль
за
соблюдением
санитарнопротивоэпидемических
требований,
дезинфекционных
и
стерилизационных
мероприятий;
36.
• д) при производстве дезинфекционных,дезинсекционных и дератизационных
средств, оказании дезинфекционных,
дезинсекционных и дератизационных услуг,
включая контроль за эффективностью
изготавливаемых и применяемых
препаратов, соблюдением требований при их
использовании, хранении, транспортировке,
утилизации, а также учет и контроль
численности (заселенности) грызунами и
насекомыми объектов производственного
контроля при проведении истребительных
37. Федеральный закон Российской Федерации от 7 декабря 2011 года №416-ФЗ "О водоснабжении и водоотведении"
Федеральный закон Российской Федерации от 7 декабря 2011года №416-ФЗ "О водоснабжении и водоотведении"
• Статья 25. Производственный контроль качества питьевой
воды, качества горячей воды
• Порядок осуществления производственного контроля
качества питьевой воды, горячей воды устанавливается
Правительством Российской Федерации в соответствии с
законодательством Российской Федерации в области
обеспечения санитарно-эпидемиологического благополучия
населения с учетом особенностей, предусмотренных
настоящим Федеральным законом.
38. Федеральный закон Российской Федерации от 7 декабря 2011 года №416-ФЗ "О водоснабжении и водоотведении"
Федеральный закон Российской Федерации от 7 декабря 2011 года№416-ФЗ "О водоснабжении и водоотведении"
• Программа производственного контроля качества
питьевой воды, горячей воды разрабатывается
организацией, осуществляющей соответственно
холодное водоснабжение или горячее
водоснабжение, и согласовывается с
территориальным органом федерального органа
исполнительной власти, осуществляющего
федеральный государственный санитарноэпидемиологический надзор.
39.
• Постановление Правительства РФ от06.01.2015 №10 «О порядке
осуществления производственного
контроля качества и безопасности
питьевой воды, горячей воды»
• Письмо Роспотребнадзора от 23.10.2015
№01/12950-15-32 «О порядке применения
правил осуществления производственного
контроля качества и безопасности
питьевой, горячей воды»
40. ПИСЬМО РОСПОТРЕБНАДЗОРА от 13 апреля 2009 г. N 01/4801-9-32 О ТИПОВЫХ ПРОГРАММАХ ПРОИЗВОДСТВЕННОГО КОНТРОЛЯ
ПИСЬМО РОСПОТРЕБНАДЗОРАот 13 апреля 2009 г. N 01/4801-9-32
О ТИПОВЫХ ПРОГРАММАХ ПРОИЗВОДСТВЕННОГО КОНТРОЛЯ
• 1. Объекты, выполнение
• лабораторно-инструментальных исследований на которых
• в рамках производственного контроля, обязательно
1. Объекты хозяйственно-питьевого водоснабжения;
2. Бассейны, аквапарки, бани-сауны с бассейнами (купелями);
3. Зоны отдыха населения (рекреации);
4. Салоны красоты, кабинеты педикюра, маникюра, кабинеты косметики и
косметологии;
5. Прачечные, химчистки;
6. Очистные сооружения хозяйственно-бытовой канализации;
7. Полигоны ТБО;
8. Предприятия пищевой промышленности;
9. Предприятия общественного питания;
10. Организации оптовой и розничной продовольственной торговли;
11. Лечебно-профилактические учреждения;
12. Организации, осуществляющие фармацевтическую деятельность в области
оборота лекарственных средств для медицинского применения
41. Санитарно-эпидемиологические требования к бассейнам
• СП 2.1.3678-20 «Санитарноэпидемиологические требования кэксплуатации помещений, зданий, сооружений,
оборудования и транспорта, а также условиям
деятельности хозяйствующих субъектов,
осуществляющих продажу товаров,
выполнение работ и оказание услуг», утверждены
Постановлением Главного государственного санитарного врача Российской
Федерации №44 от 24 декабря 2020 г.
42. СанПиН 1.2.3685-21 «Гигиенические нормативы и требования к обеспечению безопасности и (или) безвредности для человека факторов
среды обитания»,утверждены Постановлением Главного государственного санитарного
врача№2 от 28.01.2021
43. СП 2.1.3678-20
44. СП 2.1.3678-20
45. СП 2.1.3678-20
46. СП 2.1.3678-20
47. Кратность проведения производственного контроля бассейна по СП 21.3678-20
48.
49. Санитарно-эпидемиологические требования к аптекам
• СП 2.1.3678-20 «Санитарноэпидемиологические требования кэксплуатации помещений, зданий, сооружений,
оборудования и транспорта, а также условиям
деятельности хозяйствующих субъектов,
осуществляющих продажу товаров,
выполнение работ и оказание услуг», утверждены
Постановлением Главного государственного санитарного врача Российской
Федерации №44 от 24 декабря 2020 г.
50. СанПиН 1.2.3685-21 «Гигиенические нормативы и требования к обеспечению безопасности и (или) безвредности для человека факторов
среды обитания»,утверждены Постановлением Главного государственного санитарного
врача№2 от 28.01.2021
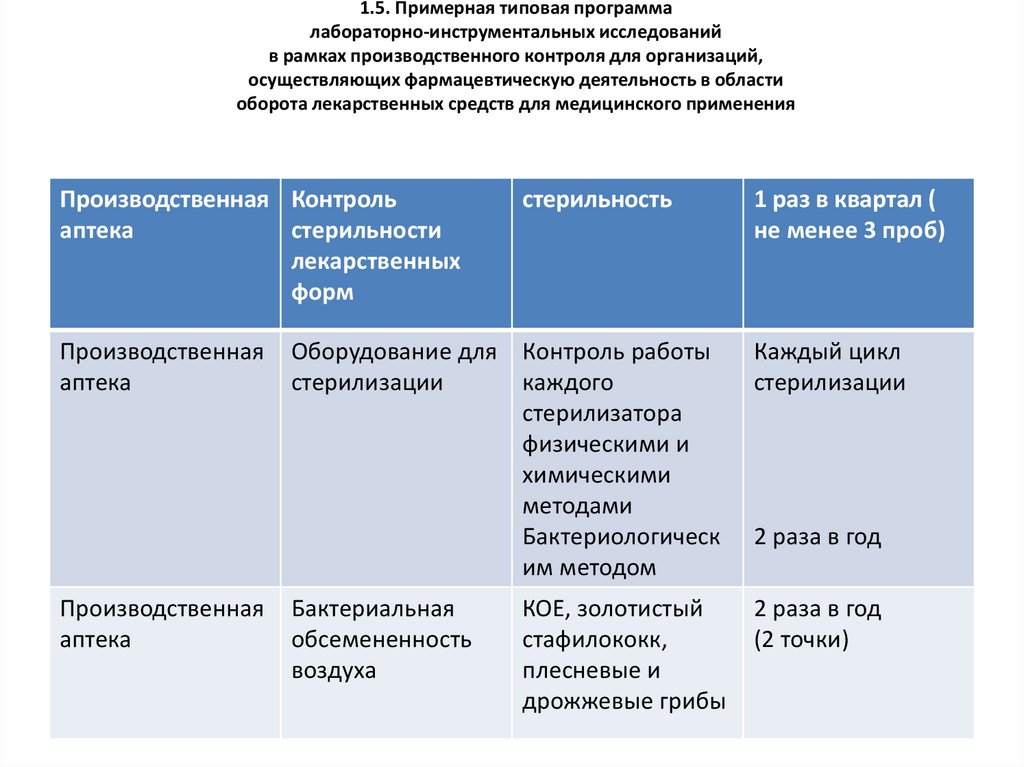
51. 1.5. Примерная типовая программа лабораторно-инструментальных исследований в рамках производственного контроля для организаций,
осуществляющих фармацевтическую деятельность в областиоборота лекарственных средств для медицинского применения
Производственная Контроль
аптека
стерильности
лекарственных
форм
Производственная
аптека
Производственная
аптека
стерильность
1 раз в квартал (
не менее 3 проб)
Оборудование для Контроль работы
стерилизации
каждого
стерилизатора
физическими и
химическими
методами
Бактериологическ
им методом
Каждый цикл
стерилизации
Бактериальная
обсемененность
воздуха
2 раза в год
(2 точки)
КОЕ, золотистый
стафилококк,
плесневые и
дрожжевые грибы
2 раза в год
52. 1.5. Примерная типовая программа лабораторно-инструментальных исследований в рамках производственного контроля для организаций,
осуществляющих фармацевтическую деятельность в областиоборота лекарственных средств для медицинского применения
Производственная Микробиологичес
аптека
кие исследования
методом смывов
(контроль
качества
дезинфекции)
Группа кишечной
палочки и
золотистый
стафилококк
2 раза в год
10-20 смывов
Производственны
е помещения
Помещения
хранения
Температура
воздуха,
относительна
влажность
2 раза в год (
теплый и
холодный
периоды)
Микроклимат
2 раза в год
Шум от
работающего
оборудования в
т.ч.
вентиляционного
Уровни звука
Уровни звукового
давления
При вводе в
эксплуатацию
При
реконструкции
53. Санитарно-эпидемиологические требования к медицинским организациям
• СП 2.1.3678-20 «Санитарноэпидемиологические требования кэксплуатации помещений, зданий, сооружений,
оборудования и транспорта, а также условиям
деятельности хозяйствующих субъектов,
осуществляющих продажу товаров,
выполнение работ и оказание услуг», утверждены
Постановлением Главного государственного санитарного врача Российской
Федерации №44 от 24 декабря 2020 г.
54. Требования к мед.отходам
• СанПиН 2.1.3684-21 «Санитарноэпидемиологические требования к содержаниютерриторий городских и сельских поселений, к
водным объектам, питьевой воде и питьевому
водоснабжению, атмосферному воздуху, почвам,
жилым помещениям, эксплуатации
производственных, общественных помещений,
организации и проведению санитарнопротивоэпидемических (профилактических)
мероприятий», утверждены Постановлением Главного
государственного санитарного врача Российской Федерации
№3 от 28.01.2021
55.
• СанПиН 3.3656-21 «Санитарноэпидемиологические требования попрофилактике инфекционных болезней»
• Утв. Постановлением Главного
государственного санитарного врача РФ №4
от 28.01.2021
56. Организация питания в МО
• СанПиН 2.3/2.4.3590-20»Санитарноэпидемиологические требования корганизации общественного питания
населения», утверждены Постановлением
Главного государственного санитарного
врача Российской Федерации №32 от
27.10.2020
57. Условия труда в МО
• СП 2.2.3670-20 «Санитарноэпидемиологические требования кусловиям труда», утверждены
Постановлением Главного государственного
санитарного врача Российской Федерации
№40 от 2 декабря 2020 г.
58. СанПиН 1.2.3685-21 «Гигиенические нормативы и требования к обеспечению безопасности и (или) безвредности для человека факторов
среды обитания»,утверждены Постановлением Главного государственного санитарного
врача№2 от 28.01.2021
59. ГОСТ Р 52539-2006
• «Чистота воздуха в лечебныхучреждениях. Общие требования»
60. 1.6. Примерная типовая программа лабораторно-инструментальных исследований в рамках производственного контроля в организациях,
осуществляющих медицинскую деятельностьА. │
Обеспечение инфекционной безопасности пациентов и персонала
Перевязочные,
Бактериальная
КОЕ, золотистый
2 раза в год ( 5
процедурные,
обсемененность
стафилококк,
точек в
хирургические
воздуха
плесневые и
стационаре)
кабинеты,
дрожжевые
эндоскопические,
грибы
процедурные
Стационары
хирургического
профиля,
родильные дома,
стоматологические
учреждения,
стационары
терапевтического
профиля.
поликлиники
Микробиологичес
кие исследования
предметов
внутрибольничной
среды методом
смывов ( контроль
качества
дезинфекции)
Группа кишечной
палочки,
золотистый
стафилококк
2 раза в год
Смывы 40-60 в
стационаре ( не
менее 5 в одном
учреждении)
Аптеки ЛПУ – 1020 смывов 2 раза в
год
Лечебнодиагностические
кабинеты и ЦСО
Изделия
медицинского
назначения (ИМН)
Контроль качества Ежедневная
предстерилизацио постановка проб
нной очистки ИМН
61. 1.6. Примерная типовая программа лабораторно-инструментальных исследований в рамках производственного контроля в
А. │1.6. Примерная типовая программа
лабораторно-инструментальных исследований
в рамках производственного контроля
в лечебно-профилактических учреждениях
Обеспечение инфекционной безопасности пациентов и персонала
Эндоскопы и
2 раза в год
инструменты к
ним, путем взятия
смывов и
смывной
жидкости
Перевязочный
материал,
инструменты,
эндоскопы,
лекарственные
формы, аптечная
посуда на
стерильная вода
Контроль
стерильности
изделий
медицинского
назначения и
лекарственных
форм
Стерильность
Лечебнодиагностические
кабинеты и ЦСО
Оборудование для Нормы загрузки
стерилизации
стерилизатора
Контроль работы
каждого
1 раз в квартал (
не менее 3 проб)
При каждой
загрузке
Каждый цикл
62.
Дезкамерный блок
Лечебнодиагностичес
кие
отделения и
кабинеты
Дезинфекционны Контроль работы
е камеры
физическими и
химическими
методами
Бактериологический
контроль (с
использованием тесткультур)
Каждый цикл
Химические
средства для
дезинфекции
1 раз в месяц
(установки для
получения растворов
дезинфицирующих
средств – в
соответствии с
инструкцией по
эксплуатации)
Определение
концентрации АДВ
(активного
действующего
вещества) в рабочих
растворах дезсредств и
соответствие
концентрации
1 раз в квартал
63.
Палатныеотделения
Бельевой
режим
Контроль за Контроль за
организацие организацией
й питания в
питания в ЛПУ
ЛПУ
Пищеблок
для
пациентов и
персонала
Камерная обработка
постельных
принадлежностей
Микробиологический
контроль качества стирки
белья собственной
прачечной путем смывов
В
терапевтически1 раз в 3 дня
1 раз в месяц
1 раз в 3 месяца
(10-15 смывов)
Контроль соблюдения
технологии изготовления и
качества готовых блюд
Контроль за наличием
сопроводительной
документации на сырье и
полуфабрикаты, контроль
качества поступающей
продукции Лабораторные
исследования готовой
продукции на калорийность,
химический состав
Микробиологическое
исследование блюд, смывов
с технологического
оборудования, рук
персонала, кухонной утвари
Ежедневно
Ежедневно
2 раза в год
(не менее 3
проб)
2 раза в год ( не
менее 3 проб
продукции, 10-20
смывов)
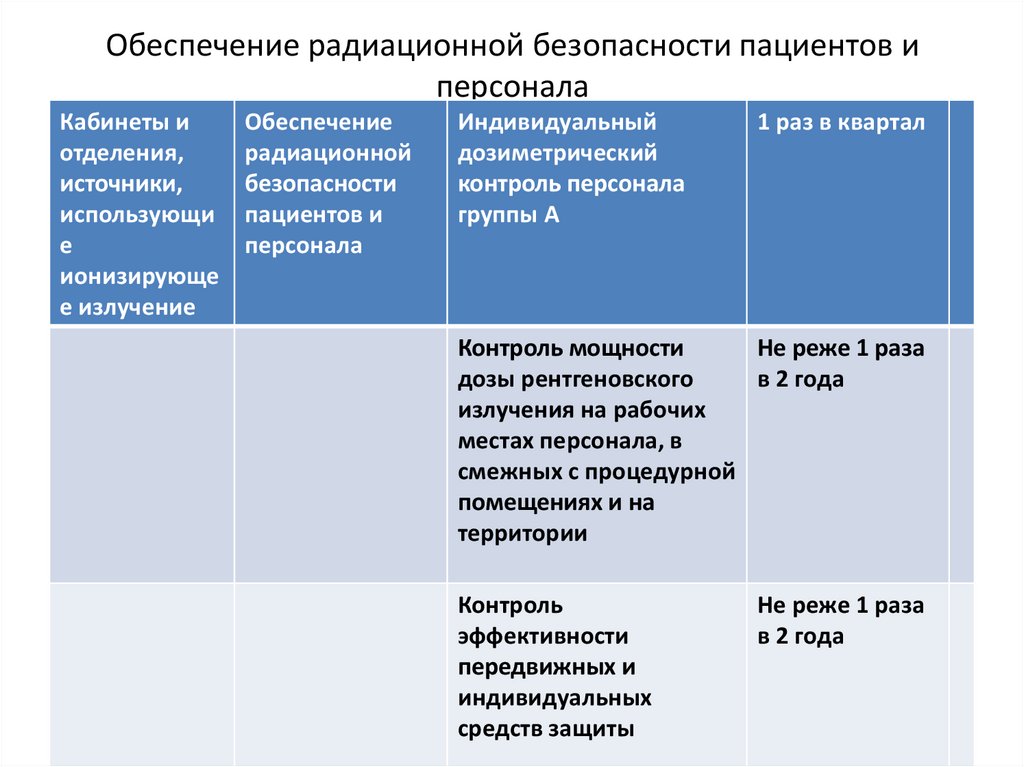
64. Обеспечение радиационной безопасности пациентов и персонала
Кабинеты иотделения,
источники,
использующи
е
ионизирующе
е излучение
Обеспечение
радиационной
безопасности
пациентов и
персонала
Индивидуальный
дозиметрический
контроль персонала
группы А
1 раз в квартал
Контроль мощности
Не реже 1 раза
дозы рентгеновского
в 2 года
излучения на рабочих
местах персонала, в
смежных с процедурной
помещениях и на
территории
Контроль
эффективности
передвижных и
индивидуальных
средств защиты
Не реже 1 раза
в 2 года
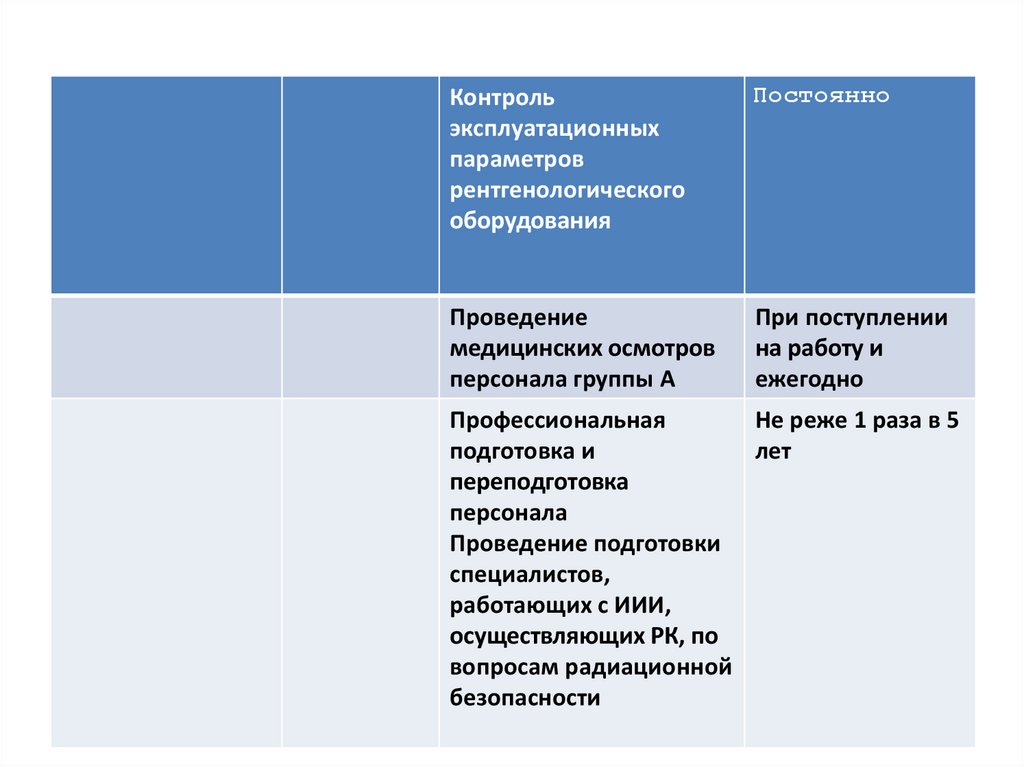
65.
Контрольэксплуатационных
параметров
рентгенологического
оборудования
Постоянно
Проведение
медицинских осмотров
персонала группы А
При поступлении
на работу и
ежегодно
Профессиональная
Не реже 1 раза в 5
подготовка и
лет
переподготовка
персонала
Проведение подготовки
специалистов,
работающих с ИИИ,
осуществляющих РК, по
вопросам радиационной
безопасности
66.
Контроль заисточниками
неионизирующих
излучений
Оценка.
регистрация и
учет дозовых
нагрузок
пациентов
При каждом
диагностическом
рентгенологическ
ом и
радиологическом
исследовании
Радиационный
контроль
пациентов при
проведении
лучевой терапии
путем введения
радиофармпрепаратов
Перед выходом из
ЛПУ
67.
ЭлектромагнитноеИзлучение(ЭМИ)
на рабочих местах
в
физиотерапевтиче
ских
диагностических
Контроль за
источниками
неионизирующих
излучений
ЭП 50 Гц,
УВЧ,СВЧ,УФ,МП
1раз в 3 года
Рабочие места в
подразделениях
магнитнорезонансной
томографии
Шум,
создаваемым
томографом
Постоянное МП
1раз в 3 года
Рабочие места с
ПЭВМ
ЭМИ от ПЭВМ
При установке
нового
оборудования
68.
Рабочие места слазерными
Лазерные установки нового
3-4 класса
оборудования
опасности
Контроль
санитарнотехнического
состояния и
содержания
учреждения
Зуботехничские
лаборатории
Операционные,
процедурные
кабинеты
Морги,ПАО, бюро
СМЭ
Исследование
На содержание
воздуха рабочей вредных
зоны
химических
веществ:
метилметакрилаты,
гипс, кремний и др.
лекарственные
средства
фенол и
формальдегид
озон
азота диоксид
1 раз в год
1 раз в 2 года
1 раз в 2 года
1 раз в 2 года
1 раз в 2 года
69.
Палаты,помещения с
постоянными
рабочими
местами и пр.
помещения с
нормируемыми
показателями
Микроклимат
Температура,
относительная
влажность,
скорость
движения воздуха
2 раза в год
(теплый и
холодный
периоды)
Палаты,
помещения с
постоянными
рабочими
местами и пр.
помещения с
нормируемыми
показателями
Освещенность
Уровни
искусственной
освещенности
1 раз в год
70. Работа с возбудителями 1-1У групп патогенности
Клиникодиагностические имикробиологичес
кие лаборатории
Работа с
возбудителями 11У групп
патогенности
Проведение
бактериологическ
ого контроля в
лаборатории
методом
исследования
смывов с
объектов
окружающей
среды
В соответствии с
планом
внутрилабораторн
ого контроля
71. Санитарно-эпидемиологические требования к медицинским организациям
• СП 2.1.3678-20 «Санитарноэпидемиологические требования кэксплуатации помещений, зданий, сооружений,
оборудования и транспорта, а также условиям
деятельности хозяйствующих субъектов,
осуществляющих продажу товаров,
выполнение работ и оказание услуг», утверждены
Постановлением Главного государственного санитарного врача Российской
Федерации №44 от 24 декабря 2020 г.
72. Мед.отходы
• СанПиН 2.1.3684-21 «Санитарноэпидемиологические требования ксодержанию территорий городских и
сельских поселений, к водным объектам,
питьевой воде и питьевому водоснабжению,
атмосферному воздуху, почвам, жилым
помещениям, эксплуатации
производственных, общественных
помещений, организации и проведению
санитарно-противоэпидемических
(профилактических) мероприятий», утверждены
Постановлением Главного государственного санитарного
врача Российской Федерации №3 от 28.01.2021 г.
73. Мед.отходы класса А
• Медицинские отходы класса А, кромепищевых, могут удаляться из структурных
подразделений организации с помощью
мусоропровода.
• Крупногабаритные медицинские отходы
класса А должны собираться медицинской
организацией в бункеры для КГО.
74. Санитарно-эпидемиологические требования условиям хранения медицинских отходов класса Б и В
• сбор в местах их образования осуществляется втечение рабочей смены. При использовании
одноразовых контейнеров для колющего и режущего
инструментария допускается их заполнение в течение
3-х суток с начала момента накопления отходов;
• хранение (накопление) более 24 часов
необеззараженных медицинских отходов класса Б и В
осуществляется в холодильных шкафах не более 7
суток или в морозильных камерах - до одного месяца
с начала момента накопления отходов;
75. Технологии утилизации, в том числе с сортировкой отходов
• только после предварительного аппаратногообеззараживания медицинских отходов класса Б и В
физическими методами
• не допускается использование вторичного сырья,
полученного из медицинских отходов, для
изготовления товаров детского ассортимента,
материалов и изделий, контактирующих с питьевой
водой и пищевыми продуктами, изделиями
медицинского назначения;
76. Размещение обезвреженных медицинских отходов класса Б и В
• на полигоне ТКО допускается только приизменении их товарного вида (измельчение,
спекание, прессование) и невозможности их
повторного применения;
77.
• персонал медицинской организацииосуществляет обеззараживание и
уничтожение вакцин.
78.
• Вывоз необеззараженных медицинскихотходов класса В, а также, относящихся к
классу Б, загрязненных и потенциально
загрязненных мокротой пациентов, лиц,
больных туберкулезом, в том числе из
лечебно-диагностических подразделений
фтизиатрических стационаров
(диспансеров), отходов микробиологических
лабораторий, осуществляющих работы с
возбудителями туберкулеза, за пределы
территории медицинский организации не
допускается
79. СанПиН 2.1.3684-21
• Производственный контроль за сбором,временным хранением, обезвреживанием
медицинских отходов включает в себя:
• Визуальную и документальную проверку (не
реже 1 раза в месяц):
• - количества расходных материалов (запас пакетов,
контейнеров и другое), средств малой механизации,
дезинфицирующих средств;
80. Производственный контроль
• визуальную и документальную проверку (нереже 1 раза в месяц):
• обеспеченности персонала средствами индивидуальной защиты,
организации централизованной стирки спецодежды и регулярной ее
смены;
• санитарного состояния и режима дезинфекции помещений временного
хранения и (или) участков по обращению с медицинскими отходами,
мусоропроводов, контейнерных площадок;
• соблюдения режимов обеззараживания, обезвреживания медицинских
отходов, средств их накопления, транспортировки, спецодежды;
• регулярности вывоза медицинских отходов.
81.
ОБ
О
Р
У
Д
О
В
А
Н
И
Е
Емкости для сбора колющих отходов
Объем:
0,7 л
Д
Л
Я
1,9 л
О
Т
Х
О
Д
О
В
3,25 л
2,5 л
Емкость-контейнер для сбора
колющих отходов ЛПУ
класса Б со специально
оборудованной крышкой для
обеспечения безопасной работы
персонала.
82.
СБОР ОТХОДОВ(сбор колющих и режущих инструментов)
83.
Тележки и баки для сбора отходовТележка для
транспортировки
бака
Бак многоразовый
с крышкой
( полиэтилен)
облегченный
стальной профиль
пластик
резина
РАЗМЕРЫ
60х50х95 см
35 л
красный, синий
84. Ответственный за обращение с отходами по учреждению
Осуществляет общее руководство
в сфере обращения с отходами.
Разрабатывает должностные
инструкции сотрудников занятых в
схеме сбора и удаления отходов.
Совместно с руководителями
структурных подразделений
больницы (отделений,
лабораторий и т.д.) определяет
места размещения пакетов,
контейнеров и межкорпусных
контейнеров для сбора всех видов
отходов, пути транспортировки
отходов;
Определяет ежемесячную
потребность медицинских
организаций в материалах,
используемых при обращении с
отходами.
• Проводит:
• Вводный инструктаж
сотрудников, вновь,
поступающих на работу
• Обучение лиц, ответственных
за обращение с отходами в
структурных подразделениях
больницы;
• Периодическую (плановую, не
реже одного раза в год) проверку
знаний персонала больницы с
принятием зачетов;
• Внеплановую проверку знаний
персонала больницы при
установлении фактов
нарушения действующих правил
и норм обращения с отходами;
85. Ответственный за обращение с отходами в подразделении
Осуществляет общее руководство по
обращению с отходами в структурном
подразделении;
Готовит совместно с ответственным
специалистом проекты должностных
инструкций для персонала своего
подразделения с учетом его специфики;
Проводит вводный инструктаж
сотрудников подразделения по вопросам
сбора, дезинфекции, упаковки и
временного хранения отходов;
Проводит периодические (плановые, не
реже двух раз в год) проверки знаний
персонала подразделения;
Определяет ежемесячную потребность
структурного подразделения в
оборудовании и материалах,
используемых при обращении с
отходами
• Обеспечивает:
• наличие необходимого
дневного запаса материалов,
используемых при обращении с
отходами;
• исправность оборудования –
правильность проведения
герметизации
ответственными
сотрудниками;
• правильность ведения учетной
документации и обобщает
данные по движению отходов в
своем структурном
подразделении;
86. Ответственный за обращение с отходами в подразделении
Осуществляет общее руководство по
обращению с отходами в структурном
подразделении;
Готовит совместно с ответственным
специалистом проекты должностных
инструкций для персонала своего
подразделения с учетом его специфики;
Проводит вводный инструктаж
сотрудников подразделения по вопросам
сбора, дезинфекции, упаковки и
временного хранения отходов;
Проводит периодические (плановые, не
реже двух раз в год) проверки знаний
персонала подразделения;
Определяет ежемесячную потребность
структурного подразделения в
оборудовании и материалах,
используемых при обращении с
отходами
• Обеспечивает:
• наличие необходимого
дневного запаса материалов,
используемых при обращении с
отходами;
• исправность оборудования –
правильность проведения
герметизации
ответственными
сотрудниками;
• правильность ведения учетной
документации и обобщает
данные по движению отходов в
своем структурном
подразделении;
87. Младший медицинский персонал
• Проводит удалениеотходов медицинских
организаций;
• Обеспечивает
наличие и исправных
контейнеров для
сбора отходов
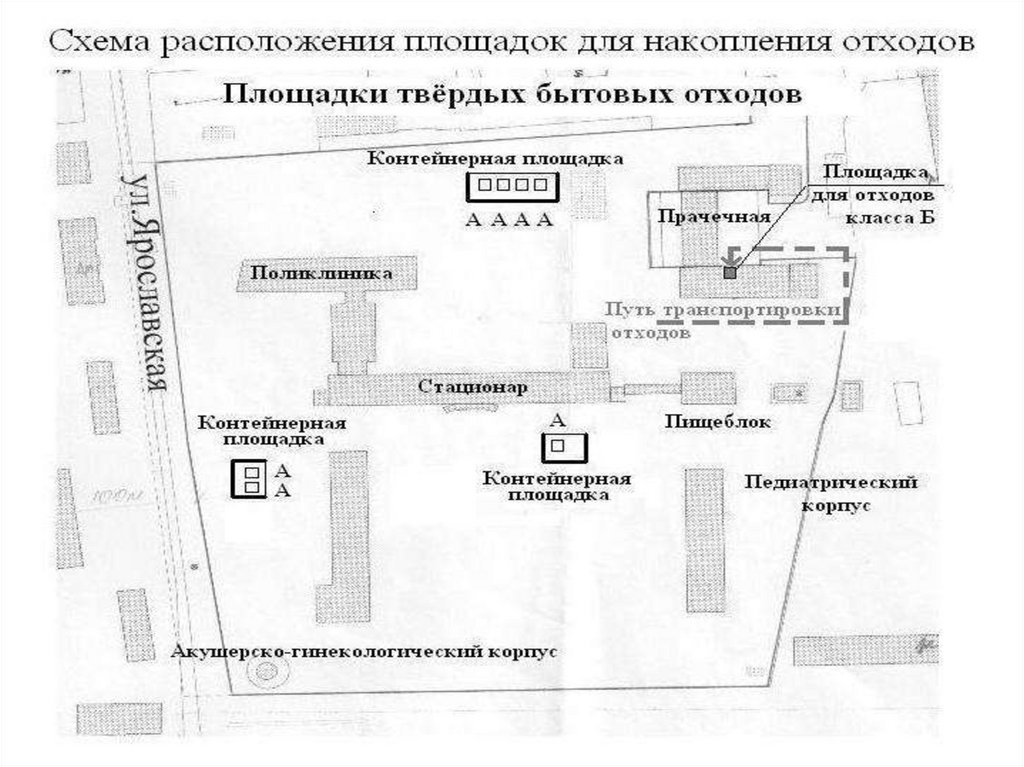
88. План расположения мест образования отходов и пути их транспортировки
89.
90.
91.
92.
93. Для учета медицинских отходов классов Б и В служат следующие документы:
• - технологический журнал учета отходовклассов Б и В в структурном
подразделении; в журнале указывается
количество единиц упаковки каждого
вида отходов;
94.
95. Технологический журнал учета отходов классов Б и В в структурном подразделении
Технологический журнал учета отходов классов Б и Вв
структурном
подразделении
Дата
Вид и
количество
упаковок
Время сдачи на
Ф.И.О.
Подпись
обеззараживание/ ответственного ответственного
временное хранение
лица
лица
96.
• - технологический журнал учета медицинских отходоворганизации. В журнале указывается количество вывозимых
единиц упаковки и/или вес отходов, а также сведения об их
вывозе с указанием организации, производящей вывоз;
• - документы, подтверждающие вывоз и обезвреживание
отходов, выданные специализированными организациями,
осуществляющими транспортирование и обезвреживание
отходов;
• - технологический журнал участка по обращению с
отходами, который является основным учетным и отчетным
документом данного участка.
97. Технологический журнал учета отходов классов Б и В организации
Технологическийклассов
журнал
Б
и
учета
отходов
В
организации
Дата Количество ед.
Вес
Наименование
вывоза
упаковки
отходов организации,
осуществляюще
й вывоз
Наименование организации ___________________________________
Сдал
(Ф.И.О. и
подпись)
Принял
(Ф.И.О. и
подпись)
98. Документация участка аппаратного обеззараживания
Технологический журнал №199.
• лабораторно-инструментальную проверку:• микробиологический контроль эффективности обеззараживания,
обезвреживания отходов на установках обеззараживания,
обезвреживания по утвержденным методикам (не реже 1 раза в год).
100. Технологический журнал участка обработки отходов классов Б и В
Наименование организации _________________________________Поступление отходов
Обработка отходов
дата
код
кол-во подписи дата, режи индикато
, подразделе ед.
врем м
ры
сдал прин
вре
ния
упаков
я
ял
мя
ки по
видам
Ф.И.О. и
подпись
ответств.
лица
101. Документация участка аппаратного обеззараживания
Технологический журнал №2102. Стикеры для обезвреженных отходов
103. Алгоритм анализа программы производственного контроля и ее выполнения
• 1. Наличие утверждения руководителеморганизации , ИП ( для питьевой воды –
согласования с Роспотребнадзором)
• 2.Наличие основных разделов,
регламентируемых СП 1.1.1058-01
• 3. Актуальность и полнота
регламентирующих документов,
фактическое наличие официально изданных
документов
104.
• Наличие перечня должностных лиц(работников), ответственных за выполнение
производственного контроля, наличие
приказов о назначении ответственных
• Наличие химических веществ,
биологических, физических факторов,
точки ,кратность – соответствие
требованиям СанПиН, СП, ГОСТ, писем
Роспотребнадзора- фактическое
подтверждение наличием договоров,
протоколов исследования
105.
• Перечень должностей работников,подлежащих медицинским осмотрам ( на
соответствие приказу Минздрава№29н,
совместный приказ Минтруда и Минздрава
№988н/1420н, СанПиН) – по факту
заключительный акт, выборочно паспорта
здоровья; профессиональной гигиенической
подготовке ( на соответствие
приказу Роспотребнадзора №402; приказу
Минздрава №229, с 01.09.2023 – приказу МЗ
№90н ) личные медицинские книжки
выборочно
106.
• Перечень осуществляемых услуг, подлежащихсертификации, лицензированию (на
соответствие №99-ФЗ, Единым санитарным
требованиям Таможенного союза, ТР ТС,ТР
ЕАЭС, )
• Мероприятия, предусматривающие
обоснование безопасности и их фактическое
подтверждение
• Перечень учета и отчетности – в соответствии
с СанПиН, СП, приказами – выборочный
контроль журналов учета, договоров,
накладных
107.
• Перечень аварийных ситуаций – приказы,№416-ФЗ, СанПиН – по каждой аварийной
ситуации адресность и сроки; анализ
фактических данных
• Другие мероприятия – фактическое
подтверждение
108. Содержание экспертного заключения
• 1. Реквизиты экспертного органа• 2. Утверждение руководителя экспертного органа
• 3. Основание для проведения экспертизы
• 4. Вопросы, поставленные перед экспертным
органом
• 5. Рассмотренные документы
• 6. Описание результатов рассмотрения
• 7. Заключение о соответствии (несоответствии )
• 8. «Реквизиты» эксперта
108





































































































 law
law life safety
life safety








