Similar presentations:
Химия фармпрепаратов. Лекция №2
1.
МИРЭА – Российский технологический университетИнститут тонких химических технологий имени
М.В. Ломоносова
Химия фармпрепаратов
(Лекция №2)
А с с и с т е н т к а ф . Х Т Б А С М и О Х , К и р и н Н.С.
2.
ХИМИОТЕРАПЕВТИЧЕСКИЕ СРЕДСТВА• Антибактериальные
• Противовирусные
• Противоопухолевые
Антибактериальные средства
• Сульфаниламидные препараты
• Антибиотики
• Синтетические антибактериальные средства разного
химического строения
3.
• Антибио́тики (от др.-греч. ἀντί — против + βίος — жизнь) — веществамикробного, животного или растительного происхождения, способные
подавлять рост определённых микроорганизмов или вызывать их гибель.
• Существуют также синтетические соединения, которые относятся к
антибиотикам, и полусинтетические антибиотики, представляющие собой
продукты частичной химической модификации природных веществ.
• Антибиотики, противоинфекционные средства и антимикробные препараты,
в основном, применяют для лечения инфекционных заболеваний, а
химиотерапевтические препараты применяются для лечения рака.
• Существуют продуцируемые микроорганизмами соединения с
противогрибковым, противоопухолевым действием, которые также
классифицируются как антибиотики.
МИК (минимальная ингибирующая концентация – эти антибиот.
останавливают рост бактерий) –
МБК(мин.бактерицидная конц.- для антибиот, которые сразу разрушают
бактериальную клетку, разрушают клеточную мембрану)
Высокие концентрации МИК могут привести к МБК
4.
1.β-Лактамные антибиотики, делящиеся на три подгруппы:
1. Пенициллины – вырабатываются колониями плесневого грибка Penicillinum;
2. Цефалоспорины – обладают схожей структурой с пенициллинами. Используются по отношению к
пенициллинустойчивым бактериям.
3. Карбапенемы – структура более устойчива к лактамазам, чем у пенициллинов и цефалоспоринов, что
значительно расширяет спектр действия.
2.
Макролиды – антибиотики со сложной циклической структурой. Действие бактериостатическое.
3.
Тетрациклины – используются для лечения инфекций дыхательных и мочевыводящих путей, лечения тяжёлых
инфекций типа сибирской язвы, туляремии, бруцеллёза. Действие – бактериостатическое.
4.
Аминогликозиды – обладают высокой токсичностью. Используются для лечения тяжёлых инфекций типа заражения
крови или перитонитов. Действие – бактерицидное.
5.
Левомицетины – использование ограничено по причине повышенной опасности серьёзных осложнений, включая
поражение костного мозга, вырабатывающего клетки крови. Действие – бактериостатическое.
6.
Гликопептидные антибиотики нарушают синтез клеточной стенки бактерий. Оказывают бактерицидное действие,
однако в отношении энтерококков, некоторых стрептококков и стафилококков действуют бактериостатически.
7.
Линкозамиды оказывают бактериостатическое действие, которое обусловлено ингибированием синтеза белка
рибосомами. В высоких концентрациях в отношении высокочувствительных микроорганизмов могут проявлять
бактерицидный эффект.
8.
Сульфаниламидные препараты – антиметаболиты, нарушающие синтез нуклеиновых кислот в бактериях.
9.
Противотуберкулёзные препараты – воздействуют преимущественно на микобактерии туберкулеза.
10. Противогрибковые антибиотики – разрушают мембрану клеток грибков и вызывают их гибель. Действие –
литическое. Постепенно вытесняются высокоэффективными синтетическими противогрибковыми препаратами.
5.
Антимикробныепрепараты
проявляют
антибактериальный эффект посредством одного из
следующих механизмов:
— ингибирование
синтеза
клеточных
стенок
микроорганизмов
(β-лактамные
антибиотики,
ванкомицин, циклосерин);
— ингибирование
синтеза
протеинов
микроорганизмов (аминогликозиды, эритромицин,
клиндамицин, хлорамфеникол и тетрациклины);
— ингибирование синтеза нуклеиновых кислот или их
функций в микроорганизмах (сульфаниламиды,
метронидазол, хинолоны и др.);
— ингибирование или изменение функций внешних
и/или
цито-плазматических
мембран
микроорганизмов (полимиксин).
6.
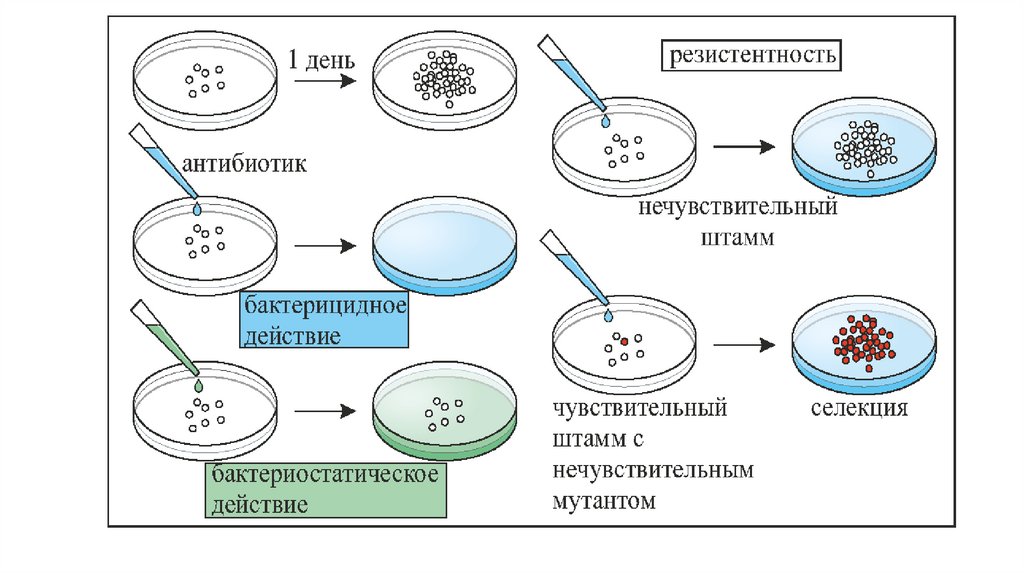
• По характеру воздействия на бактериальную клетку антибиотикиможно разделить на две группы:
• бактериостатические (бактерии остаются живы, но не в
состоянии размножаться), пример: тетрациклины,
сульфаниламиды.
• бактерицидные (бактерии погибают, а затем выводятся из
организма), пример: пенициллины.
• Бактериостатические препараты ингибируют бактериальный рост,
но не уничтожают эти организмы в клинически достижимых
концентрациях. Следует ожидать, что МБК таких препаратов
значительно выше, чем МИК.
• Бактерицидные препараты вызывают гибель микробных клеток и
их лизис в клинически достижимых концентрациях. Для этих
препаратов МБК близка или равна МИК.
7.
8.
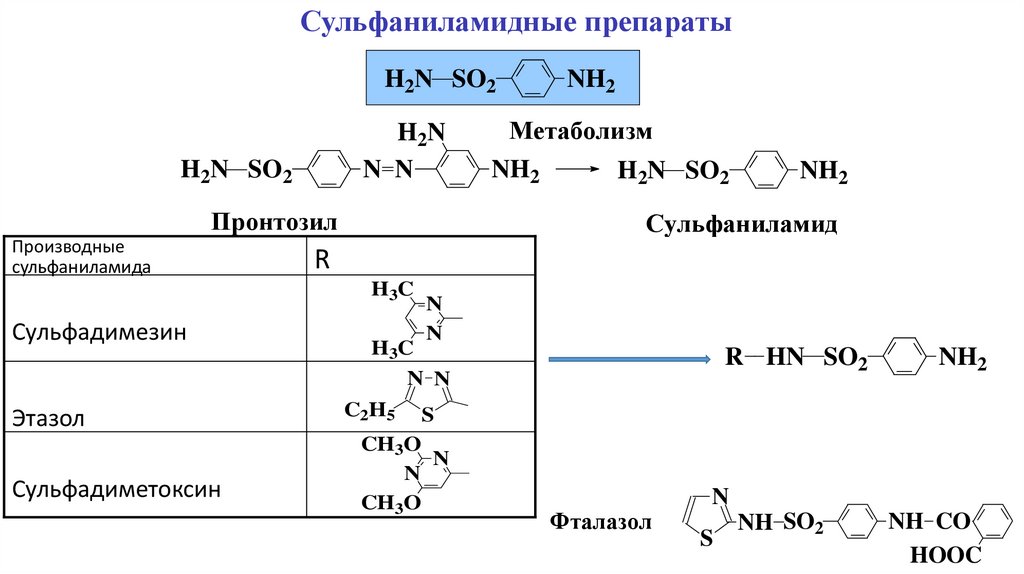
Сульфаниламидные препаратыH2N SO2
H2N
N N
H2N SO2
Пронтозил
Производные
сульфаниламида
Этазол
Сульфадиметоксин
Метаболизм
NH2
H2N SO2
NH2
Сульфаниламид
R
H 3C
Сульфадимезин
NH2
N
N
H 3C
N N
C2H5
R HN SO2
NH2
S
CH3O
N
N
CH3O
Фталазол
N
S
NH SO2
NH CO
HOOC
9.
H2NCOOH
n-аминобензойная кислота (ПАБК)
NH2
NH2
o
o
6,7A
COOH
o
2,3 A
n-аминобензойная
кислота
6,9 A
SO2NH
2
o
2,4 A
сульфаниламид
H2N N N
COOH
N N CH2 NH
CONH CH CH2CH2 COOH
H
OH
Глутаминовая кислота
Дигидроптеридинил ПАБК
10.
Локализация действия сульфаниламидов итриметоприма
Сульфаниламид
Дигидроптероат
синтетаза
ПАБК
Дигидроптеридин
Дигидроптероевая
кислота
Угнетение
ферментов
Glu
Дигидрофолиевая
кислота
Триметоприм
CH3O
CH3O
CH3O
Дигидрофолат
редуктаза
N
C H2
NH2
N
H2N
Тетрагидрофолиевая
кислота
Синтез пуринов
Конкурентный антагонизм
сульфаниламидов и ПАБК
ДНК
РНК
11.
12.
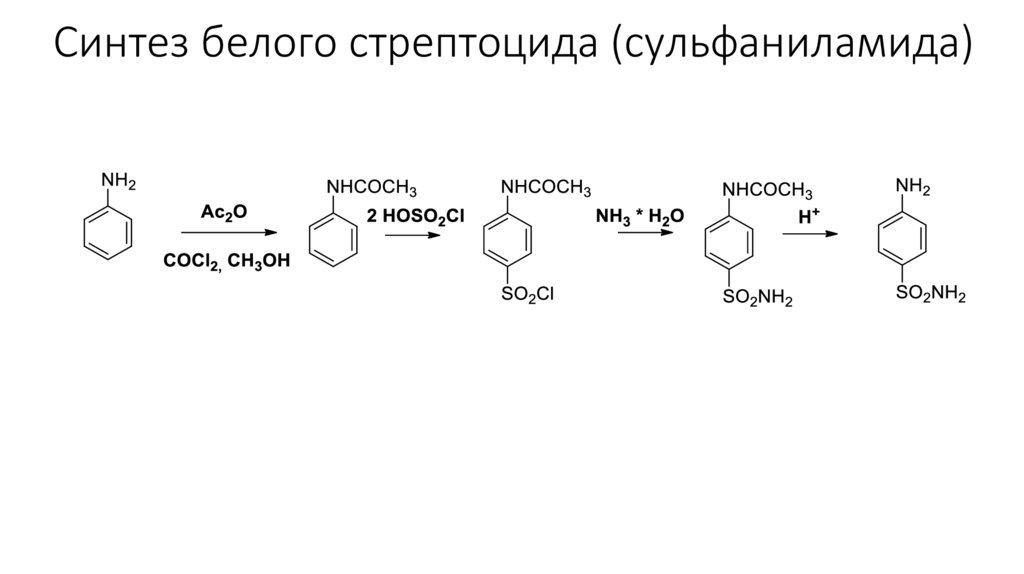
Синтез белого стрептоцида (сульфаниламида)13.
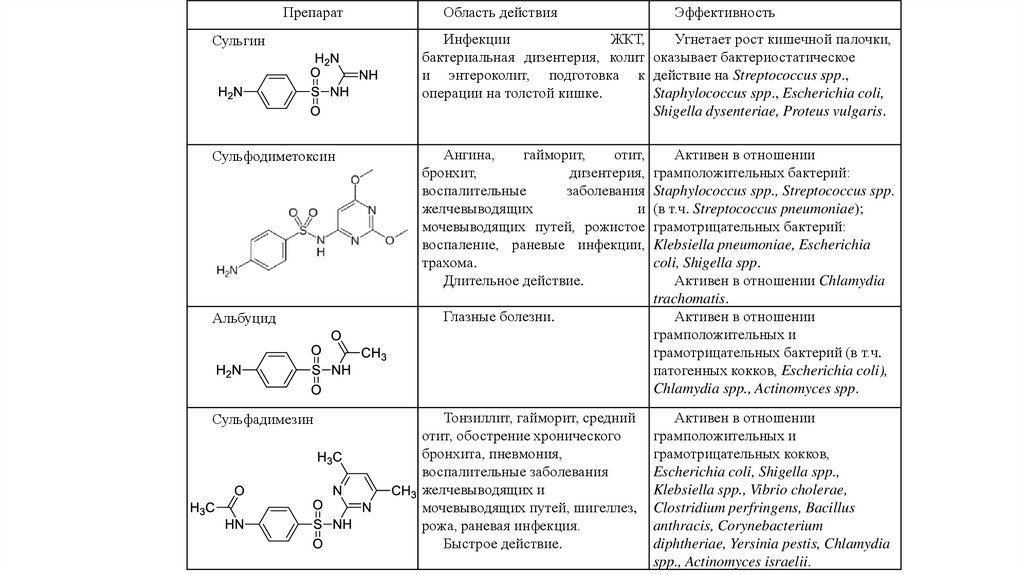
ПрепаратОбласть действия
Эффективность
Сульгин
Инфекции
ЖКТ,
Угнетает рост кишечной палочки,
бактериальная дизентерия, колит оказывает бактериостатическое
и энтероколит, подготовка к действие на Streptococcus spp.,
операции на толстой кишке.
Staphylococcus spp., Escherichia coli,
Shigella dysenteriae, Proteus vulgaris.
Сульфодиметоксин
Ангина,
гайморит,
отит,
Активен в отношении
бронхит,
дизентерия, грамположительных бактерий:
воспалительные
заболевания Staphylococcus spp., Streptococcus spp.
желчевыводящих
и (в т.ч. Streptococcus pneumoniae);
мочевыводящих путей, рожистое грамотрицательных бактерий:
воспаление, раневые инфекции, Klebsiella pneumoniae, Escherichia
трахома.
coli, Shigella spp.
Длительное действие.
Активен в отношении Chlamydia
trachomatis.
Глазные болезни.
Активен в отношении
грамположительных и
грамотрицательных бактерий (в т.ч.
патогенных кокков, Escherichia coli),
Chlamydia spp., Actinomyces spp.
Альбуцид
Сульфадимезин
Тонзиллит, гайморит, средний
отит, обострение хронического
бронхита, пневмония,
воспалительные заболевания
желчевыводящих и
мочевыводящих путей, шигеллез,
рожа, раневая инфекция.
Быстрое действие.
Активен в отношении
грамположительных и
грамотрицательных кокков,
Escherichia coli, Shigella spp.,
Klebsiella spp., Vibrio cholerae,
Clostridium perfringens, Bacillus
anthracis, Corynebacterium
diphtheriae, Yersinia pestis, Chlamydia
spp., Actinomyces israelii.
14.
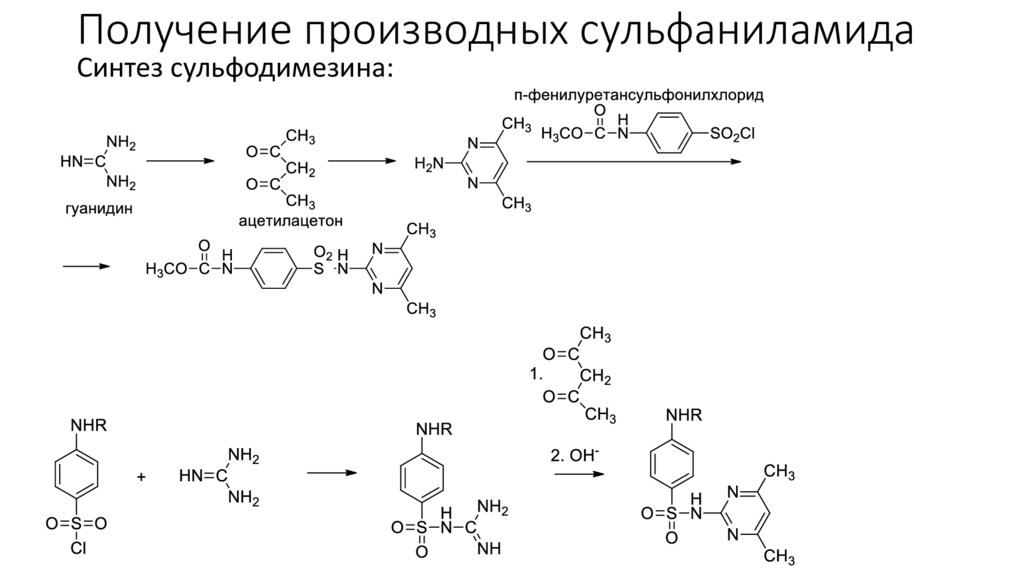
Получение производных сульфаниламидаСинтез сульфодимезина:
15.
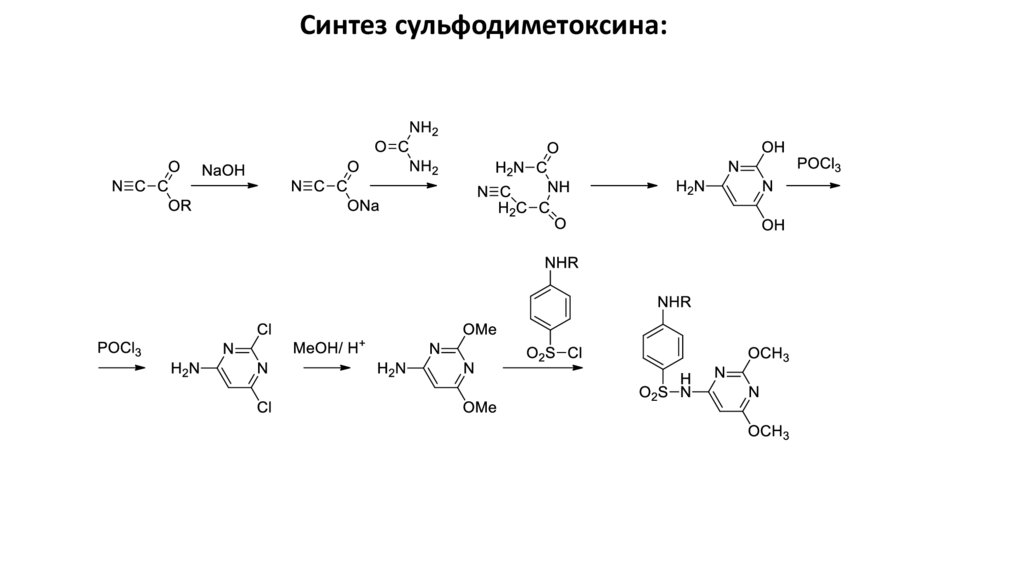
Синтез сульфодиметоксина:16.
• Сульфаниламидные препараты достаточно эффективны при лечениибактериальной инфекции, однако имеют ряд ограничений и недостатков:
• Недостаточный спектр действия. на некоторые группы действует
неэффективно или вообще не действует.
• Имеет ряд побочных эффектов главным, из которых является аллергия.
Нарушение в количестве и качестве мочи. Побочное действие на
кроветворную систему. Угнетающие действие на ЦНС.
• Появляется резистентность к ряду сульфаниламидных препаратов.
• Тем не менее они перспективны для лечения определенных инфекций:
• Лечение дыхательных путей
• Лечение мочеполового тракта
• Различные раны (даже тропические язвы)
17.
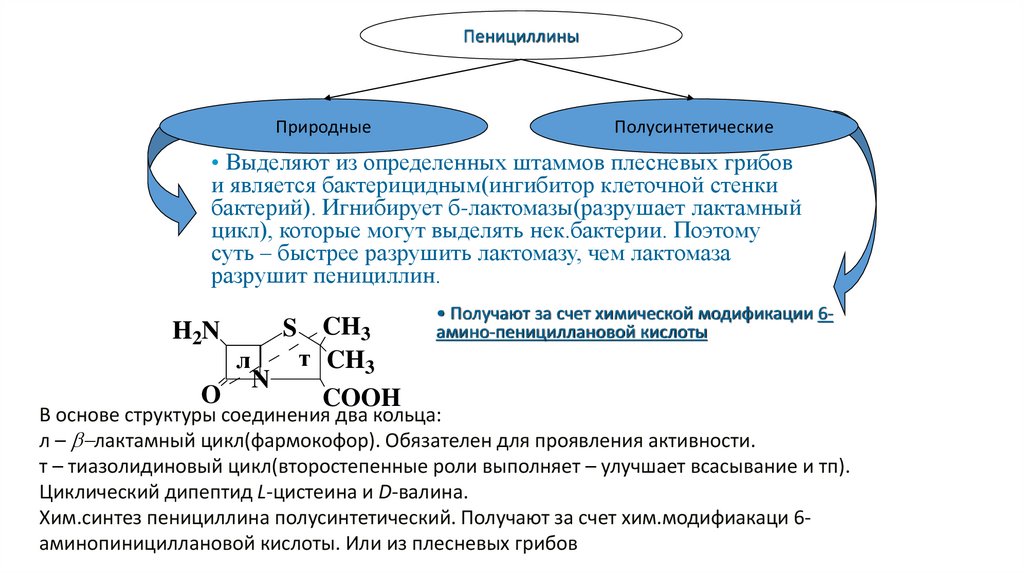
ПенициллиныПриродные
Полусинтетические
• Выделяют из определенных штаммов плесневых грибов
и является бактерицидным(ингибитор клеточной стенки
бактерий). Игнибирует б-лактомазы(разрушает лактамный
цикл), которые могут выделять нек.бактерии. Поэтому
суть – быстрее разрушить лактомазу, чем лактомаза
разрушит пенициллин.
S CH3
т CH3
л
N
O
COOH
H 2N
• Получают за счет химической модификации 6амино-пенициллановой кислоты
В основе структуры соединения два кольца:
л – b-лактамный цикл(фармокофор). Обязателен для проявления активности.
т – тиазолидиновый цикл(второстепенные роли выполняет – улучшает всасывание и тп).
Циклический дипептид L-цистеина и D-валина.
Хим.синтез пенициллина полусинтетический. Получают за счет хим.модифиакаци 6аминопинициллановой кислоты. Или из плесневых грибов
18.
• В медицинской практике наибольшее распространениеполучил бензилпенициллин, или пенициллин G
C6H5CH2COHN
O
S CH3
CH3
N
COO-
1 ЕД (единица действия) соответствует
активности 0,6 мкг чистого
кристаллического бензилпенициллина
в виде натриевой соли(влияет на
фармококинетику)
- или 2-)аминоадипиновая кислота
HOOC CH (CH2)3COHN
NH2
O
S CH3
CH3 пенициллин N
N
COO-
19.
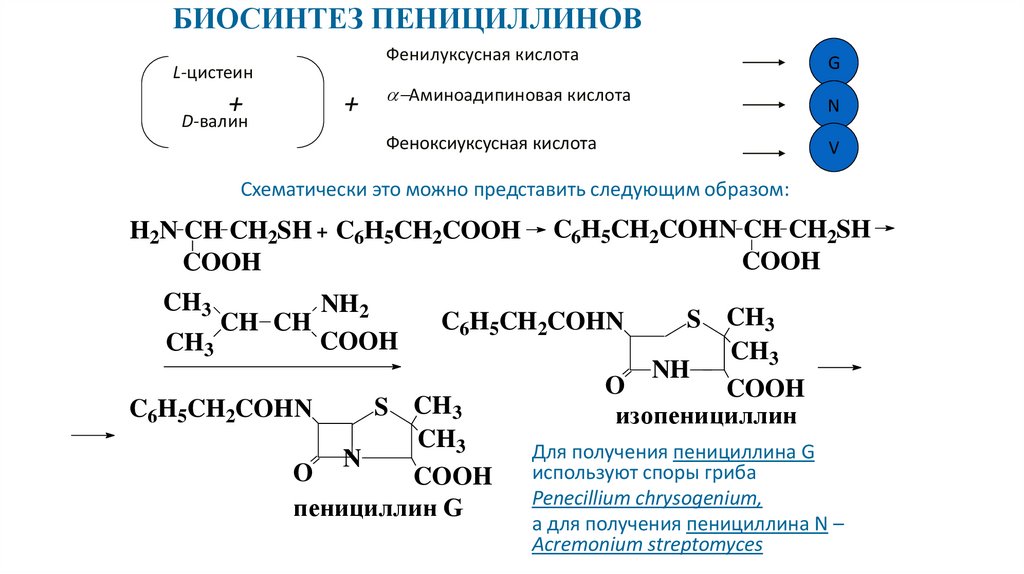
БИОСИНТЕЗ ПЕНИЦИЛЛИНОВФенилуксусная кислота
L-цистеин
+
D-валин
+
G
-Аминоадипиновая кислота
Феноксиуксусная кислота
N
V
Схематически это можно представить следующим образом:
H2N CH CH2SH + C6H5CH2COOH
COOH
CH3
NH2
CH CH
COOH
CH3
S CH3
CH3
NH
O
COOH
изопенициллин
C6H5CH2COHN
S CH3
CH3
N
O
COOH
пенициллин G
C6H5CH2COHN
C6H5CH2COHN CH CH2SH
COOH
Для получения пенициллина G
используют споры гриба
Penecillium chrysogenium,
а для получения пенициллина N –
Acremonium streptomyces
20.
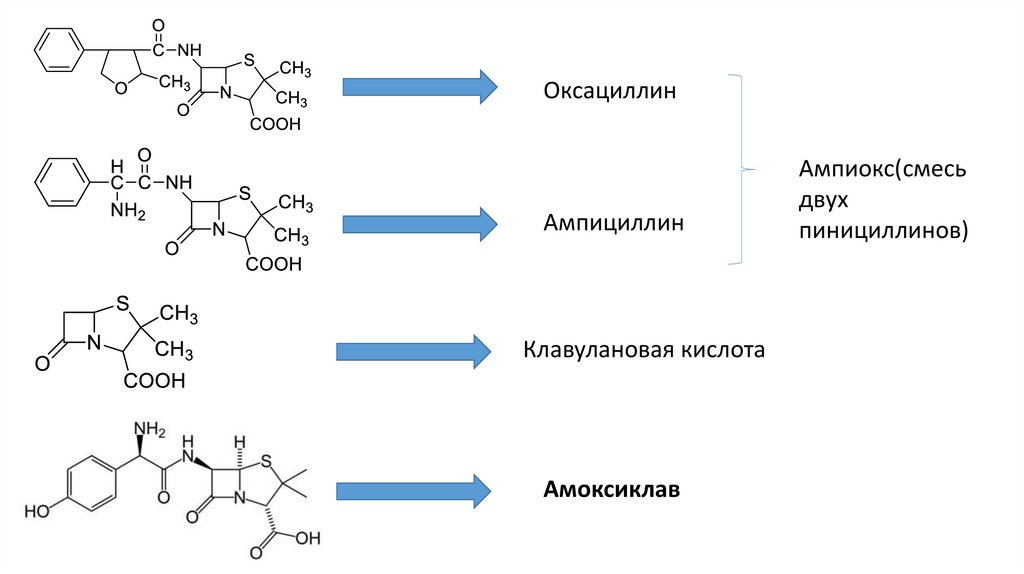
ОксациллинАмпициллин
Клавулановая кислота
Амоксиклав
Ампиокс(смесь
двух
пинициллинов)
21.
• Амоксиклав лучше• Показатели антибиотиков:
• 1. Кислотность. За счет желудочного сока разрушается блактамный цикл
• 2. Ингибирование б-лактомаз
• 3.Спектр действия. На какие бактерии могут действовать
препараты
• 4. МБК
• Ампиокс –устойчив к кислой среде, чувствителен к б-лактомазам,
широкий спектр действия(т.к. бактерицидный), МБК средняя
• Амоксиклав - устойчив к кислой среде(б-лактамный цикл
сохраняется), устойчив к б-лактомазам, широкий спектр
действия(т.к. бактерицидный), МБК средняя
22.
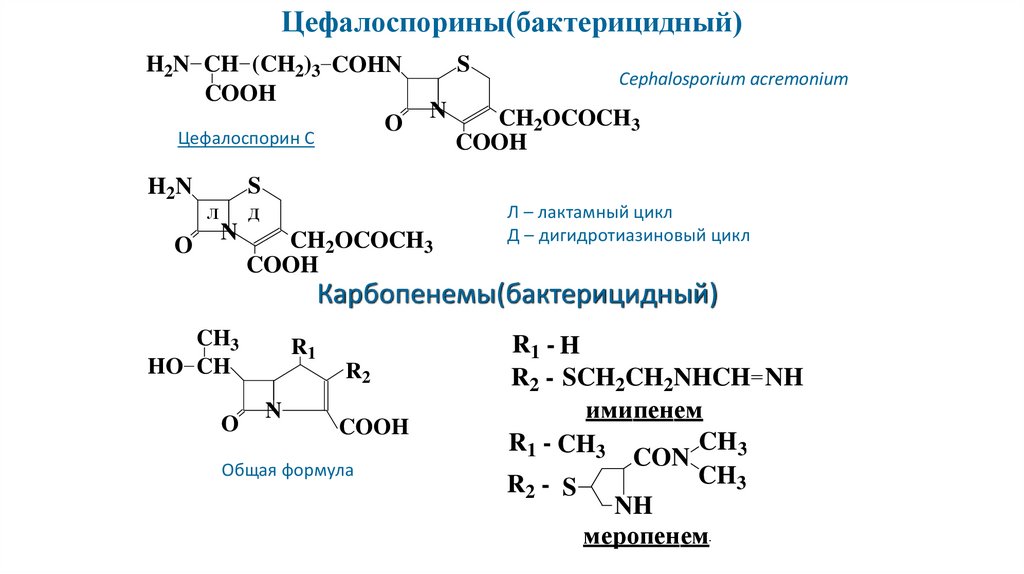
Цефалоспорины(бактерицидный)H2N CH (CH2)3 COHN
COOH
O
S
N
Цефалоспорин C
CH2OCOCH3
COOH
S
H 2N
Л
O
Cephalosporium acremonium
Д
N
CH2OCOCH3
COOH
Л – лактамный цикл
Д – дигидротиазиновый цикл
Карбопенемы(бактерицидный)
CH3
HO CH
O
R1
N
R2
COOH
Общая формула
R1 - H
R2 - SCH2CH2NHCH NH
имипенем
CH3
R1 - CH3
CON
CH3
R2 - S
NH
меропенем
23.
АМФЕНИКОЛЫАнтибиотики широкого спектра действия – производные диоксиаминофенилпропана
Основной представитель – хлорамфеникол
Выделен из в 1947 году
Обычно под хлорамфениколом (левомицетином) подразумевают Dтрео изомер(L-трео токсическая)
Рацемат без предварительного разделения на D- и L-эритро
формы называется синтомицином
Милдред Ребсток (1919 – 2011 гг.)
1949 год – химический синтез
хлорамфеникола
24.
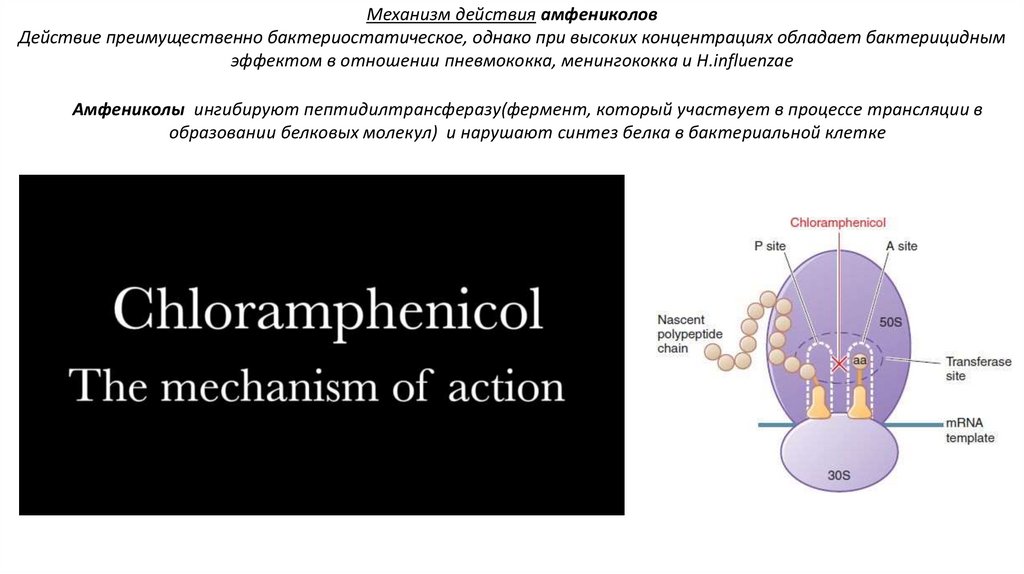
Механизм действия амфениколовДействие преимущественно бактериостатическое, однако при высоких концентрациях обладает бактерицидным
эффектом в отношении пневмококка, менингококка и H.influenzae
Амфениколы ингибируют пептидилтрансферазу(фермент, который участвует в процессе трансляции в
образовании белковых молекул) и нарушают синтез белка в бактериальной клетке
25.
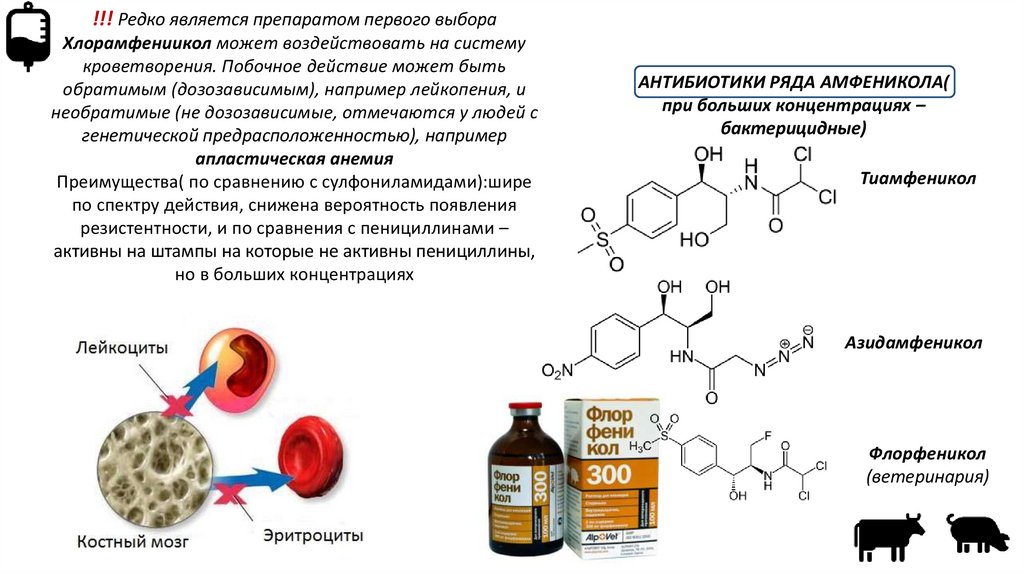
!!! Редко является препаратом первого выбораХлорамфениикол может воздействовать на систему
кроветворения. Побочное действие может быть
обратимым (дозозависимым), например лейкопения, и
необратимые (не дозозависимые, отмечаются у людей с
генетической предрасположенностью), например
апластическая анемия
Преимущества( по сравнению с сулфониламидами):шире
по спектру действия, снижена вероятность появления
резистентности, и по сравнения с пенициллинами –
активны на штампы на которые не активны пенициллины,
но в больших концентрациях
АНТИБИОТИКИ РЯДА АМФЕНИКОЛА(
при больших концентрациях –
бактерицидные)
Тиамфеникол
Азидамфеникол
Флорфеникол
(ветеринария)
26.
Тетрациклины(бактериостатик, при больших – бактерицидный(С в 30 раз большедля этих) и следующие)
Антибиотики, относятся к классу поликетидов и содержат четыре шестичленных цикла
Общая структурная формула
Бенджамин Даггер – выделил
хлортетрациклин из культуральной
жидкости лучистого гриба
Streptomyces aureofaciens в 1945
году
Хлортетрациклин
Сегодня
хлортетрациклин
применяется только в
ветеринарии
27.
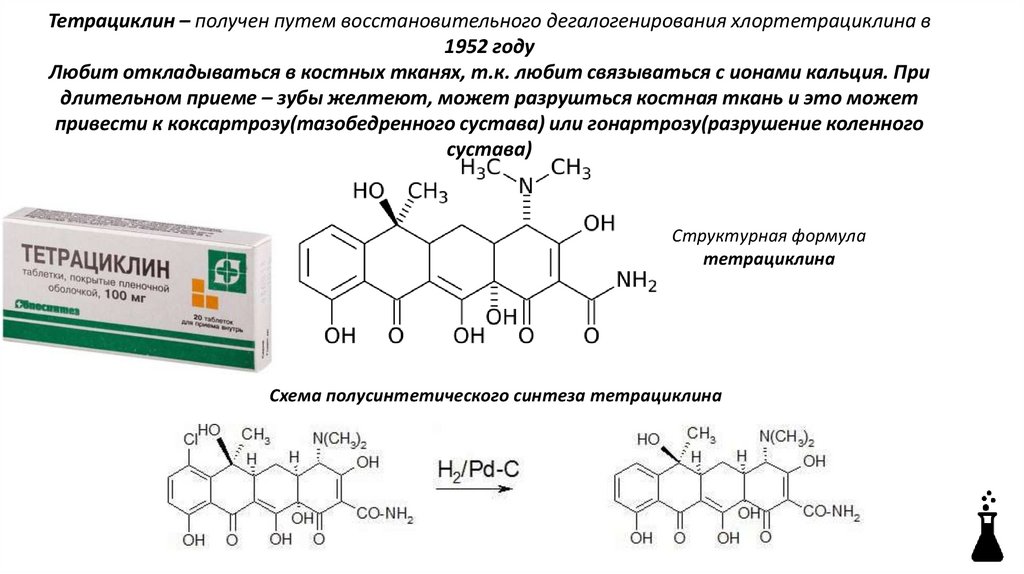
Тетрациклин – получен путем восстановительного дегалогенирования хлортетрациклина в1952 году
Любит откладываться в костных тканях, т.к. любит связываться с ионами кальция. При
длительном приеме – зубы желтеют, может разрушться костная ткань и это может
привести к коксартрозу(тазобедренного сустава) или гонартрозу(разрушение коленного
сустава)
Структурная формула
тетрациклина
Схема полусинтетического синтеза тетрациклина
28.
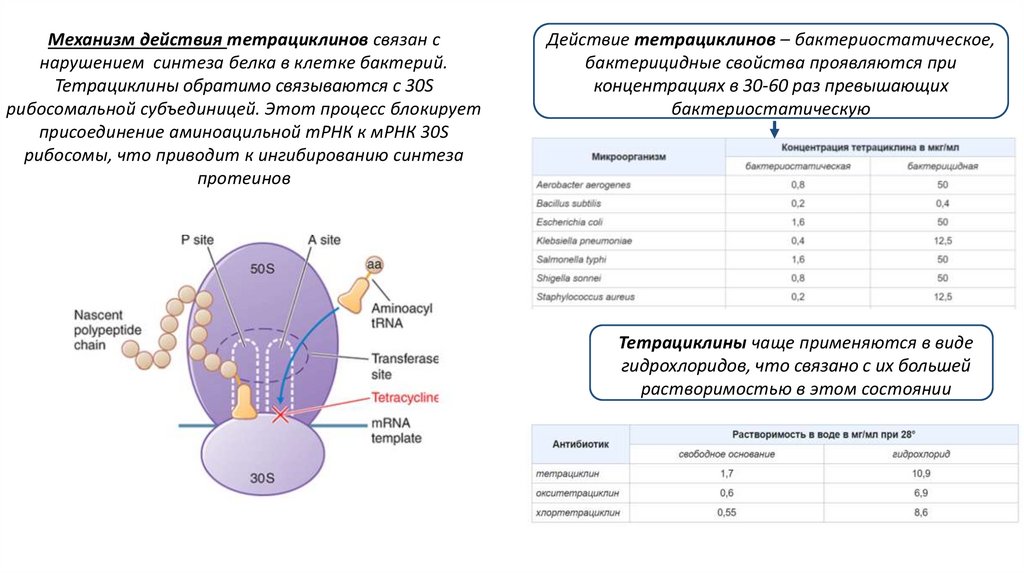
Механизм действия тетрациклинов связан снарушением синтеза белка в клетке бактерий.
Тетрациклины обратимо связываются с 30S
рибосомальной субъединицей. Этот процесс блокирует
присоединение аминоацильной тРНК к мРНК 30S
рибосомы, что приводит к ингибированию синтеза
протеинов
Действие тетрациклинов – бактериостатическое,
бактерицидные свойства проявляются при
концентрациях в 30-60 раз превышающих
бактериостатическую
Тетрациклины чаще применяются в виде
гидрохлоридов, что связано с их большей
растворимостью в этом состоянии
29.
Побочные эффектыПри длительном
приеме тетрациклины
проникают в кости или
зубы и не выводятся
Кроме того,
тетрациклины обладают
тератогенными
побочными эффектами
Основные представители
Хлортетрациклин
Доксициклин
Тетрациклин
Миноциклин
30.
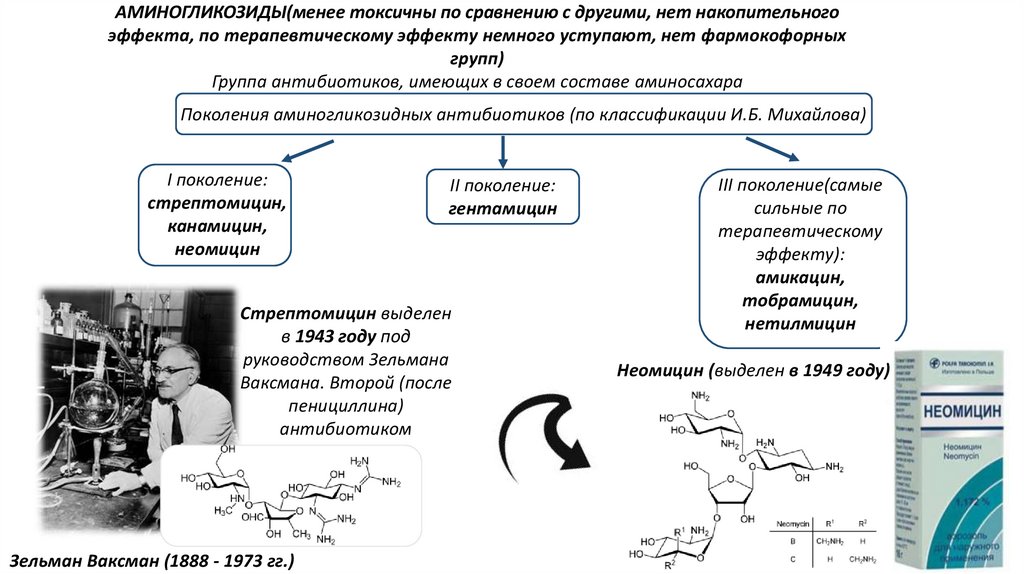
АМИНОГЛИКОЗИДЫ(менее токсичны по сравнению с другими, нет накопительногоэффекта, по терапевтическому эффекту немного уступают, нет фармокофорных
групп)
Группа антибиотиков, имеющих в своем составе аминосахара
Поколения аминогликозидных антибиотиков (по классификации И.Б. Михайлова)
I поколение:
стрептомицин,
канамицин,
неомицин
II поколение:
гентамицин
Стрептомицин выделен
в 1943 году под
руководством Зельмана
Ваксмана. Второй (после
пенициллина)
антибиотиком
Зельман Ваксман (1888 - 1973 гг.)
III поколение(самые
сильные по
терапевтическому
эффекту):
амикацин,
тобрамицин,
нетилмицин
Неомицин (выделен в 1949 году)
31.
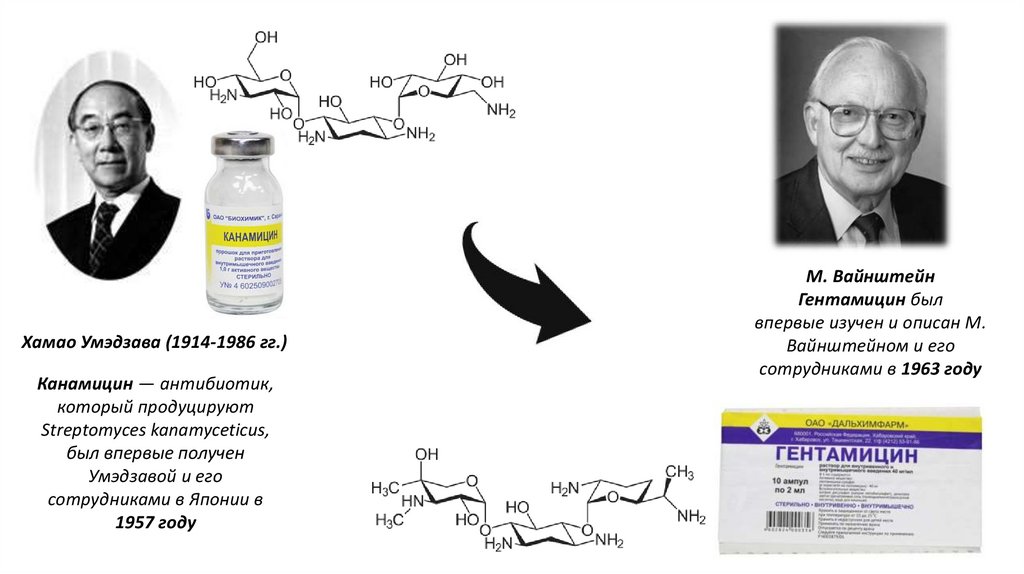
Хамао Умэдзава (1914-1986 гг.)Канамицин — антибиотик,
который продуцируют
Streptomyces kanamyceticus,
был впервые получен
Умэдзавой и его
сотрудниками в Японии в
1957 году
М. Вайнштейн
Гентамицин был
впервые изучен и описан М.
Вайнштейном и его
сотрудниками в 1963 году
32.
Тобрамицин и амикацин были внедрены в клиническую практику в 70-х гг.Амикацин получается химической модификацией канамицина:
Тобрамицин
Нетилмицин
Нетилмицин оказывает менее выраженное
ототоксическое действие по сравнению с другими
аминогликозидами
33.
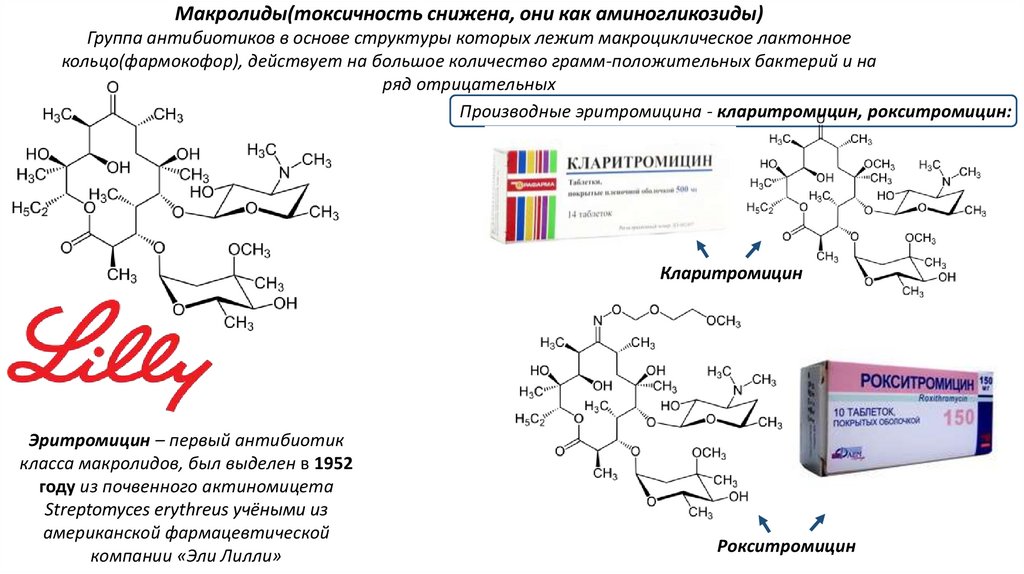
Макролиды(токсичность снижена, они как аминогликозиды)Группа антибиотиков в основе структуры которых лежит макроциклическое лактонное
кольцо(фармокофор), действует на большое количество грамм-положительных бактерий и на
ряд отрицательных
Производные эритромицина - кларитромицин, рокситромицин:
Кларитромицин
Эритромицин – первый антибиотик
класса макролидов, был выделен в 1952
году из почвенного актиномицета
Streptomyces erythreus учёными из
американской фармацевтической
компании «Эли Лилли»
Рокситромицин
34.
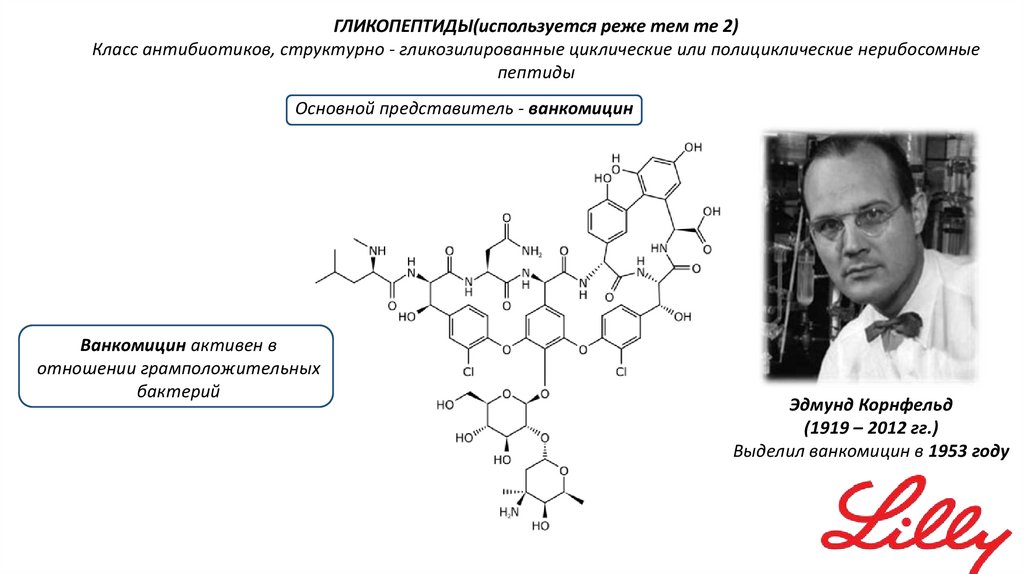
ГЛИКОПЕПТИДЫ(используется реже тем те 2)Класс антибиотиков, структурно - гликозилированные циклические или полициклические нерибосомные
пептиды
Основной представитель - ванкомицин
Ванкомицин активен в
отношении грамположительных
бактерий
Эдмунд Корнфельд
(1919 – 2012 гг.)
Выделил ванкомицин в 1953 году
35.
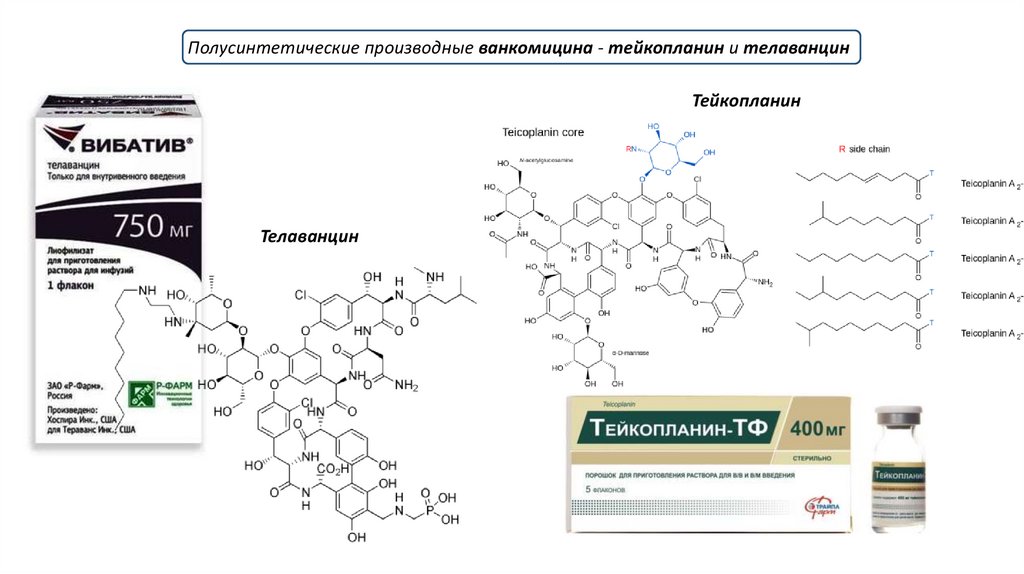
Полусинтетические производные ванкомицина - тейкопланин и телаванцинТейкопланин
Телаванцин
















 medicine
medicine chemistry
chemistry