Similar presentations:
Антибиотики. Причины широко использования в ветеринарной практике
1.
12. Антибиотики
(от др. греч. anti — против, bios — жизнь)вещества природного или полусинтетического
происхождения, подавляющие рост живых клеток
3.
Антибиотики представляют собойсамую многочисленную группу
лекарственных средств. Так, в
России в настоящее время
используется 30 различных групп
антибиотиков, а число препаратов
(без учета дженериков)
приближается к 200.
Найдено и описано более 100 000
видов микроорганизмов, из которых
можно было бы получить
антибиотики.
4. Причины широко использования в ветеринарной практике
1) специфический механизм действия2) широкий и четко выраженный спектр
противомикробного действия
3) эффективность в очень малых дозах
4) сохранение активности в условиях
макроорганизма
5) ярко выраженное и быстро проявляющееся
лечебное и профилактическое действие
6) низкая токсичность для животных
5. История создания антибиотиков
• В Судано-нубийской • Самый первый известныйнам антибиотик появился в
цивилизации тип
Китае две с половиной
тетрациклина
тысячи лет назад. В то
использовался уже в время, китайцы
350 году.
обнаружили, что если
• В Европе в Средние прикладывать
створожившееся соевое
века экстракты
молочко к месту поражения
растений и сырная
инфекцией, то такой
сыворотка
компресс оказывает
использовались для определенное
терапевтическое действие.
лечения инфекций.
6.
ИСТОРИЯ ОТКРЫТИЯ АНТИБИОТИКОВАЛЕКСАНДР ФЛЕМИНГ
(1881 — 1955)
британский бактериолог,
лауреат Нобелевской премии
в области физиологии и
медицины (1945)
Однажды, когда Флеминг был простужен, он
посеял слизь из собственного носа на чашку
Петри, в которой находились бактерии, и через
несколько дней обнаружил, что в местах, куда
была
нанесена
слизь,
бактерии
были
уничтожены.
Так
им
был
открыл ЛИЗОЦИМ (антибактериальный ферме
нт,
вырабатываемый
человеческим
организмом).
Первая
статья
о лизоциме вышла в 1922 году.
В 1928 году он обнаружил, что на агаре в одной
из чашек Петри с бактериями Staphylococcus
aureus выросла колония плесневых грибов.
Колонии бактерий вокруг плесневых грибов
стали прозрачными из-за разрушения клеток.
Флемингу
удалось
выделить
активное
вещество,
разрушающее
бактериальные
клетки — ПЕНИЦИЛЛИН, работа была
опубликована в 1929 году. Это привело к
разработке
антибиотика
новой
эры
–
пенициллина . Двумя годами позже в 1932 году
была напечатана инструкция, как лечить
инфицированные
раны
при
помощи
пенициллина.
7.
Го́вард Уо́лтерФло́ри
(1898 -1968)
английский
фармаколог,
лауреат
Нобелевской
премии по
физиологии и
медицине (1945)
Эрнст Бори́с
Чейн
(1906 -1979)
британский
биохимик,
лауреат
Нобелевской
премии по
физиологии и
медицине (1945)
В 1939-1940 гг. Флори и Чейн занимались поисками новых методов по выращиванию
больших количеств плесени рода Penicillium, отрабатывали условия, при которых
плесень вырабатывала пенициллин, и технические приемы по экстрагированию и
очистке активного антибиотика.
В мае 1940 г им удалось получить достаточное количество неочищенного пенициллина
для проверки его действия на инфицированной мыши. Первые клинические испытания
в начале 1941 г. подтвердили результаты экспериментов на животных: пенициллин
оказался намного более эффективным и намного менее токсичным, чем любой другой
из известных антибиотиков.
В июне 1941 г. Флори отправился в Соединенные Штаты, чтобы запустить
промышленное производство пенициллина. В 1944 г. американские фармацевтические
лаборатории сумели произвести пенициллин в количествах, достаточных для нужд
7
армии.
8.
ИСТОРИЯ ОТКРЫТИЯ АНТИБИОТИКОВВ 1942 году З. В. Ермольевой и ее
сотрудниками
во
Всесоюзном
институте
эпидемиологии и микробиологии был найден
активный продуцент пенициллина и выделен
первый
отечественный
пенициллин
—
КРУСТОЗИН.
ЗИНАИДА ВИССАРИОНОВНА
ЕРМОЛЬЕВА
(1898—1974)
выдающийся советский ученыймикробиолог и эпидемиолог,
академик АН СССР, лауреат
государственной (Сталинской)
премии СССР (1943)
Уже в 1943 г. лаборатория начала готовить
пенициллин для клинических испытаний.
Первые испытания проводились хирургами
нескольких клиник Москвы под руководством
профессора И. Г. Руфанова, но в основном — в
Яузской
больнице,
где
размещался
эвакогоспиталь. В начале 1944 г. здесь было
проведено
сравнение
эффективности
отечественного и английского пенициллинов,
которые привез один из его создателей,
знаменитый Г. Флори из Оксфорда. Лечение
проводили в двух группах раненых с сепсисом,
находившихся в одинаково тяжелом состоянии.
И хотя отечественный пенициллин — крустозин
был менее очищен и его применяли в меньших
дозах, эффект лечения был не хуже, чем при
применении английского препарата.
9.
ТЕРМИН «АНТИБИОТИК» БЫЛ ВВЕДЕН ЗЕЛЬМАНОМ ВАКСМАНОМВАКСМАН, ЗЕЛЬМАН
ЭЙБРАХАМ
(1888–1973)
американский микробиолог,
лауреат Нобелевской премии
по физиологии и медицине
(1952) за открытие
стрептомицина – первого
эффективного
противотуберкулезного
антибиотика.
В 1932 г. Американская ассоциация по борьбе с туберкулезом поручила Ваксману провести
исчерпывающие поиски продуцентов антимикробных веществ. Исследуя причину гибели
туберкулезной палочки в почве, он сделал вывод, что исчезновение бацилл связано с
микробным антагонизмом: одна бактерия продуцирует вещество, убивающее другую
бактерию. Для подобных веществ им было предложено общее название «антибиотики».
В 1943 г. Ваксман получил мощный антибиотик СТРЕПТОМИЦИН, синтезируемый грибами
из группы актиномицетов. Он великолепно дополнял пенициллин, уничтожая те бактерии,
которые еще оставались неуязвимыми. В частности, испытания, проведенные в клинике
Мейо в Рочестере, показали его эффективность при терапии неизлечимых ранее форм
туберкулеза. Помимо стрептомицина Ваксман выделил: актиномицин (1940), гризеин
(1946), неомицин (1948), фрадицин, кандицидин, кандидин и другие антибиотики.
10.
ХРОНОЛОГИЯ ВЫПУСКА НАИБОЛЕЕ ИЗВЕСТНЫХ АНТИБИОТИКОВза период с 1940 по 1970 год в мире было выделено десять различных классов антибиотиков, каждый из
которых обладал уникальным механизмом действия
1944 год – стрептомицин
1948 год – хлортетрациклин
1949 год – левомицетин и неомицин
1950 год - окситетрациклин
1952 год - эритромицин
1954 год – бензилпенициллин
1961 год - ампициллин
1964 год - гентамицин
1967 год - рифампицин
1968 год – клиндамицин
1970 год - цефалексин
1971 год - цефазолин
1972 год - амоксициллин и цефрадин
1977 год - цефуроксим
1979 год – цефаклор
1980 год- цефатаксим
1982 год - цефтриаксон
1983 год – норфлоксацин
1985 год – офлоксацин
1989 год – энрофлоксацин
1990 год - кларитромицин
1994 год – цефепим
в 2006 году только шесть новых антибиотиков прошли первую стадию проверки
11.
Антибиотики – природные вещества микробного (позднее –растительного и
животного) происхождения и продукты их
химической модификации, способные в низких концентрациях (10–3–
10–2 мкг/мл) подавлять развитие
бактерий, низших грибов,
простейших, вирусов или клеток злокачественных опухолей по
принципу антибиоза (биологического антагонизма).
Известно несколько тысяч природных антибиотиков, среди которых
наиболее представительными группами и часто применяемыми в
ветеринарной медицине являются 4 основных структурных типа
(практически все – гетероциклические соединения):
b-лактамы
тетрациклины
макролиды
аминогликозиды
Значительно больше существует синтетических и полу-синтетических
аналогов и производных, обладающих большей активностью и
устойчивостью, чем природные прототипы. Лишь 3% находят
применение
в
ветеринарной
медицине.
Пенициллины
и
цефалоспорины – более половины всех производимых антибиотиков.
12.
ИСТОЧНИКИ ПОЛУЧЕНИЯ АНТИБИОТИКОВ1.
2.
3.
4.
5.
6.
7.
8.
Плесневые грибы (пенициллин)
Актиномицеты (стрептомицины, тетрациклины)
Бактерии (полимиксины, грамицидин)
Грибы (фузидин)
Лишайники (усниновая кислота)
Растения (иманин, рафанин, фитонциды)
Животные (экмолин, эритрин, лизоцим)
Синтетические аналоги природных
антибиотиков (оксацилин, доксициклин).
13. Методы получения антибиотиков
• Методкультивирования
продуцентов в
ферментерах
• Метод химического
синтеза
• Метод генной
инженерии
14. Классификация антибиотиков в зависимости от очистки
1. Очищенные (фармакопейные) – постоянныйсостав, применяют внутрь и парентерально
для лечения и профилактики
2. Полуфабрикаты (сухие концентраты) –
стандартное и высокое содержание
антибиотика, для лечения, профилактики и
ускорения роста, только для животных !
3. Нативные (неочищенные) - небольшое
содержание антибиотика, короткий срок
годности, применяют внутрь.
15. Классификация антибиотиков по происхождению
1. Антибиотики, полученные из грибов, например рода Penicillium(пенициллин), рода Cephalosporium (цефалоспорины).
2. Антибиотики, полученные из актиномицетов; группа включает около
80% всех антибиотиков, это представители рода Streptomyces,
являющиеся продуцентами стрептомицина, эритромицина,
левомицетина.
3. Антибиотики, продуцентами которых являются собственно бактерии.
Чаще всего с этой целью используют представителей рода Bacillus и
Pseudomonas (полимиксины, бацитрацины, грамицидин)
4. Антибиотики животного происхождения; из рыбьего жира получают
эктерицид, из молок рыб – экмолин, из эритроцитов – эритрин.
5. Антибиотики растительного происхождения. Это фитонциды, которые
выделяют лук, чеснок, сосна, ель, сирень, другие растения. В чистом
виде они не получены, так как являются чрезвычайно нестойкими
соединениями. Антимикробным действием обладают многие растения,
например, ромашка, шалфей, календула.
6. Синтетические и полусинтетические антибиотики.
16.
КЛАССИФИКАЦИЯ АНТИБИОТИКОВпо механизму действия
1. ингибиторы синтеза бактериальной клеточной стенки
(антибиотики бета-лактамной группы и гликопептиды) – бактерицидный эффект
2. ингибиторы функционирования цитоплазматической
мембраны (полимиксины и полиеновые антибиотики) – бактерицидный
эффект
3. ингибиторы матричного (рибосомального) синтеза белка
4.
(тетрациклины, левомицетины, аминогликозиды, макролиды) бактериостатический эффект
ингибиторы синтеза нуклеиновых кислот (рифампицин и
антибластомные антибиотики) - бактерицидный эффект
по направленности фармакологического действия
1.
2.
3.
4.
антибактериальные
противогрибковые
противоопухолевые
стимуляторы роста и продуктивности животных
17.
КЛАССИФИКАЦИЯ АНТИБИОТИКОВпо широте спектра антимикробного действия
1. Антибиотики узкого спектра
а) с преимущественным действием на Грам+ бактерии (природные
пенициллины, макролиды, гликопептиды)
б) с преимущественным действием на Грам- бактерии
(полимиксины, монобактамы)
в) с действием, ограниченным одной группой патогенных
микроорганизмов (противомикозные)
2. Антибиотики широкого спектра - полусинтетические
пенициллины:
1.
цефалоспорины
2.
карбапенемы
3.
аминогликозиды
4.
тетрациклины
5.
левомицетины
6.
рифамицины
17
18. Классификация антибиотиков по химическому строению
1.Антибиотики, имеющие в структуре β-лактамовое кольцо
(бета-лактамные антибиотики): пенициллины,
цефалоспорины, монобактамы, карбопенемы
2.
Антибиотики со структурой макроциклического лактонного
кольца (макролиды): эритромицин, тилозин, фармазин,
фрадизин, олеандомицин, рокситромицин, азитромицин,
кларитромицин, спирамицин, диритромицин
3.
Антибиотики, структурой которых являются четыре
конденсированных шестицикличных кольца
(тетрациклины): тетрациклин, окситетрациклин,
хлортетрациклин, диметилхлортетрациклин, метациклин,
морфоциклин, гликоциклин, хлортетрин, доксициклин,
миноциклин, ролитетрациклин
19. Классификация антибиотиков по химическому строению
4. Антибиотики, содержащие в молекулеаминосахара (аминогликозиды): стрептомицин,
неомицин, гентамицин, мономицин, канамицин,
сизомицин, тобрамицин, спектиномицин, амикацин
нетилмицин
5. Антибиотики, производные
диоксиаминфенилпропана (ароматические
антибиотики): левомицетина сукцинат и стеарат;
левомицетин, синтомицин
6. Антибиотики со структурой циклических
полипептидов (полимиксины): полимиксина М
сульфат, полимиксина В сульфат, бацитрацин,
колистин, грамицидин
20. Классификация антибиотиков по химическому строению
7. Антибиотики противогрибковые, содержащие в своеймолекуле несколько сопряженных двойных связей
(полиены): амфотерицин В, нистатин, леворин,
натамицин, гризеофульвин
8. Антибиотики, содержащие в своей молекуле
замещенные пептидные соединения
(гликопептиды): ванкомицин (ванкацин, диатрацин),
тейкопланин (таргоцид), даптомицин;
9. Антрациклинновые антибиотики (противоопухолевые
антибиотики): доксорубицин, карминомицин,
рубомицин, акларубицин
21. Классификация антибиотиков
Антибиотики, не относящихся ни к одной изперечисленных химических групп фосфомицин, фузидиевая кислота (фузидин),
фумагиллин, линкомицин, рифампицин и
клиндамицин
Комбинированные препараты: ампиокс,
олететрин, димет, оксикан, леновит,
биофарм, мастисан
Кормовые антибиотики: бацитрацин, гризин
22. Фармакокинетика антибиотиков
• В ротовой полости частичное всасывание (у жвачныхсильнее), в желудке и толстом кишечнике
незначительное, в тонком кишечнике всасывается
основная масса
• В крови концентрируются через 40-90 минут после
введения внутрь, через 20-30 минут после подкожной
или внутримышечной инъекции
• Распределяются в зависимости от степени
кровоснабжения органов. Накапливаются в
паренхиматозных органах и стенках ЖКТ.
• Выведение начинается через 10-15 минут после
появления в крови, выводятся из организма в
течение 4-6 часов или 7-12 суток.
23. Фармакокинетика
• Большинство антибиотиков при введении внутрьлегко всасываются слизистыми оболочками рта
(0,5%), желудка (3-11%), тонкого кишечника (4866 %) и толстого кишечника (7-15 %).
• Процесс всасывания антибиотиков из ЖКТ
зависит от его содержимого. Молоко и корма
задерживают всасывание тетрациклинов,
феноксиметилпенициллина и эритромицина.
• Поэтому антибиотики необходимо вводить за 30
мин до кормления.
• При длительном применении антибиотики
нарушают всасывающую способность слизистых
23
оболочек.
24. Фармакокинетика
• Распеределение антибиотиков в организмепроисходит неравномерно. Большая часть
их концентрируется в почках, печени,
сердце, легких, меньшая – в
лимфатических узлах, селезенке, мышцах
и стенках ЖКТ, еще меньшая в матке,
плодах и ЦНС.
• Тетрациклин хорошо проникает в кости,
левомицетин – через серозные оболочки.
24
25. Фармакокинетика
• В малых дозах большинство антибиотиковусиливают, а в больших – угнетают моторносекреторную функцию желудочно-кишечного
тракта.
• Угнетающий эффект больших доз антибиотиков
на процессы пищеварения особенно выражен у
жвачных животных и незначителен у птиц.
• Улучшение пищеварения от применения малых
доз антибиотиков наблюдается у животных со
средним и высоким уровнем секреции.
25
26. Фармакодинамика антибиотиков
По антимикробной активности антибиотики делятна:
1) Препараты с узким спектром действия :
а) действуют только на грам + микроорганизмы
(пенициллины, макролиды, цефалоспориновые
антибиотики 1-го поколения )
б) действуют только на грам – микроорганизмы
(полимиксины, цефалоспорины 3-го поколения )
2) Препараты с широким спектром действия :
(тетрациклины, левомицетины, аминогликозиды,
цефалоспорины 2-го поколения )
27. Механизм действия антибиотиков
28.
ОСОБЕННОСТИ ДЕЙСТВИЯАНТИБИОТИКОВ
1. Мишень-рецептор находится не в тканях
животного, а в клетке микроорганизма.
2. Активность антибиотиков не является
постоянной, а снижается со временем, что
обусловлено формированием лекарственной
устойчивости (резистентности).
29. РЕЗИСТЕНТНОСТЬ К АНТИБИОТИКАМ
Нерациональное использование антибиотиковприводит к снижению чувствительности
микробов к их действию.
Очень быстро развивается стойкость к
антибиотикам у стафилококков, эшерихий,
сальмонелл, микоплазм, синегнойной палочки.
Среди антибиотиков чаще всего развивается
резистентность к стрептомицину,
эритромицину, олеандомицину, линкомицину,
фузидину и рифампицину
29
30.
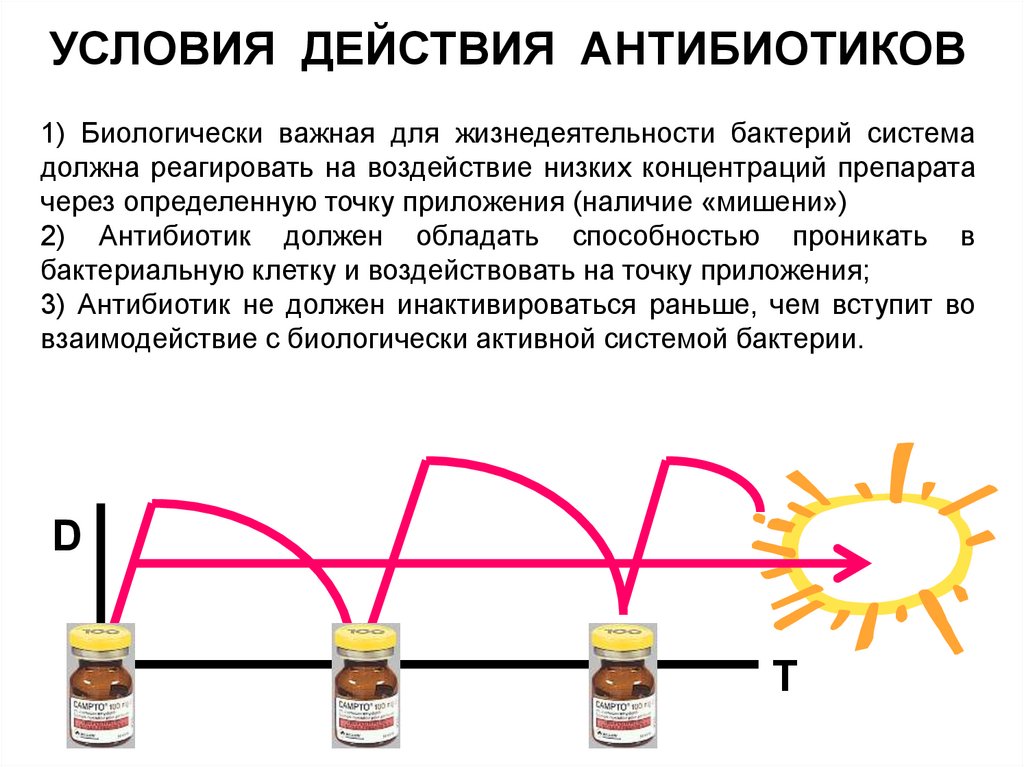
УСЛОВИЯ ДЕЙСТВИЯ АНТИБИОТИКОВ1) Биологически важная для жизнедеятельности бактерий система
должна реагировать на воздействие низких концентраций препарата
через определенную точку приложения (наличие «мишени»)
2) Антибиотик должен обладать способностью проникать в
бактериальную клетку и воздействовать на точку приложения;
3) Антибиотик не должен инактивироваться раньше, чем вступит во
взаимодействие с биологически активной системой бактерии.
D
Т
31.
БИОЛОГИЧЕСКАЯ АКТИВНОСТЬАНТИБИОТИКОВ
Содержание антибиотика обозначают в граммах
активного вещества или в условных единицах действия
— ЕД
За 1 ЕД большинства антибиотиков принимают
специфическую активность, содержащуюся в 1 мкг
чистого препарата.
Например: для бензилпенициллина 1 ЕД равна 0,5988 мкг
химически чистой натриевой соли препарата.
31
32. Дозирование антибиотиков
• Антибактериальные препараты дозируют на 1 кгживой массы, на одно животное или на 1 т корма
(для птицы также применяется дозировка на 1 л
питьевой воды).
• Количество препарата указывают в микрограммах
(мкг), миллиграммах (мг), килограммах (кг), для
жидких лекарственных форм — в миллилитрах
(мл) или кубических сантиметрах (см3), а для
некоторых антибиотиков (пенициллины и
полимиксин) — в единицах действия (ЕД).
33. Дозирование антибиотиков
• Антибактериальные препараты следует применятьживотным в течение определенного периода времени
(курса лечения), необходимого для полного подавления
инфекции и клинического их выздоровления, а в
некоторых случаях, при рецидивирующих инфекциях, —
по возможности до полной санации организма.
Продолжительность лечения колеблется в зависимости
от течения и тяжести заболевания и заранее не может
быть строго регламентирована.
• Хронические инфекции обычно требуют более
длительной, а острые — кратковременной, но
интенсивной терапии. При острых инфекциях
антимикробные препараты обычно назначают на 5 -7
дней, если клинический эффект не наблюдается через 34 дня после начала лечения, то следует перейти к
терапии другими препаратами.
34. Введение антибиотиков
• Препараты чаще назначают перорально, внутримышечно,внутривенно, внутрибрюшинно, внутриматочно,
внутрицистернально, наружно и реже — подкожно.
• Внутривенный и внутримышечный способы введения следует
использовать при необходимости быстрого создания
антимикробных концентраций препарата в организме, а также
в тех случаях, когда вещество плохо всасывается или
разрушается в желудочно-кишечном тракте.
• Подкожное введение менее эффективно, чем
внутримышечное, вследствие неравномерного всасывания
лекарств из подкожной клетчатки.
• Поросятам антибактериальные препараты в растворах можно
вводить внутрибрюшинно, что, как и внутримышечное
введение, обеспечивает быстрое распределение
лекарственного вещества в органах и тканях, особенно
брюшной и тазовой полостей.
• Для уменьшения количества инъекций применяют
пролонгированные лекарственные формы, например
бициллины
35. Нежелательные эффекты антибиотикотерапии
36. Побочное действие антибиотиков
• Аллергические реакции (анафилактический шок,поражения кожи, слизистых оболочек, сывороточная
болезнь, астматический бронхит, зуд, дерматит )
• Токсические реакции (нейротоксичность ,
нефротоксичность, ототоксичность)
• Угнетение иммунной системы, кроветворения, роста
соединительной ткани, свертывающей системы
крови.
• Реинфекции или суперинфекции (кандидоз и
дизбактериоз, псевдомембранозный колит,
неспецифическая диарея)
• Гиповитаминозы (витамины группы В, С, К)
• Изменения в биохимическом анализе крови
(эозинофилия, лейкоцитоз, агранулоцитоз)
37. Общие принципы антибиотикотерапии
38. Общие принципы антибиотикотерапии
39. ПРИНЦИПЫ РАЦИОНАЛЬНОЙ АНТИБИОТИКОТЕРАПИИ
1.2.
3.
4.
5.
6.
Раннее начало лечения.
Правильный выбор препарата с учетом его спектра действия,
чувствительности. возбудителя и чувствительности
животного.
Определение оптимальной дозы, режима и
продолжительности применения препарата.
Выбор способа введения препарата в организм с учетом его
фармакокинетики.
Комбинированное лечение с применением нескольких
антибиотиков с разным механизмом действия, к которым
чувствительный возбудитель.
Строго учитывать ограничения для применения
антибиотиков.
39
40. ПРИНЦИПЫ РАЦИОНАЛЬНОЙ АНТИБИОТИКОТЕРАПИИ
Комплексное лечение с применением наряду с антибиотикамипрепаратов, укрепляющих иммунитет, поливитаминов и
препаратов, предупреждающих осложнения
антибиотикотерапии (дисбактериоз, кандидамикоз).
8. Сохранение санитарно-гигиенического режима в помещениях,
где находятся животные, с целью предупреждения
распространения резистентных штаммов возбудителей.
9. Наличие резервных антибиотиков на случай
полирезистентности возбудителя.
10. Местное применение антибиотиков ограничивать
специальными препаратами или лекарственными формами для
местного применения.
7.
40
41. Профилактика антибиотиками
• Антибиотики часто назначают животным еще до появленияклинических признаков заболевания, чтобы предупредить его
развитие.
• Принципы профилактического применения антимикробных
препаратов (главным образом антибиотиков) в
ветеринарии разработаны недостаточно.
• Беспорядочное использование антибиотиков в качестве
профилактических средств может принести больше вреда, чем
пользы, вследствие отбора устойчивых штаммов, возможности
побочных реакций, сенсибилизации животных.
• Профилактическое применение антибиотиков целесообразно
при реальной угрозе возникновения болезни бактериальной
этиологии среди определенных групп животных. При выявлении
инфекционного заболевания на ферме массовая обработка
всех животных, включая клинически больных, а также
подозреваемых в заражении, дает возможность прервать
инфекционный цикл и добиться излечения всего поголовья.
42. Стимулирующее действие антибиотиков на рост и развитие молодняка
Под действием малых доз антибиотиков улучшаютсяпроцессы обмена между пищеварительной системой,
кровью и тканями.
Это способствует физиологической стимуляции
резервных возможностей организма, повышению
его жизнеспособности и направленности обменных
процессов в сторону ассимиляции.
В результате этого ускоряются пластические процессы. Повышается продуктивность животных и снижается вероятность возникновения заболеваний.
42
43. Стимулирующее действие антибиотиков на рост и развитие молодняка
Кормовые антибиотики не рекомендуется применятьв первые 10 дней после родов, у беременных, дойных и племенных животных.
В качестве стимуляторов роста и продуктивности
животных используются только те антибиотики,
которые не применяются с лечебной и профилактической целью (гризин, бацитрацин, флавоми-
цин).
Кормовые антибиотики входят в состав премиксов,
белково-витаминных добавок, комбикормов, заменителей несобранного молока.
Большинство антибиотиков быстро выводятся из
организма ( через 24-48 часов).
43
44. Стимулирующее действие антибиотиков на рост и развитие молодняка
В кишечнике снижается количество клостридий идругих бактерий, выделяющих токсины.
Наибольший стимулирующий эффект наблюдается
у животных, которые отстают в росте, а у быстрорастущих (свиней и птиц) в ранний период жизни :
цыплят от 20-30-дневного до 2-месячного, у поросят
– от 30-45-дневного до 3-месячного, у ягнят и телят –
до 4-месячного возраста при условии использования
минимальных доз ( от 5 до 100 г антибиотика на 1г
корма.
При этом масса животных увеличивается на 3-5%, а
усвоение корма – на 2,5 %.
44
45. Побочные эффекты антибиотико-терапии
Побочные эффекты антибиотикотерапииНерациональное использование антибиотиков в
больших дозах в течение длительного времени без
учета вида и роста животных приводит к возникновению побочных и даже токсических реакций:
Аллергические реакции.(Для их предупреждения перед
лечением проводят пробу на чувствительность).
Угнетение сапрофитной флоры ЖКТ приводит к
суперинфекции, что проявляется диареей, дисбактериозом, кандидамикозом.
Нейротоксические, гематотоксические, гепатотоксическте, нефротоксические реакции.
Развитие флебитов и тромбофлебитов при внутривенных инъекциях.
45
46.
Пенициллины.Относятся к b-лактамным антибиотикам. Впервые выделены из плесневого грибка
Penicillium notatum. Известно 6 основных структурных типов пенициллинов.
S
O
N
карбапенам
O
N
NH3
COOH
OOC
L- -аминоадипиновая кислота
H2N
O
H
O
пенам
S CH
3
N
CH3
COOH
+
S
O
N
клавам
NH3
OOC
O
N
O
цефам
L-цистеин
CH3
CH3
L-валин
S
S
N
O
оксацефам
NH3
SH + OOC
S
O
тиацефам
H
N
R
N
O
O
H
S CH
3
N
CH3
COOH
пенициллины
6-аминопенициллановая кислота
Аминопенициллановая кислота – дипептид (L-цистеин и
D-валин). В процессе биосинтеза происходит обращение
L-конфигурации валина на D.
Пенициллины тормозят одну из последних стадий в сборке пептогликановой
структуры
клеточной
стенки
бактерий.
Однако
ингибируется
только
карбоксипептидаза микроорганизмов. Ферментная система животного организма, не
способного использовать аминокислоты D-ряда, не затрагивается.
47.
Практически важные пенициллиныR1
H
N
H
O
тиазолидин
S CH
3
N
CH3
COOR2
Довольно нестабильные вещества, в щелочной среде и при
нагревании легко раскрывается
лактамный цикл с образованием
биологически не активных пенициллоиновых кислот. Аналогично
действуют
b-лактамазы
–
ферменты устойчивых к пенициллинам штаммов микроорганизмов. Через усиление активности этого фермента развива-
ется резистентность организма.
48.
Важнейшие цефалоспорины и цефамициныR2 H
R2 = H цефалоспорины
R1
S
R2 = OCH3 цефамицины
N
R3
O
1,3-тиазин
COOH
H
O
N
S
O
цефалоспорановая
кислота
COOH O
Выделены из грибков рода Cephalosporium и Streptomyces. Тормозят
рост некоторых штаммов бактерий,
устойчивых к пенициллинам.
Пенициллины
и
цефалоспорины
проявляют активность в отношении
многих грамположительных микроорганизмов (стафилококков, пневмококков, стрептококков), некоторых
грамотрицательных кокков (гонококков, менингококков), палочек сибирской язвы, клостридий, спирохет и
некоторых грибков.
Обладают низкой токсичностью для
теплокровных, но могут вызывать
бурную
аллергическую
реакцию,
вплоть до анафилактического шока.
49.
Важнейшие тетрациклины.HO
R2 R1
R
3
N
X
H
A B C D
R4
O
O
OH
OH O
OH
Относятся к производным частично гидрированных нафтаценов
(или тетраценов).
Выделены
из
грибков
рода
Streptomyces. Занимают второе
место
по
распространённости
после b-лактамных антибиотиков.
Специфически ингибируют синтез
белка.
Высокоактивны против грамположительных и большинства грамотрицательных бактерий.
Применяются для лечения пневмонии, дизентерии, коклюша, гонореи, бруцеллеза,
туляремии, сыпного тифа, холецистита, менингита и других инфекционных
заболеваний, а также при гнойных послеоперационных осложнений.
50.
Аминогликозиды. Группа стрептомицина.Относятся к аминогликозидам. Занимают четвёртое место по использованию после
b-лактамов, тетрациклинов и неполиеновых макролидов.
Общее в строении – 6-членные карбоциклические аминоспирты (аминоинозиты),
гликозилированные обычным сахаром или специфическими аминосахарами.
дигуанидиновое производное
- стрептидин
L-стрептоза
NH
OHC O
H2N NH
OH
H3C
O HO
N H NH
HO O
OH
HO
NH2
O H
HO
N
N-метил-L-глюкозамин
HO
CH3
Стрептомицин
HO
NH2
O
L-глюкозамин
R OH O H2N
HO
O
NH2
O
OH
O OH
HO
HO
O
NH2
R = OH паромомицин
R = H ливидомицин
Насчитывается более 100 природных соединений (продуцентов микроорганизмов рода Streptomyces, Micromonospora, Bacillus) и огромное количество полусинтетических антибиотиков (неомицин, канамицин, сизомицин, гентамицин).
А.М. Чибиряев "Биологически активные соединения живых организмов", 2009
51.
Аминогликозиды.Аминогликозидные антибиотики I-го, II-го и III-го поколений
HO
OH
OH
O
NH2
O
HO
HO
H2N
HO
NH
H2N
O
HO
NH2
OH
OH OH N
2
канамицин
HO HN
O
NH2
HO
HO
O
H2N
гентамицин
OH
O
HO
HO
H2N
O
HO
O
H2N
O
OH
O
NH2
O
N
H
OH
амикацин
Активны против грамотрицательных бактерий, особенно против палочки Коха
(туберкулёза), против некоторых патогенных грибков.
Аминогликозидные антибиотики ингибируют процесс синтеза матричного (рибосомального) белка.
Применению аминогликозидов препятствуют три обстоятельства:
1) очень гидрофильны и плохо всасываются при приёме внутрь;
2) сильные аллергены, обладают повышенной нейротоксичностью, вызывают ряд
побочных эффектов (нефротоксичность, глухота и др.);
3) к ним быстро развивается резистентность у патогенных организмов.
А.М. Чибиряев "Биологически активные соединения живых организмов", 2009
52.
ЭритромициныОтносятся к неполиеновым макролидам. Насчитывается около 100 природных
соединений этой группы. Продуцируются грибами Streptomyces. Занимают одно из
первых мест в мире по широте клинического применения.
Общее в строении – 12-, 14- и 16-членные лактоны (макролиды).
CH3 CH
R4
3
HO
CH3
OH
O
HO
CH3
O
H3C
R1
O
O
H3C
HO
H3C
CH3
NH2
O
CH3
R3
CHO
R2
O
CH3
CH3
R2
O
R5
O
R1
эритромицины
R1, R2 = H, OH, CH3
O
O-Gly
OR6
16-членные макролиды
Активны против грамположительных бактерий и микоплазмы, но практически не
действует на грамотрицательные. Ингибируют процесс синтеза матричного (рибосомального) белка.
В фармакологии: олеандомицин, эритромицин
спирамицин, тилозин (16-членные макролиды).
(14-членные),
лейкомицин,
53.
МакролидыN
HO
O
HO
HO
O
Et
O
O
O
O
O
H3CO
O
H3C
метимицин
HO
H3C
(12-членный макролид)
O
Et
эритромицин
(14-членный макролид)
OH
OH
OH
O
O
HO
O
Et O
N
HO
CHO
HO
O
O
O
O
OH
HO
CH3
OH OH OH
OH O
COOH
O
O
O
OH
N
розарамицин
(16-членный макролид)
нистатин
(38-членный полиеновый
макролид)
O
O
OH
NH2
OH
А.М. Чибиряев "Биологически активные
соединения живых организмов", 2009
54.
КЛАССИФИКАЦИЯ АБ (Р. Таушниц)b-лактамные антибиотики (бактерицидные)
(время-зависимые - Dраз., кратность):
Пенициллины
Несовместимы с аминогликозидами в 1 шприце, с
аллопуринолом – «ампициллиновая» сыпь
Природные: Гр « + »
бензилпенициллин (натриевая,
калиевая, новокаиновая соли),
бензициллин (бициллин) - 1, 3, 5,
бензатин бензилпенициллин,
феноксиметилпенициллин.
55.
Полусинтетические:1. Изоксазолилпенициллины
(пенициллиназоста-бильные,
антистафилококковые): оксациллин
2. Аминопенициллины: ампициллин,
амоксициллин
3. Карбоксипенициллины (антисинегнойные):
карбенициллин
4. Уреидопенициллины: азлоциллин,
пиперациллин
5. Ингибитор-защищенные пенициллины:
амоксициллин/клавуланат,
Гр « + » Гр « - »
(панклав, ранклав и др.)
амоксициллин/сульбактам
56.
b-лактамные антибиотики -Цефалоспорины
При сочетании с аминогликозидами и/или петлевыми диуретиками
возможно повышение риска нефротоксичности (особенно у
пациентов с нарушениями функции почек)
I поколение
Парентеральные
Цефазолин – лидер продаж 2005 г.
Пероральные
Цефалексин
Цефадроксил
Гр « + »
57.
II поколениеПарентеральные
Цефуроксим
Пероральные
Цефуроксим аксетил
Цефаклор
Гр « + » Гр « - »
58.
III поколениеПарентеральные
Цефтриаксон (Азаран, Цефаксон) – лидер закупок ЛПУ в 2006 г.
Цефотаксим (Цефантрал) – на втором месте по закупкам 2006 г.
Цефтазидим (Тизим) – на 5-м месте, но самый быстрый рост за год.
Цефоперазон – спад закупок на 35%
Пероральные
Цефиксим (Супракс)
Цефтибутен
Гр « - »
59.
IV поколениеПарентеральные
Активны в отношении некоторых штаммов, устойчивых к III поколению
цефалоспоринов.
Более высокая устойчивость к b-лактамазам широкого и расширенного
спектра действия.
Показания - лечение тяжелых нозокомиальных инфекций, вызванных
полирезистентной флорой; инфекций на фоне нейтропении.
Цефепим (Максипим
Цефпиром
–
спад
закупок
на
,
11%)
60. Достижения ветеринарной фармацевтики
Достижения ветеринарнойфармацевтики
Для лечения животных создан специализированный противобактериальный препарат из
группы цефалоспоринов , не применяющийся в медицине, - ЦЕФТИОФУР.
Цефтиофур ― ветеринарный цефалоспорин последнего поколения, который оказывает
бактерицидное действие
на
грамотрицательные и грамположительные бактерии,
включая штаммы, продуцирующие β-лактамазу, и некоторые анаэробные бактерии.
Быстро подвергается метаболизму с образованием десфуроилцефтиофура, который
обладает эквивалентной цефтиофуру активностью в отношении бактерий. Данный
метаболит обратимо связывается с белками плазмы и накапливается в очаге воспаления.
Активность препарата не снижается в присутствии некротизированных тканей.
На основе цефтиофура выпускается ряд ветеринарных препаратов, в том числе Актионис
(Laboratorios SYVA), Алцефур 50 (ALPOVET), Иноксел RTU (Vetanko), Наксел
(Zoetis Inc.), Тиоцефур («ВИК — здоровье животных»), Тиеркал (Livisto), Цефтимаг
10% суспензия («Мосагроген»), Цефтиофур 5% (KELA), Цемай (Laboratorios
Maymo), Цефтисил («Ареал Медикал»/«АВЗ С-П»), Цефтонит Форте (NITA-FARM),
Цефтиосан («Апиценна»), Эфикур (Laboratorios Hipra), Эксенел стерильный
порошок (Zoetis Inc.) и другие препараты.
60
61. Цефтимаг (цефтиофур) - антибиотик группы цефалоспоринов III поколения
Цефтимаг(10%
суспензия)
производится
компанией «Мосагроген». Цефтимаг вводят
животному в два раза меньшем объеме по
сравнению
с
ветеринарными
5%-ными
цефтиофурами.
Благодаря
этому
препарат
всасывается
из
внутримышечного
или
подкожного депо быстрее, чем препараты с
низкой концентрацией активного вещества. По
сравнению
с
аналогами,
имеющими
концентрацию в 2 раза меньше, Цефтимаг
высокоэффективен при лечении бактериальных
патологий и экономичен, так как для лечения
требуется вдвое меньший объем лекарственного
средства,
безопасен
в
продовольственном
отношении,
так
как
сокращаются
сроки
разрешенного
убоя
после
последнего
применения
препарата,
что
позволяет
использовать молоко без ограничений.
61
62.
b-лактамные антибиотикиКарбапенемы:
Меропенем, эртапенем
(4-6 место по закупкам в 2006 г.)
Препараты резерва, более устойчивые к
действию бактериальных b-лактамаз, более
быстро проникают через наружную мембрану
грамотрицательных бактерий, обладают более
широким спектром активности и применяются
при тяжелых инфекциях различной
локализации, включая нозокомиальные
(внутрибольничные).
Несовместимы с другими бета-лактамами !
Гр « + » Гр « - » Анаэроб
63.
b-лактамные антибиотикиМонобактамы: (моноциклические b-лактамы)
Азтреонам – нет регистрации
Препарат резерва, узкого спектра
действия, назначаемый в сочетании с
препаратами, активными в отношении Гр «+»
кокков (оксациллин, цефалоспорины,
линкосамиды, ванкомицин), и анаэробов
(метронидазол)
Гр « - » аэробы
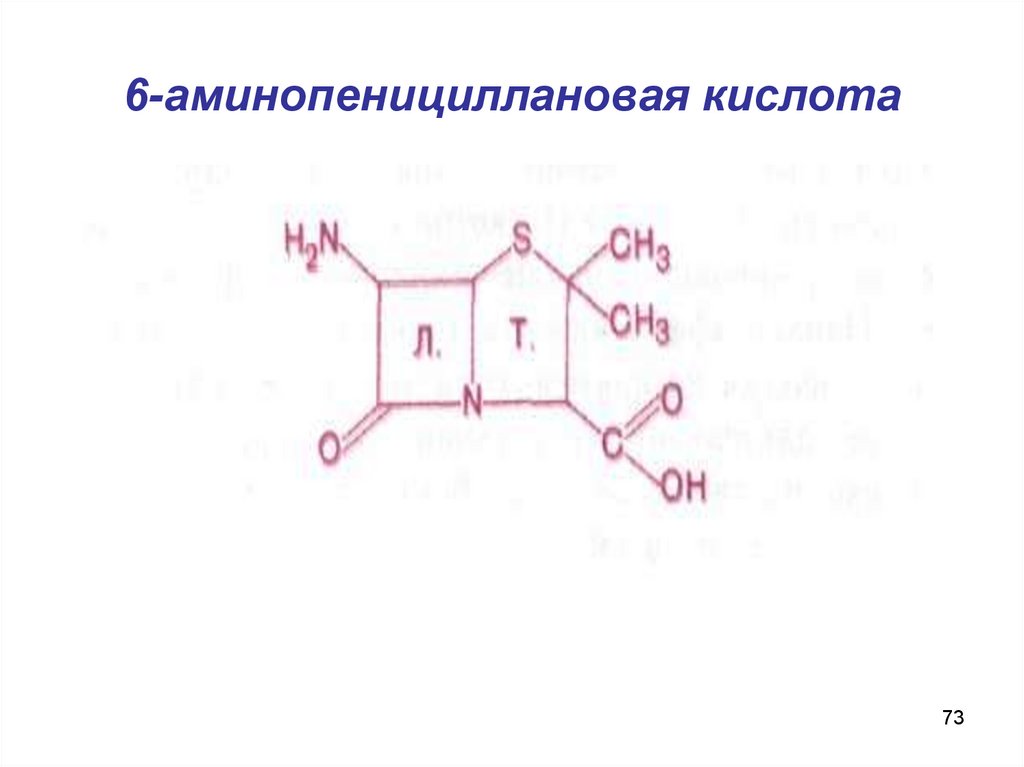
64. Пенициллины
Основой структуры препаратов является 6-ами-нопенициллиновая кислота, в состав которой
входят тиазолидиновое и бета-лактамное кольцо.
Пенициллины оказывают бактерицидное
действие.
Они влияют только на делящиеся клетки, в которых
наблюдается образование клеточной стенки.
Механизм актибактериального эффекта связан
с нарушением поздних этапов синтеза клеточной
стенки (образование мукопептида), т.к пенициллины препятствуют образованию пептидных связей за счет ингибирования фермента транспепти-
дазы.
64
65. Пенициллины
Особенностью фармакодинамики пеницил-линов является сильное бактерицидное
действие, низкая токсичность, хорошее
всасывание, большая широта терапевтического действия.
Низкая токсичность пенициллинов для
животных связана с тем, что пептидогликан,
синтез которого они ингибируют, отсутствует в клетках животного организма.
65
66. Классификация
I. Препараты пенициллинов, получаемые путембиологического синтеза (биосинтетические или
природные пенициллины)
Для парентерального введения (разрушаются в
кислой среде желудка)
а) Непродолжительного действия
Бензилпенициллина натриевая соль
Бензилпенициллина калиевая соль
б) Продолжительного действия
Бензилпенициллина новокаиновая соль
Бициллин-1, бициллин-3, бициллин-5
Для энтерального введения (кислотоустойчивы)
Феноксиметилпенициллин
66
67. Классификация
II. Полусинтетические пенициллиныДля парентерального введения
(разрушаются в кислой среде желудка)
а) Устойчивые к действию пенициллиназы
Метициллина натриевая соль
б) Широкого спектра действия
(антисинегнойные)
Карбенициллина динатриевая соль
Карфециллин
Пиперациллин
67
68. Классификация
Для парентерального и энтерального введения(кислотоустойчивы)
а) Устойчивые к действию пенициллиназы
(антистафилококковые)
Оксациллина натриевая соль
Диклоксациллина натриевая соль
б) Широкого спектра действия
Ампициллин
в) Комбинированные
Уназин (Ампициллин +Сульбактам)
Аугментин (Амоксициллин+ Клавулановая к-та)
Ампиокс (Ампициллин +Оксациллин)
68
69. Биосинтетические (природные пенициллины)
Получают культивированием гриба родаPenicillium.
Действуют антимикробно на грамположительные и
некоторые грамотрицательные микроорганизмы
(стрепто-, стафилококки, пневмококки, диплококки,
спирохеты, палоч-ки сибирки).
Бактерии кишечно-тифозной группы, бруцеллы,
микобактерии не реагируют на эти препараты, т.к.
вырабатывают пеницилиназу, разрушающую беталактамное кольцо.
69
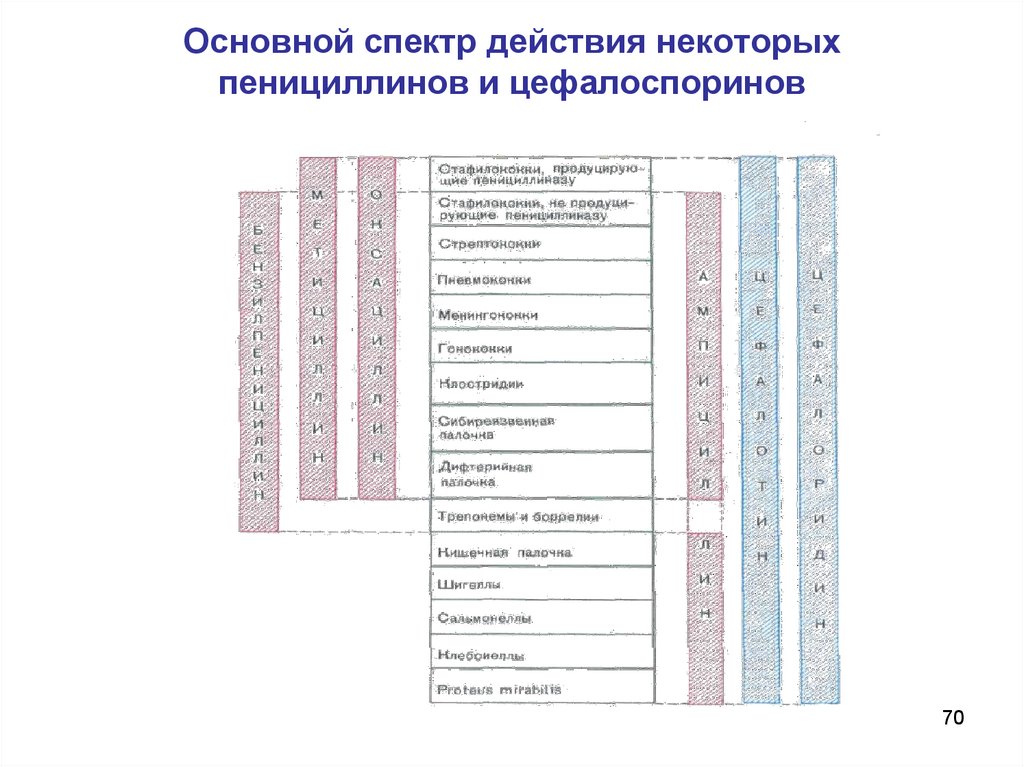
70. Основной спектр действия некоторых пенициллинов и цефалоспоринов
7071. Биосинтетические (природные пенициллины)
Вводят преимущественно в/м (кроме феноксиме-тилпенициллина), т.к. препараты разрушаются под
действием соляной кислоты желудочного сока.
Препараты короткого действия вводят 2-3 раза в
сутки, а препараты длительного действия 1 раз в 730 суток.
Применяют при некробактериозе, пастереллезе,
пневмониях, маститах, раневых инфекциях, инфекциях мочевыводящих путей, стахиботриотоксикозе
лошадей, гриппе, чуме пушных зверей и собак,
рожистом воспале-нии у свиней, спирохитозе птиц,
стрептококковой инфекции у КРС.
71
72. Полусинтетические пенициллины
Значительные возможности усовершенствования пенициллинов открылись с выделением их структурной основы — 6-аминопе-нициллановой кислоты.
Исследования были направлены на создание
пенициллинов:
а) устойчивых к действию пенициллиназы
б)кислотоустойчивых
в)пенициллинов широкого спектра
действия
72
73. 6-аминопенициллановая кислота
7374. Полусинтетические пенициллины
Характеризуются широким спектром антимикробно-го действия, стойкостью к разрушающему действию
кислот и пенициллиназ и повышенной частотой
развития аллергических реакций у животных.
Оксациллин, клоксациллин, флуклоксациллин –
действуют на Г+ флору (антистафилококковые пенициллины). Стойкие к действию бета-лактамаз. При
инфекциях другой этиологии уступают препаратам
естественного происхождения.
Ампициллин активный также к Г- флоре: кишечной
палочке, шигелле, сальмонелле. Разрушается пенициллиназой.
Карбенициллин – антибиотик широкого спектра
действия, активный к синегнойной палочке, протею.
74
75. Комбинированные пенициллины
Пенициллины, комбинированные с клавула-новой кислотой или сульбактамом,
которые имеют слабое противомикробное
действие, но угнетают активность бета-лактамаз многих микроорганизмов: гемофильной
и кишечной палочки, стафилококков.
Препараты предназначены только для
парентерального применения.
75
76. Побочные эффекты пенициллинов
Алергические реакцииДисбактериоз
Диспепсия (оксациллин, ампициллин)
Кровотечения, гипокалиемия (карбенициллин)
Нефротоксическое действие бензилпеницилли-
на проявляется в виде эпилептичес-ких судорог
(пенициллинова эпилепсия). Иногда такие приступы заканчиваются гибелью больного животного.
76
77.
Лекарственные взаимодействияПенициллины нельзя смешивать в одном
шприце или в одной инфузионной системе с
аминогликозидами ввиду их физикохимической несовместимости.
При сочетании ампициллина с
аллопуринолом возрастает риск
"ампициллиновой" сыпи.
Применение высоких доз
бензилпенициллина калиевой соли в сочетании
с калийсберегающими диуретиками,
препаратами калия или ингибиторами АПФ
предопределяет повышенный риск
гиперкалиемии.
78.
Лекарственные взаимодействияТребуется соблюдать осторожность при
сочетании пенициллинов, активных в
отношении синегнойной палочки, с
антикоагулянтами и антиагрегантами
ввиду потенциального риска повышенной
кровоточивости.
Следует избегать применения
пенициллинов в сочетании с
сульфаниламидами, так как при этом
возможно ослабление их бактерицидного
эффекта.
79.
Лекарственные взаимодействияПри сочетании с аминогликозидами и/или
петлевыми диуретиками, особенно у пациентов с
нарушениями функции почек, возможно повышение
риска нефротоксичности.
Антациды снижают всасывание пероральных
цефалоспоринов в ЖКТ. Между приемами этих
препаратов должны быть интервалы не менее 2 ч.
При сочетании цефоперазона с
антикоагулянтами, тромболитиками и
антиагрегантами возрастает риск кровотечений,
особенно желудочно-кишечных.
В случае употребления алкоголя на фоне
лечения цефоперазоном может развиваться
дисульфирамоподобная реакция.
80.
Лекарственные взаимодействияКарбапенемы нельзя применять в
сочетании с другими b-лактамными
антибиотиками ввиду их антагонизма.
Не рекомендуется смешивать
карбапенемы в одном шприце или
инфузионной системе с другими препаратами.
81.
Группа аминогликозидовБактерицидный эффект
I поколение:
Стрептомицин, Неомицин, Канамицин
II поколение:
Гентамицин, Тобрамицин, Нетилмицин
III поколение:
Амикацин
Гр « + » Гр « - » аэробы
82.
Механизм действия аминогликозидовБактерицидное действие, нарушение
синтеза белка рибосомами.
Степень антибактериальной активности
аминогликозидов зависит от их концентрации.
При совместном использовании с
пенициллинами или цефалоспоринами
наблюдается синергизм в отношении
грамотрицательных и грамположительных
аэробных микроорганизмов.
83.
Основное клиническое значениеаминогликозиды имеют при лечении
нозокомиальных инфекций, вызванных
аэробными грамотрицательными
возбудителями, а также инфекционного
эндокардита.
Стрептомицин и канамицин
используют при лечении туберкулеза.
Неомицин как наиболее токсичный
среди аминогликозидов применяется
только внутрь и местно.
84.
Лекарственные взаимодействияНельзя смешивать в одном шприце или одной
инфузионной системе с b-лактамными антибиотиками или
гепарином вследствие физикохимической несовместимости.
Усиление токсических эффектов при одновременном
назначении двух аминогликозидов или при их сочетании
с другими нефро- и ототоксичными препаратами:
полимиксином В, амфотерицином В, этакриновой
кислотой, фуросемидом, ванкомицином.
Усиление нервно-мышечной блокады при
одновременном применении средств для ингаляционного
наркоза, опиоидных анальгетиков, магния сульфата и
переливании больших количеств крови с цитратными
консервантами.
Индометацин, фенилбутазон и другие НПВП,
нарушающие почечный кровоток, замедляют скорость
выведения аминогликозидов.
85.
Группа макролидов и азалидовБактериостатический, а в больших дозах - бактерицидный эффект
14-членные (время-зависимые, D , кратность):
Природные - Эритромицин
Полусинтетические - Кларитромицин,
Рокситромицин
15-членные (азалиды – С-зависимые, Dсут.):
Полусинтетические – Азитромицин (Азивок,
раз.
Сумамед)
16-членные (время-зависимые, D , кратность):
Природные - Спирамицин, Джозамицин,
Мидекамицин
Полусинтетические - Мидекамицина ацетат
раз.
Гр « + »
86.
Механизм действияМакролиды временно прекращают
размножение грамположительных кокков.
Эффект обусловлен нарушением синтеза
белка рибосомами микробной клетки.
Как правило, макролиды оказывают
бактериостатическое действие, но в высоких
концентрациях способны действовать
бактерицидно на бета-гемолитический
стрептококк группы А, пневмококк,
возбудителей коклюша и дифтерии.
Обладают умеренной
иммуномодулирующей и
противовоспалительной активностью.
87.
Лекарственные взаимодействия (12)Макролиды ингибируют метаболизм и
повышают концентрацию в крови непрямых
антикоагулянтов, теофиллина,
карбамазепина, вальпроевой кислоты,
дизопирамида, препаратов спорыньи,
циклоспорина.
Опасно сочетать макролиды с
терфенадином, астемизолом и цизапридом
ввиду опасности развития тяжелых нарушений
сердечного ритма, обусловленных удлинением
интервала QT.
Макролиды увеличивают биодоступность
88.
Лекарственные взаимодействия (22)Антациды снижают всасывание
макролидов, особенно азитромицина, в ЖКТ.
Рифампицин усиливает метаболизм
макролидов в печени и снижает их
концентрацию в крови.
Макролиды не следует сочетать с
линкосамидами ввиду сходного механизма
действия и возможной конкуренции.
Эритромицин, особенно при в/в введении,
способен усиливать всасывание алкоголя в
ЖКТ и повышать его концентрацию в крови.
89.
Группа тетрациклиновПриродные: тетрациклин
Полусинтетические: доксициклин
Сохраняют клиническое значение при
хламидийных инфекциях, риккетсиозах,
боррелиозах и некоторых особо опасных
инфекциях, тяжелой угревой сыпи.
Механизм действия
Обладают бактериостатическим
эффектом,
нарушая синтез
Гр « + » клетке.
Грбелка
« - »в микробной
90.
Лекарственные взаимодействия (12)При приеме внутрь одновременно с
антацидами, содержащими кальций,
алюминий и магний, с натрия
гидрокарбонатом и холестирамином может
снижаться их биодоступность вследствие
образования невсасывающихся комплексов и
повышения рН желудочного содержимого.
Поэтому между приемами перечисленных
препаратов и антацидов необходимо
соблюдать интервалы 1-3 ч.
Не рекомендуется сочетать тетрациклины
с препаратами железа, поскольку при этом
91.
Лекарственные взаимодействия (22)Карбамазепин, фенитоин и
барбитураты усиливают печеночный
метаболизм доксициклина и снижают его
концентрацию в крови, что может потребовать
коррекции дозы данного препарата или замены
его на тетрациклин.
При сочетании с тетрациклинами
возможно снижение надежности
эстрогенсодержащих пероральных
контрацептивов.
Тетрациклины могут усиливать действие
непрямых антикоагулянтов вследствие
92.
Группа линкозамидовПриродные: линкомицин
Его полусинтетический аналог: клиндамицин
Механизм действия
Бактериостатическое действие
обусловлено ингибированием синтеза белка
рибосомами.
В высоких концентрациях - бактерицидный
эффект.
Узкий спектр антимикробной активности Гр «+» кокки (в качестве препаратов второго
ряда) и анаэробнаяГр
флора
« + »(неспорообразующая).
93.
Лекарственные взаимодействияАнтагонизм с хлорамфениколом и
макролидами.
При одновременном использовании с
опиоидными анальгетиками,
ингаляционными наркотическими
средствами или миорелаксантами возможно
угнетение дыхания.
Каолин- и аттапульгит-содержащие
противодиарейные препараты снижают
всасывание линкосамидов в ЖКТ, поэтому
между приемами этих препаратов необходимы
интервалы 3-4 ч.
94.
Группа гликопептидовПриродные:
(Капреостат)
ванкомицин,
капреомицин
(рост закупок в 2006 г.)
Механизм действия
Нарушают синтез клеточной стенки
бактерий. Оказывают бактерицидное действие,
однако в отношении энтерококков, некоторых
стрептококков и коагулазонегативных
стафилококков действуют бактериостатически.
Препараты выбора при инфекциях,
вызванных MRSA, а также энтерококками,
резистентными
к
ампициллину
и
Гр « + »
аминогликозидам. TBC.
95.
Лекарственные взаимодействияПри одновременном применении с
местными анестетиками увеличивается риск
развития гиперемии и других симптомов
гистаминовой реакции.
Аминогликозиды, амфотерицин В,
полимиксин В , циклоспорин, петлевые
диуретики увеличивают риск нейротоксических
эффектов гликопептидов.
Аминогликозиды и этакриновая
кислота повышают риск ототоксического
действия гликопептидов.
96.
Группа полимиксиновПолимиксин В - парентеральный
Полимиксин М - пероральный
Механизм действия
Оказывают бактерицидное действие,
которое связано с нарушением целостности
цитоплазматической мембраны микробной
клетки.
Узкий спектр активности, высокая
токсичность. Полимиксин В - резервный
препарат, применяемый при лечении
синегнойной инфекции, Полимиксин М Гр
«
»
инфекции ЖКТ.
97.
Лекарственные взаимодействияНе следует сочетать полимиксин В с
аминогликозидами и амфотерицином В
(повышение риска нефротоксичности),
а также с миорелаксантами и анестетиками
(угроза развития паралича дыхательных
мышц).
98.
Группа ансамициновПриродные: рифамицин
Полусинтетические: рифампицин, рифабутин
Механизм действия
Бактерицидный эффект, специфические
ингибиторы синтеза РНК.
Широкий спектр активности.
Рифампицин - ПТП
(противотуберкулезный
препарат) первого
ряда,
Гр « + » Гр « - »
Рифабутин - ПТП второго ряда.
99.
Лекарственные взаимодействияРифампицин - индуктор микросомальных
ферментов системы цитохрома P-450; ускоряет
метаболизм многих лекарственных препаратов:
непрямых антикоагулянтов, пероральных
контрацептивов, глюкокортикоидов,
пероральных противодиабетических
средств; дигитоксина, хинидина,
циклоспорина, хлорамфеникола,
доксициклина, кетоконазола, итраконазола,
флуконазола.
Пиразинамид снижает концентрацию
рифампицина в плазме крови в результате
воздействия на печеночный или почечный
100.
Группа амфениколовПриродный: Хлорамфеникол (Левомицетин, Синтомицин)
Полусинтетические:Тиамфеникол
Механизм действия
Бактериостатическое действие, из-за
нарушения синтеза белка рибосомами.
В высоких концентрациях обладает
бактерицидным эффектом в отношении
пневмококка, менингококка и H.influenzae.
Используется как препарат II ряда при
лечении менингита, риккетсиозов,
сальмонеллезов и анаэробных инфекций.
101.
Лекарственные взаимодействияАнтагонист макролидов и линкосамидов.
Снижает эффективность
препаратов железа, фолиевой кислоты и
витамина В12 за счет ослабления их
стимулирующего действия на гемопоэз.
Ингибитор микросомальных ферментов
печени, усиливает эффекты пероральных
противодиабетических препаратов,
фенитоина, варфарина.
Индукторы микросомальных ферментов
печени (рифампицин, фенобарбитал и
фенитоин) снижают концентрацию
хлорамфеникола в сыворотке крови.
102.
Благодарю за внимание !102


































































































 medicine
medicine








