Similar presentations:
Растворы. Основные положения
1. РАСТВОРЫ
2. Основные положения
Растворение – это физико-химическийпроцесс.
Физическая сторона – растворяющее
вещество теряет свою структуру,
разрушается.
Химическая сторона – растворяемое
вещество взаимодействует с
растворителем- сольватация- образуются
сольваты, если растворение идет в воде, то
процесс называется гидратацией образуются гидраты.
3.
Насыщенный раствор– это раствор который
находится в равновесии
с растворяющимся
веществом.
4. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ
5.
Концентрация раствора –это количество растворенного
вещества, содержащегося в
единице массы и объема
раствора или растворителя.
6. 1. Молярная концентрация
Молярная концентрация –характеризует число молей
растворенного вещества в одном
литре раствора
m( р.в.)
n( р.в.)
СМ
М ( р.в.) V
V
моль
[СМ ]
л
7.
m (р.в.) - масса растворенноговещества, г;
М (р.в.) – молярная масса
растворенного вещества,
г/моль;
V – объем раствора, л.
8. 2. Молярная концентрация эквивалента или нормальность
Молярная концентрацияэквивалента или нормальность –
выражает число моль эквивалентов в
одном литре раствора
m( р.в.)
СМ Э
М Э ( р.в.) V
моль экв
[СМ Э ]
л
9. 5. Массовая доля
Массовая доля – это число единицмассы растворенного вещества
содержащееся в ста единицах массы
раствора
m( р.в.)
100%
m( р ра)
10. 6. Титр раствора
Титр раствора – массарастворенного вещества в 1
мл раствора
m( р.в.)
Т
V
г
[T ]
мл
11.
Екип – это моляльная константаповышения температуры кипения
растворителя или его
эбуллиоскопическая константа,
которая зависит от природы
растворителя.
Екип приведена в справочниках.
12. ПРИМЕР:
Вычислить температурукипения 4,6% раствора
глицерина в воде.
Молекулярная масса
глицерина С3Н8О3 равна 92,
Екип для воды равна 0,52.
13. 2б. Понижение температуры затвердевания растворов
Второй закон Рауля:б) Понижение температуры
затвердевания растворов
пропорционально моляльной
концентрации раствора
Tзатв К затв Сm
14.
Кзатв – это моляльнаяконстанта понижения
температуры
затвердевания или
криоскопическая константа
(для растворителя).
15. ПРИМЕР
Вычислить температурузатвердевания раствора
состоящего из 100 гр
этиленгликоля С2Н6О2
(М=62) и 900 граммов
воды, Кзатв=1,86.
16. 3. Осмотическое давление
Раствор представляет собойоднородную систему.
Частицы растворенного вещества и
растворителя находятся в
беспорядочном тепловом движении
и равномерно распределяются по
всему объему раствора.
17.
Молекулы растворителя ирастворенного вещества будут
диффундировать преимущественно
в том направлении, где их
концентрация ниже.
Такая двухсторонняя диффузия
приведет к выравниванию
концентраций и С1=С2.
18.
Однакодиффузия бывает односторонней,
если растворы разделить полупроницаемой
перегородкой,
пропускающей
только
молекулы растворителя.
При этом условии, что С2>С1 молекулы
растворителя с большей скоростью будут
диффундировать в направлении С1 С2 и
объем раствора с концентрацией С2
несколько возрастет. Такая односторонняя
диффузия называется осмосом.
19.
Для количественной характеристикиосмотических свойств вводится понятие
осмотического давления.
Осмотическое давление – это такое
давление, которое нужно приложить, чтобы
осмос прекратился.
.
20.
Вант –Гофф предложил, что дляосмотического давления можно
применять уравнение состояния
идеального газа
PV nRT
n
P RT
V
21.
n( р.в.)СМ
V
P CM RT
СМ – молярная концентрация
раствора. Растворы с одинаковым
осмотическим давлением
называются изотоническими.
22. ПРИМЕР:
Вычислить осмотическоедавление при 270 С раствора
сахара С12Н22О11 (М=342) 1
литр которого содержит 91г
сахара.
23. СВОЙСТВА РАСТВОРОВ ЭЛЕКТРОЛИТОВ
24.
Процесс распада вещества на ионыпри растворении называется
электролитической
диссоциацией.
Количественной характеристикой
этого процесса является степень
электролитической
диссоциации ( )
25.
Cтепень электролитическойдиссоциации ( ) - это
количество распавшихся на
ионы молекул к общему
количеству растворенных
молекул.
26.
По величине различают:а) сильные электролиты
> 0,3
б) электролиты средней силы
0,03 < < 0,3
в) слабые электролиты
< 0,03
27.
При диссоциации в растворахслабых электролитов
устанавливается равновесие
между недиссоциированными
молекулами и продуктами их
диссоциации – ионами.
28. Пример: диссоциация уксусной кислоты
СН3СООН=СН3СОО– + Н+В водном растворе устанавливается
равновесие которое количественно
характеризуется константой равновесия,
иначе константой диссоциации:
29.
Обозначим концентрации каждого изионов:
CH CCH COO C
3
а концентрацию СH3COOH:
CCH3COOH (1 )C
30.
Тогда константу диссоциации2
запишем:
(C )
KД
C (1 )
С
KД
1
2
31.
это закон1
КД
С
разбавления
Оствальда для
слабых электролитов
Степень диссоциации
возрастает при
разбавлении
раствора.
32.
Сильные электролиты врастворе диссоциируют на
ионы.
Рассмотрим примеры
диссоциации кислот,
оснований, солей.
33. Диссоциация H2SO4
Диссоциация H2SO4Серная кислота
двум ступеням:
диссоциирует
H2SO4 = H+ + HSO4 –
HSO4 – = H+ + SO4 2–
+
2–
H2SO4 = 2H + SO4
по
34. Диссоциация NaOН
+–
NaОH = Na + OH
35. Диссоциация солей
KCI = K+ + CI–3+
2–
Al2(SO4)3 = 2Al + 3SO4
36.
Экспериментальноопределяемые для сильных
электролитов степени
диссоциации называют
кажущимися ( каж)
как правило каж не равно 100%
(или 1).
37.
Диссоциация электролита приводит к тому, что общеечисло частиц растворенного вещества молекул и
ионов в растворе возрастает по сравнению с
раствором неэлектролита той же молярной
концентрации, а коллигативные свойства зависят от
концентрации растворенного вещества, то поэтому
коллигативные свойства для растворов электролитов
сильно отличаются в равных по концентрации
растворах неэлектролитов.
Это различие учитывается с помощью изотонического
коэффициента ( i )
38. Изотонический коэффициент
Это отношение общего числа частиц врастворе к числу растворенных молекул
В растворах электролитов реально
существующее число частиц > числа
растворенных молекул
Поэтому вводится поправочный
коэффициент (i), учитывающий изменение
числа частиц:
n реальное
i
nобщее
39.
Изотонический коэффициент (i) –показывает во сколько раз
концентрация частиц в растворе больше
числа растворенных молекул.
Тогда коллигативные свойства для
растворов электролитов, будут
определятся по формулам с учетом
изотонического коэффициента.
40.
Изотонический коэффициент ( i ) можетбыть вычислен как отношение Р, Ткип,
Тзатв, Росм, найденных на опыте к тем же
величинам, вычисленным без учета
диссоциации электролита:
Pопыт Tзатв.( опыт ) Tкип.( опыт )
i
Pвыч Tзатв.( выч ) Tкип.( выч )
41.
Изотонический коэффициент ( i ) истепень электролитической диссоциации
( ) связаны между собой соотношением:
i 1
n 1
n – число ионов на которые распадается при
диссоциации молекула электролита:
KCI = K+ + CI–
n=2
Al2(SO4)3 = 2Al3+ + 3SO4 2–
n=5
42. Пример:
Вычислить осмотическое давление(170С) раствора Na2SO4 в 1 литре
которого содержится 7,1 грамма
растворенной соли. Кажущаяся
степень электролитической
диссоциации соли в растворе равна
0,69 или (69%)
43. ПРОИЗВЕДЕНИЕ РАСТВОРИМОСТИ
44.
В насыщенном растворемалорастворимых соединений
устанавливается равновесие между
осадком и ионами электролита в
растворе
BaSO4 → Ba2+ + SO4 2–
KP = ПР = [Ba2+]·[SO4 2–] = 1,1·10–10
45. Произведение растворимости
Произведение растворимости равноконстанте равновесия реакции, равно
произведению молярных концентраций
ионов участвующих в равновесии каждая
из которых введена в степень, равную
стехиометрическому коэффициенту при
соответствующем ионе в уравнении
равновесия.
46. Пример:
2+3Ca3(PO4)2 = 3Ca + 2PO4
ПР=[Ca2+]3·[PO43-]2 =Kp
47. ПРИМЕР 1.
Растворимость гидроксидамагния при 180С равна 1,7*10–
4 моль/л. Найти произведение
растворимости.
48. ПРИМЕР 2
Произведениерастворимости СаF2
=3,9·10–11. Какова
растворимость СаF2 в воде(
в г/литр и молях/литр).
49.
Условием образования осадкаявляется превышение
произведения концентраций
ионов малорастворимого
электролита над его
произведением
растворимости.
50.
Будет ли образовываться присмешении
равных
объемов
нитрата свинца с концентрацией
12·10–4 моль/л и сульфата натрия
с концентрацией 8·10–3 .
ПР = [Pb2+]·[SO42-]=1,6·10–8.
51. Константа диссоциации воды
Вода - слабый электролит+
–
Н2О = Н + ОН
[ H ] [OH ]
16
KД
1,86 10
[ H 2O ]
52. Ионное произведение воды:
1 л. H2O содержит 55,5 моль H2OKд.[H2O] = 1,86.10–16.55,5 =
= [H+].[OH–] = 10–14 = Кw
Кw не зависит от
концентрации ионов
53. Водородный показатель
Кислотность или основность водныхрастворов характеризуется концентрацией
[Н+] или [ОН–] ионов
Удобнее использовать логарифмическое
выражение:
рН = - lg [H+] и pOH = - lg [OH–]
Для воды [Н+] = [ОН–] = 10–7
рН = рОН = 7 - нейтральная среда
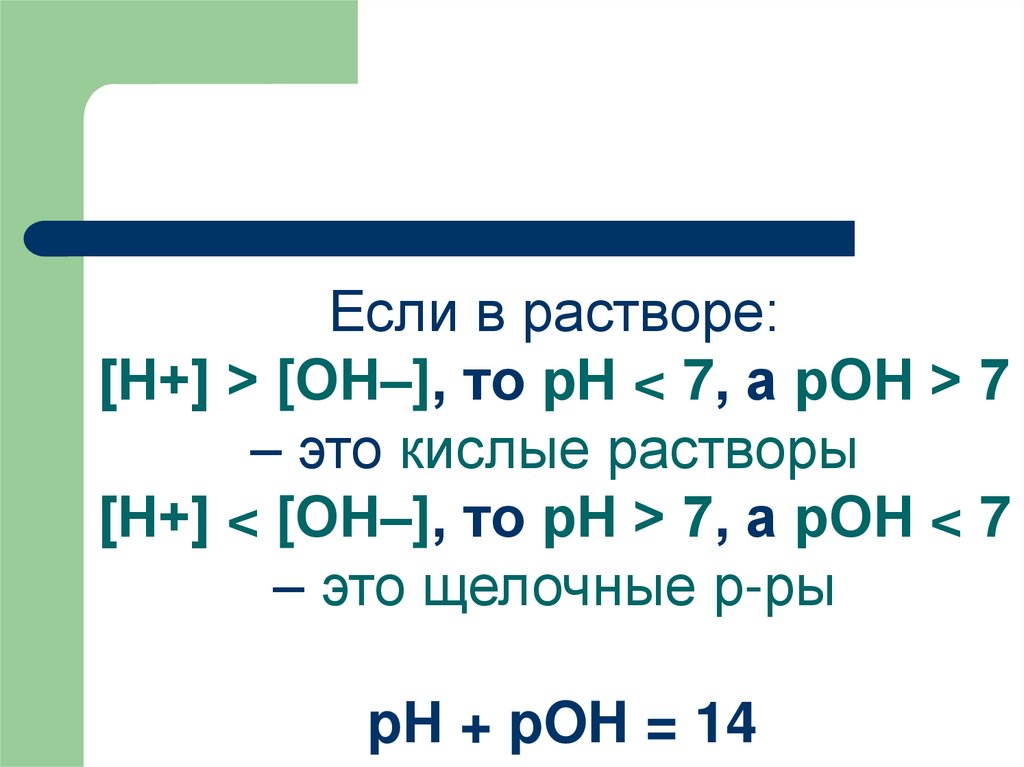
54.
Если в растворе:[Н+] > [ОН–], то рН < 7, а рОН > 7
– это кислые растворы
[Н+] < [ОН–], то рН > 7, а рОН < 7
– это щелочные р-ры
pН + pOH = 14

































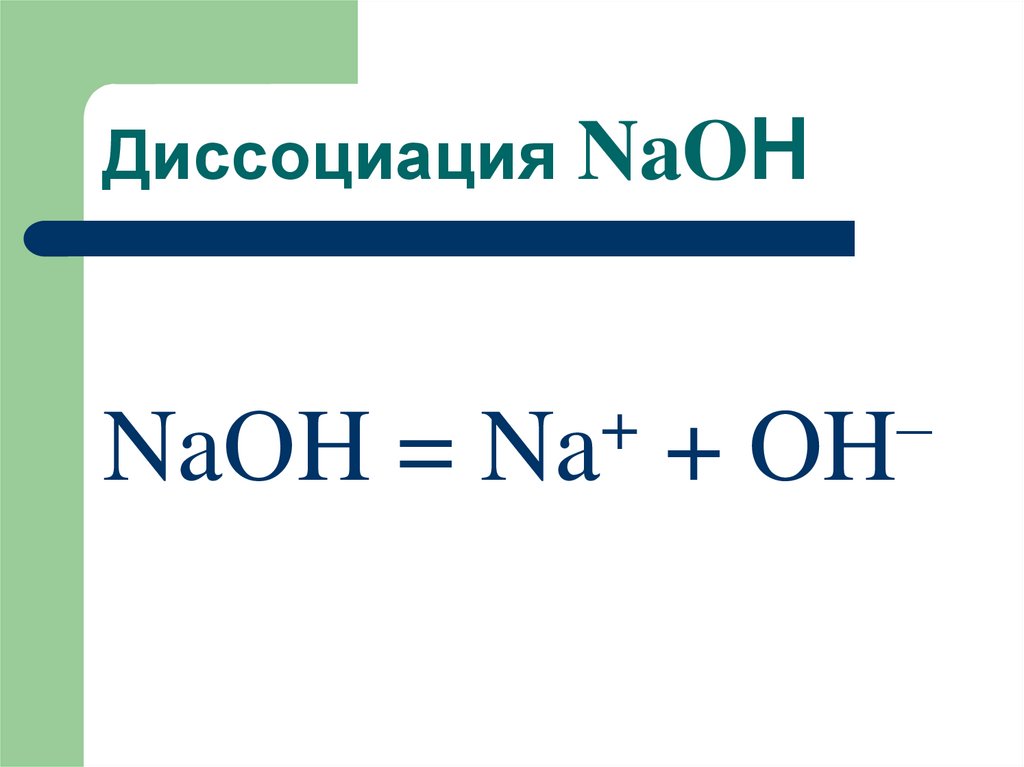



















 chemistry
chemistry








