Similar presentations:
Оксиды. Физические и химические свойства
1. Тема урока «Оксиды»
2. План работы по теме «Оксиды»
ОпределениеКлассификация
Номенклатура
Физические свойства
Химические свойства
Получение
Применение
3. Подумай, закончи строфу!
С кислородом ходит парой,То металл, то неметалл он,
Дружбу связями скрепит
Всем известный класс - …
4.
Слайд – «ключ»Оксиды – это сложные вещества,
которые состоят из двух элементов,
одним из которых является кислород.
Общая формула оксидов – RnOm.
5. Относятся к оксидам:
MgO, H2O, Na2O, CO2, FeO, CO, SO3,N2O5, K2O, SO2, CaO, Fe2O3
6.
Слайд – «ключ»Оксиды
Оксиды
металлов
Оксиды
неметаллов
7. Классификация оксидов
Оксидыосновные
Li2O + H2O = 2LiOH
растворимое основание
– гидроксид лития
I,II,III
СaO – оксид кальция
CuO – оксид меди (II)
кислотные
P2O5 + 3H2O = 2H3PO4
ортофосфорная
кислота
Me
V,VI,VII
P2O5 – оксид фосфора (V)
SO3 – оксид серы (VI)
8. Запомни!
Неметаллы, знай, мой друг,Строго все себя ведут:
Коль в оксиды он подался –
Так «кислотным» и назвался!
Металл хотел запутать нас,
Но я найду опору:
Валентность меньше четырех –
Оксид зову «основным».
Ну а уж если повезло,
Валентность пять и выше –
Я буду помнить, всем назло,
Оксид «кислотным» кличут.
9. Номенклатура оксидов
MgO – оксид магния,H2O – оксид водорода,
Na2O – оксид натрия.
10. Дайте названия оксидам
CO2, FeO, CO, SO3, N2O5, K2O, SO2,CaO, Fe2O3
11. Примеры названия оксидов, в которые входят элементы с переменной валентностью
IICO – оксид углерода (II)
IV
CO2 – оксид углерода (IV)
12. Физические свойства оксидов
Широка натура у оксидов,Камнем вниз, а то рекой течет,
А захочет – газ различных видов,
И веществ создаст круговорот.
Может черным быть, и белым,
Может с запахом и без,
Не оставит вас без дела:
«Изучайте – мир чудес!»
13.
Слайд – «ключ»Широка натура у оксидов,
Камнем вниз (CuO, CaO), а то рекой течет (H2O),
А захочет – газ различных видов (CO2, SO2),
И веществ создаст круговорот (CO2, H2O, SO3) .
Может черным быть (CuO), и белым (CaO),
Может с запахом (SO2) и без (CO2),
Не оставит вас без дела:
«Изучайте – мир чудес!»
14. Химические свойства оксидов
основных1.
2.
Основные оксиды
взаимодействуют с
кислотами, получаются соль
и вода:
CuO + H2SO4 = CuSO4 + H2O
Оксиды активных металлов
взаимодействуют с водой с
образованием растворимых
оснований - щелочей:
Li2O + H2O = 2LiOH
кислотных
1.
2.
Кислотные оксиды
взаимодействуют с
растворимыми основаниями,
получаются соль и вода:
СO2 + Ca(OH)2 = CaCO3 +
H2O
Большинство кислотных
оксидов взаимодействуют с
водой с образованием
кислоты:
P2O5 + 3H2O = 2H3PO4
3. Основные и кислотные оксиды взаимодействуют между собой
с образованием соли: CaO + СО2 = CaCO3
4. Менее летучие кислотные
оксиды вытесняют более летучие
из их солей:
CaCO3 + SiO2 = CaSiO3 + CO2
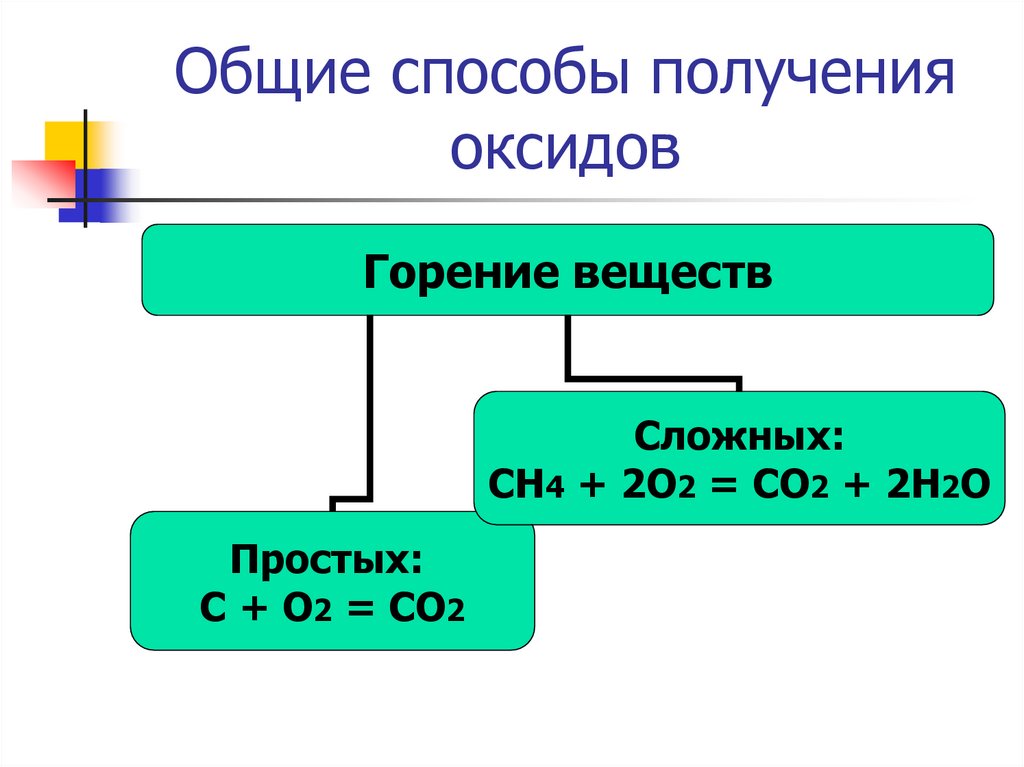
15. Общие способы получения оксидов
Горение веществСложных:
CH4 + 2O2 = CO2 + 2H2O
Простых:
C + O2 = CO2
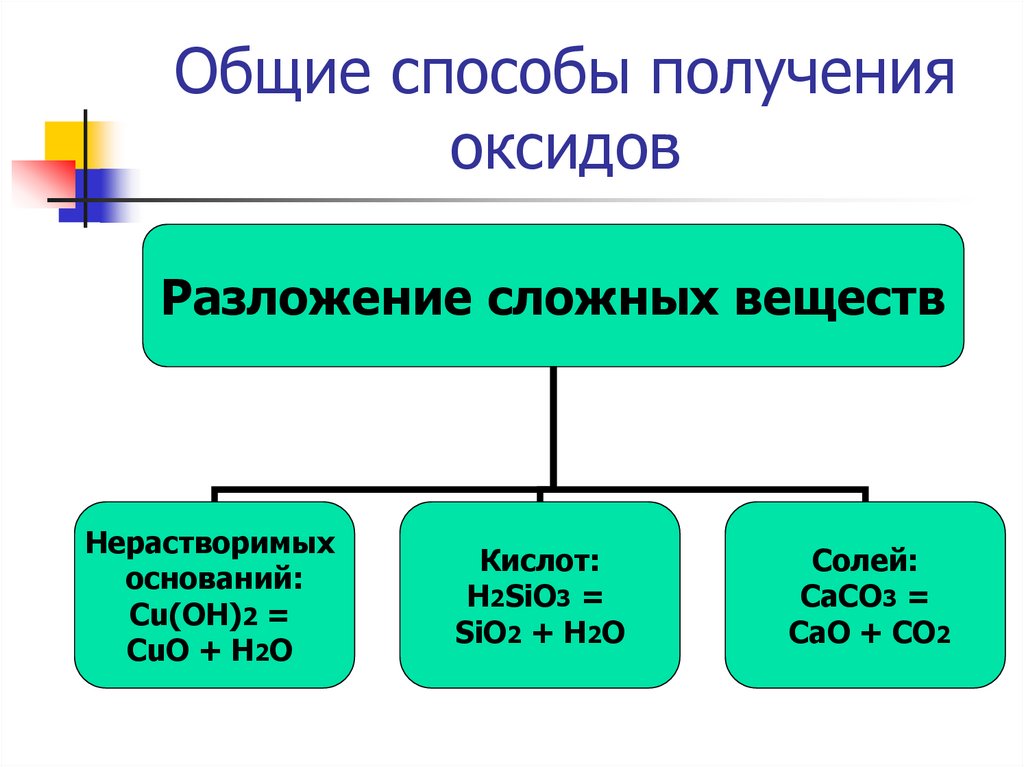
16. Общие способы получения оксидов
Разложение сложных веществНерастворимых
оснований:
Cu(OH)2 =
CuO + H2O
Кислот:
H2SiO3 =
SiO2 + H2O
Солей:
CaCO3 =
CaO + CO2
17. Основные области применения оксидов
В промышленности: Fe2O3 и Fe3O4 – производствочугуна и стали, СaO и SiO2 – производство строительных
материалов, CO2 - в пищевой промышленности для
производства газированных напитков, H2O – в
производственных охладительных системах, для
получения новых веществ, в системах орошения, в
качестве растворителя и т.д.
В быту: H2O – в питьевых и хозяйственных целях, SiO2 –
входит в состав чистящих веществ, ZnO – входит в состав
белой краски.
В природных процессах: H2O и CO2 – обеспечивают
осуществление процесса фотосинтеза, H2O – естественный
растворитель, составляет основную часть цитоплазмы
животных и растительных клеток и т.д.
18.
1. Напишите формулы оксидов следующих элементов: а) натрия, б) железа II, в)калия, г) фосфора (V), д) водорода, е) лития.
2. В каком из предложенных вариантов приведены формулы только кислотных
оксидов: А) SO3, Na2O, CuO
Б) SO2, CO2, P2O5,
B) BaO, Cl2O7, K2O.
Г) Br2O7, NO2 ,SiO2,
Д) Li2O, Fe2O3, CaO,
Е) CaO, K2O, Li2O
3. Допишите уравнения химических реакций и уравняйте:
P + … = P2O5
CH4 + O2 = ….. + H2O
Li + ….. = Li2O.
С + …. = СО2
Li2O + …. = LiOH
…. + H2O = H2SO4
… + K2O = KOH
CaO + … = Ca(OH)2
…. + O2 = Fe2O3.















 chemistry
chemistry








