Similar presentations:
Метаболизм липидов
1.
МЕТАБОЛИЗМ ЛИПИДОВSvetlana Protopop
doctor în științe medicale,
conferențiar universitar
2.
Структура и функциилипидов
3.
Липиды• Гетерогенная группа химических
соединений, общим свойством которых
является:
нерастворимость в воде;
растворимость в органических
растворителях (эфир, хлороформ, бензол).
4.
Функции липидов• Энергетическая – 9,3 kcal/g (жирные кислоты)
• Резервная – триглицериды
• Структурная (все амфифильные липиды)
• Теплоизоляция – триглицериды
• Электроизоляция – липиды нервных клеток
• Механическая защита – триглицериды
• Регуляторная – гормоны, производные
холестерола
• Витаминная – витамины А, D, E, K
5.
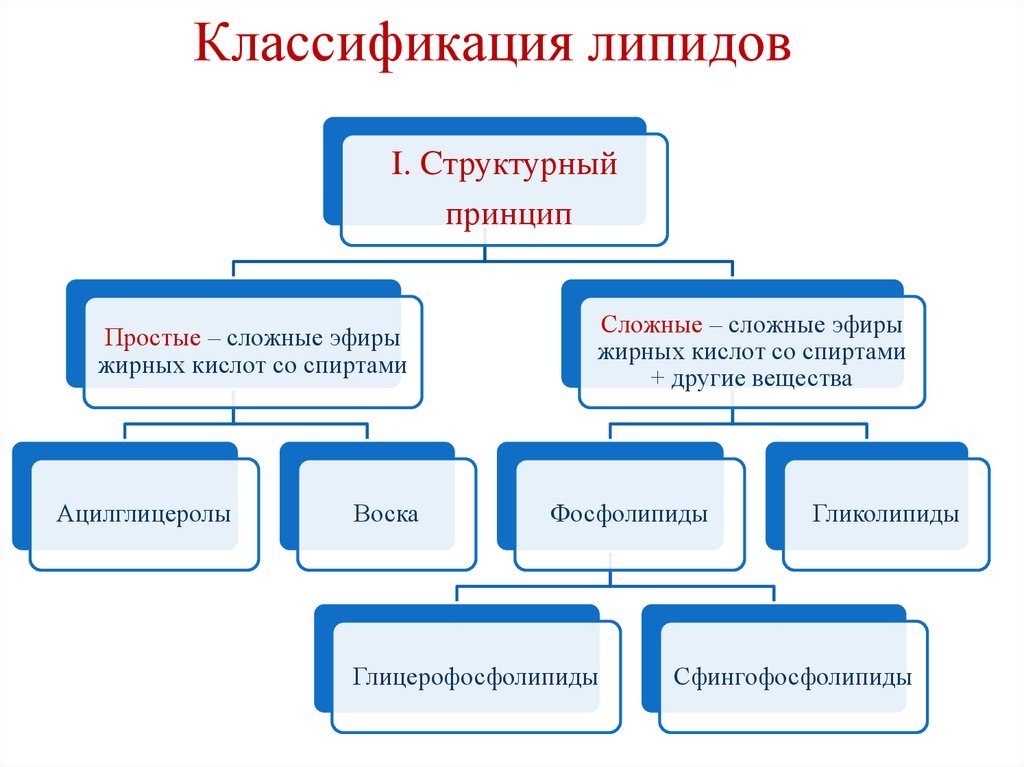
Классификация липидовI. Cтруктурный
принцип
Простые – сложные эфиры
жирных кислот со спиртами
Ацилглицеролы
Воска
Сложные – сложные эфиры
жирных кислот со спиртами
+ другие вещества
Фосфолипиды
Глицерофосфолипиды
Гликолипиды
Сфингофосфолипиды
6.
Классификация липидовII. Физико-химический принцип:
1. Нейтральные – триглицериды и эфиры
холестерола;
2. Полярные (амфифильные) – все остальные.
III. Функциональный принцип:
1. Резервные – триглицериды и эфиры
холестерола;
2. Структурные – все остальные.
7.
Жирные кислоты (ЖК)R COOH
I. Насыщенные (окончание -ановая)
II. Ненасыщенные (окончание -еновая):
• Моноеновые;
• Полиеновые.
В состав природных жиров обычно входят
ЖК с четным числом атомов углерода.
Двойные связи обычно в цис-конфигурации.
8.
Стеариновая и олеиновая кислоты9.
Насыщенные жирные кислотыСимвол Название
Распространение
С2
Уксусная
Главный конечный продукт углеводного брожения у
жвачных животных.
С4
Масляная
Присутствует в сливочном масле.
С6
Капроновая
Присутствует в сливочном масле.
С8
Каприловая
Присутствует в сливочном масле и в животных жирах.
С10
Каприновая
Присутствует в сливочном масле и в животных жирах.
С12
Лауриновая
Спермацетовый жир, кокосовое масло.
С14
Миристиновая
Мускатный орех, кокосовое масло.
С16
Пальмитиновая Во всех животных и растительных жирах.
С18
Стеариновая
Во всех животных и растительных жирах.
С20
Арахидиновая
Арахисовое масло.
С22
Бегеновая
Семена растений.
С24
Лигноцеровая
Цереброзиды, арахисовое масло.
10.
Ненасыщенные жирные кислотыСимвол
Название
Распространение
С16:1; Δ9
Пальмитолеиновая
(цис-9-гексадеценовая)
Почти во всех жирах.
С18:1; Δ9
Олеиновая
(цис-9-октадеценовая)
Самая распространенная во всех
природных жирах.
С24:1; Δ15
Нервоновая (цис-15тетракозеноевая )
Присутствует в цереброзидах.
С18:2; Δ9,12
Линолевая (цис-9,12октадекадиеновая)
Пшеница, арахис, соя, многие
растительные масла.
С18:3; Δ9,12,15
Линоленовая (цис-9,12,15- Часто обнаруживается вместе с
октадекатриеновая)
линолевой к-той.
С20:4; Δ5,8,11,14
Арахидоновая
(цис-5,8,11,14эйкозатетраеноевая)
Часто обнаруживается вместе с
линолевой к-той; важный компонент
фосфолипидов животных.
С20:5; Δ5,8,11,14,17
Тимнодоновая
(цис-5,8,11,14,17эйкозапентаеноевая, EPA)
Важный компонент рыбьего жира
(печень трески).
11.
Незаменимые жирные кислоты• Полиеновые жирные кислоты (линолевая и
линоленовая) не синтезируются в
человеческом организме – незаменимые
жирные кислоты (витамин F).
• Арахидоновая кислота синтезируется из
линолевой кислоты.
• Ω – углерод концевой метильной группы.
• Ω 6 – С18:2; Δ9,12
С20:4; Δ5,8,11,14
• Ω 3 – С18:3; Δ9,12,15 С20:5; Δ5,8,11,14,17
12.
АцилглицеролыСостав – глицерол + 1, 2 или 3 жирные кислоты
CH2 OH
CH
OH
R COOH
CH2 OH
Триацилглицеролы, триглицериды (ТАГ)
– сложные эфиры глицерола и 3-х
жирных кислот.
ТАГ являются нейтральными жирами.
Функция – резервная (жировая ткань) –
до 20% массы тела составляют ТАГ.
CH2 O
CH O
CH2 O
O
C
O
C
O
C
R1
R2
R3
13.
Глицерофосфолипиды(фосфоглицериды)
Состав:
Глицерол
2 жирные кислоты
Фосфорная кислота
Аминоспирт
CH2 O
CH
O
CH2 O
O
C
O
C
O
P
O-
R1
R2
O R3
14.
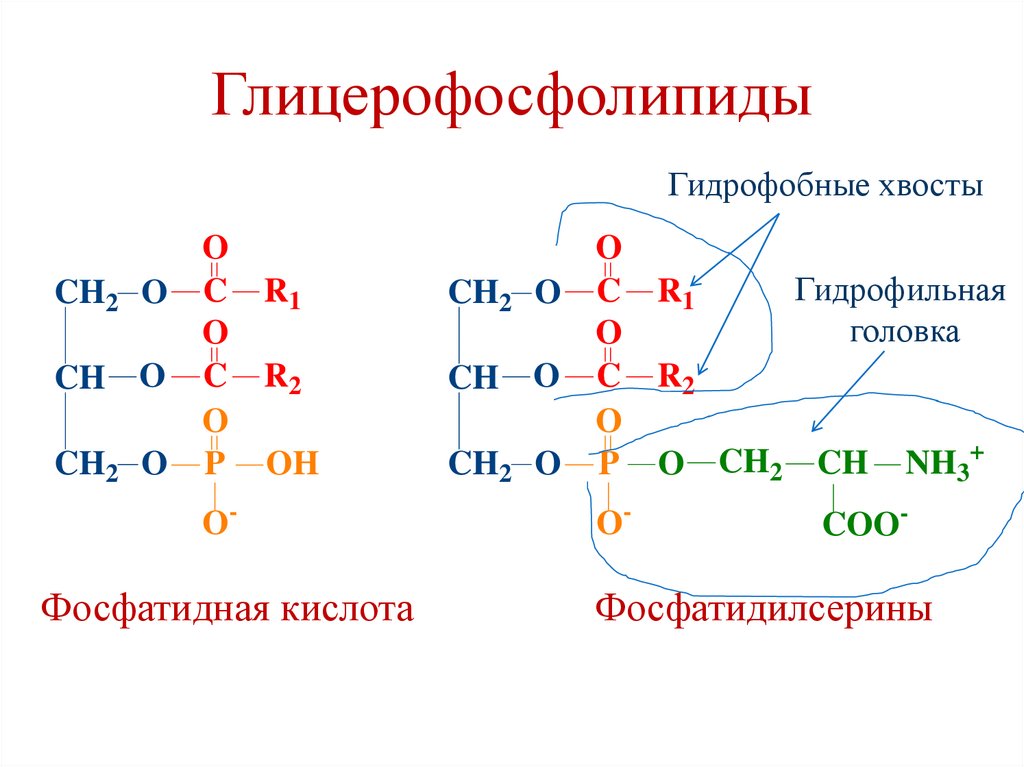
ГлицерофосфолипидыГидрофобные хвосты
CH2 O
CH
O
CH2 O
O
C
O
C
O
P
R1
CH2 O
R2
CH O
OH
CH2 O
O-
Фосфатидная кислота
O
C
O
C
O
P
O-
R1
Гидрофильная
головка
R2
O CH2
CH
NH3+
COO-
Фосфатидилсерины
15.
ГлицерофосфолипидыCH2 O
CH O
CH2 O
O
C
O
C
O
P
R1
R2
O CH2
Фосфатидилэтаноламины
(кефалины)
CH2 NH3+
O-
CH2 O
CH O
CH2 O
O
C
O
C
O
P
O-
R1
R2
O CH2
Фосфатидилхолины
(лецитины)
CH2 N+(CH3)3
16.
Функции глицерофосфолипидовГлицерофосфолипиды являются основными
структурными компонентами клеточных
мембран.
17.
ГлицерофосфолипидыCH2 O
CH
O
CH2 O
O
C R1
O
C R2
OH OH
O
P O
O-
OH
OH
OH
CH2 O
CH O
CH2 O
O
C R1
O
C R2
OH OH
O
P O
O-
Pi O
OH
O Pi
Фосфатидилинозитолы
– в ходе 2-х реакций
фосфорилирования
превращается в
фосфатидилинозитол
-4,5-дифосфат.
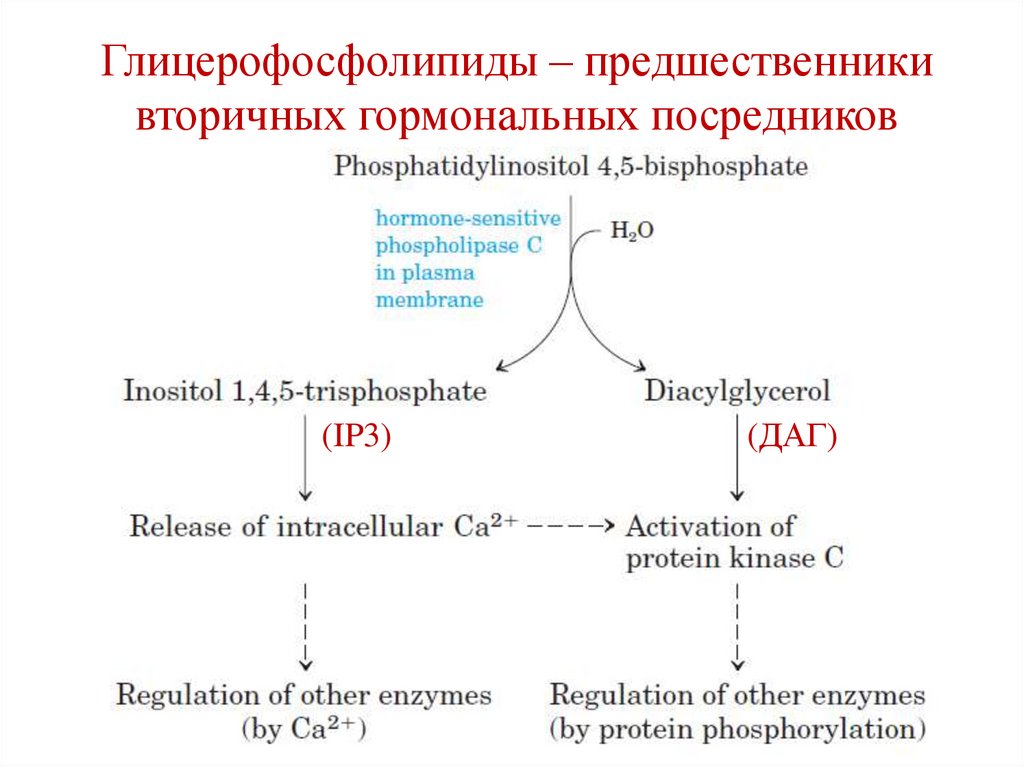
Фосфатидилинозитол
-4,5-дифосфат является
предшественником
вторичных посредников –
ДАГ и IP3.
18.
Глицерофосфолипиды – предшественникивторичных гормональных посредников
(IP3)
(ДАГ)
19.
ГлицерофосфолипидыПлазмалогены – состав:
• Глицерол
• 1 положение – длиноцепочечный спирт
• (простая эфирная связь)
• 2 положение – ЖК
CH2 O CH CH R1
O
• Фосфорная кислота
CH O C R2
• Аминоспирт
Плазмалогены – составляют до
10% фосфолипидов нервной и
мышечной ткани.
CH2 O
O
P
O-
O R3
20.
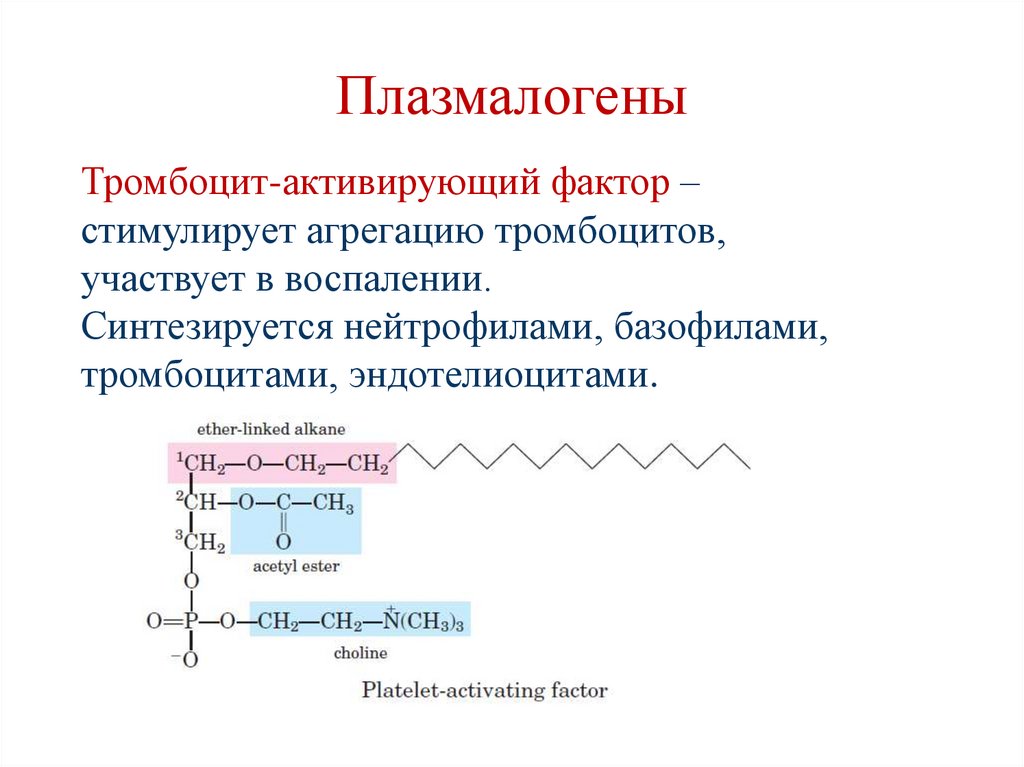
ПлазмалогеныТромбоцит-активирующий фактор –
стимулирует агрегацию тромбоцитов,
участвует в воспалении.
Синтезируется нейтрофилами, базофилами,
тромбоцитами, эндотелиоцитами.
21.
Глицерофосфолипиды• Кардиолипины (дифосфатидилглицеролы)
CH2 O
CH O
CH2 O
CH OH
CH2 O
O
C
O
C
R1
R2
O
P O CH2
OO
P O CH2
O-
CH O
CH2 O
O
C
O
C
R2
R3
Кардиолипины
содержатся во внутренней
мембране митохондрий.
Являются единственными
фосфоглицеридами,
обладающие
антигенными свойствами.
22.
Функции глицерофосфолипидов• Структурные компоненты клеточных мембран.
• Предшественники вторичных гормональных
посредников (Пример – фосфатидилинозитол-4,5дифосфат является предшественником
диацилглицерола и инозитол-1,4,5-трифосфата).
• Предшественники арахидоновой кислоты для
синтеза эйкозаноидов.
• Выстилают поверхность альвеол легких,
предотвращая их слипание во время выдоха
(Пример – дипальмитиллецитин входит в состав
сурфактанта легких).
23.
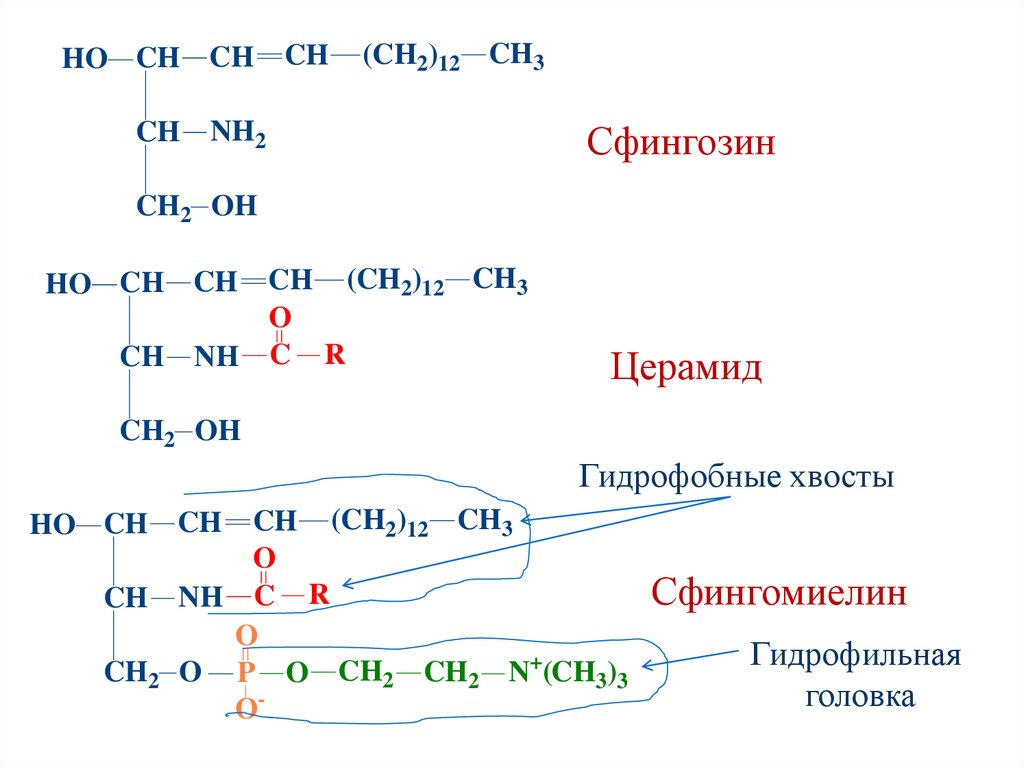
СфингофосфолипидыСфингомиелины – состав:
Сфингозин
Жирная кислота
Фосфорная кислота
Аминоспирт
Функция – структурная (входят в состав
клеточных мембран, особенно нервных
клеток).
Являются амфифильными веществами.
24.
HO CH CHCH
CH
(CH2)12 CH3
NH2
Сфингозин
CH2 OH
CH (CH2)12 CH3
O
NH C R
HO CH CH
CH
Церамид
CH2 OH
Гидрофобные хвосты
CH (CH2)12 CH3
O
CH NH C R
O
CH2 O P O CH2 CH2 N+(CH3)3
O-
HO CH CH
Сфингомиелин
Гидрофильная
головка
25.
ГликолипидыГликосфинголипиды – состав:
Сфингозин
Жирная кислота
Углеводы
Классификация
Цереброзиды
Сульфатиды
Глобозиды
Ганглиозиды
26.
Цереброзидысостоят из церамида и моносахарида (глюкозы или
галактозы).
Жирная кислота в церамиде обычна представлена С24.
CH (CH2)12 CH3
O
C R
HO CH CH
CH
NH
CH2 O
O
CH2OH
OH
OH 4
CH (CH2)12 CH3
O
C R
HO CH CH
CH
NH
CH2 O
CH2OH
O
OH
4
OH
OH
Галактоцереброзиды
содержится в основном
в нервных тканях
OH
Глюкоцереброзиды
содержится в основном
в тканях, отличных от
нервных
27.
СульфатидыЯвляются производными цереброзидов, у
которых в 3-м положении углевода
содержится сульфат.
HO CH
CH
CH
NH
CH (CH2)12
O
C R
CH2 O
O
OH
CH2OH
OH
O SO3-
CH3
Сульфогалактоцереброзид
в больших количествах
содержится в миелине.
28.
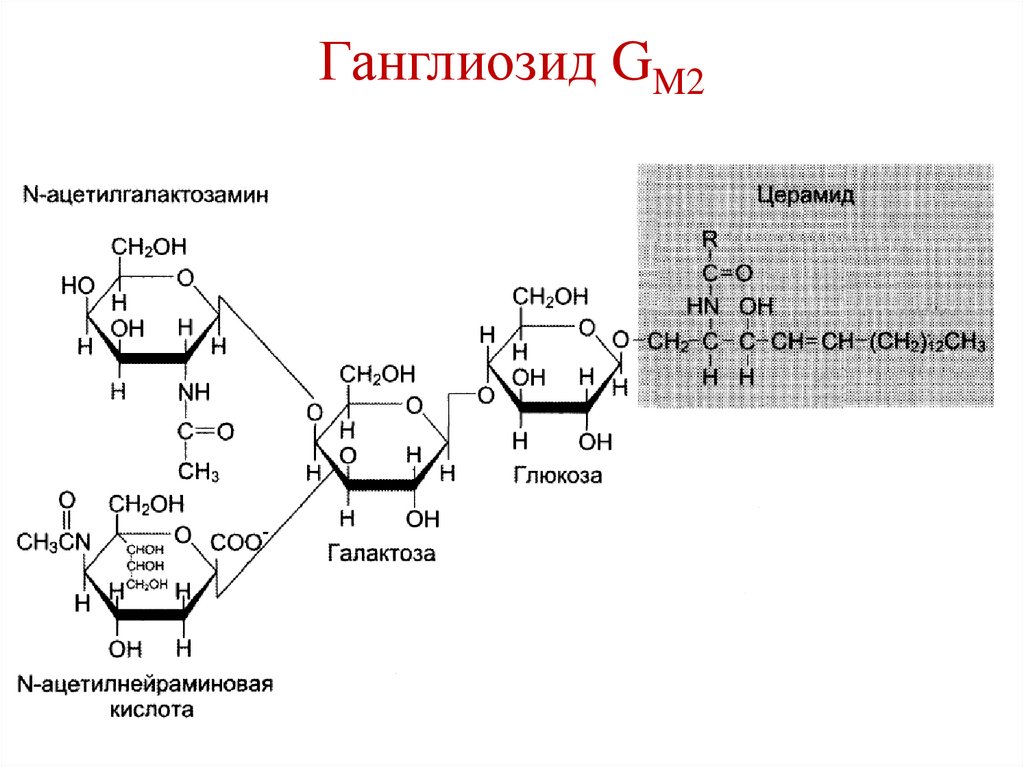
ГанглиозидыСостоят из церамида,
гетероолигосахарида и 1, 2, 3 сиаловых
кислот.
• Классы ганглиозидов:(G – ганглиозид):
• GM – моносиаловый ганглиозид;
• GD – дисиаловый ганглиозид;
• GT – трисиаловый ганглиозид;
• GQ – тетрасиаловый ганглиозид.
Содержатся в основном в нервной ткани.
Выполняют рецепторную функцию.
29.
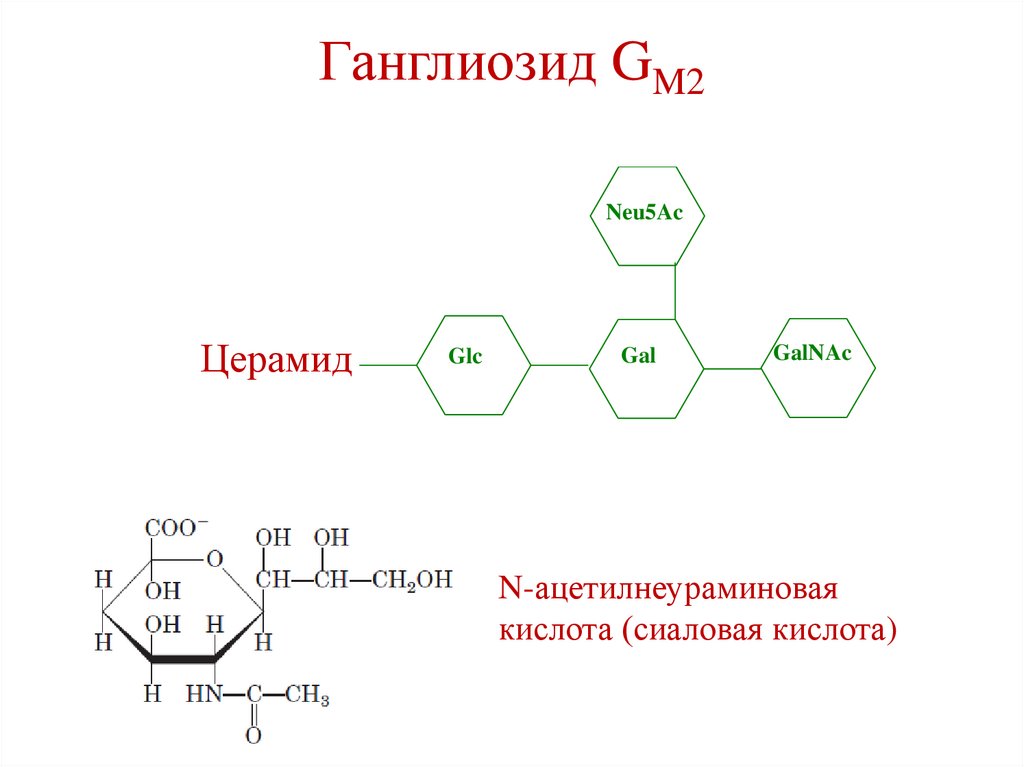
Ганглиозид GM2Neu5Ac
Церамид
Glc
Gal
GalNAc
N-ацетилнеураминовая
кислота (сиаловая кислота)
30.
Ганглиозид GM231.
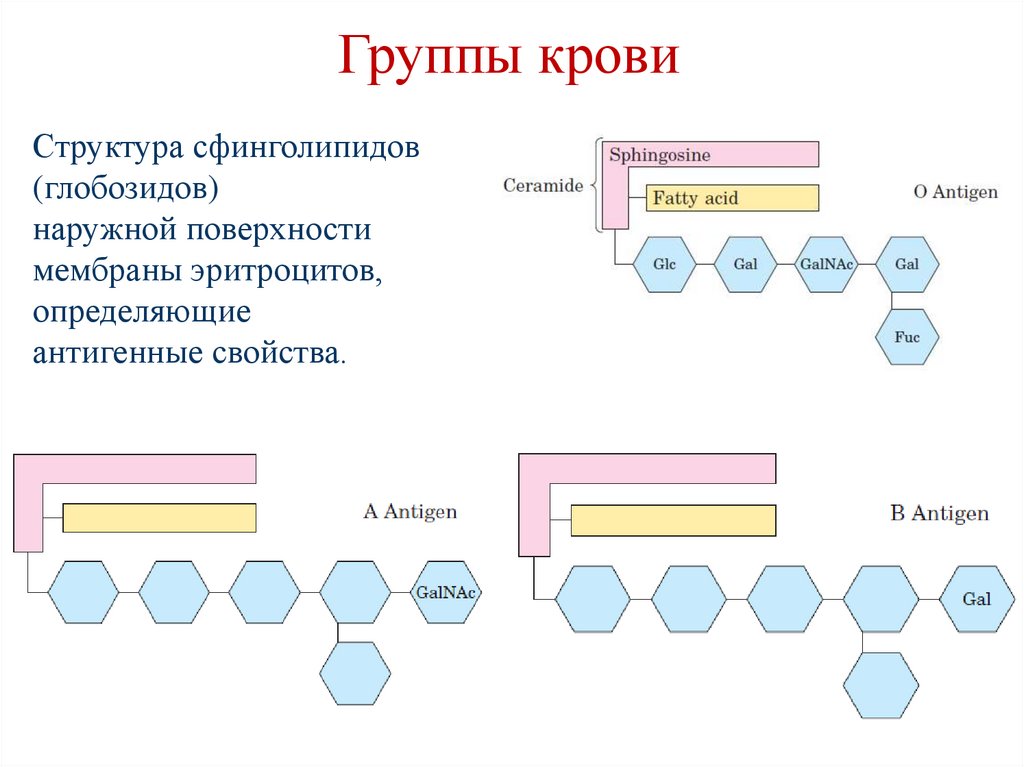
Группы кровиСтруктура сфинголипидов
(глобозидов)
наружной поверхности
мембраны эритроцитов,
определяющие
антигенные свойства.
32.
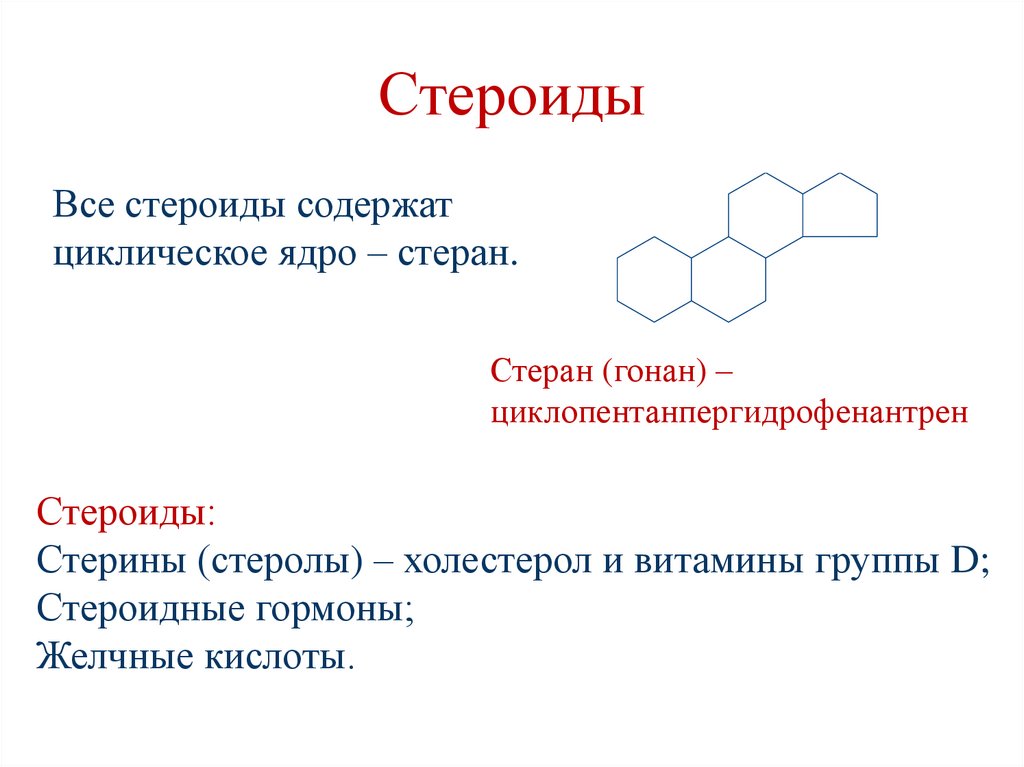
СтероидыВсе стероиды содержат
циклическое ядро – стеран.
Стеран (гонан) –
циклопентанпергидрофенантрен
Стероиды:
Стерины (стеролы) – холестерол и витамины группы D;
Стероидные гормоны;
Желчные кислоты.
33.
Стерины (стеролы)Холестан
(10,13-диметил-17 сек. изо-октилстеран)
Стерины – производные холестана, содержащие –ОН в 3-м
положении – холестерол, провитамины D.
Зоостерины, фитостерины, микостерины.
34.
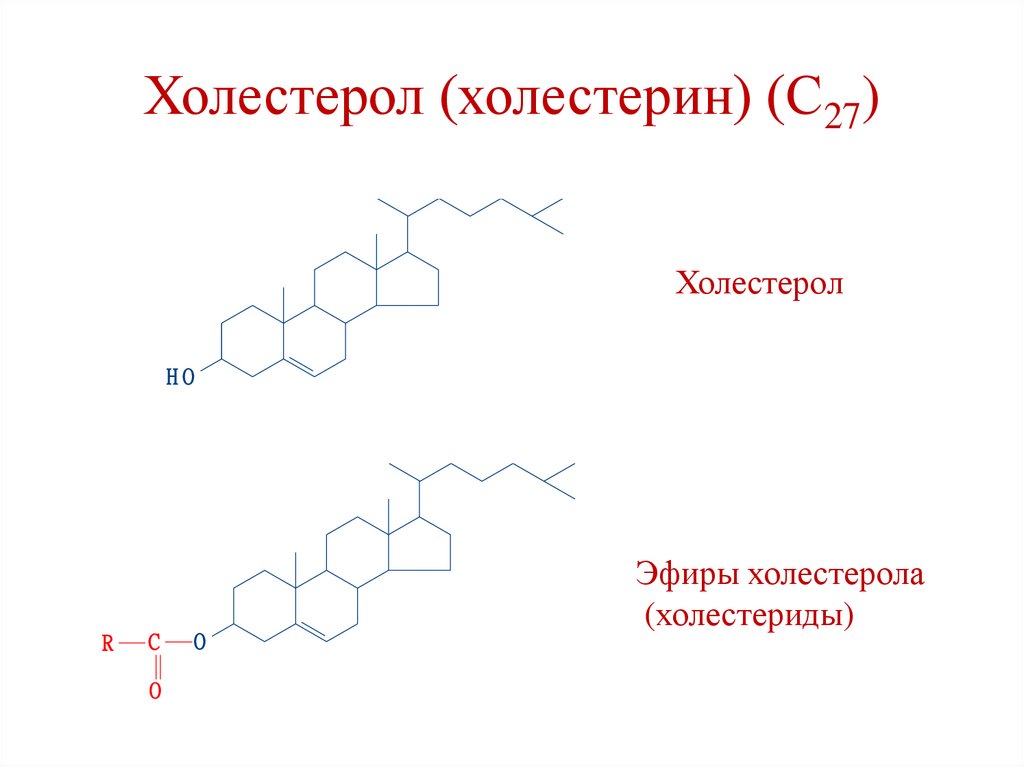
Холестерол (холестерин) (С27)Холестерол
HO
R
C
O
O
Эфиры холестерола
(холестериды)
35.
Метаболическая роль холестеролаВходят в состав клеточных мембран;
Является предшественником стероидных
гормонов (эндокринные стероидогенные
железы);
Является предшественником витаминов D
(кожа);
Является предшественником желчных
кислот (печень).
36.
Переваривание и всасываниелипидов
37.
Основными пищевыми липидамиявляются
• Триацилглицеролы
• Холестерол и холестериды
• Фосфолипиды
Суточная норма липидов – 80 г
Значение пищевых липидов:
• Источники энергии (9,3 kcal/g)
• Источники незаменимых жирных кислот
• С липидами поступают жирорастворимые
витамины A, D, E, K
38.
Переваривание липидов в ЖКТ• У детей начинается в ротовой полости под
действием лингвальной липазы; продолжается в
желудке под действием желудочной липазы.
• Лингвальная и желудочная липазы гидролизуют
в основном коротко- и среднецепочечные ЖК.
• Имеет значение для новорожденных (гидролиз
ТАГ молока в которых содержится много
коротко- и среднецепочечных ЖК) и лиц с
недостаточностью поджелудочной железы.
39.
Переваривание липидов в кишечнике(необходимые условия)
• Щелочная среда – рН = 8
(бикарбонаты панкреатического сока)
• Липолитические ферменты
• Колипаза
• Желчные кислоты
40.
Желчные кислоты• Синтезируются в печени из холестерола.
• Являются производными холановой
кислоты.
• В печени синтезируются 2 желчные
кислоты – холевая и хенодезоксихолевая
кислоты (первичные желчные кислоты).
• В толстом кишечнике под действием
кишечной микрофлоры превращаются в
дезоксихолевую и литохолевую кислоты
(вторичные желчные кислоты).
41.
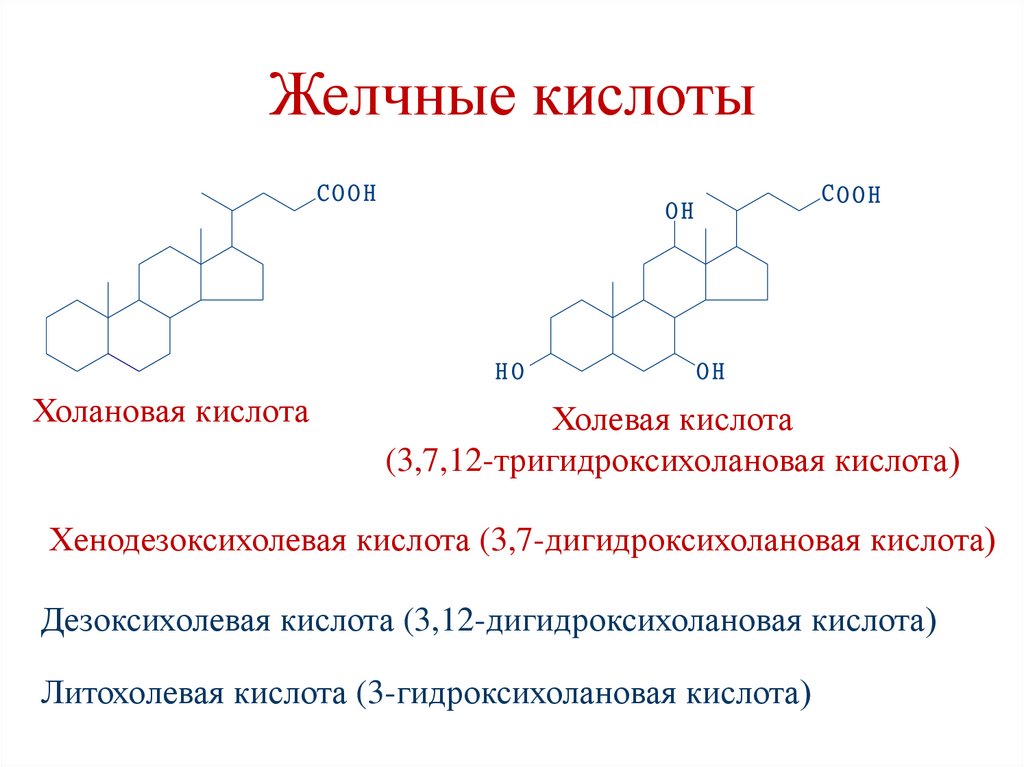
Желчные кислотыCOOH
HO
Холановая кислота
COOH
OH
OH
Холевая кислота
(3,7,12-тригидроксихолановая кислота)
Хенодезоксихолевая кислота (3,7-дигидроксихолановая кислота)
Дезоксихолевая кислота (3,12-дигидроксихолановая кислота)
Литохолевая кислота (3-гидроксихолановая кислота)
42.
Желчные кислоты• Карбоксильные группы желчных кислот
имеют рК~6, поэтому при физиологических
значениях рН в кишечнике они не полностью
диссоциированны и не являются
эффективными эмульгаторами.
• В печени происходит конъюгация желчных
кислот с глицином и таурином, которые
полностью ионизированны при рН кишечного
сока (поэтому называются солями желчных
кислот). Именно они служат главными
эмульгаторами липидов в кишечнике.
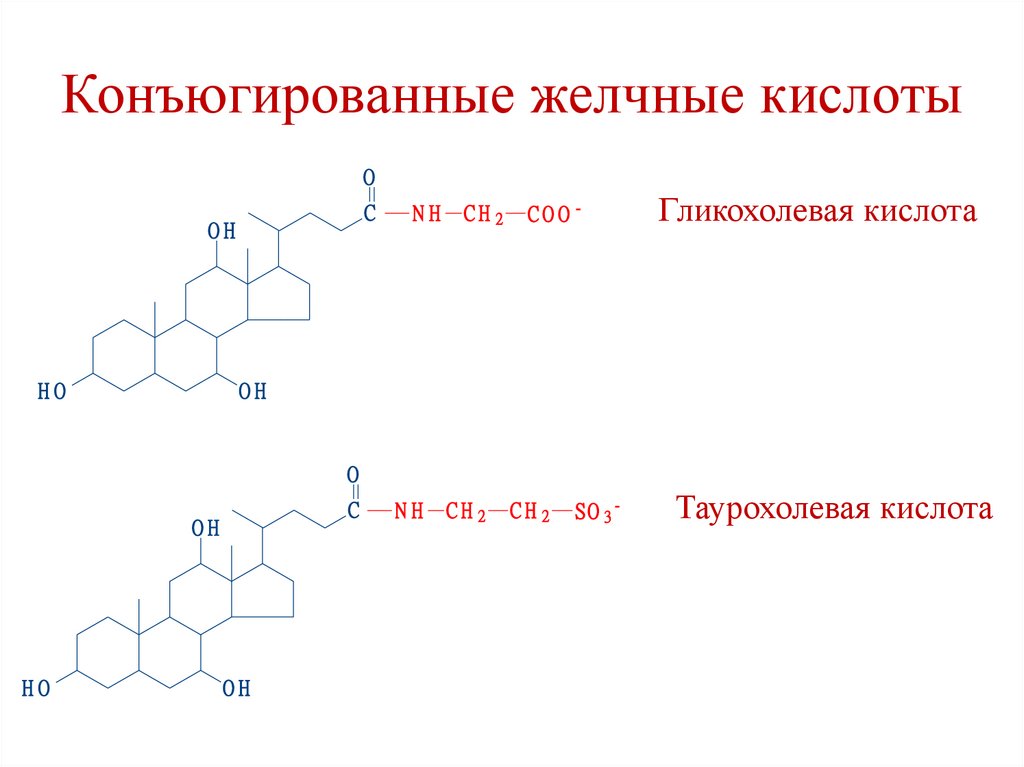
43.
Конъюгированные желчные кислотыO
C
OH
HO
NH
CH2
COO-
Гликохолевая кислота
OH
O
C
OH
HO
OH
NH
CH2
CH2
S O 3-
Таурохолевая кислота
44.
Функции желчных кислот• Обладают поверхностно-активными
свойствами – эмульгируют пищевые жиры,
делая их доступными для действия липазы.
• Активируют поджелудочную липазу
(фермент, который гидролизует пищевые
триглицериды).
• Участвует во всасывании продуктов
гидролиза липидов и жирорастворимых
витаминов.
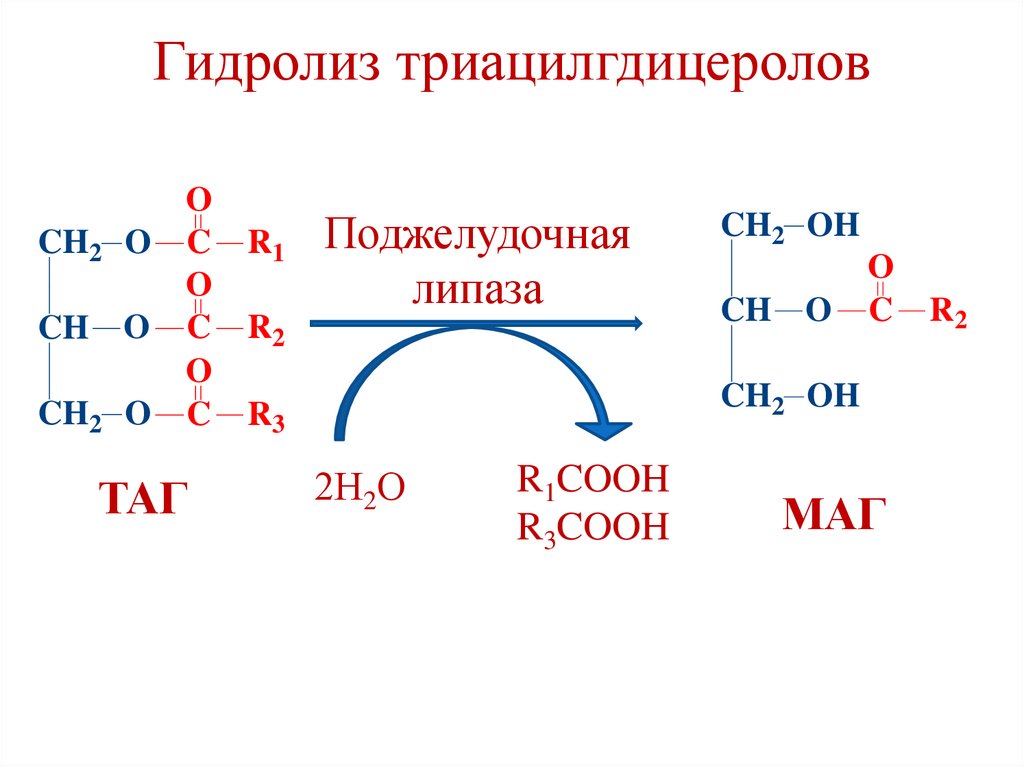
45.
Гидролиз триацилгдицероловCH2 O
CH O
CH2 O
O
C
O
C
O
C
ТАГ
R1
Поджелудочная
липаза
R2
CH2 OH
CH O
O
C
CH2 OH
R3
2Н2О
R1COOH
R3COOH
МАГ
R2
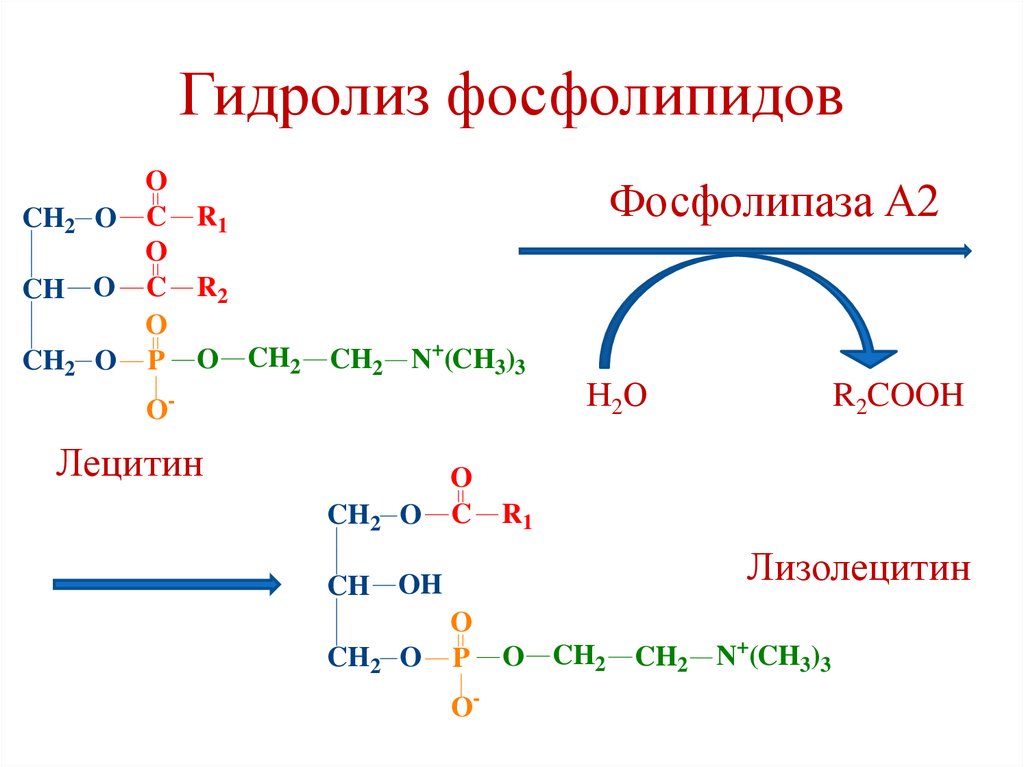
46.
Гидролиз фосфолипидовCH2 O
CH O
CH2 O
O
C
O
C
O
P
Фосфолипаза А2
R1
R2
O CH2
CH2 N+(CH3)3
O-
Лецитин
CH2 O
O
C
Н2О
R1
Лизолецитин
CH OH
CH2 O
R2COOH
O
P
O-
O CH2
CH2 N+(CH3)3
47.
Гидролиз фосфолипидов• Фосфолипаза А2 активируется трипсином,
Са2+, желчными кислотами
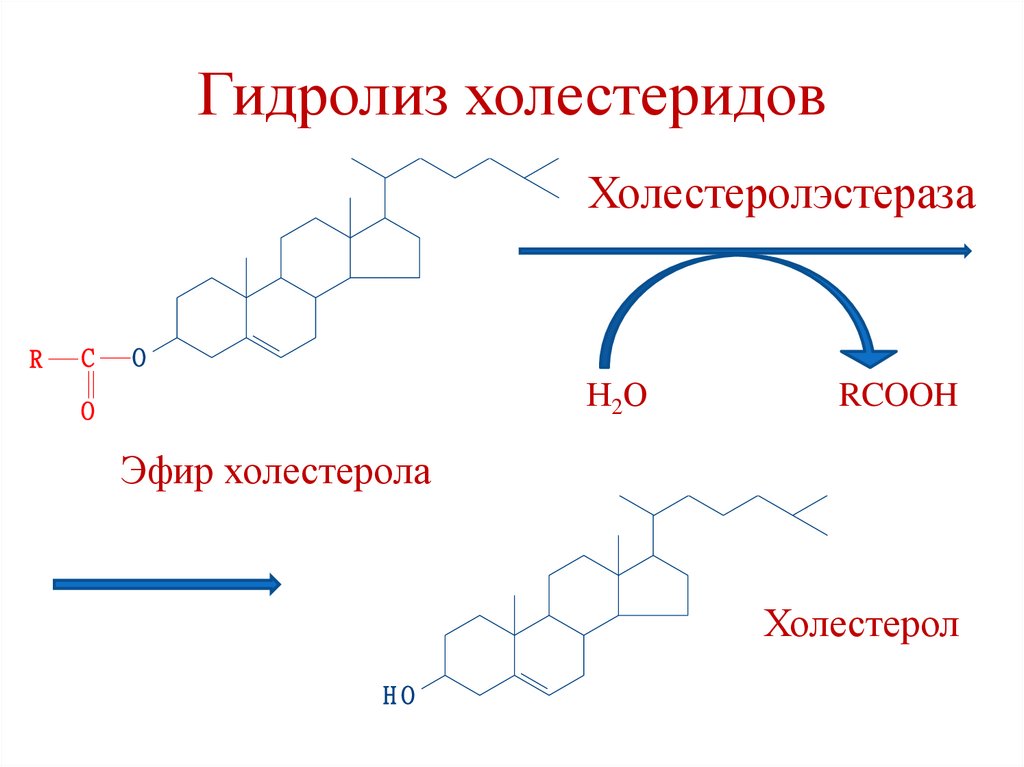
48.
Гидролиз холестеридовХолестеролэстераза
R
C
O
Н2О
O
RCOOH
Эфир холестерола
Холестерол
HO
49.
Всасывание продуктовгидролиза липидов
• Глицерол, коротко- и среднецепочечные ЖК
– свободная диффузия.
• МАГ, длинноцепочечные ЖК, холестерол
образуют с желчными кислотами мицеллы,
которые поступают в энтероциты –
мицеллярная диффузия.
50.
51.
• В энтероцитах мицеллы распадаются.• Продукты гидролиза липидов подвергаются
ресинтезу.
• Желчные кислоты всасываются в кровь,
поступают в печень, повторно выделяются в
ЖКТ (кишечно-печеночная циркуляция
желчных кислот).
52.
Регуляция переваривания липидовСекретин
• стимулирует выделение печенью и
поджелудочной железой водянистого
раствора с высоким содержанием
бикарбонатов.
Холецистокинин
• стимулирует выделение богатого
липолитическими ферментами
поджелудочного сока
• стимулирует выделение желчи.
53.
Нарушения переваривания и всасываниялипидов
Стеаторея – появление в фекалиях
непереваренных липидов.
• Печеночная (желчнокаменная болезнь,
дискинезия желчного пузыря).
• Поджелудочная (панкреатиты).
• Кишечная (энтериты).
Последствия – нарушение всасывания
жирорастворимых витаминов и
незаменимых ЖК
гиповитаминозы
(примеры: нарушение свертывания крови,
«куриная слепота»).
54.
Ресинтез липидов в энтероцитах• Моноацилглицерол + 2 R-CO-S-CoA
триацилглицерол + 2 НS-CoA
• Лизолецитин + R-CO-S-CoA
лецитин + НS-CoA
• Холестерол + R-CO-S-CoA
эфир холестерола + НS-CoA
• Ресинтезированные липиды образуют
хиломикроны, которые доставляют жиры к
тканям.
55.
56.
Метаболизмрезервных липидов
57.
Синтез триацилглицеролов• Локализация процесса – печень, жировая
ткань.
• Синтез происходит из глицерол-3-фосфата
и ацил-СоА (главным образом стеариновой,
пальмитиновой и олеиновой).
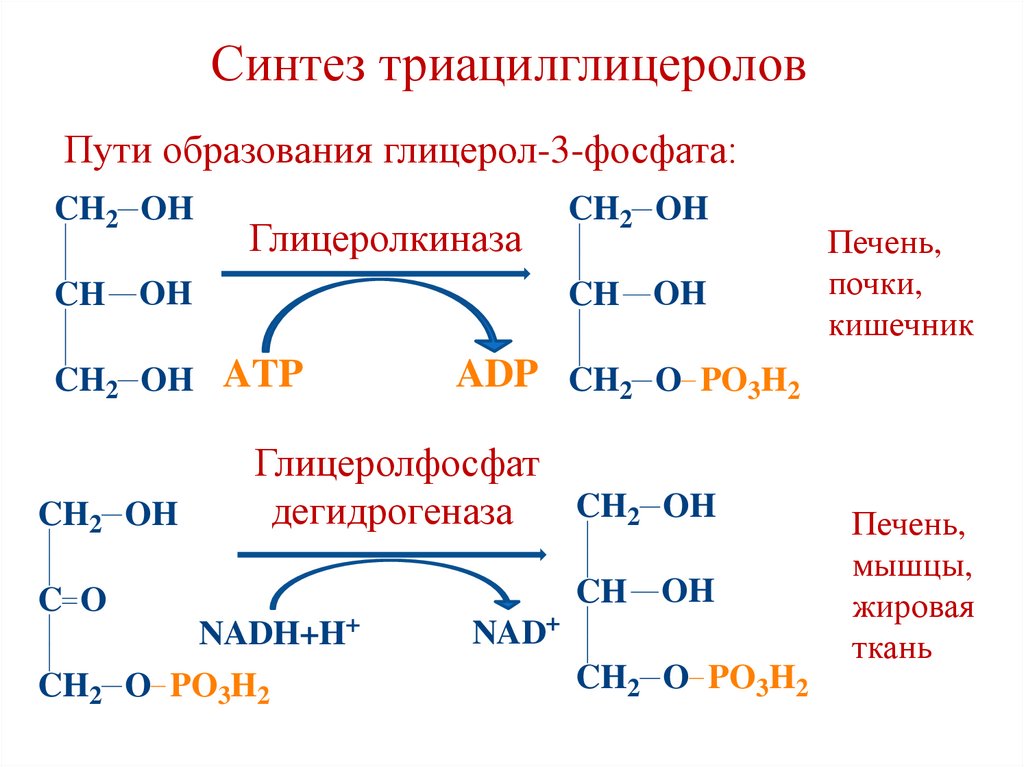
58.
Синтез триацилглицероловПути образования глицерол-3-фосфата:
CH2 OH
Глицеролкиназа
CH2 OH
OH
CH OH
CH2 OH ATP
ADP CH2 O PO3H2
CH
CH2 OH
C O
Глицеролфосфат
CH2 OH
дегидрогеназа
CH OH
NADH+H+
CH2 O PO3H2
NAD+
CH2 O PO3H2
Печень,
почки,
кишечник
Печень,
мышцы,
жировая
ткань
59.
Синтез триацилглицероловO
CH2 O C R
O
CH O C R
CH2 OH
CH OH
2 R CO SCoA
H2O
2 HSCoA
CH2 O PO3H2
CH2 O PO3H2
O
CH2 O C R
O
CH O C R
CH2 OH
H3PO4
R CO SCoA
HSCoA
O
CH2 O C R
O
CH O C R
O
CH2 O C R
60.
Мобилизация жиров из жировойткани (тканевой липолиз)
• Резервные липиды обеспечивают энергией
организм в течение 7-8 недель.
• Липолиз происходит интенсивно при
голодании, стрессе и физической нагрузке.
• Липолиз стимулируется адреналином,
глюкагоном, соматотропином, кортизолом.
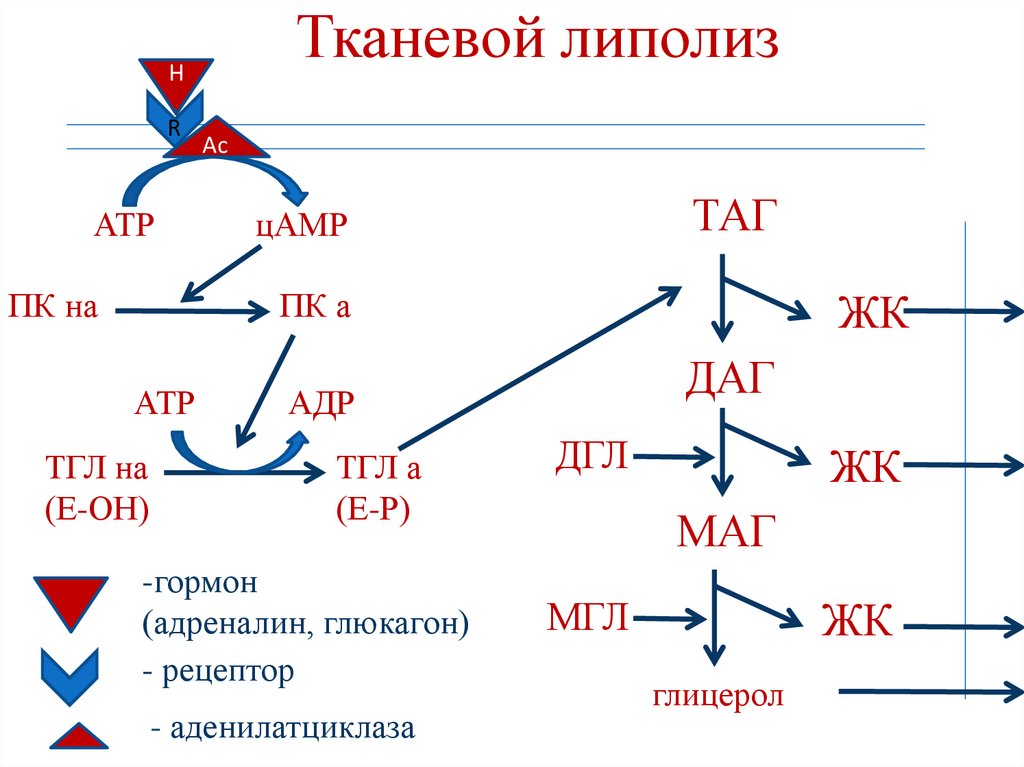
61.
Тканевой липолизH
R
АТР
ПК на
Aс
ТАГ
цАМР
ПК а
АТР
ТГЛ на
(Е-ОН)
ЖК
ДАГ
АДР
ТГЛ а
(Е-Р)
-гормон
(адреналин, глюкагон)
- рецептор
- аденилатциклаза
ДГЛ
ЖК
МАГ
МГЛ
ЖК
глицерол
62.
Использование глицерола ижирных кислот
Использование глицерола:
1. Глюконеогенез;
2. Окисление;
3. Синтез ТАГ в печени.
Использование жирных кислот:
1. Окисление.
63.
Регуляция липолизаАдреналин, глюкагон
• стимулируют липолиз (активируют
триглицеридлипазу – фосфорилирование
фермента);
Глюкокортикоиды (кортизол)
• стимулируют липолиз (индуцирует
триглицеридлипазу);
Инсулин
• ингибирует липолиз (ингибирует
триглицеридлипазу – дефосфорилирование
фермента).
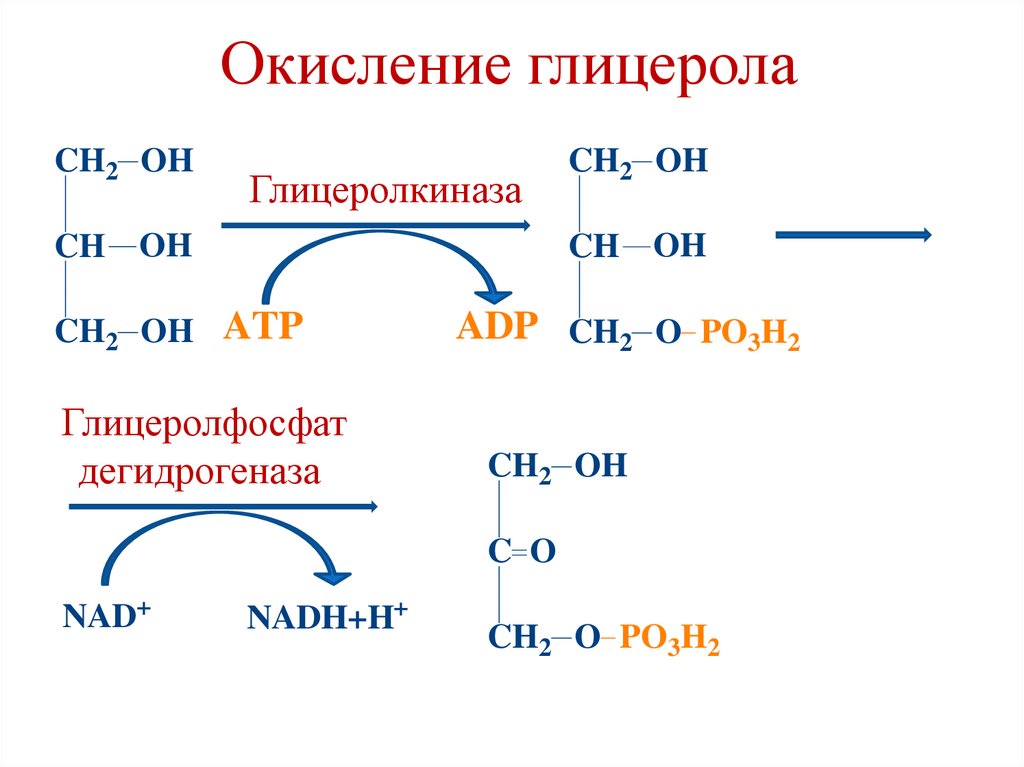
64.
Окисление глицеролаCH2 OH
Глицеролкиназа
CH2 OH
OH
CH OH
CH2 OH ATP
ADP CH2 O PO3H2
CH
Глицеролфосфат
дегидрогеназа
CH2 OH
C O
NAD+
NADH+H+
CH2 O PO3H2
65.
ГлицеролATP
ADP
Глицерол-3фосфат
NAD+
NADH+H+
Глицеральдегид-3-фосфат
Дигидроксиацетонфосфат
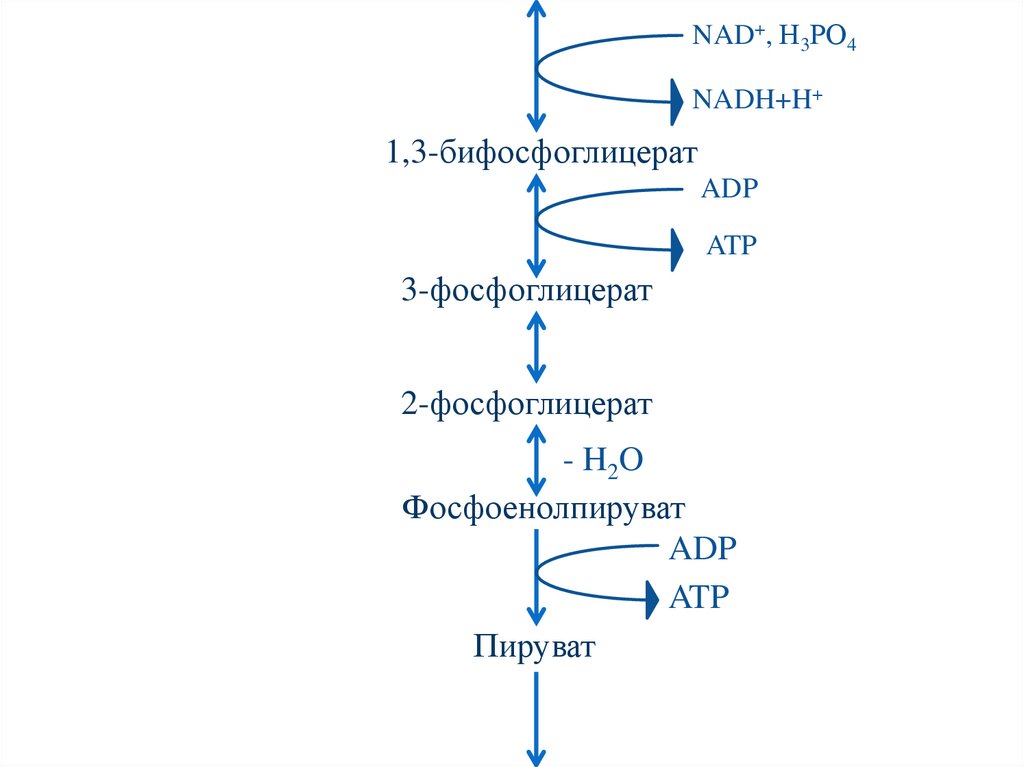
66.
NAD+, Н3РО4NADH+H+
1,3-бифосфоглицерат
ADP
ATP
3-фосфоглицерат
2-фосфоглицерат
- H2O
Фосфоенолпируват
ADP
ATP
Пируват
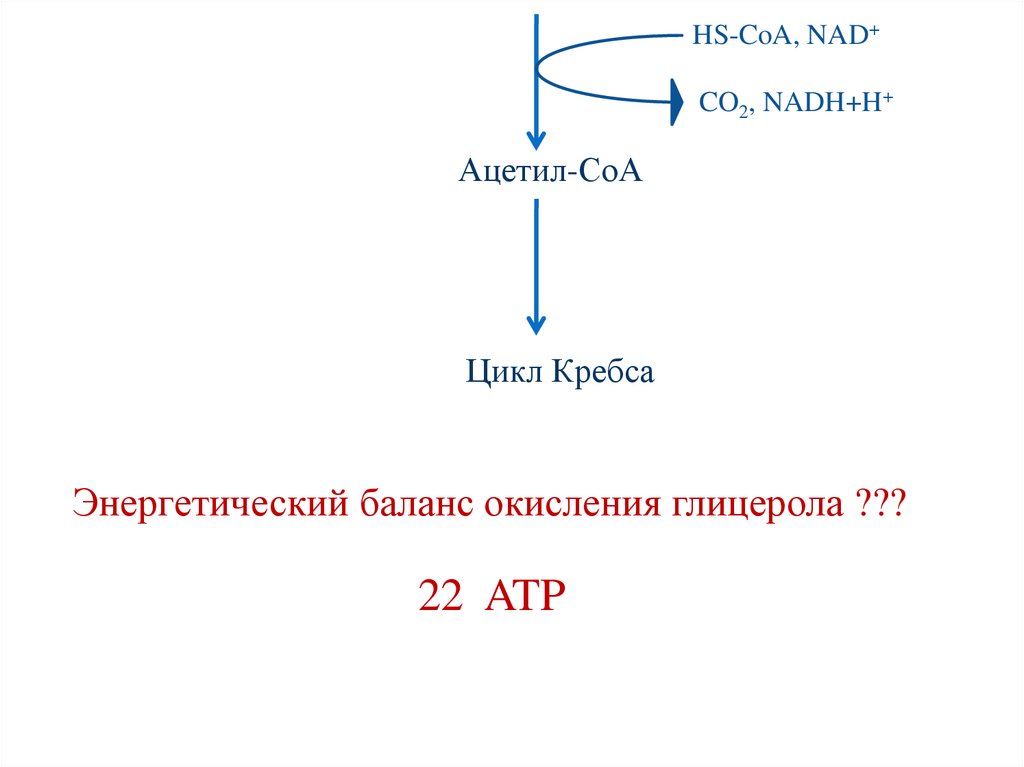
67.
HS-CoA, NAD+CO2, NADH+H+
Ацетил-СоА
Цикл Кребса
Энергетический баланс окисления глицерола ???
22 ATP
68.
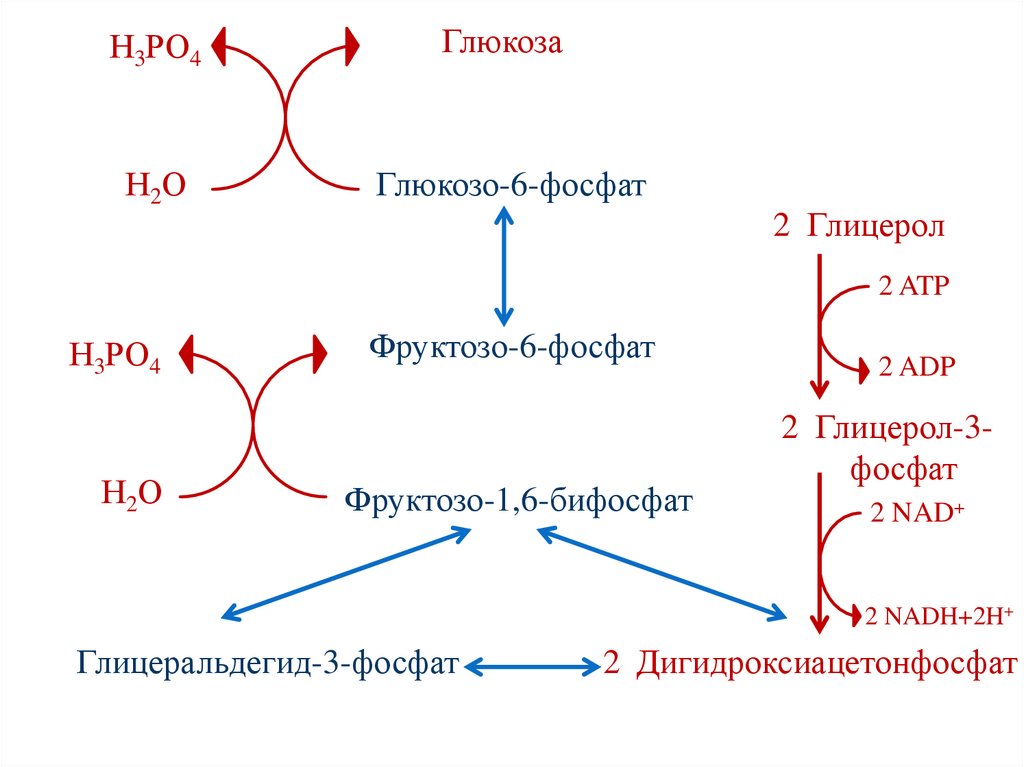
Глюконеогенез из глицерола• Происходит в печени
69.
Н3РО4Глюкоза
Н2О
Глюкозо-6-фосфат
2 Глицерол
2 ATP
Н3РО4
Н2О
Фруктозо-6-фосфат
Фруктозо-1,6-бифосфат
2 ADP
2 Глицерол-3фосфат
2 NAD+
2 NADH+2H+
Глицеральдегид-3-фосфат
2 Дигидроксиацетонфосфат
70.
Метаболизм жирных кислоти кетоновых тел
71.
Бета-окисление жирных кислот• Локализация – скелетные мышцы, миокард,
печень, почки.
• Не происходит в нервной ткани,
эритроцитах.
Этапы:
1. Активация ЖК (цитозоль);
2. Перенос ацил-СоА в митохондрии;
3. Собственно-окисление ЖК (митохондрии).
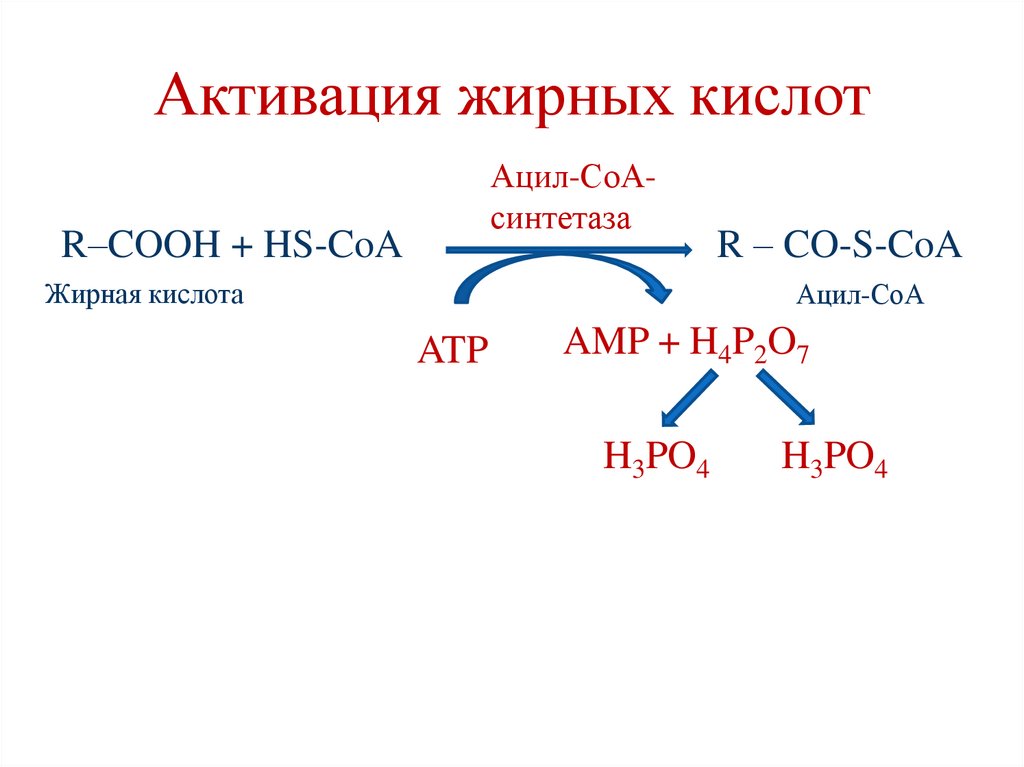
72.
Активация жирных кислотАцил-СоАсинтетаза
R–COOH + HS-CoA
Жирная кислота
R – CO-S-CoA
Ацил-СоА
ATP
AMP + H4P2O7
H3PO4
H3PO4
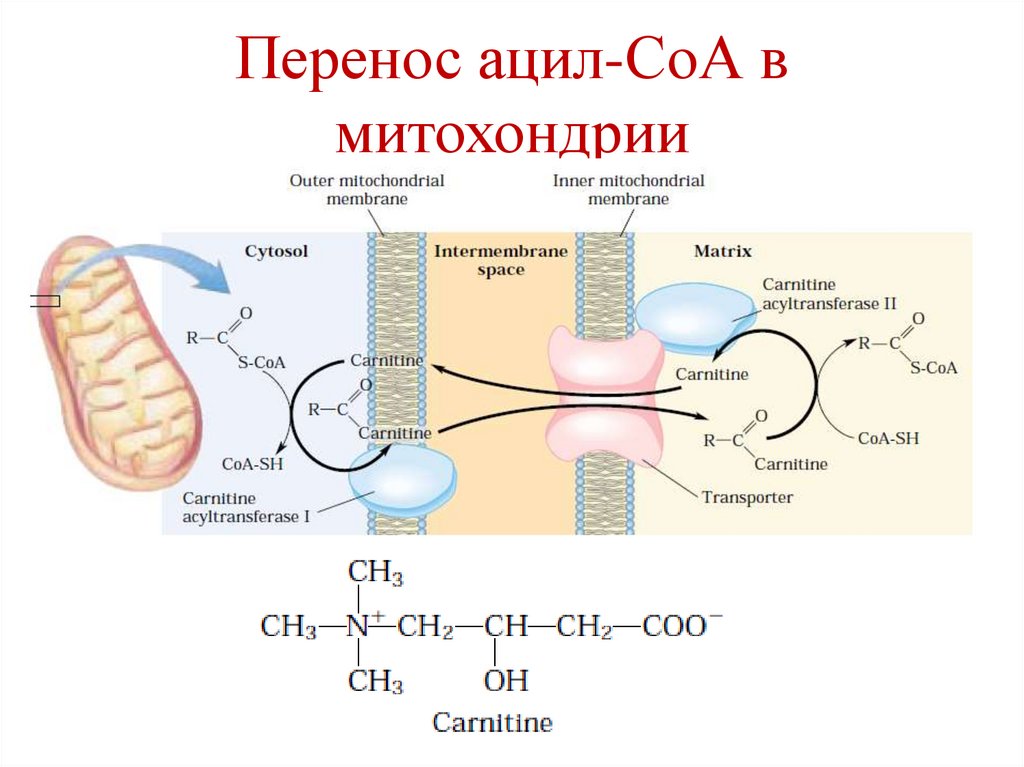
73.
Перенос ацил-СоА вмитохондрии
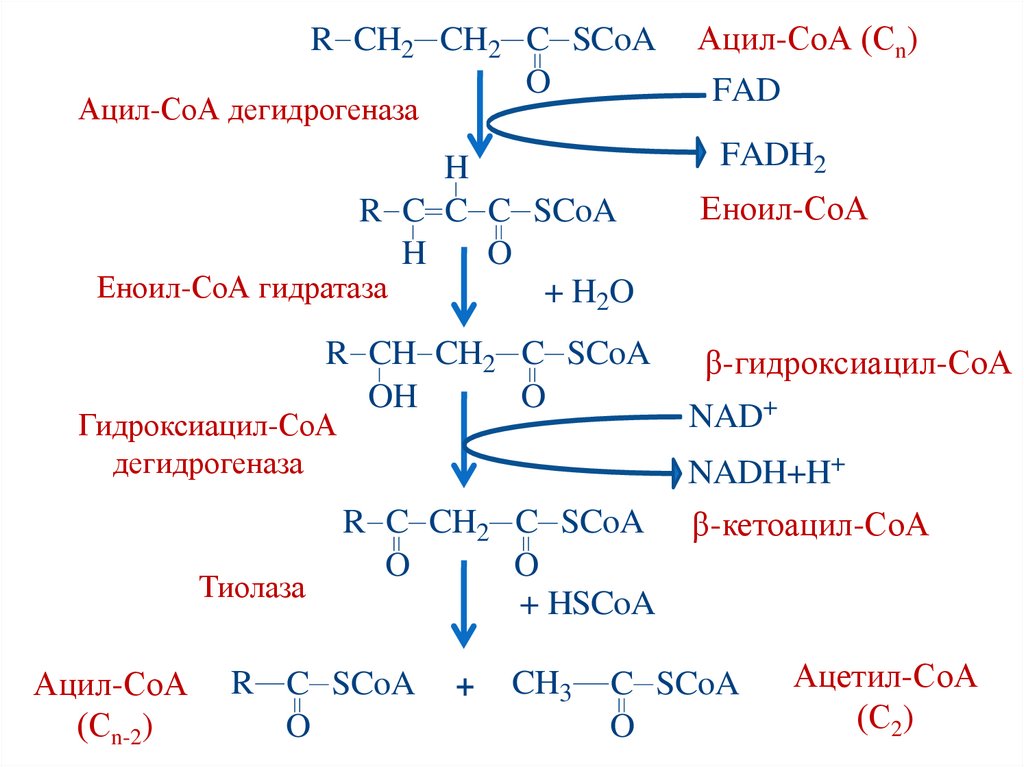
74.
R CH2 CH2 C SCoAO
Ацил-СоА дегидрогеназа
H
R C C C SCoA
H
O
Еноил-СоА гидратаза
+ H2O
R CH CH2 C SCoA
OH
O
Гидроксиацил-СоА
дегидрогеназа
Тиолаза
Ацил-СоА
(Сn-2)
Ацил-СоА (Сn)
FAD
FADH2
Еноил-СоА
β-гидроксиацил-СоА
NAD+
NADH+H+
R C CH2 C SCoA
O
O
+ HSCoA
R C SCoA
O
+
CH3
β-кетоацил-СоА
C SCoA
O
Ацетил-СоА
(С2)
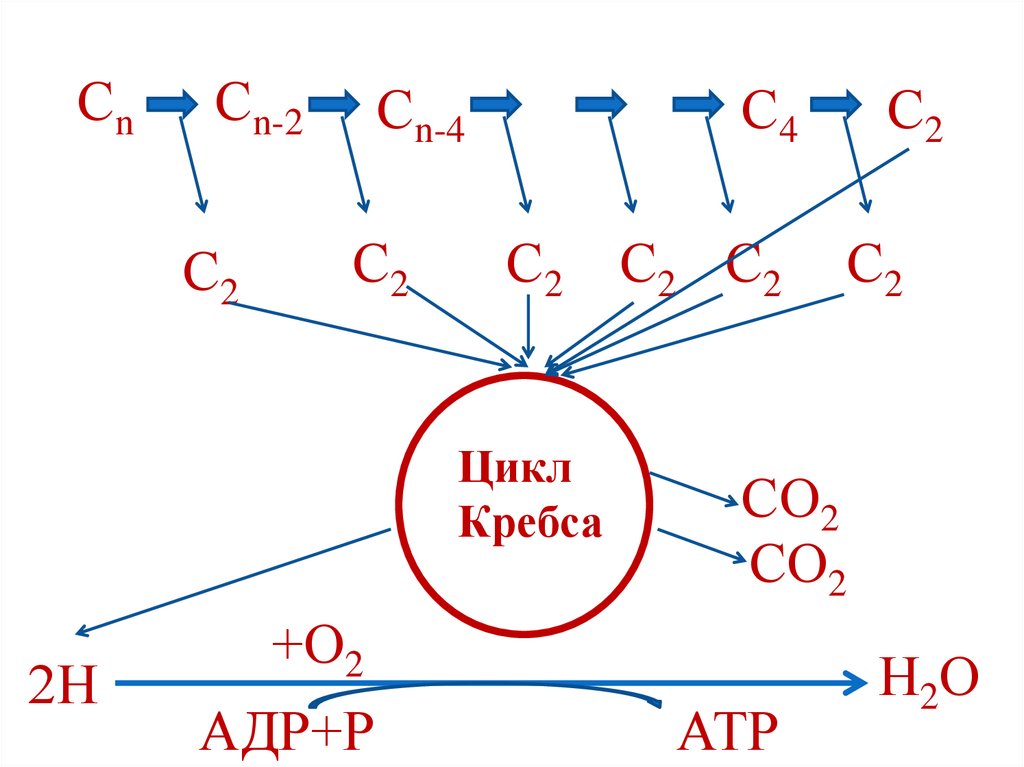
75.
СnСn-2
Сn-4
С2
С2
С4
С2 С2 С2
Цикл
Кребса
2Н
С2
СО2
СО2
+О2
АДР+Р
С2
АТР
Н2О
76.
Энергетический баланс бета-окисления• N – количество атомов углерода ЖК
• N/2-1 – количество циклов бета-окисления
• N/2 – количество ацетил-СоА
(N/2-1) х 5АТР + N/2 х12 АТР – 1АТР (– 2)
77.
Особенности окисленияненасыщенных жирных кислот
• При окислении ненасыщенных ЖК, после 3-х циклов
бета-окисления, образуется Δ3,4-цис-еноил-СоА, а при
окислении насыщенных ЖК, промежуточные продукты
имеют Δ2,3-транс-конфигурацию.
Δ3,4-цис –> Δ2,3-транс-еноил-КоА-изомераза
осуществляет перемещение двойной связи из
положения 3–4 в положение 2–3, а также изменяет цисконфигурацию двойной связи в транс-конфигурацию.
При окислении полиеновых ЖК требуется
дополнительный фермент –
2,4-диеноил-СоА редуктаза.
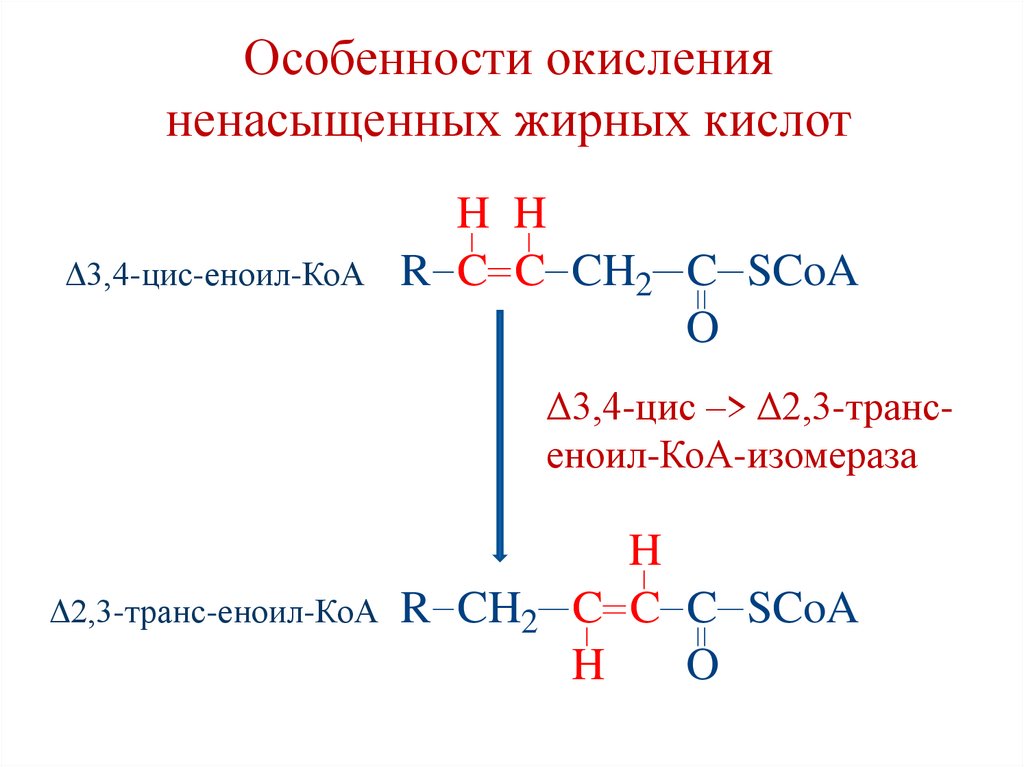
78.
Особенности окисленияненасыщенных жирных кислот
Δ3,4-цис-еноил-КоА
H H
R C C CH2 C SCoA
O
Δ3,4-цис –> Δ2,3-трансеноил-КоА-изомераза
Δ2,3-транс-еноил-КоА R
CH2
H
C C C SCoA
H
O
79.
Особенностиокисления
моноеновых
жирных кислот
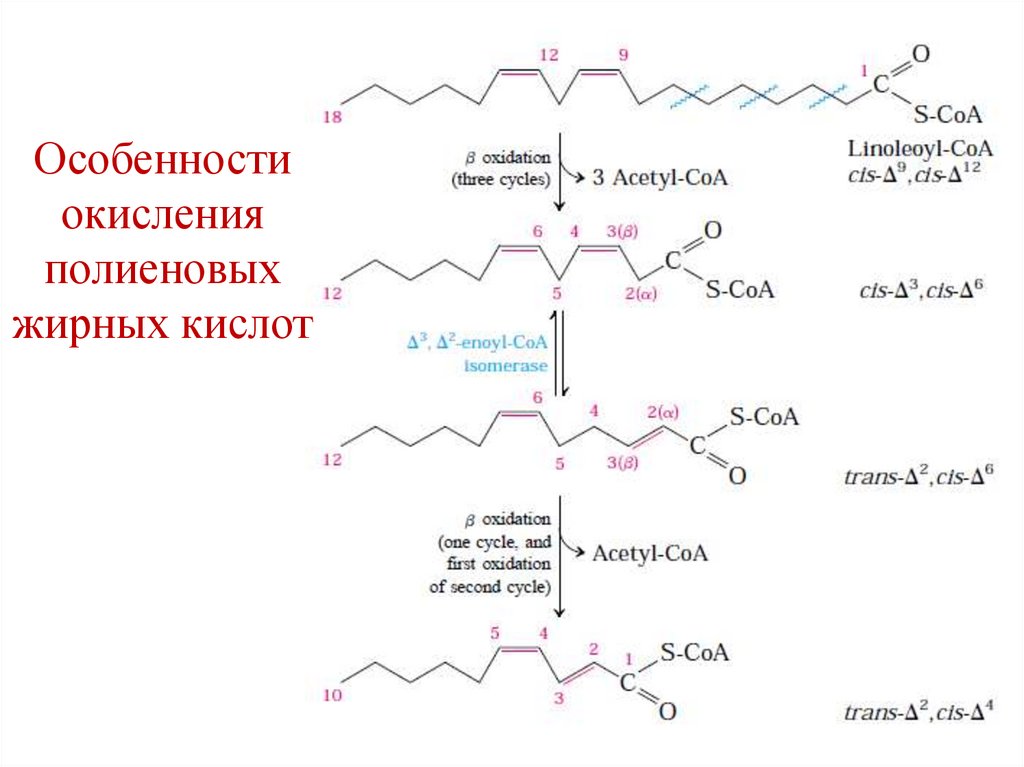
80.
Особенностиокисления
полиеновых
жирных кислот
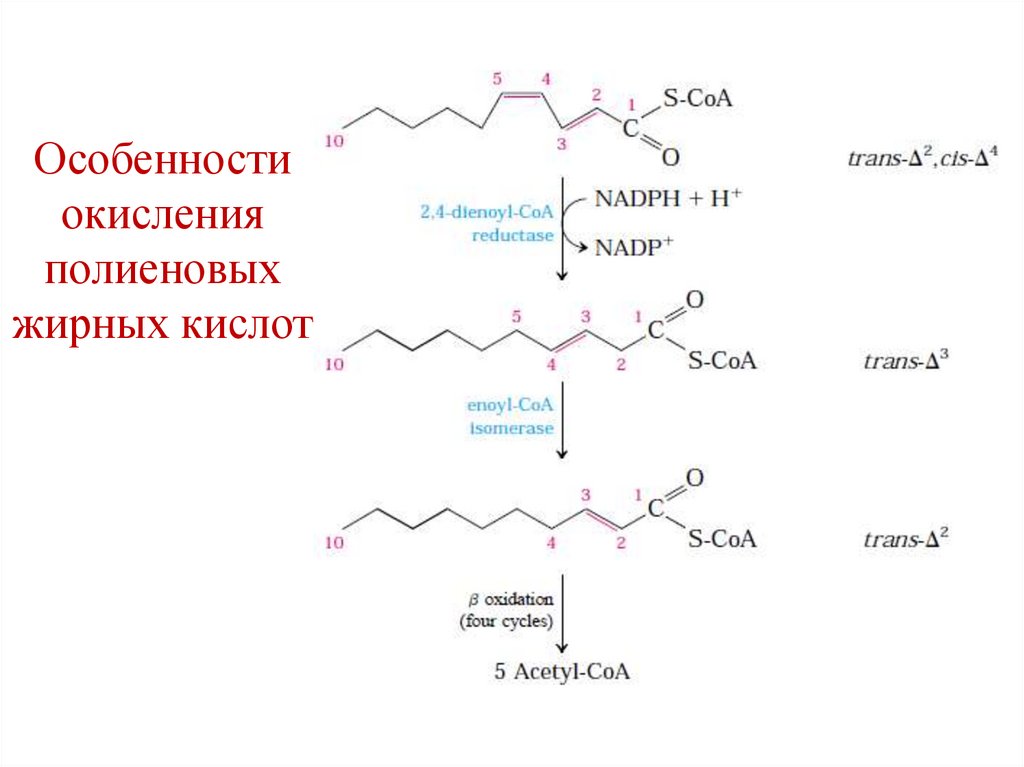
81.
Особенностиокисления
полиеновых
жирных кислот
82.
Особенности окисления жирных кислотс нечетным числом атомов углерода
• Происходит аналогично окислению
жирных кислот с четным числом атомов
углерода, но в последнем цикле бетаокисления образуется одна молекула
ацетил-СоА и одна молекула пропионилСоА, который в ходе трех реакций
превращается в сукцинил-СоА.
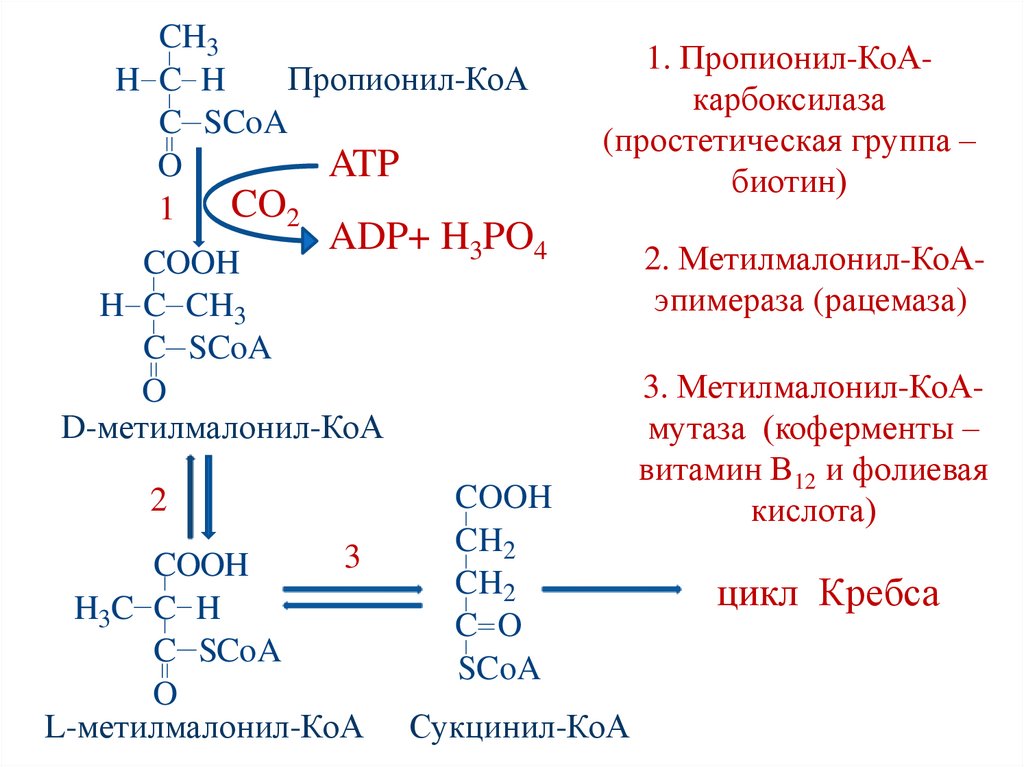
83.
CH3Пропионил-КоА
H C H
C SCoA
O
ATP
CO2
1
1. Пропионил-КоАкарбоксилаза
(простетическая группа –
биотин)
ADP+ H3PO4
COOH
H C CH3
C SCoA
O
D-метилмалонил-КоА
2
3
COOH
H3C C H
C SCoA
O
L-метилмалонил-КоА
COOH
CH2
CH2
C O
SCoA
Сукцинил-КоА
2. Метилмалонил-КоАэпимераза (рацемаза)
3. Метилмалонил-КоАмутаза (коферменты –
витамин В12 и фолиевая
кислота)
цикл Кребса
84.
Особенности окисления жирных кислот впероксисомах
• Характерно для ЖК с 20-26 атомами углерода.
• Особенности – первая реакция:
R-(CH2)n-CH2-CH2-CO-SCoA+O2
R-(CH2)-CH=CH-CO-SCoA + H2O2
2H2O2
2H2O+O2
• Количество пероксисом растет при сахарном
диабете, голодании, при приеме аспирина,
гиполипемических препаратов.
• Отсутствие пероксисом – синдром Zellweger:
накопление ЖК с длинной цепью, смерть в
первые месяцы жизни.
85.
Биосинтез жирных кислот• Локализация процесса – печень, жировая
ткань, лактирующая молочная железа.
• Происходит в цитоплазме.
• Субстрат – ацетил-СоА, образующийся при
окислении глюкозы в абсорбтивном периоде.
Этапы:
1. Транспорт ацетил-СоА из митохондрий в
цитоплазму;
2. Синтез малонил-СоА;
3. Собственно-биосинтез ЖК.
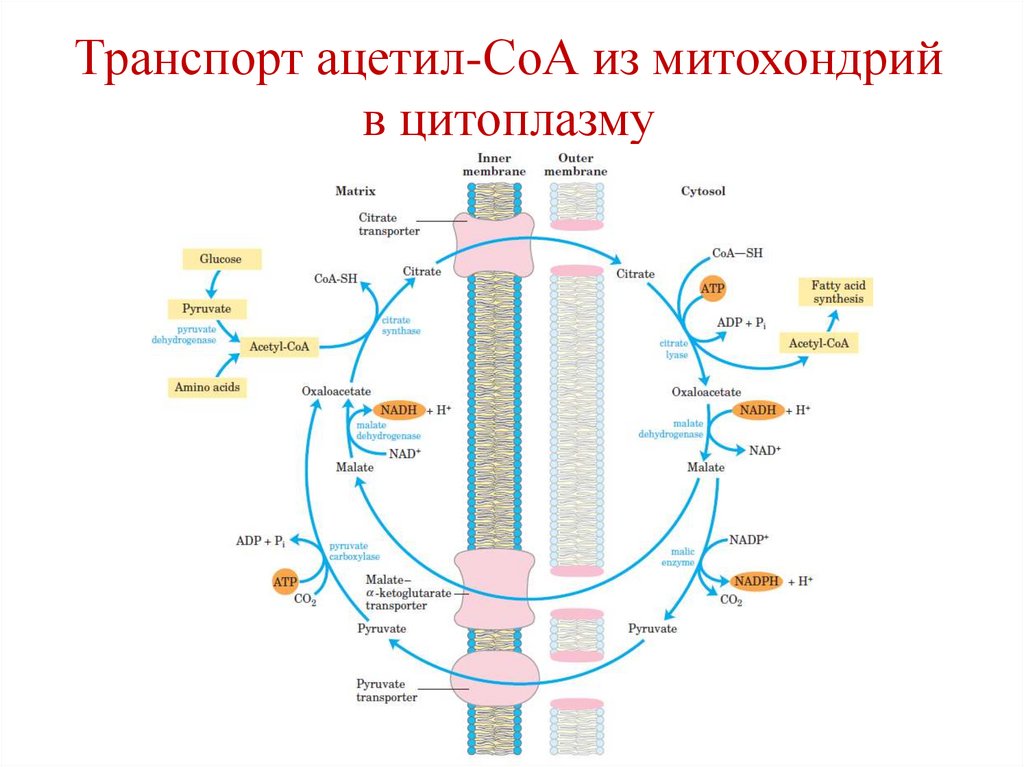
86.
Транспорт ацетил-СоА из митохондрийв цитоплазму
87.
Синтез малонил-СоАCH3-CO-SCoA + CO2
Ацетил-CoAкарбоксилаза
Ацетил-CoA
ATP
HOOC-CH2-CO-SCoA
Малонил-CoA
Простетическая группа фермента –
биотин (витамин Н)
ADP+
H3PO4
88.
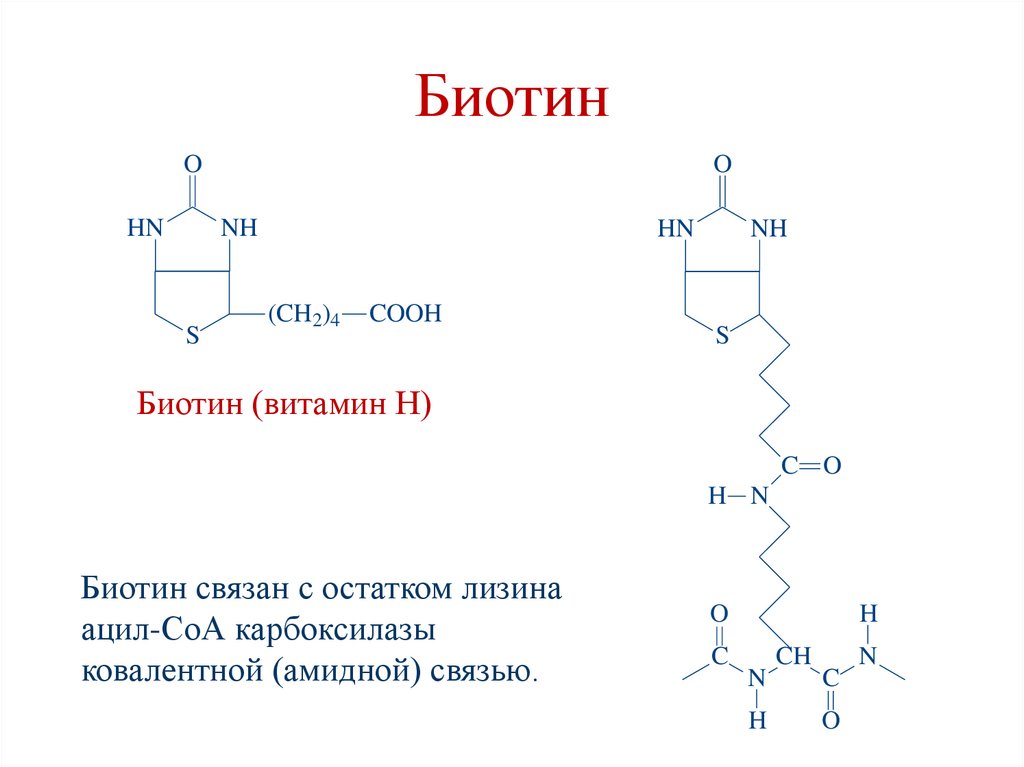
БиотинO
HN
O
NH
S
HN
(CH2)4
COOH
NH
S
Биотин (витамин Н)
C O
H N
Биотин связан с остатком лизина
ацил-СоА карбоксилазы
ковалентной (амидной) связью.
O
C
H
N
H
CH
C
O
N
89.
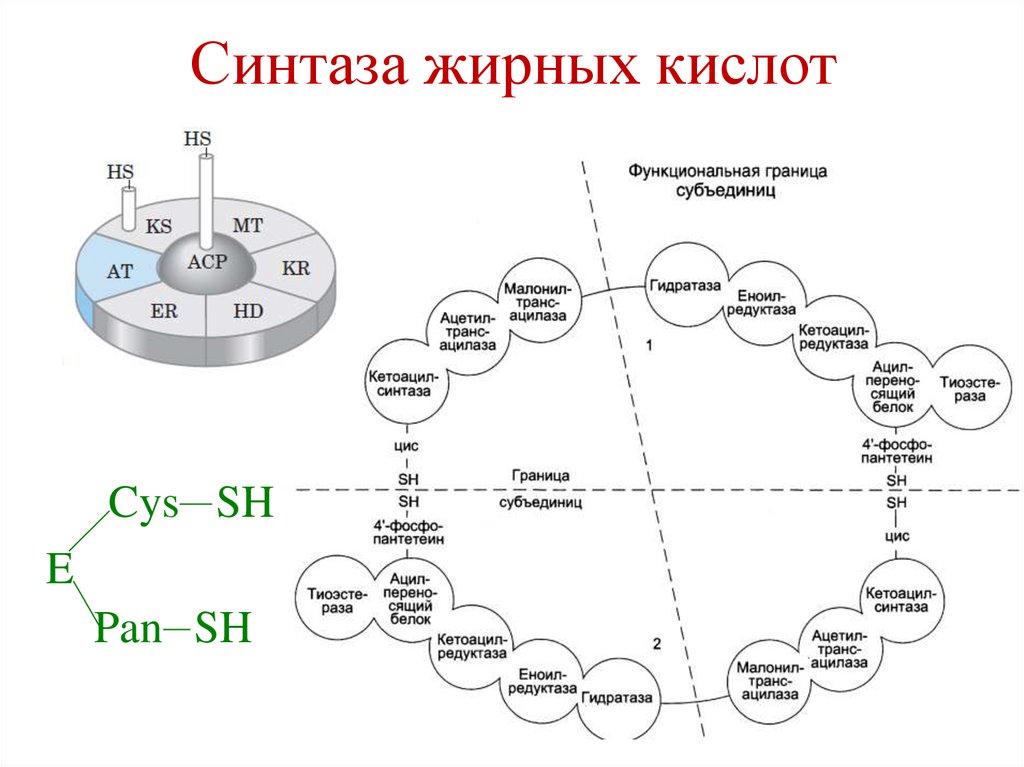
Собственно-биосинтез жирных кислот• Происходит под действием мультиферментного
комплекса, синтаза жирных кислот (пальмитат
синтаза), состоящего из 2-х идентичных
протомеров, каждый из которых имеет 7 доменов,
обладающих разными каталитическими
активностями и связан с ацилпереносящим
белком (АПБ) – аcyl carrier protein (ACP).
• Пальмитат синтаза имеет 2 свободные HS-группы
(одна HS-группа принадлежит цистеину третьего
фермента, а вторая – фосфопантетеиновому
остатку, связанного с АПБ).
90.
Синтаза жирных кислотCys SH
E
Pan SH
91.
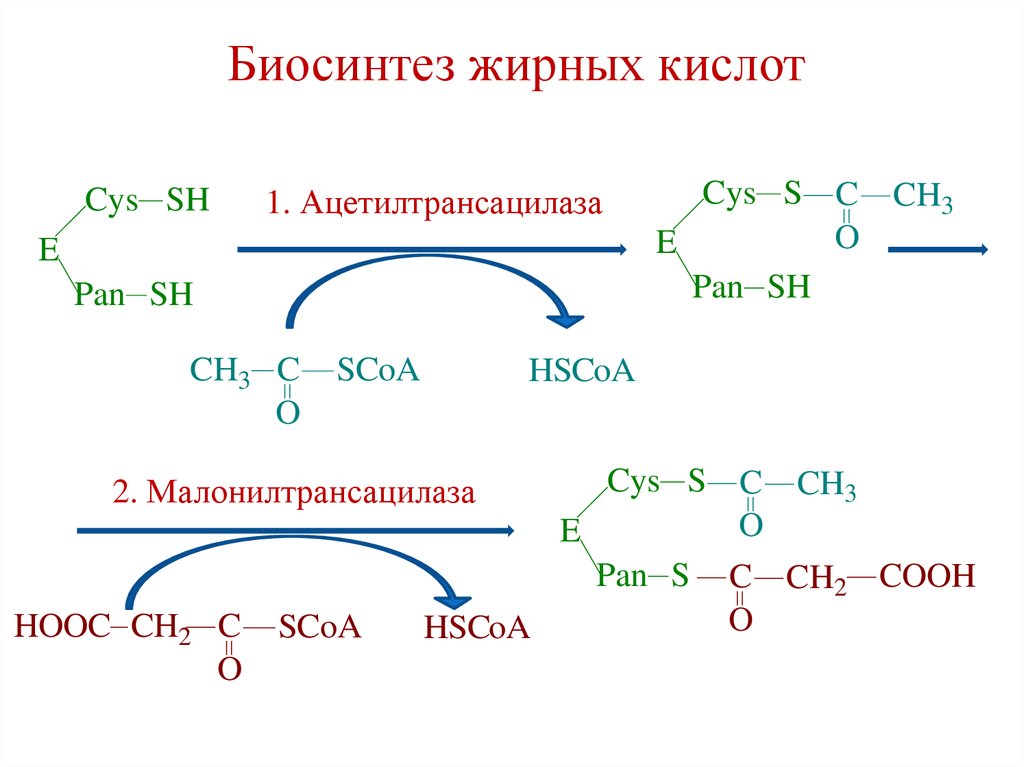
Биосинтез жирных кислотCys SH
1. Ацетилтрансацилаза
E
Pan SH
CH3 C
O
SCoA
HSCoA
Cys S C CH3
O
E
Pan S C CH2 COOH
O
HSCoA
2. Малонилтрансацилаза
HOOC CH2 C
O
SCoA
Cys S C CH3
O
E
Pan SH
92.
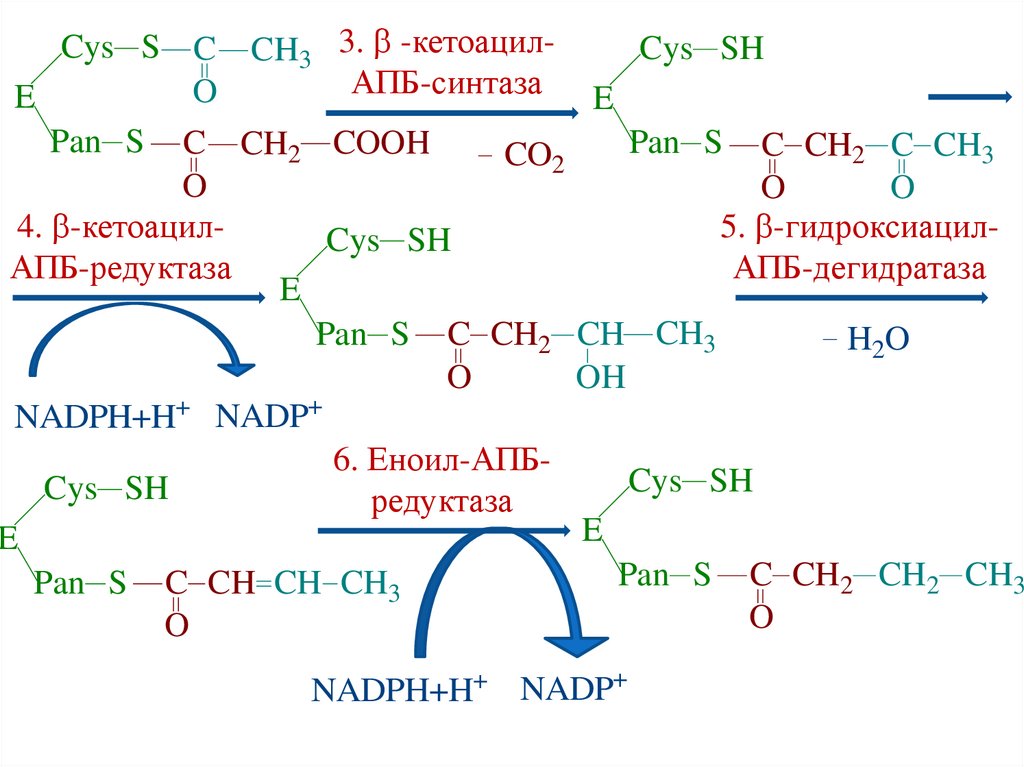
Cys S C CH3 3. -кетоацилCys SHАПБ-синтаза E
O
E
Pan S C CH2 COOH
Pan S C CH2 C CH3
CO2
O
O
O
4. -кетоацил5. -гидроксиацилCys SH
АПБ-редуктаза
АПБ-дегидратаза
E
Pan S C CH2 CH CH3
H2O
O
OH
NADPH+H+ NADP+
6. Еноил-АПБCys SH
Cys SH
редуктаза
E
E
Pan S C CH2 CH2 CH3
Pan S C CH CH CH3
O
O
NADPH+H+ NADP+
93.
Биосинтез жирных кислотРеакции повторяется 7 раз до синтеза пальмитилАПБ. Завершается синтез жирной кислоты
отщеплением пальмитиновой кислоты от АПБ под
действием деацилазы (тиоэстеразы).
Cys SH
7. Деацилаза
(тиоэстераза)
Cys SH
E
E
Pan S
C (CH2)14 CH3
O
CH3 (CH2)14 COOH
H2O
Pan SH
94.
Суммарная реакциябиосинтеза пальмитиновой кислоты
СН3–СО–SСoA + 7НООС–СН2–СО–SСoA +
14НАДФН +14Н+ → СН3–(СН2)14–СООН +
7СO2 + 8HS–KoA + 14НАДФ+ + 6Н2O
95.
Регуляция биосинтеза жирных кислотОсновной регуляторный фермент –
ацетил-СоА карбоксилаза
1. Цитрат – активатор, пальмитоил-СоА –
ингибитор (ассоциация-диссоциация
фермента).
2. Глюкагон, адреналин ингибируют фермент,
инсулин – активирует (фосфорилирование –
дефосфорилирование фермента).
3. Индукция синтеза фермента под действием
инсулина (при потреблении богатой
углеводами пищи).
96.
Элонгация (удлинение) жирных кислот• Происходит в ЭР под действием
энзиматической системы элонгаза.
• Удлинение цепи жирной кислоты
происходит путем последовательного
присоединения к соответствующему ацилСоА двухуглеродных фрагментов от
малонил-СоА при участии НАДФН.
97.
Синтез ненасыщенных жирных кислот• Моноеновые жирные кислоты –
пальмитоолеиновая и олеиновая –
синтезируются из пальмитиновой и
стеариновой кислот под действием фермента
десатураза.
• Процесс протекает в ЭР клеток печени и
жировой ткани при участии молекулярного
кислорода, НАДФН, цитохрома b5, ФАД.
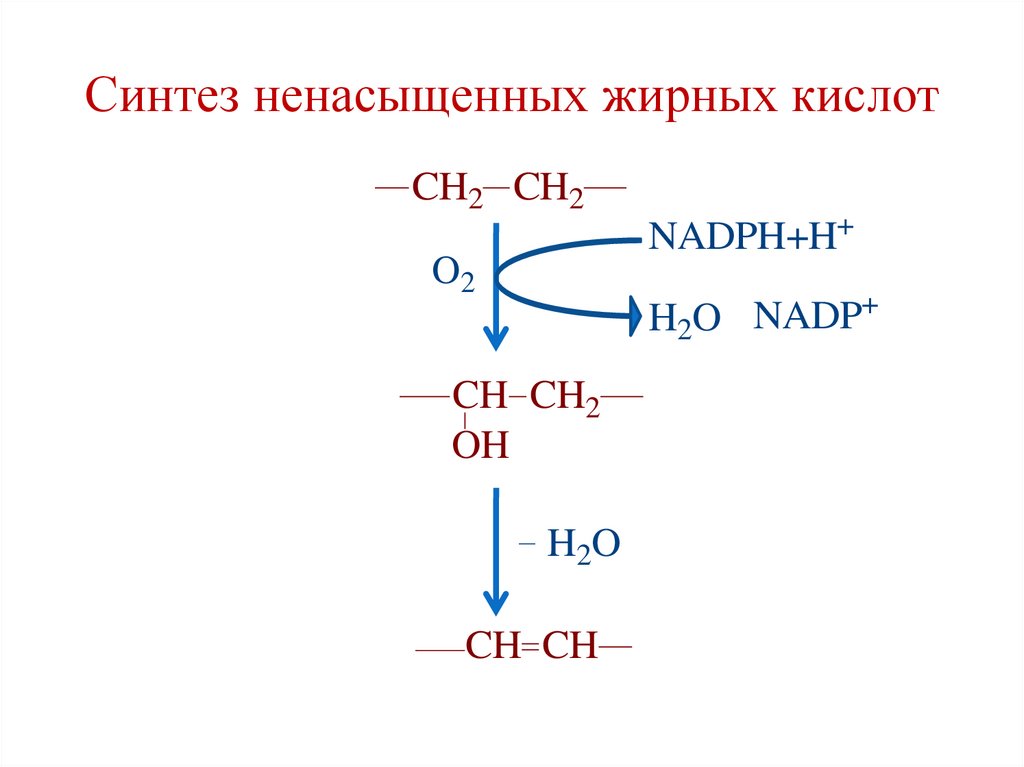
98.
Синтез ненасыщенных жирных кислотCH2 CH2
O2
NADPH+H+
H2O NADP+
CH CH2
OH
H2O
CH CH
99.
• Десатураза млекопитающих может образоватьдвойные связи только на участке цепи жирной
кислоты от 9-го до 1-го углеродных атомов.
• Поэтому в организме млекопитающих, в том
числе и человека, не синтезируются
линолевая (18:2; 9,12) и линоленовая (18:3;
9,12,15) кислоты – незаменимые жирные
кислоты.
• Арахидоновая кислота (20:4; 5,8,11,14) у
большинства млекопитающих синтезируется
из линолевой кислоты.
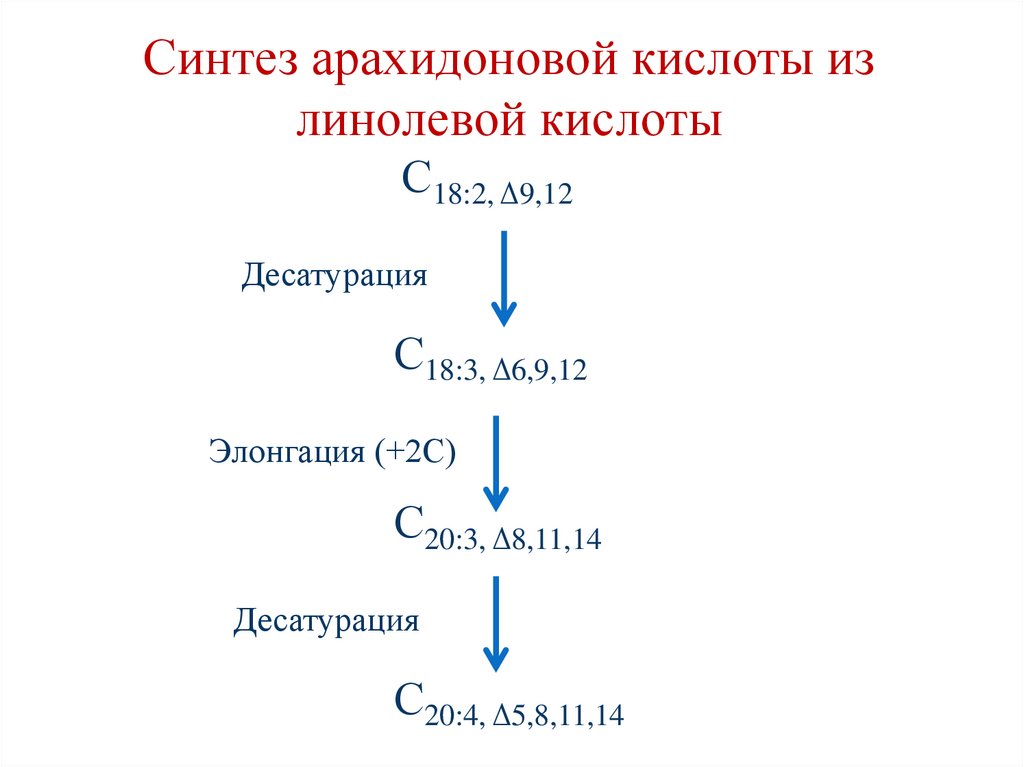
100.
Синтез арахидоновой кислоты излинолевой кислоты
С18:2, Δ9,12
Десатурация
С18:3, Δ6,9,12
Элонгация (+2С)
С20:3, Δ8,11,14
Десатурация
С20:4, Δ5,8,11,14
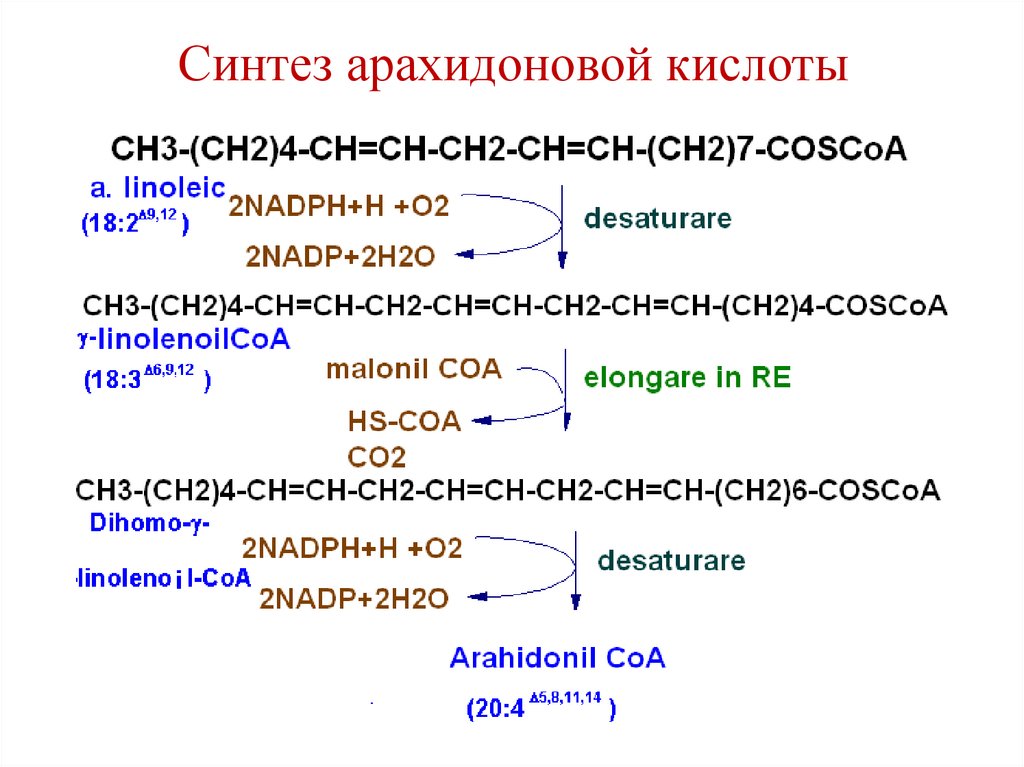
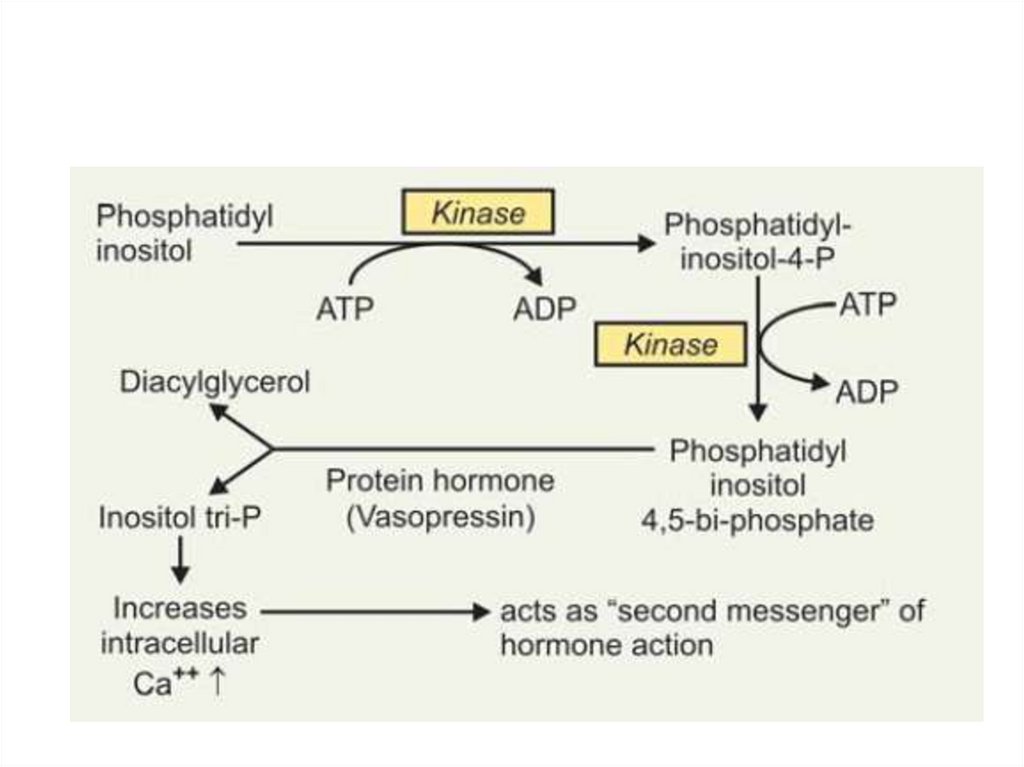
101.
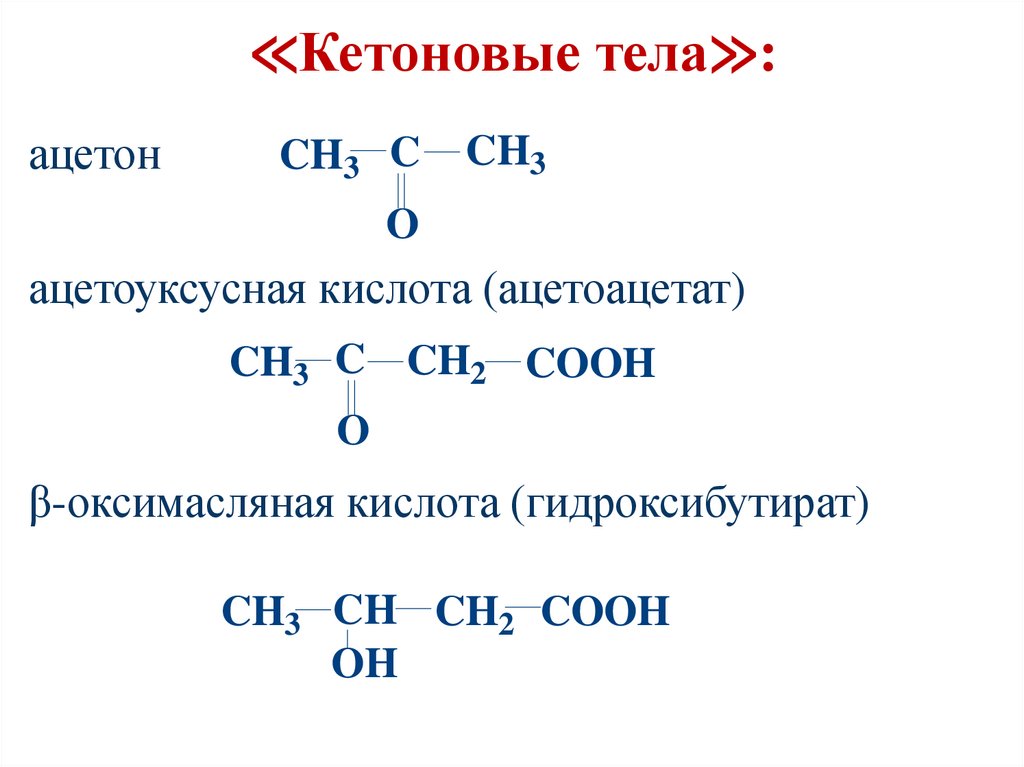
Синтез арахидоновой кислоты102.
≪Кетоновые тела≫:ацетон
CH3 C
CH3
O
ацетоуксусная кислота (ацетоацетат)
CH3 C CH2 COOH
O
β-оксимасляная кислота (гидроксибутират)
CH3 CH CH2 COOH
OH
103.
Синтез ≪кетоновых тел≫• Происходит только в печени.
• Субстратом является ацетил-СоА.
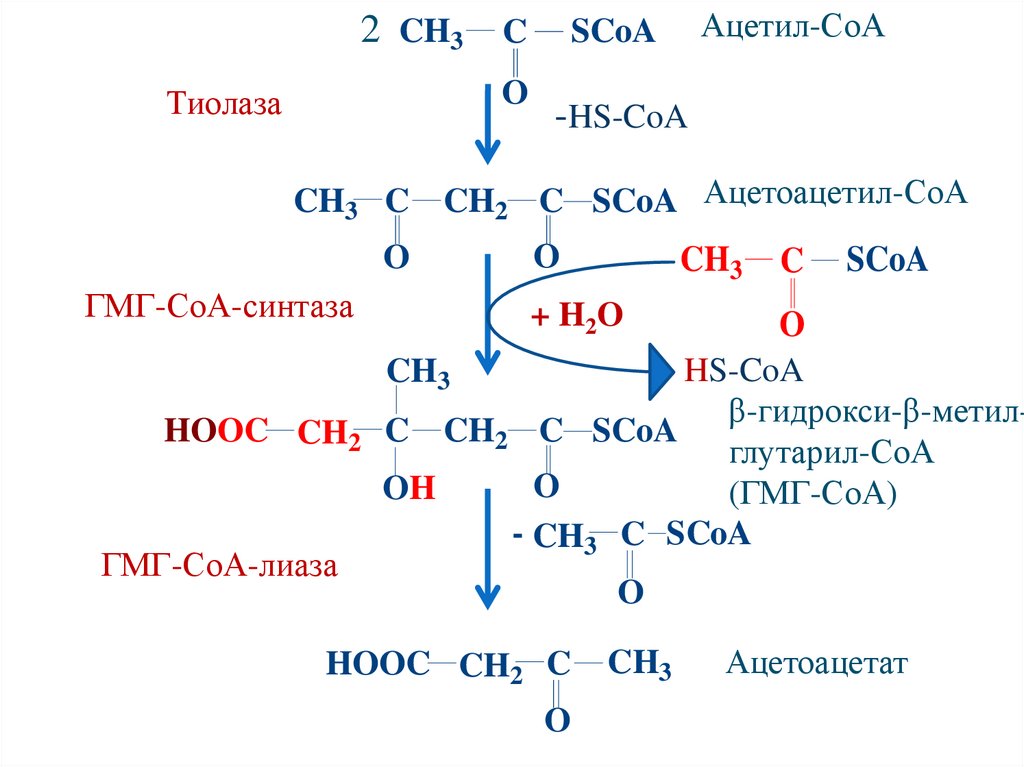
104.
2 CH3 CO
Тиолаза
Ацетил-СоА
SCoA
-HS-CoA
CH3 C CH2 C SCoA Ацетоацетил-СоА
O
ГМГ-СоА-синтаза
O
CH3
C
SCoA
+ H2O
O
HS-CoA
CH3
β-гидрокси-β-метилHOOC CH2 C CH2 C SCoA
глутарил-СоА
O
OH
(ГМГ-СоА)
- CH3 C SCoA
ГМГ-СоА-лиаза
O
HOOC CH2 C
O
CH3
Ацетоацетат
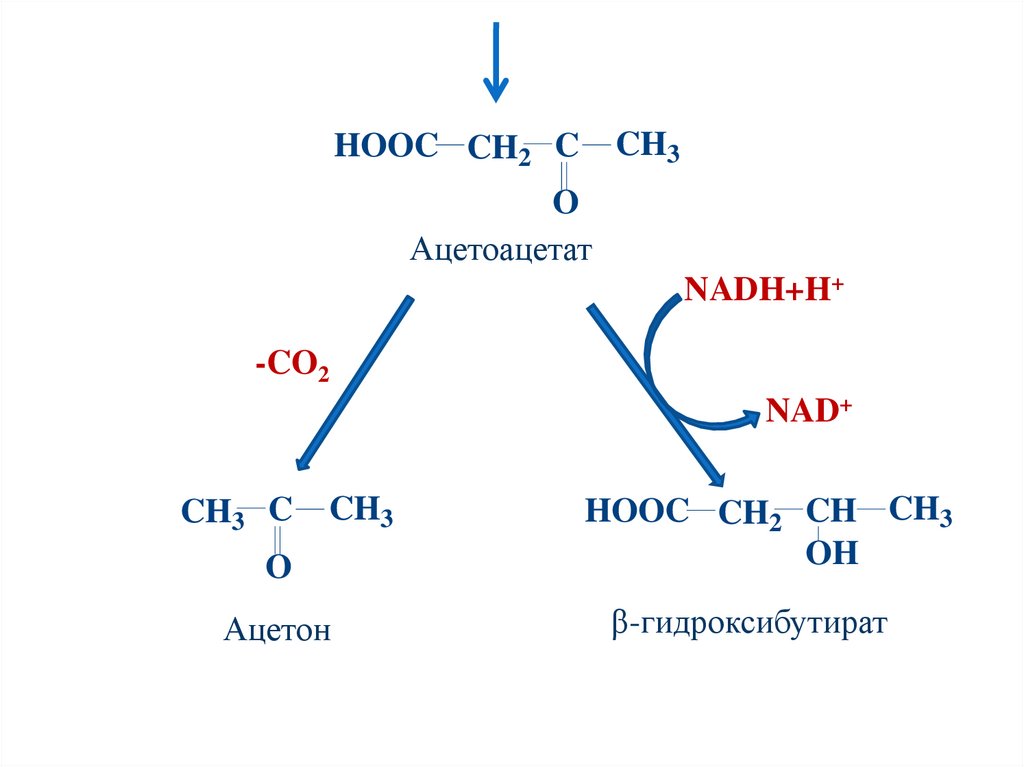
105.
CH3HOOC CH2 C
O
Ацетоацетат
NADH+H+
-CO2
NAD+
O
HOOC CH2 CH CH3
OH
Ацетон
β-гидроксибутират
CH3 C
CH3
106.
Использование «кетоновых тел»в тканях
• используются в качестве ≪топлива≫
сердечной мышцей, корковым слоем почек
(в нормальных условиях), головным мозгом
(при голодании и диабете).
107.
CH3 CH CH2 COOHOH
NAD+
NADH+H+
CH3 C CH2 COOH
ATP, HS-CoA
Сукцинил-SСоА
O
Сукцинат
AMP, H4P2O7
CH3 C CH2 C SCoA
O
O
+ HS-CoA
2 CH3 C SCoA
O
2 циклa Кребса (СО2, Н2О)
108.
• Нормальная концентрация «кетоновых тел»(0,03–0,2 ммоль/л).
• При патологических состояниях (сахарный
диабет, голодание) концентрация кетоновых
тел в сыворотке крови увеличивается до
16–20 ммоль/л.
• Кетонемия –увеличение концентрации
кетоновых тел в крови.
• Кетонурия – выделение кетоновых тел с
мочой.
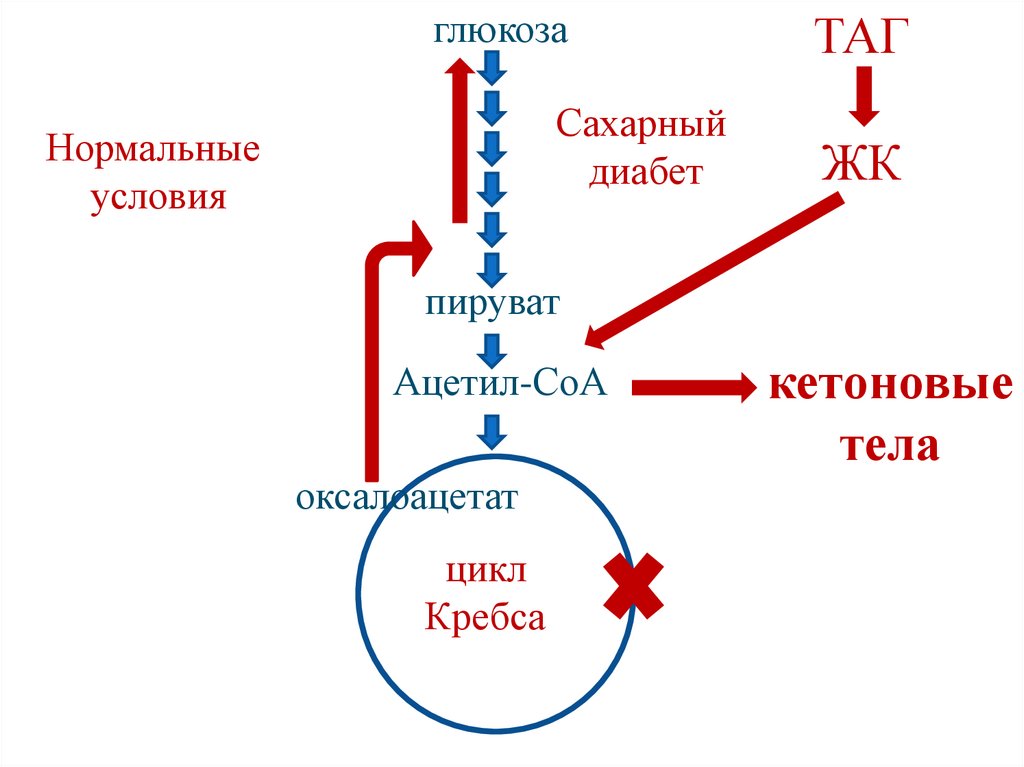
109.
Причины кетонемии1. Увеличение концентрации ацетил-СоА
(усиленное расщепление липидов).
2. Уменьшение концентрации оксалоацетата
(при отсутствии углеводов или нарушении
их использования оксалоацетат
расходуется на образование глюкозы).
110.
глюкозаСахарный
диабет
Нормальные
условия
ТАГ
ЖК
пируват
Ацетил-СоА
оксалоацетат
цикл
Кребса
кетоновые
тела
111.
Метаболизмструктурных липидов
112.
Синтез холестерола• За сутки синтезируется 1г холестерола.
• С пищей поступает 0,3-0,5г.
• Локализация синтеза – цитозоль.
• Органы и ткани – печень (50%), эпителий
кишечника (20%), кожа, кора надпочечников,
половые железы.
• Субстрат – ацетил-СоА.
Этапы:
1. Синтез мевалоновой кислоты;
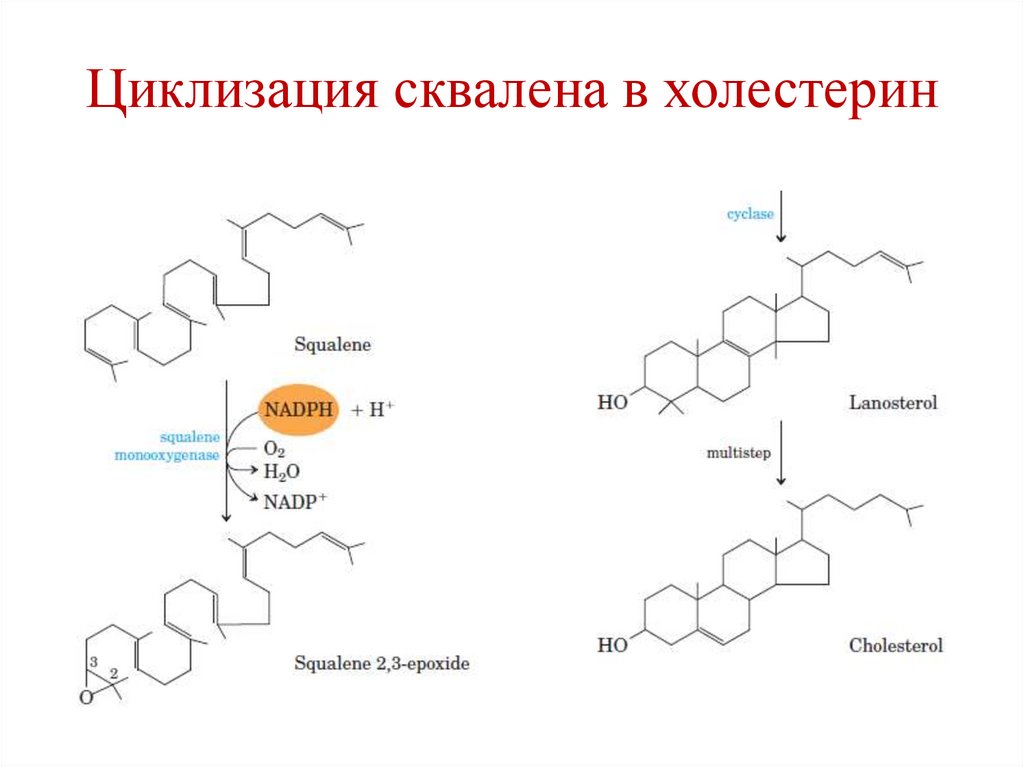
2. Синтез сквалена;
3. Циклизация сквалена в холестерин.
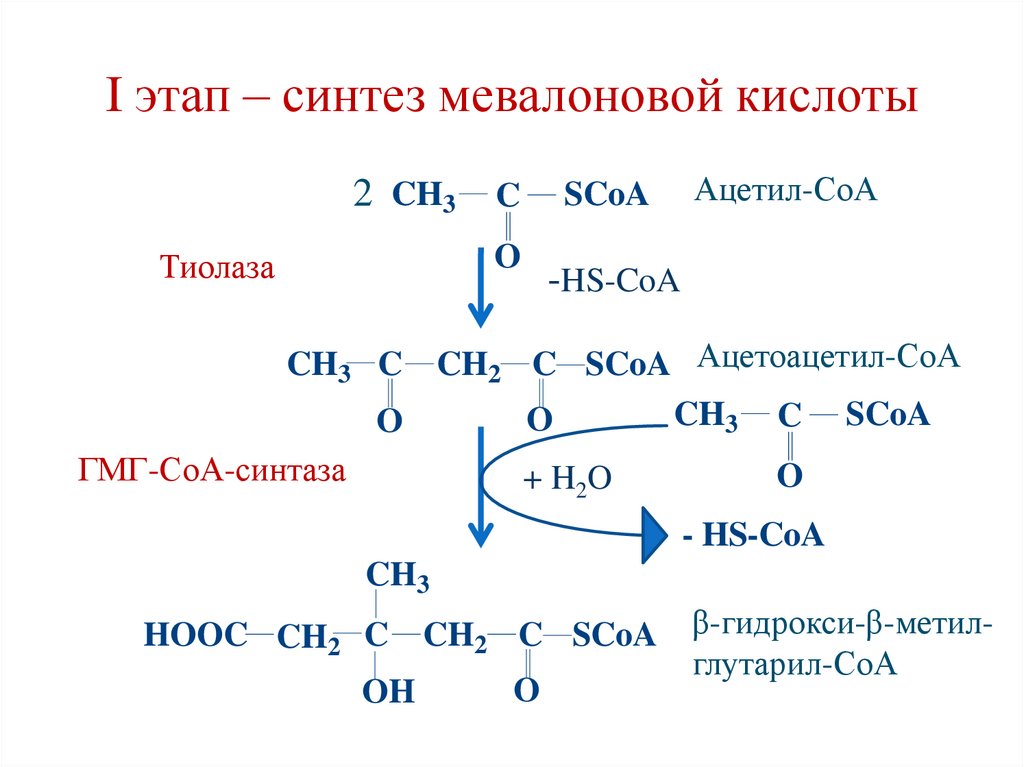
113.
I этап – синтез мевалоновой кислоты2 CH3 C
O
Тиолаза
SCoA
Ацетил-СоА
-HS-CoA
CH3 C CH2 C SCoA Ацетоацетил-СоА
CH3 C SCoA
O
O
ГМГ-СоА-синтаза
+ H2O
O
- HS-CoA
CH3
HOOC CH2 C CH2 C SCoA β-гидрокси-β-метилглутарил-СоА
O
OH
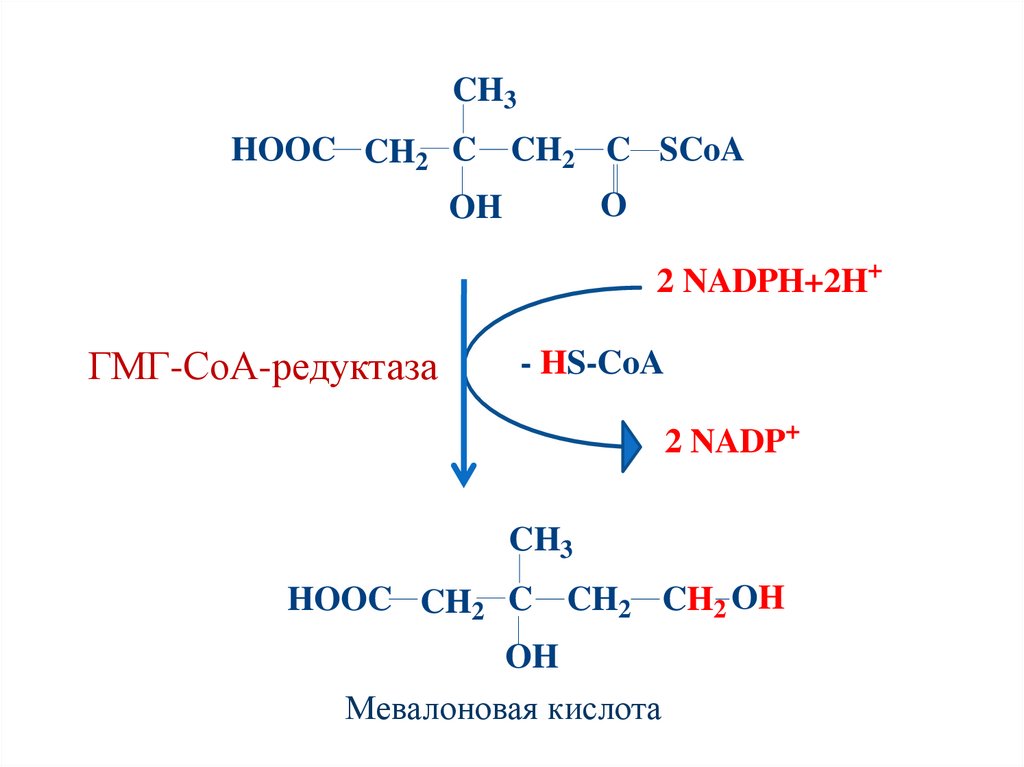
114.
CH3HOOC CH2 C CH2 C SCoA
O
OH
2 NADPH+2H+
ГМГ-СоА-редуктаза
- HS-CoA
2 NADP+
CH3
HOOC CH2 C CH2 CH2 OH
OH
Мевалоновая кислота
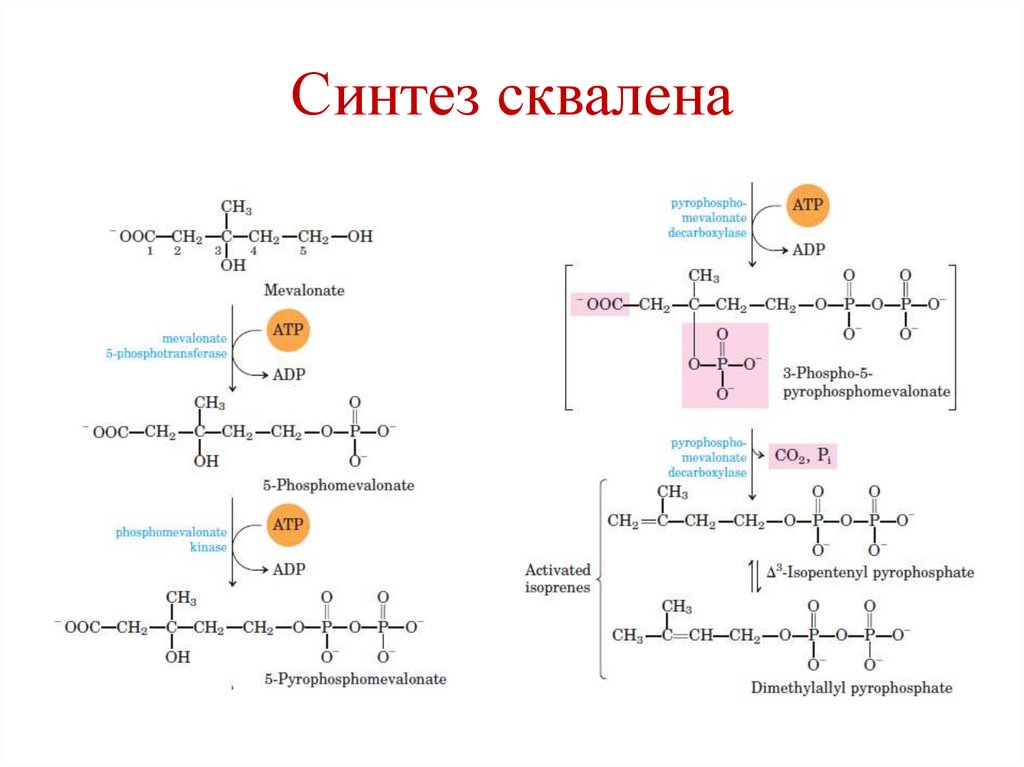
115.
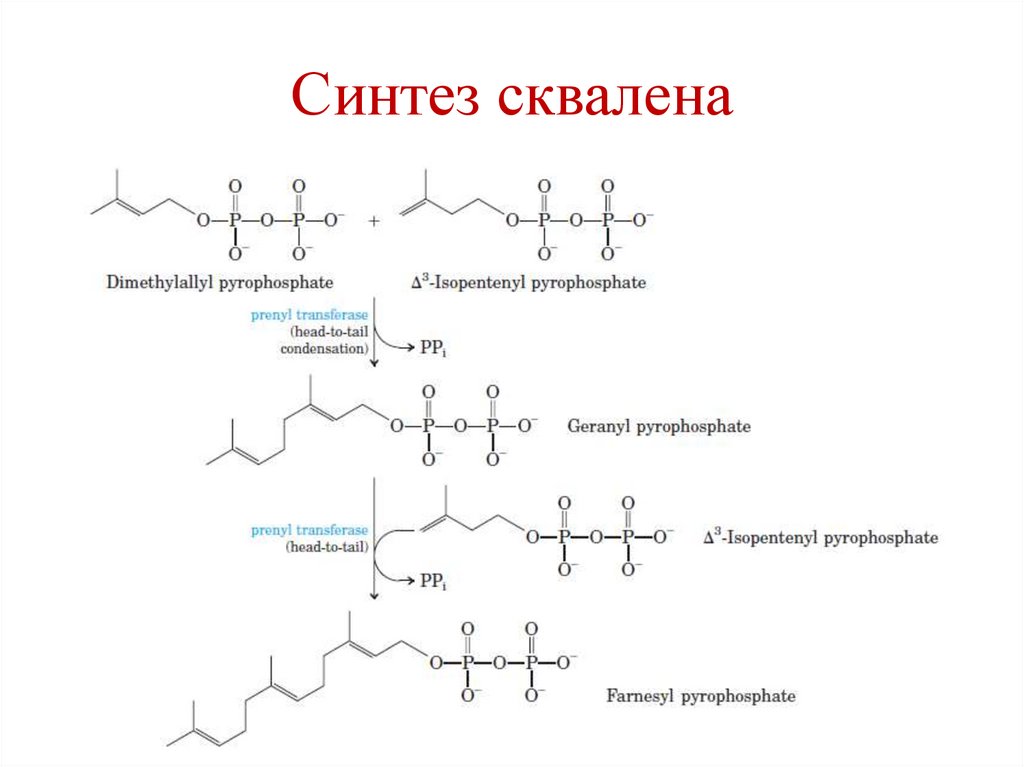
Синтез сквалена116.
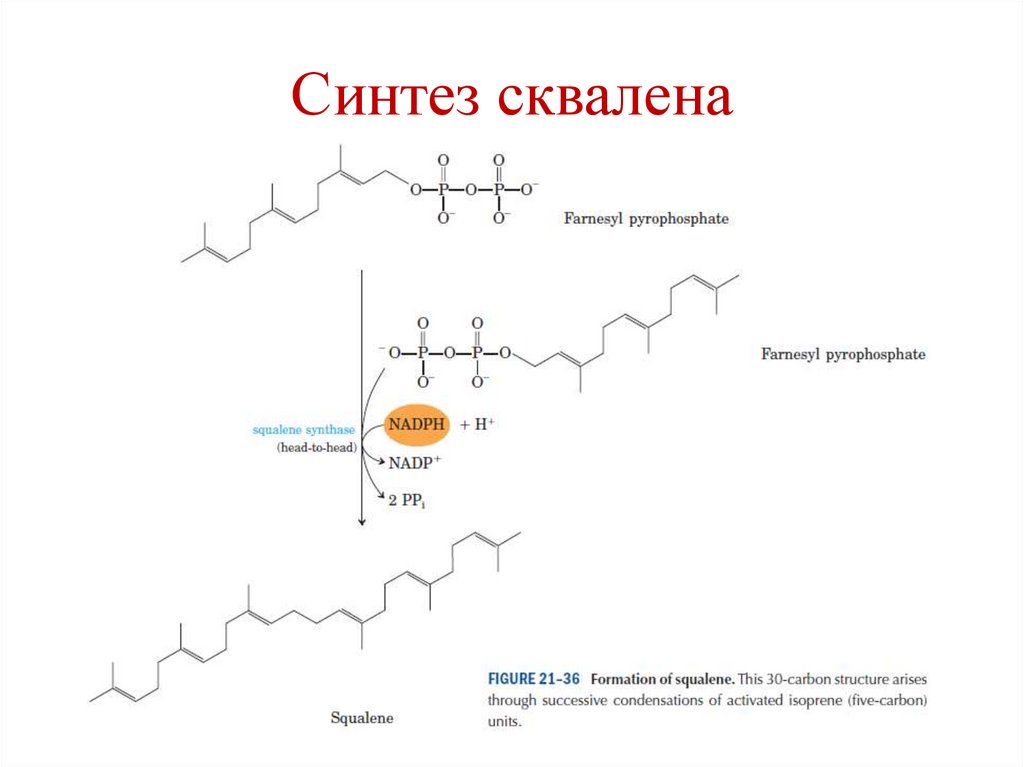
Синтез сквалена117.
Синтез сквалена118.
Циклизация сквалена в холестерин119.
Регуляция биосинтеза холестеролаРегуляторный фермент –
ГМГ-СоА-редуктаза
• Ингибиторы – холестерол, мевалоновая
кислота, желчные кислоты.
Гормональная регуляция:
• Активаторы: инсулин (дефосфорилирует
фермент), тиреоидные гормоны.
• Ингибиторы: глюкагон (фосфорилирует
фермент) и глюкокортикоиды.
120.
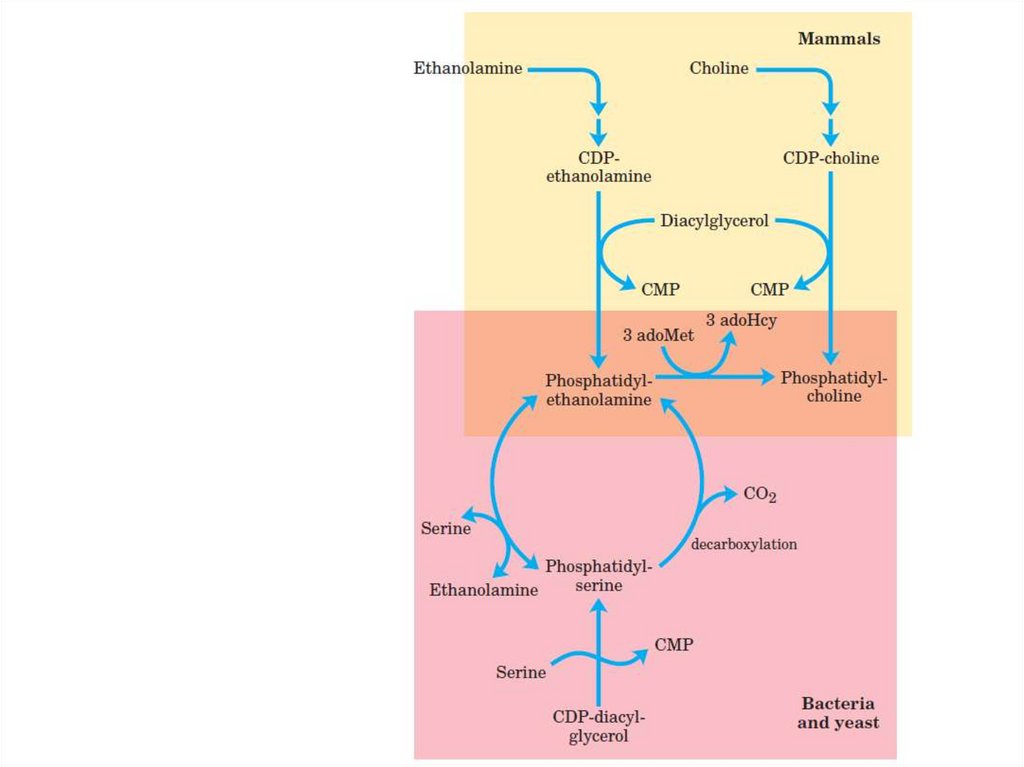
Синтез фосфолипидов• интенсивно происходит в печени, стенке
кишечника, семенниках, яичниках,
молочной железе.
• Протекает в эндоплазматической сети.
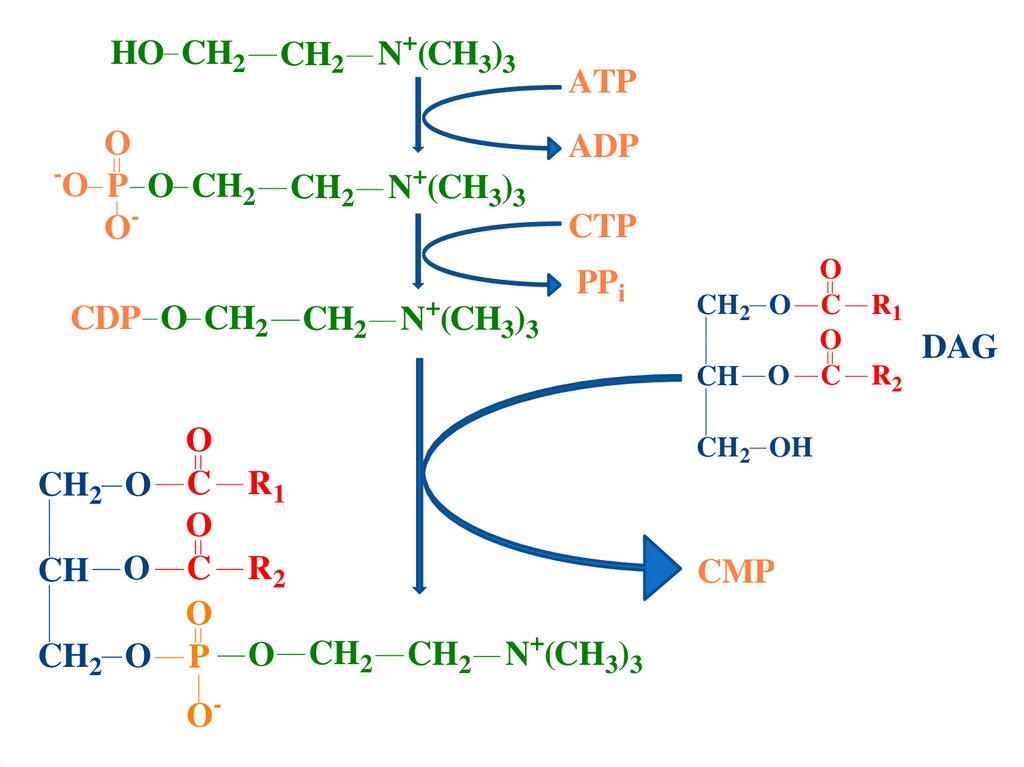
121.
HO CH2 CH2 N+(CH3)3O
O P O CH2
O-
ATP
ADP
CH2 N+(CH3)3
CTP
CDP O CH2 CH2 N+(CH3)3
PPi
CH2 O
CH O
CH2 O
CH O
CH2 O
O
C
O
C
O
P
O-
CH2 OH
R1
R2
O CH2
CMP
CH2 N+(CH3)3
O
C
O
C
R1
R2
DAG
122.
CH2 OCH O
CH2 O
O
C
O
C
O
P
R1
R2
O CH2
CH2 NH3+
O-
HO CH2 CH
NH3+
COOCH2 O
CH O
CH2 O
O
C
O
C
O
P
O-
R1
HO CH2 CH2 NH3+
R2
O CH2
CH
NH3+
COO-
123.
CH2 OCH O
CH2 O
CH2 O
CH O
CH2 O
O
C
O
C
O
P
R1
R2
O CH2
CH
NH3+
O-
COO-
O
C
O
C
O
P
- CO2
O-
R1
R2
O CH2
CH2 NH3+
124.
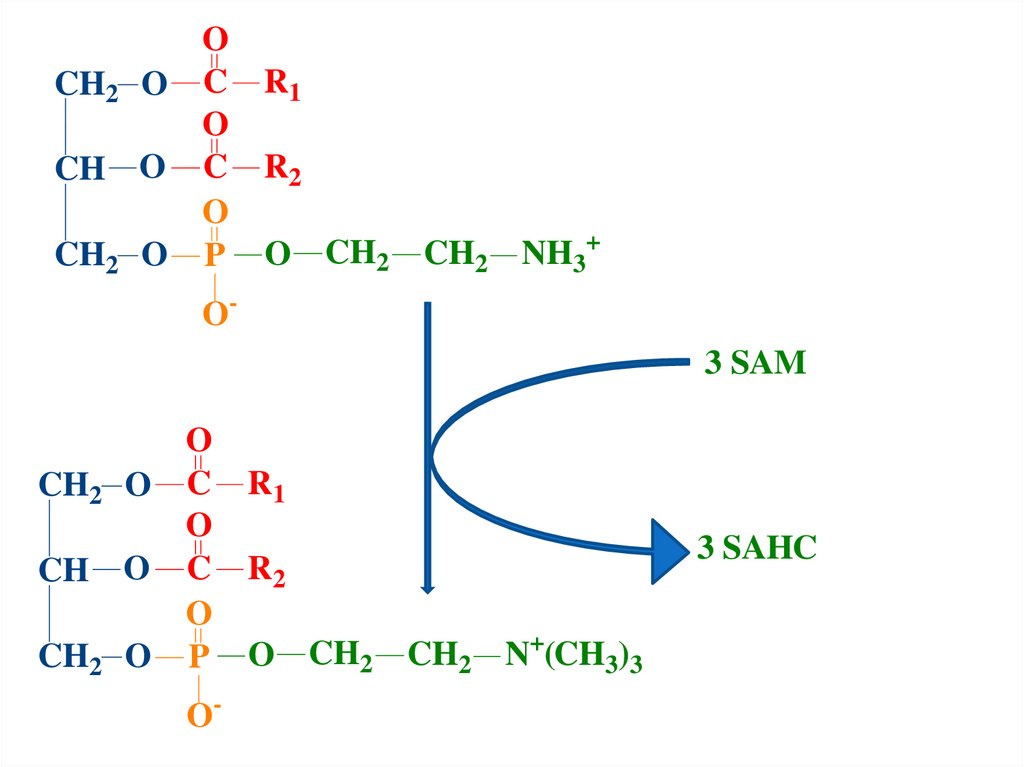
CH2 OCH O
CH2 O
O
C
O
C
O
P
R1
R2
O CH2
CH2 NH3+
O3 SAM
CH2 O
CH O
CH2 O
O
C
O
C
O
P
O-
R1
3 SAHC
R2
O CH2
CH2 N+(CH3)3
125.
NH2N
CH3
N
H2C
+S
O
CH2
CH2
CH NH2
OH
OH
COOH
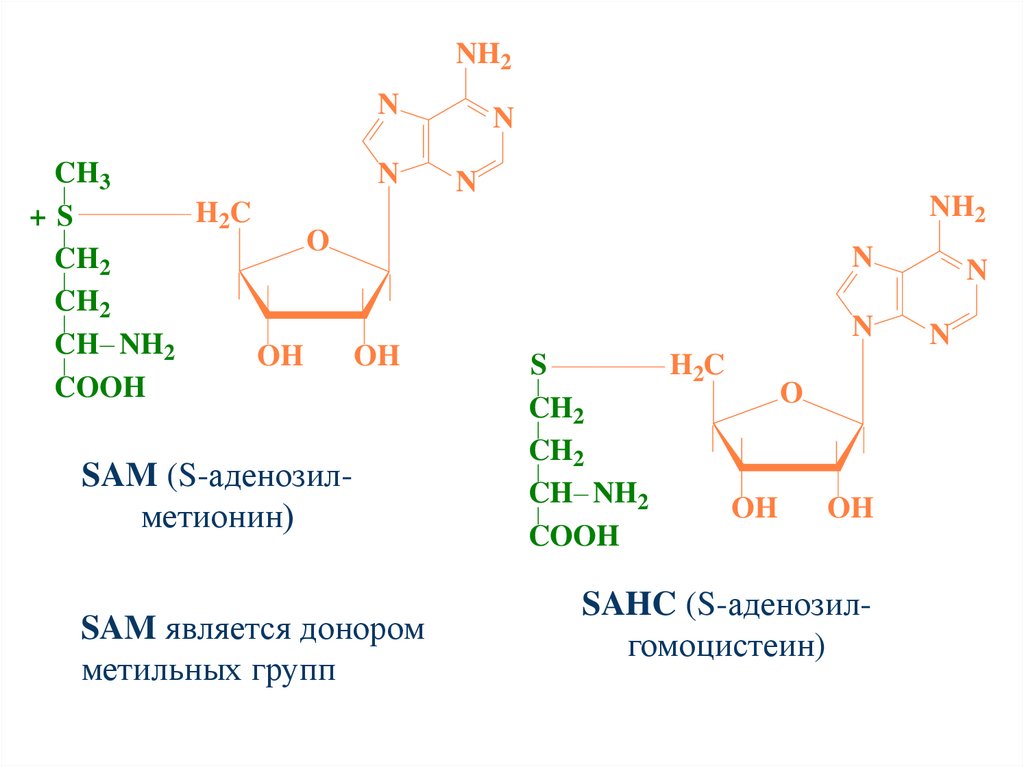
SAM (S-аденозилметионин)
SAM является донором
метильных групп
N
N
NH2
N
N
S
H2C
O
CH2
CH2
CH NH2
OH
OH
COOH
SAHC (S-аденозилгомоцистеин)
N
N
126.
127.
128.
129.
130.
Липотропные вещества131.
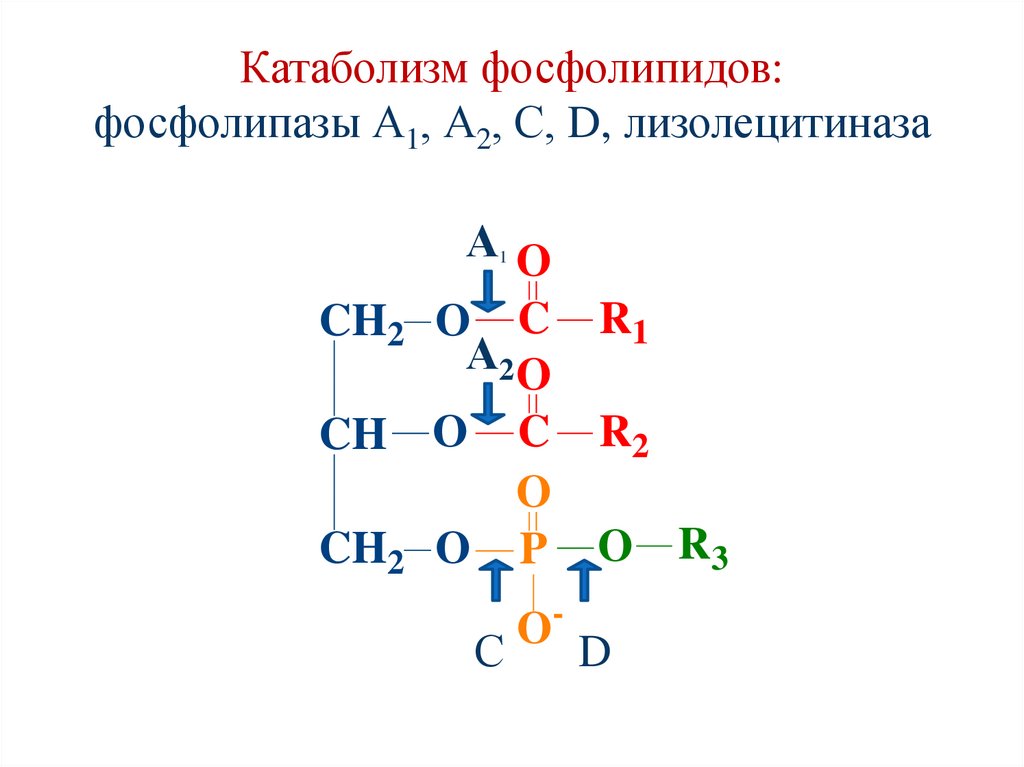
Катаболизм фосфолипидов:фосфолипазы А1, А2, С, D, лизолецитиназа
АO
1
CH2 O C
А2 O
R1
C
O
P
R2
CH
O
CH2 O
С
O-
O R3
D
132.
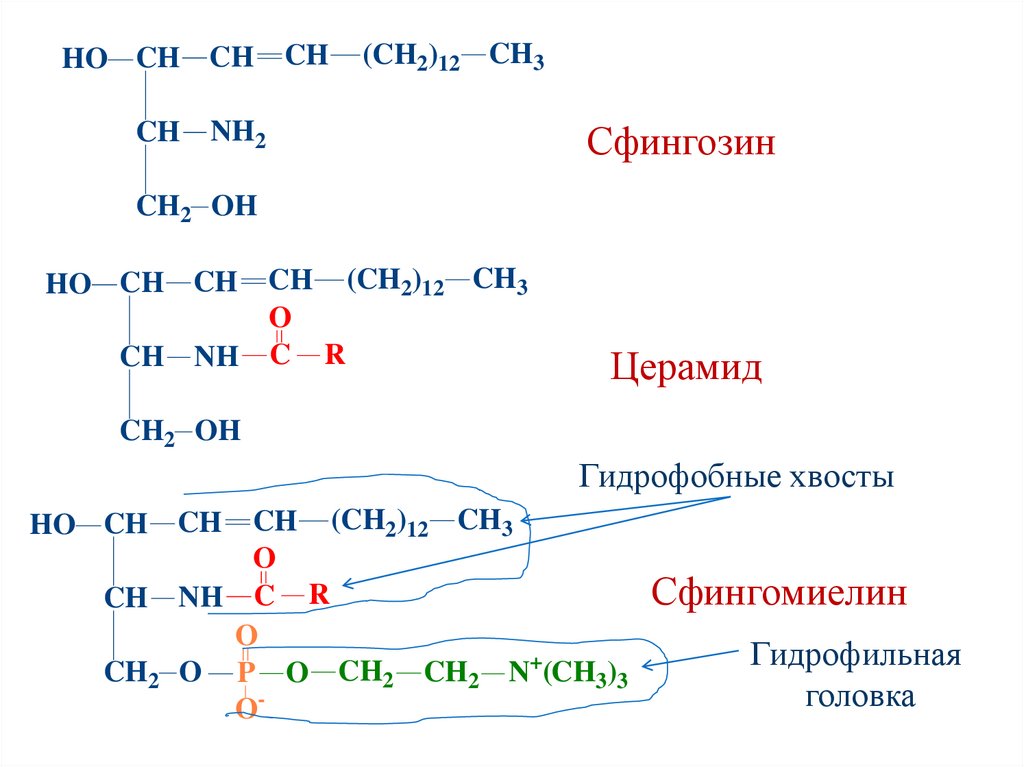
СфингофосфолипидыСфингомиелины – состав:
Сфингозин
Жирная кислота
Фосфорная кислота
Аминоспирт
Функция – структурная (входят в состав
клеточных мембран, особенно нервных
клеток).
Являются амфифильными веществами.
133.
HO CH CHCH
CH
(CH2)12 CH3
NH2
Сфингозин
CH2 OH
CH (CH2)12 CH3
O
NH C R
HO CH CH
CH
Церамид
CH2 OH
Гидрофобные хвосты
CH (CH2)12 CH3
O
CH NH C R
O
CH2 O P O CH2 CH2 N+(CH3)3
O-
HO CH CH
Сфингомиелин
Гидрофильная
головка
134.
ГликолипидыГликосфинголипиды – состав:
Сфингозин
Жирная кислота
Углеводы
Классификация
Цереброзиды
Сульфатиды
Глобозиды
Ганглиозиды
135.
Цереброзидысостоят из церамида и моносахарида (глюкозы или
галактозы).
Жирная кислота в церамиде обычна представлена С24.
CH (CH2)12 CH3
O
C R
HO CH CH
CH
NH
CH2 O
O
CH2OH
OH
OH 4
CH (CH2)12 CH3
O
C R
HO CH CH
CH
NH
CH2 O
CH2OH
O
OH
4
OH
OH
Галактоцереброзиды
содержится в основном
в нервных тканях
OH
Глюкоцереброзиды
содержится в основном
в тканях, отличных от
нервных
136.
СульфатидыЯвляются производными цереброзидов, у
которых в 3-м положении углевода
содержится сульфат.
HO CH
CH
CH
NH
CH (CH2)12
O
C R
CH2 O
O
OH
CH2OH
OH
O SO3-
CH3
Сульфогалактоцереброзид
в больших количествах
содержится в миелине.
137.
ГанглиозидыСостоят из церамида,
гетероолигосахарида и 1, 2, 3 сиаловых
кислот.
• Классы ганглиозидов:(G – ганглиозид):
• GM – моносиаловый ганглиозид;
• GD – дисиаловый ганглиозид;
• GT – трисиаловый ганглиозид;
• GQ – тетрасиаловый ганглиозид.
Содержатся в основном в нервной ткани.
Выполняют рецепторную функцию.
138.
Ганглиозид GM2Neu5Ac
Церамид
Glc
Gal
GalNAc
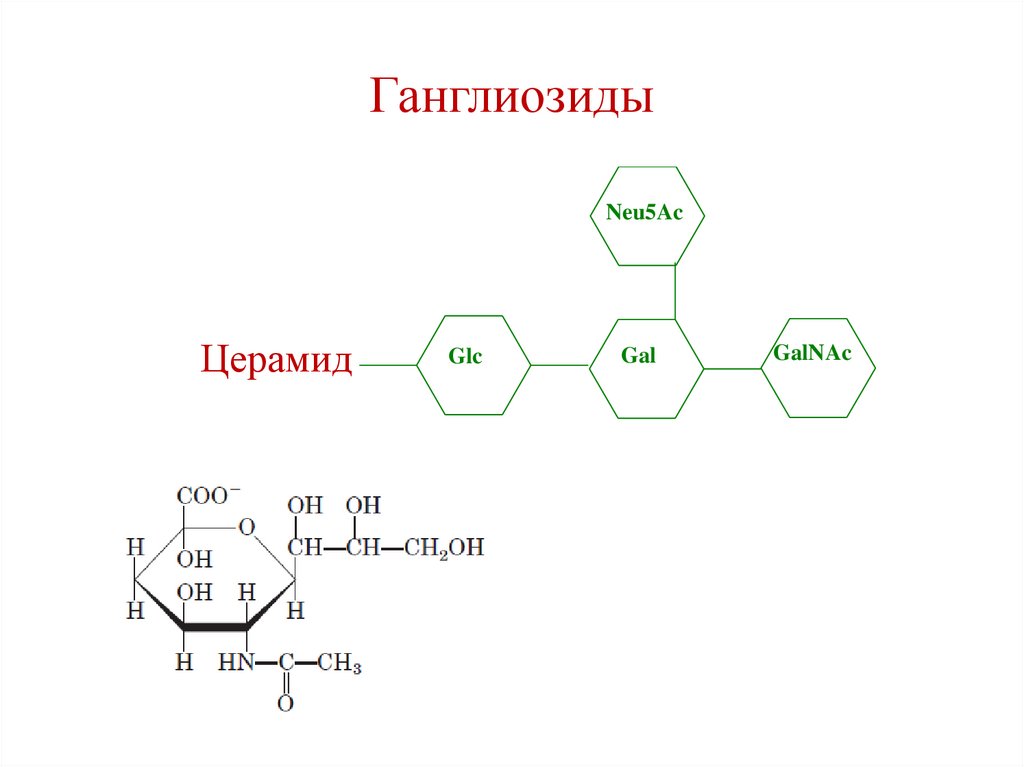
N-ацетилнеураминовая
кислота (сиаловая кислота)
139.
Ганглиозид GM2140.
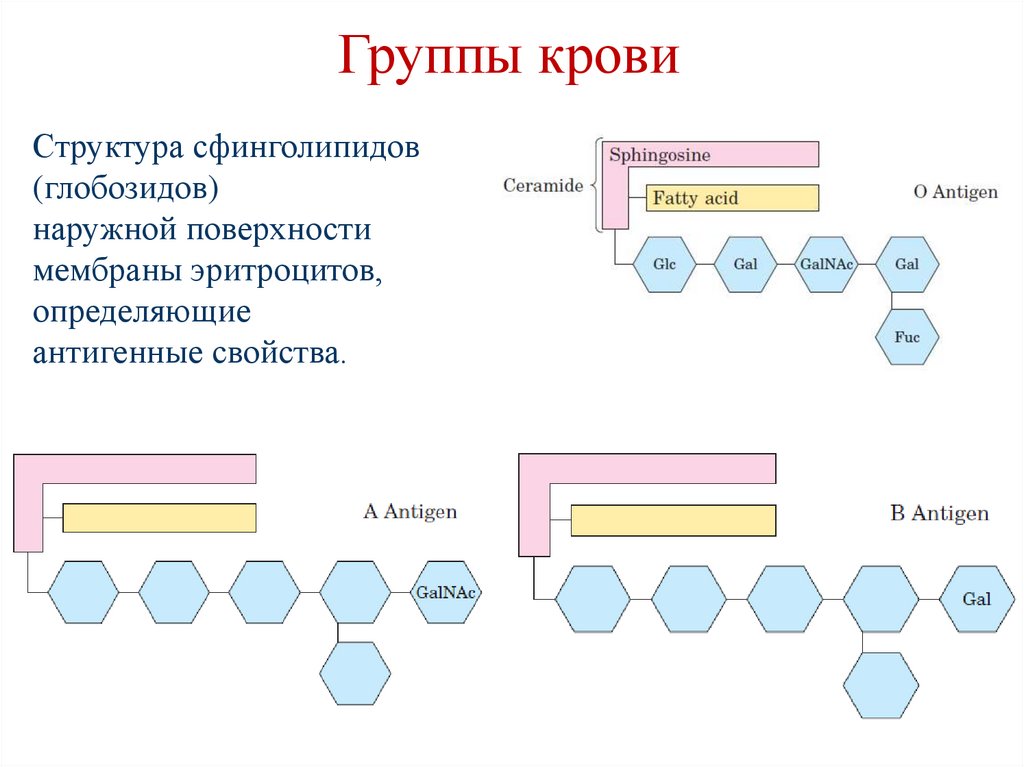
Группы кровиСтруктура сфинголипидов
(глобозидов)
наружной поверхности
мембраны эритроцитов,
определяющие
антигенные свойства.
141.
Синтез сфинголипидовCH (CH2)12 CH3
O
CH NH C R
O
CH2 O P O CH2 CH2 N+(CH3)3
O-
HO CH CH
CH (CH2)12 CH3
O
C R
HO CH CH
CH
NH
CH2 O
O
OH
CH2OH
OH
OH
Вначале синтезируется церамид, который далее
является общим предшественником в синтезе
сфингомиелинов и гликолипидов.
Церамид синтезируется из пальмитил-СоА, серина и
ацил-СоА.
При синтезе сфингомиелинов участвуют CDPпроизводные.
При синтезе гликолипидов участвуют UDPпроизводные углеводов.
142.
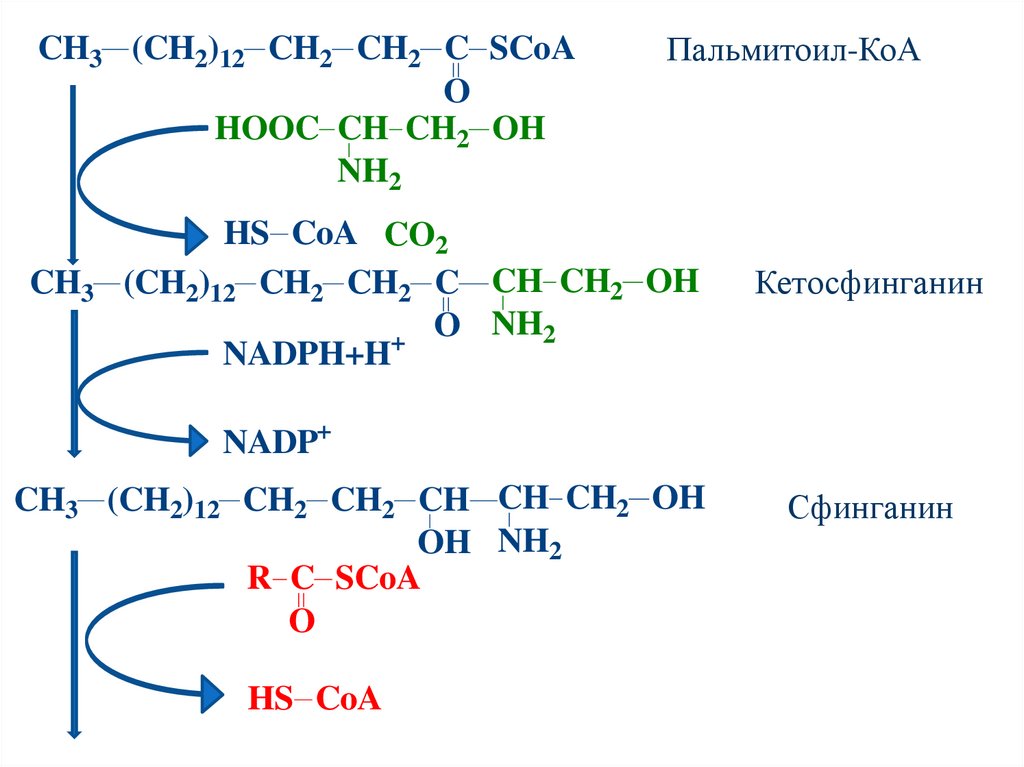
CH3 (CH2)12 CH2 CH2 C SCoAO
HOOC CH CH2 OH
NH2
CH3
Пальмитоил-КоА
HS CoA CO2
(CH2)12 CH2 CH2 C CH CH2 OH
O NH2
+
NADPH+H
Кетосфинганин
NADP+
CH3 (CH2)12 CH2 CH2 CH CH CH2 OH
OH NH2
R C SCoA
O
HS CoA
Сфинганин
143.
CH3 (CH2)12 CH2 CH2 CH CH CH2 OHOH NH
N-ацилсфинганин
FAD
C O
R
FADH2
CH3 (CH2)12 CH CH CH CH CH2 OH
OH NH
Церамид
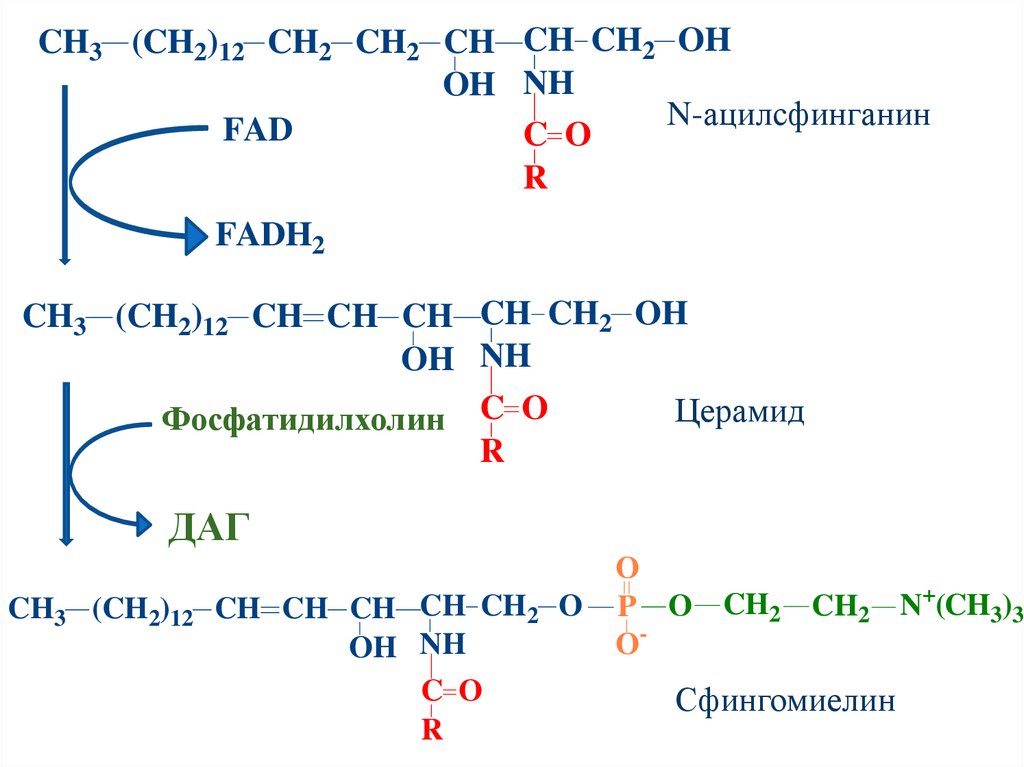
Фосфатидилхолин C O
R
ДАГ
CH3 (CH2)12 CH CH CH CH CH2 O
OH NH
C O
R
O
P O CH2
O-
CH2 N+(CH3)3
Сфингомиелин
144.
Синтез сфингомиелиновПальмитоил-СоА + серин + ацил-СоА
(NADPH, FAD) →→→→ церамид
Церамид
Фосфатидилхолин
ДАГ
CDP-холин
CMP
Сфингомиелин
145.
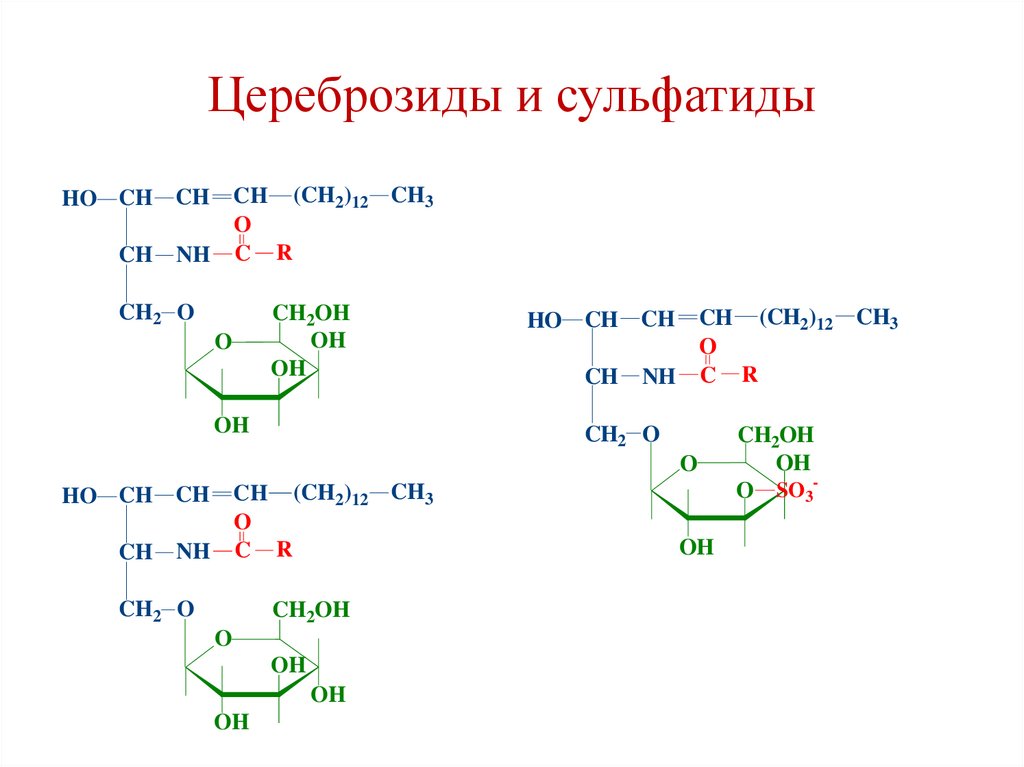
Цереброзиды и сульфатидыCH (CH2)12 CH3
O
C R
HO CH CH
CH
NH
CH2 O
CH2OH
OH
OH
O
OH
HO CH
CH
CH
NH
CH (CH2)12
O
C R
CH2 O
O
CH (CH2)12 CH3
O
C R
HO CH CH
CH
NH
CH2 O
CH2OH
O
OH
OH
OH
OH
CH2OH
OH
O SO3-
CH3
146.
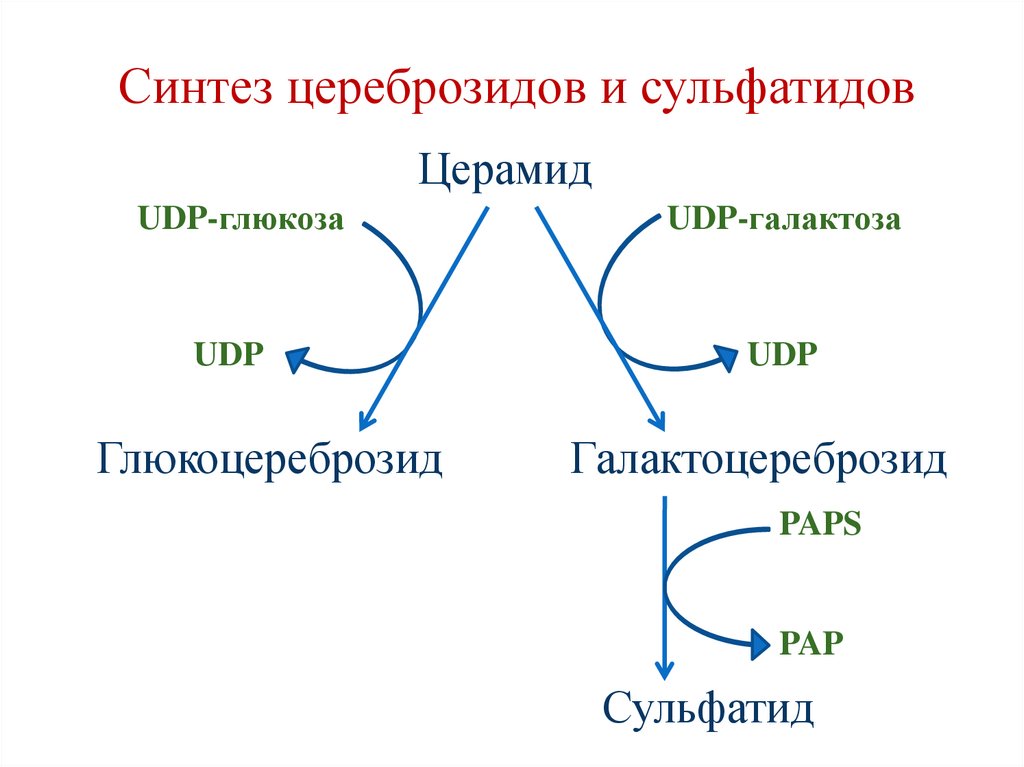
Синтез цереброзидов и сульфатидовЦерамид
UDP-глюкоза
UDP-галактоза
UDP
UDP
Глюкоцереброзид
Галактоцереброзид
PAPS
PAP
Сульфатид
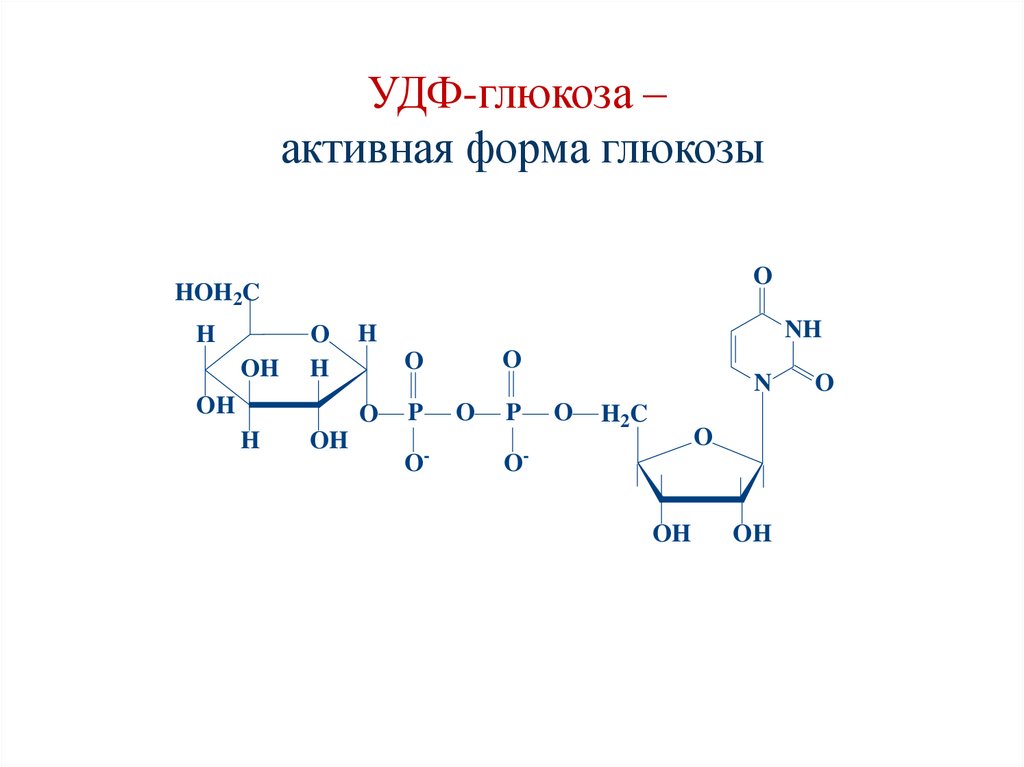
147.
УДФ-глюкоза –активная форма глюкозы
O
HOH2C
H
OH
O
H
OH
OH
O
O
O
H
NH
H
P
O-
N
O
P
O
H2C
O
OOH
OH
O
148.
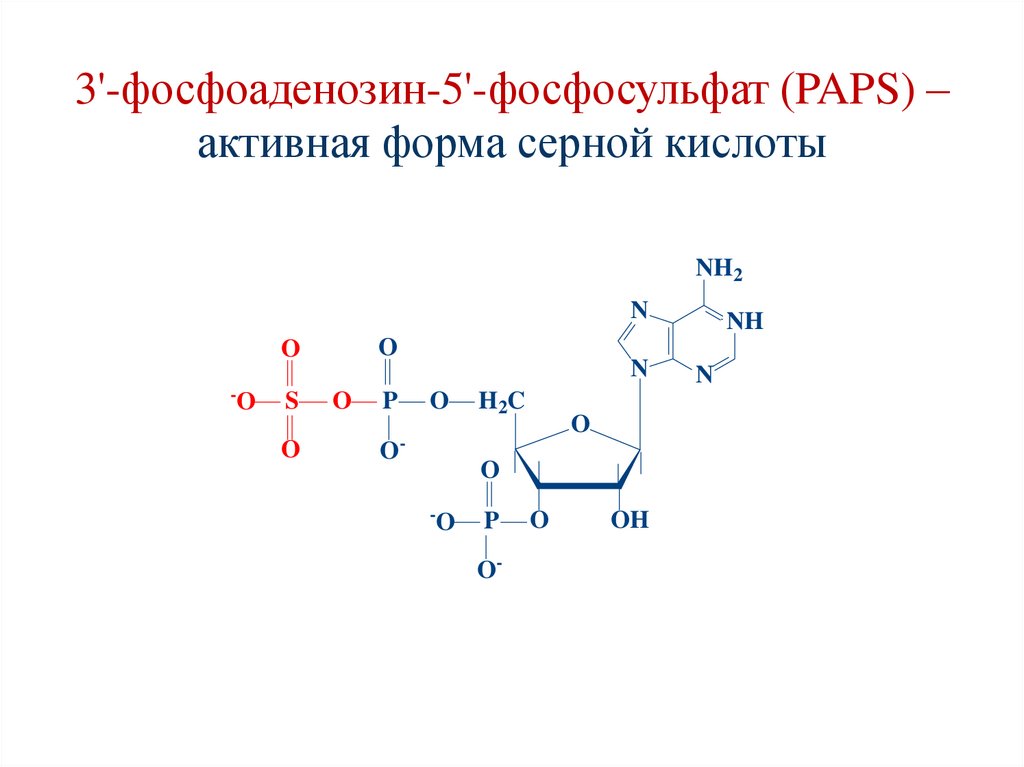
3'-фосфоаденозин-5'-фосфосульфат (PAPS) –активная форма серной кислоты
NH2
N
O
O
-O
S
O
O
P
N
O
O-
H2C
O
O
-O
P
O-
O
OH
NH
N
149.
ГанглиозидыNeu5Ac
Церамид
Glc
Gal
GalNAc
150.
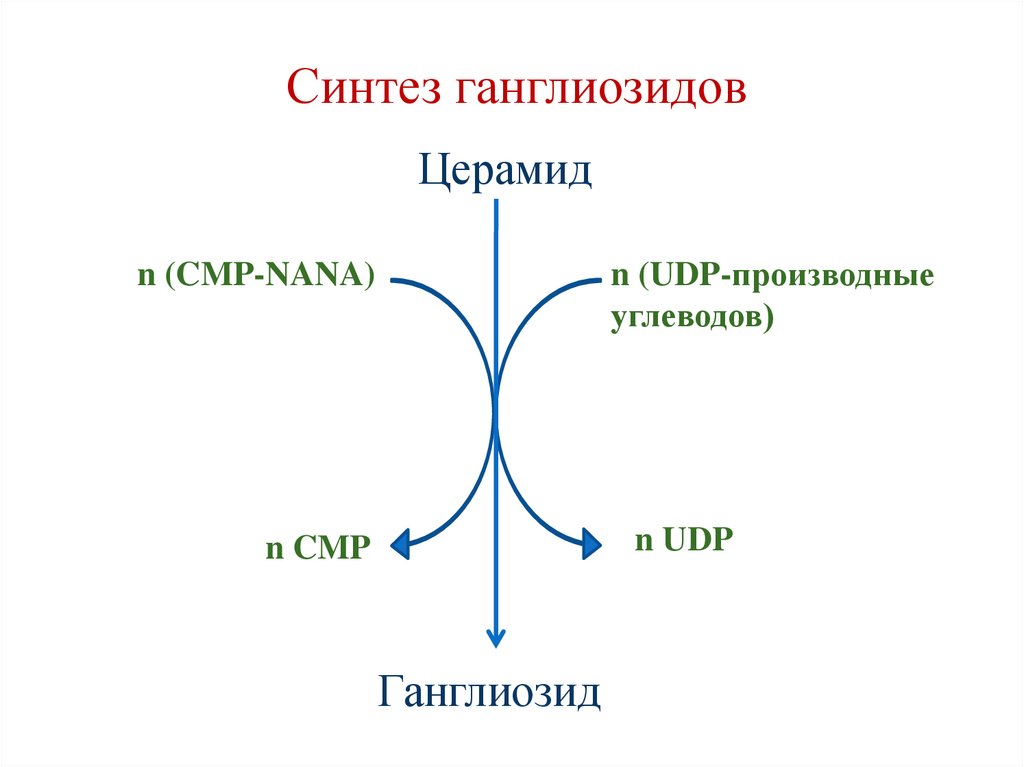
Синтез ганглиозидовЦерамид
n (CMP-NANA)
n (UDP-производные
углеводов)
n UDP
n CMP
Ганглиозид
151.
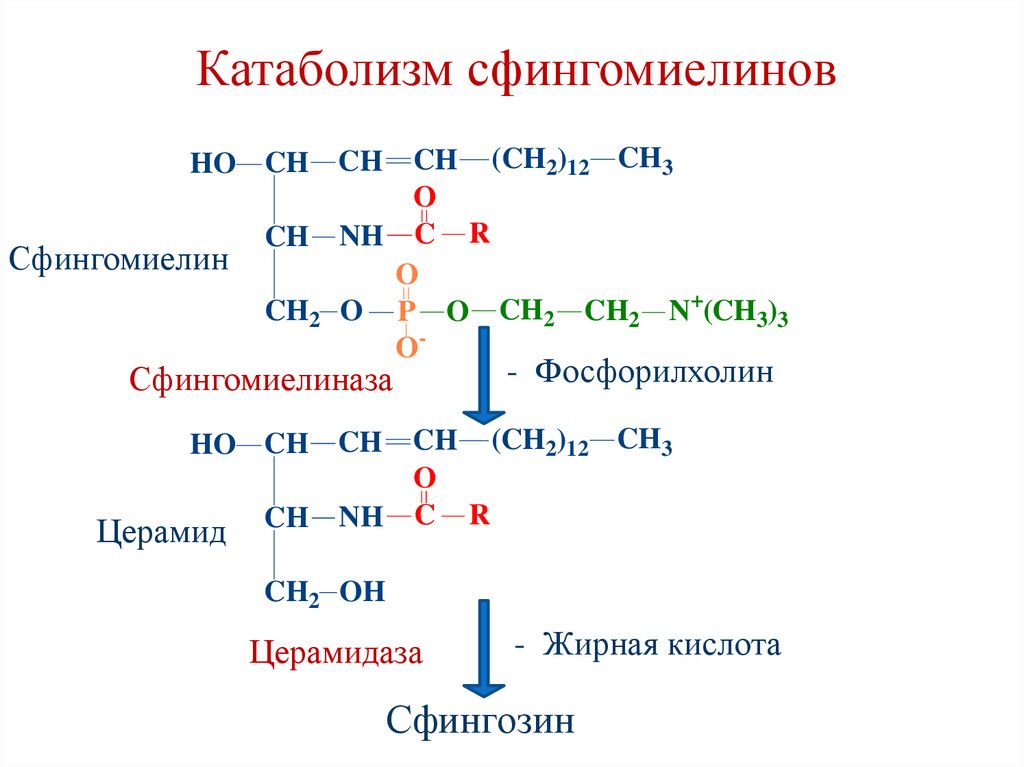
Катаболизм сфингомиелиновCH (CH2)12 CH3
O
CH NH C R
O
CH2 O P O CH2 CH2 N+(CH3)3
O-
HO CH CH
Сфингомиелин
Сфингомиелиназа
- Фосфорилхолин
CH (CH2)12 CH3
O
NH C R
HO CH CH
Церамид
CH
CH2 OH
Церамидаза
- Жирная кислота
Сфингозин
152.
Болезнь Ниманна-ПикаПричина – генетический дефект фермента
сфингомиелиназа.
В лизосомах накапливается сфингомиелин.
Клинические симптомы:
•Гепатоспленомегалия
•Умственная отсталость
•Ранняя смерть
153.
Катаболизм гликолипидов• Начинается с перемещения гликолипидов с
поверхности клетки в цитоплазму по
механизму эндоцитоза. Эндосомы,
содержащие гликолипиды, сливаются с
лизосомами, где содержатся ферменты,
необходимые для расщепления
гликолипидов: альфа- и бета-галактозидазы,
бета-глюкозидаза, нейраминидаза,
гексозаминидазы, церамидаза
154.
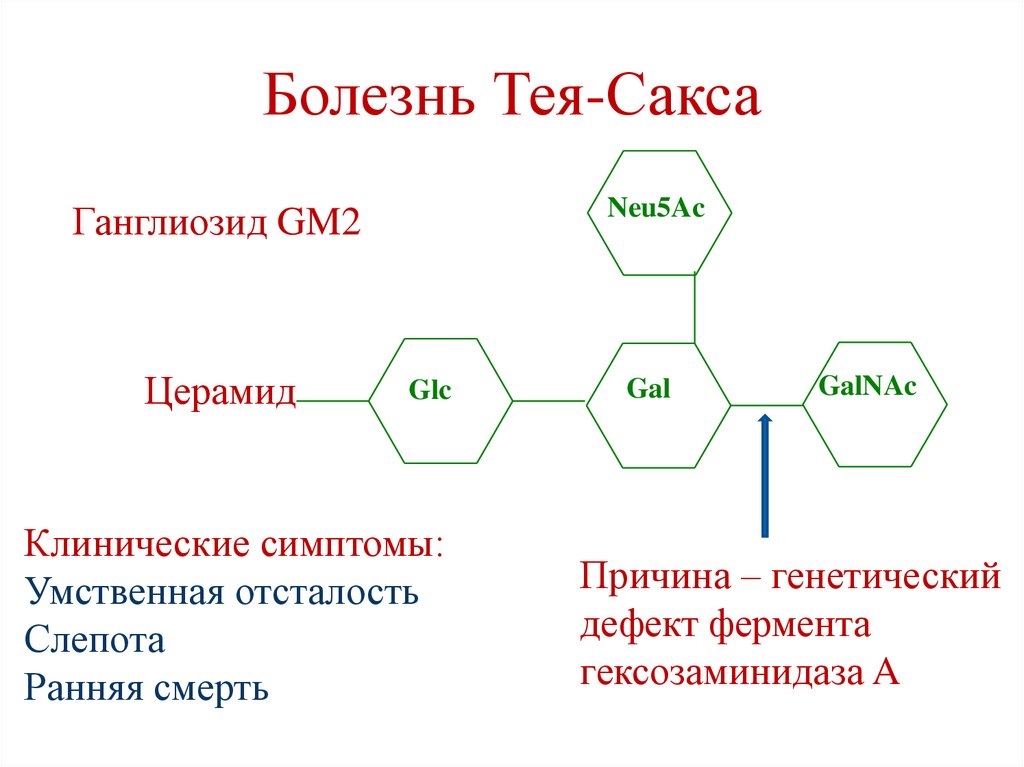
Болезнь Тея-СаксаNeu5Ac
Ганглиозид GM2
Церамид
Glc
Клинические симптомы:
Умственная отсталость
Слепота
Ранняя смерть
Gal
GalNAc
Причина – генетический
дефект фермента
гексозаминидаза A
155.
Регуляция липидного обмена• Адреналин, норадреналин и глюкагон
увеличивают скорость липолиза в жировой
ткани; в результате усиливается
мобилизация жирных кислот из жировых
депо и повышается содержание свободных
жирных кислот в плазме крови.
• Активация триглицеридлипазы
(фосфорилирование фермента).
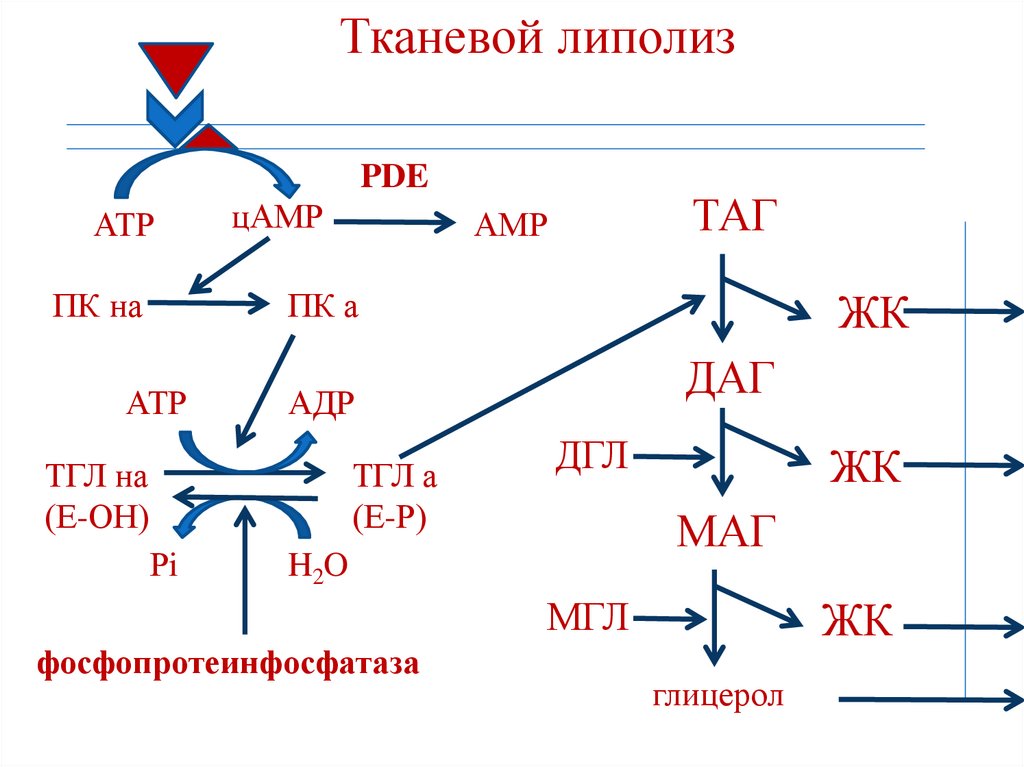
156.
Тканевой липолизАТР
ПК на
ПК а
АТР
ТГЛ на
(Е-ОН)
ТАГ
цАМР
ЖК
ДАГ
АДР
ТГЛ а
(Е-Р)
-гормон
(адреналин, глюкагон)
- рецептор
- аденилатциклаза
ДГЛ
ЖК
МАГ
МГЛ
ЖК
глицерол
157.
Регуляция липидного обмена• Инсулин оказывает противоположное
адреналину и глюкагону действие на
липолиз.
• Ингибирование триглицеридлипазы:
1. Активация фосфопротеинфосфатазы
(дефосфорилирование фермента).
2. Активация фосфодиэстеразы (PDE), что
приводит к снижению концентрации
цАМФ.
158.
Тканевой липолизPDE
АТР
ПК на
цАМР
ТАГ
АМР
ПК а
АТР
ДАГ
АДР
ТГЛ на
(Е-ОН)
ТГЛ а
(Е-Р)
Рi
ЖК
ДГЛ
ЖК
МАГ
H2O
МГЛ
фосфопротеинфосфатаза
ЖК
глицерол
159.
Регуляция липидного обменаИнсулин стимулирует липогенез:
• Активирует липопротеинлипазу
обеспечивает липогенез жирными
кислотами.
• Стимулирует гликолиз (Глюкоза
дигидроксиацетонфосфат глицерол-3фосфат).
• Активирует ацетил-СоА карбоксилазу.
160.
Регуляция липидного обмена• Глюкокортикоиды:
• Стимулируют липолиз в конечностях и
липогенез в других частях тела (лицо,
туловище).
• Усиливают липолитическое действие
катехоламинов и соматотропина.
• Индуцируют триглицеридлипазу.
• Стимулируют глицеронеогенез.
161.
Регуляция липидного обмена• Соматотропин:
• Усиливает липолиз в жировой ткани (за счет
усиления синтеза аденилатциклазы и
триглицеридлипазы).
• Стимулирует -окисление жирных кислот в
периферических тканях.
• Липотропины стимулируют липолиз.
162.
Регуляция липидного обмена• Тиреоидные гормоны:
• Повышают чувствительность адренорецепторов к действию адреналина и
косвенно стимулирует липолиз в жировой
ткани.
• Индуцируют синтез рецепторов ЛПНП.
• Активируют ГМГ-СоА редуктазу.
163.
Липопротеины плазмы крови.Дислипопротеинемии
164.
Липопротеины плазмы кровилипидно-белковые комплексы,
транспортные формы липидов.
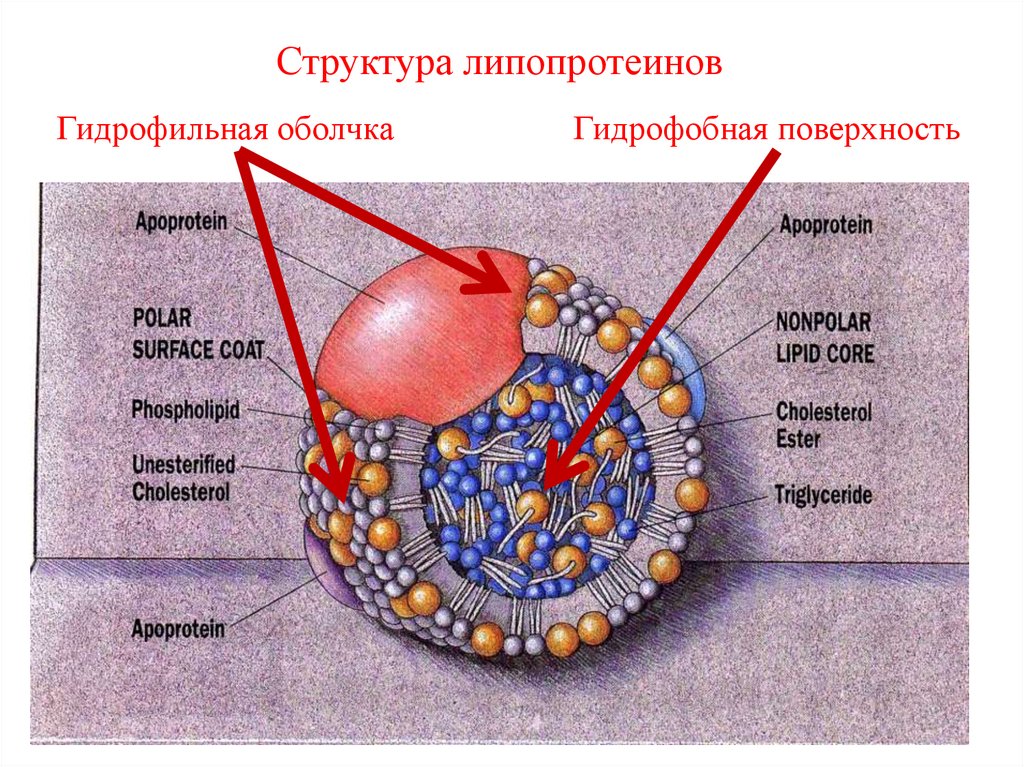
Все липопротеины имеют одинаковую
структуру:
• гидрофобное ядро (эфиры ХС и
триглицериды) и
• гидрофильная поверхность (фосфолипиды,
свободный ХС и специфические белки –
аполипопротеины).
165.
Структура липопротеиновГидрофильная оболчка
Гидрофобная поверхность
166.
Липопротеины различаются по содержаниюлипидов и апопротеинов, что определяет их
различную плотность и электрический
заряд.
Методы разделения липопротеинов:
• Ультрацентрифугирование (зависит от
плотности);
• Электрофорез (зависит от заряда).
167.
Разделение липопротеиновультрацентрифугированием
Хиломикроны (CM);
Липопротеины очень низкой
плотности - ЛПОНП
VLDL
VLDL
(VLDL – very low density
lipoproteins);
LDL
LDL
Липопротеины низкой
плотности - ЛПНП
(LDL – low density lipoproteins);HDLHDL
Липопротеины высокой
плотности - ЛПВП
(HDL – high density lipoproteins).
168.
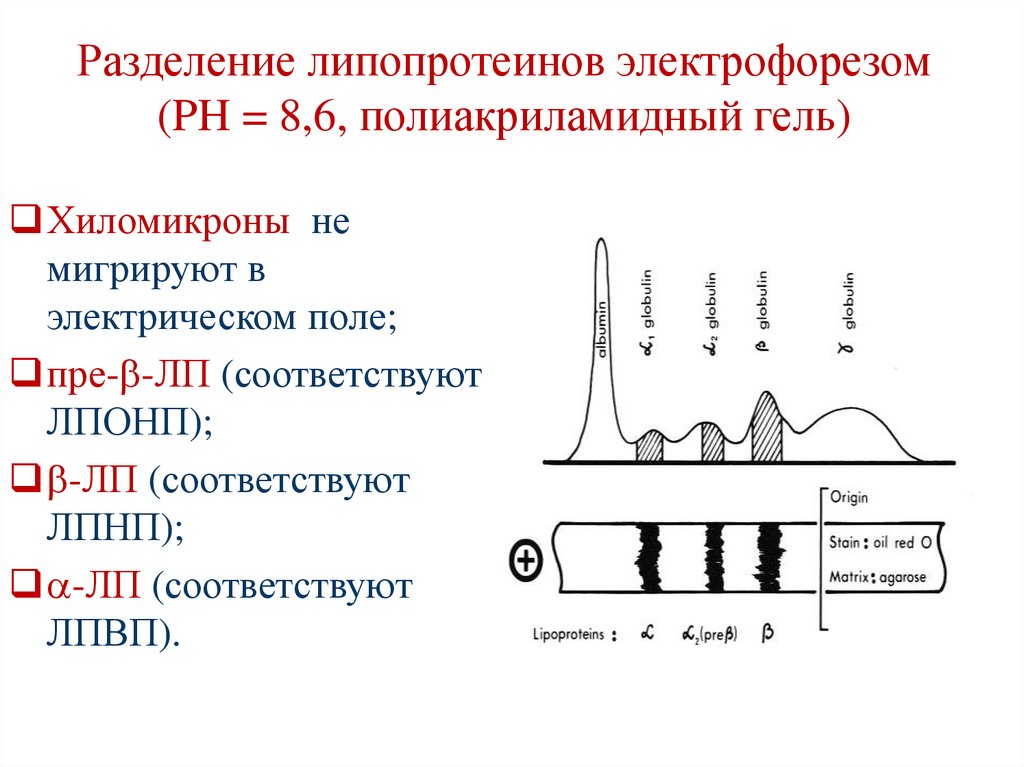
Разделение липопротеинов электрофорезом(PH = 8,6, полиакриламидный гель)
Хиломикроны не
мигрируют в
электрическом поле;
пре- -ЛП (соответствуют
ЛПОНП);
-ЛП (соответствуют
ЛПНП);
-ЛП (соответствуют
ЛПВП).
169.
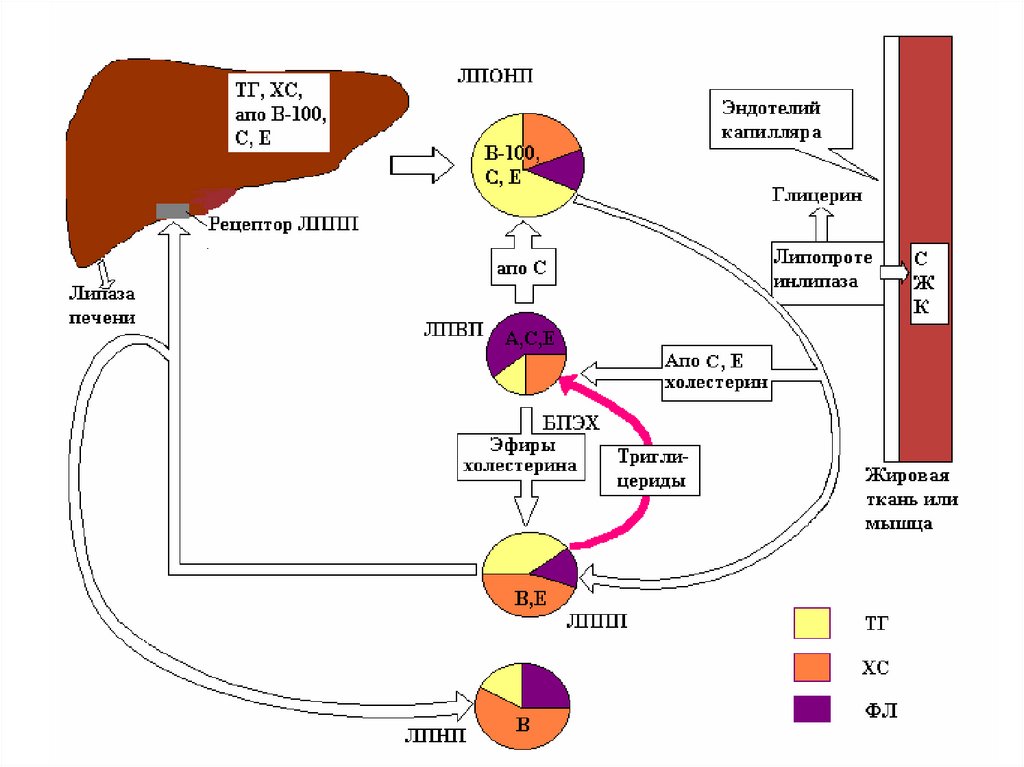
170.
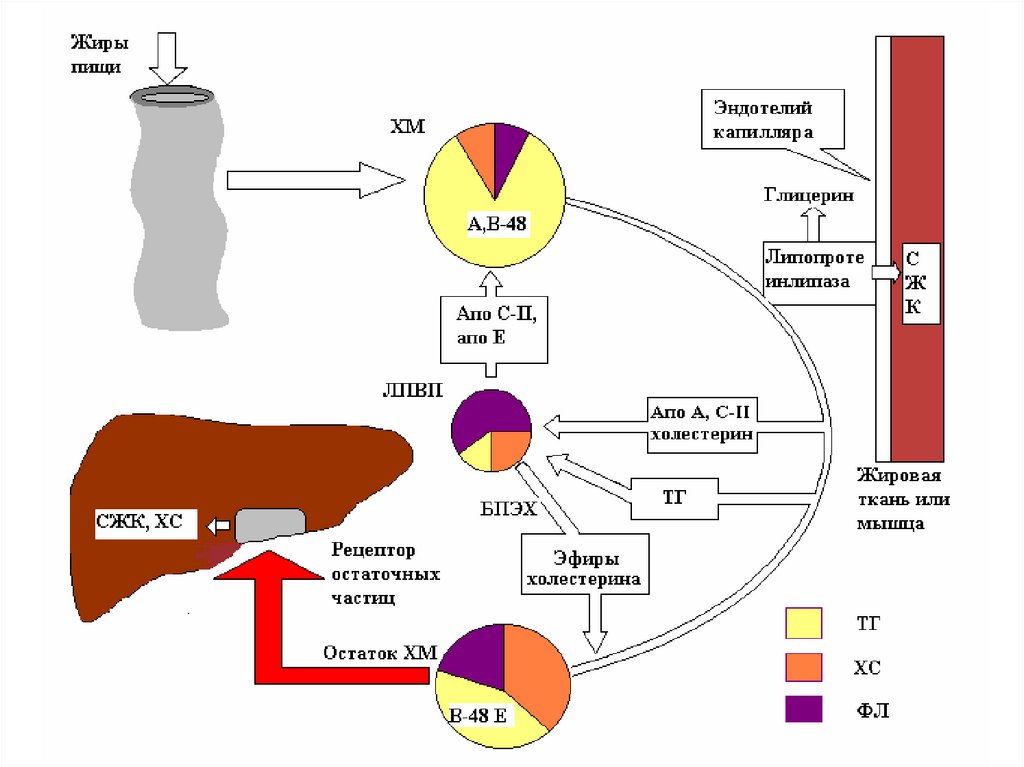
Обмен хиломикронов• образуются в эпителии кишечника;
• содержат много ТАГ (85%), содержат
апопротеин В-48 в качестве главного
структурного белка;
• транспортируют экзогенные (пищевые) жиры
из кишечника к периферическим тканям и
печени.
• Плазма крови здоровых людей, при взятии
крови натощак, не содержит хиломикронов.
171.
Обмен хиломикронов• после синтеза секретируются в лимфу и через
грудной проток попадают в кровь;
• в крови хиломикроны получают апопротеины
Е, С-I, C-II и C-III от ЛПВП;
• Катаболизм хиломикронов происходит под
действием фермента липопротеинлипаза
(ЛПЛ).
• ЛПЛ связанна с протеогликанами
эндотелиальных клеток (в скелетных
мышцах, миокарде, жировой ткани).
• ЛПЛ активируется апопротеином C-II.
172.
Обмен хиломикронов• ЛПЛ гидролизует ТАГ из хиломикронов.
• ЖК поступают в скелетные мышцы, миокард
(используются для энергии), в жировую ткань
(депонируются).
• После гидролиза ТАГ, хиломикроны
превращаются в остатки (ремнанты).
• Ремнанты хиломикронов захватываются
гепатоцитами, где происходит их распад.
173.
174.
Обмен ЛПОНП• Образуются в печени;
• Содержат много ТАГ (65%) и апоВ-100 в
качестве главного структурного белка.
• ЛПОНП являются транспортной формой
эндогенных триглицеридов.
• В пробах крови, взятых натощак, на долю
ЛПОНП приходится около 10–15% общего ХС
и практически все ТАГ крови.
175.
Обмен ЛПОНП• Катаболизм ЛПНП происходит под
действием фермента ЛПЛ (аналогично
хиломикронам).
• После гидролиза ТАГ, ЛПОНП
преобразуется в липопротеины
промежуточной плотности (ЛППП).
• Часть ЛППП удаляется из кровотока
печенью.
• Другая часть ЛППП подвергается
воздействию печеночной липазы, что ведет к
гидролизу оставшихся ТАГ с образованием
ЛПНП.
176.
177.
Обмен ЛПНП• Образуются в кровотоке из ЛПОНП.
• Являются основными переносчиками
эндогенного ХС к внепеченочным тканям
(транспортирует около 70% общего ХС
плазмы).
• ЛПНП имеют два потенциальных
метаболических исхода (регулируемый и
нерегулируемый пути).
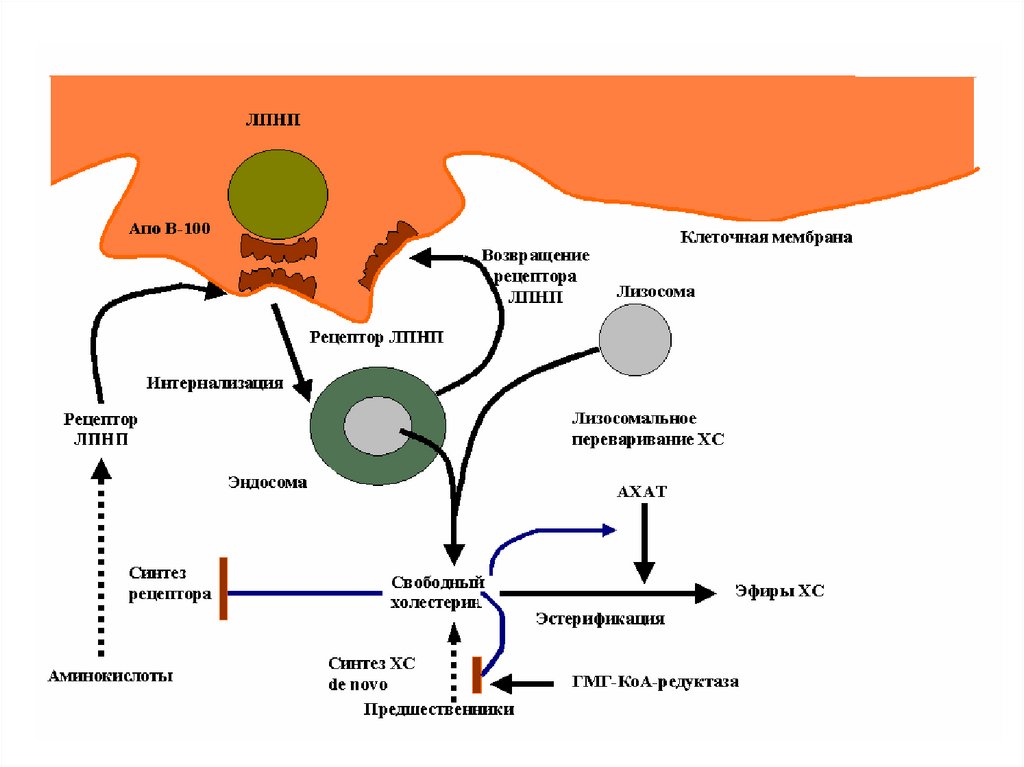
178.
Обмен ЛПНП• Регулируемый путь катаболизма – связывание с апо
В/Е-рецепторами печени, клеток надпочечников и
периферических клеток.
• После проникновения в клетку эндоцитозом, ЛПНП
подвергаются деградации с высвобождением
свободного ХС, который выполняет регуляторную
роль:
1. подавляет синтез рецепторов к ЛПНП;
2. ингибирует регуляторный фермент синтеза ХС
гидрокси-метил-глутарил-СоА-редуктазу;
3. активирует фермерт ацил-холестерол-ацилтрарсферазу (АХАТ) –депонирование эфиров ХС.
179.
180.
Обмен ЛПНП• Альтернативный путь (нерегулируемый) –
характерен для окисленных ЛПНП.
• Перекисно-модифицированные ЛПНП
распознаются и захватываются скэвенджеррецепторами макрофагов (в переводе с англ. –
мусорщик).
• Этот путь катаболизма ЛПНП не регулируется,
что приводит к превращению макрофагов в
переполненные эфирами ХС пенистые клетки –
компоненты жировых пятен, предшественники
атеросклеротической бляшки.
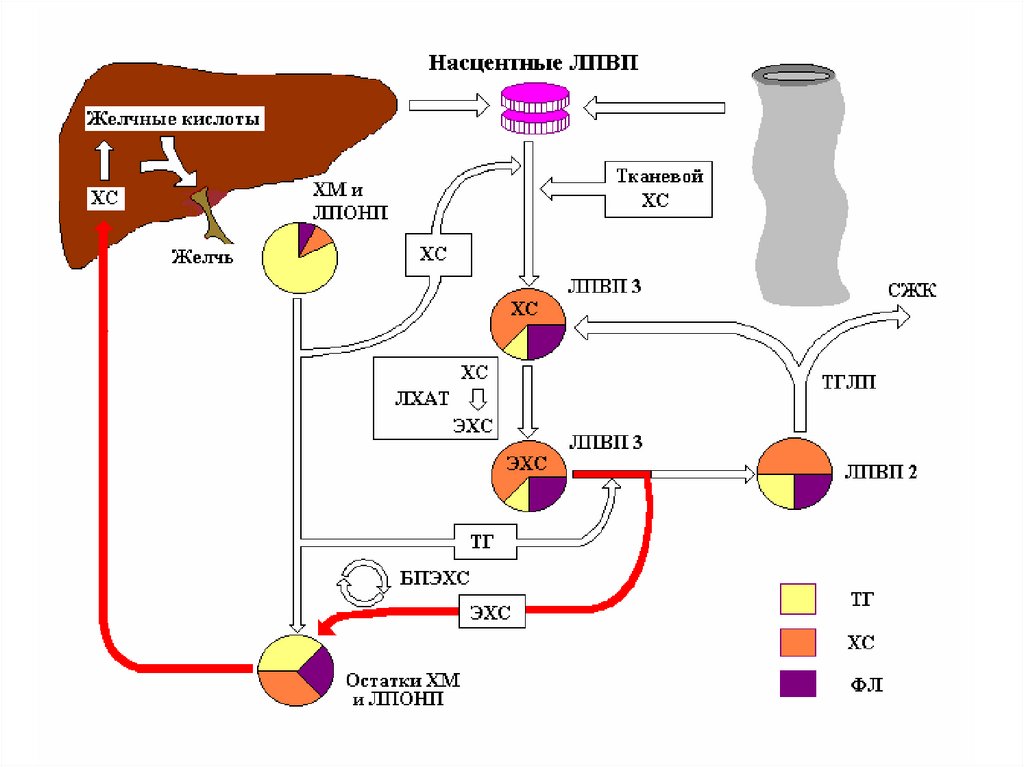
181.
Обмен ЛПВП• ЛПВП образуются в печени в виде незрелых
дисковидных частиц, состоящих из
фосфолипидов и апопротеинов А.
• Основная функция ЛПВП – транспорт ХС от
периферических тканей к печени.
• На долю ЛПВП приходится 20–30% общего
ХС крови, но содержат наибольшее
количество фосфолипидов и белка.
182.
Обмен ЛПВП• ЛПВП – хорошие акцепторы свободного ХС из
периферических тканей.
• Свободный ХС из клеточных мембран
поступает на поверхность ЛПВП.
• На поверхности ЛПВП, ХС эстерифицируется
под действием фермента лецитин-холестеролацил-трансфераза (ЛХАТ).
• Активатором ЛХАТ является апо А-1,
структурный белок ЛПВП.
183.
Обмен ЛПВП• Эфиры ХС перемещаются с поверхности
частиц ЛПВП в гидрофобное ядро,
освобождая таким образом дополнительную
поверхность для свободного ХС.
• По мере накопления в ядре эфиров ХС,
дисковидные частицы преобразуются в
сферические, богатые холестерином ЛПВП.
• Эфиры ХС из ЛПВП захватываются
гепатоцитами.
• В печени ХС превращается в желчные
кислоты (конечный продукт обмена ХС),
которые выделяются с желчью в кишечник.
184.
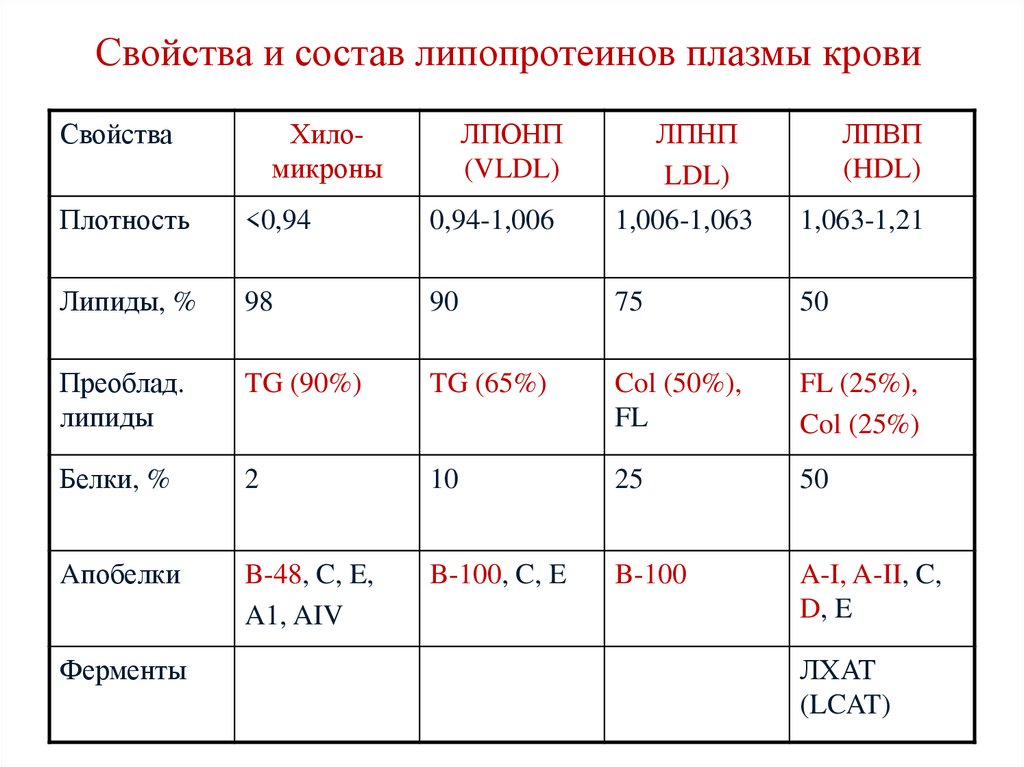
185.
Свойства и состав липопротеинов плазмы кровиСвойства
Хиломикроны
ЛПОНП
(VLDL)
ЛПНП
LDL)
ЛПВП
(HDL)
Плотность
<0,94
0,94-1,006
1,006-1,063
1,063-1,21
Липиды, %
98
90
75
50
Преоблад.
липиды
TG (90%)
TG (65%)
Col (50%),
FL
FL (25%),
Col (25%)
Белки, %
2
10
25
50
Aпобелки
B-48, C, E,
A1, AIV
B-100, C, E
B-100
A-I, A-II, C,
D, E
Ферменты
ЛХАТ
(LCAT)
186.
187.
Концентрация холестерина• Нормальный уровень –
менее 5,2 ммоль/л
• Пограничный уровень –
5,2-6,2 ммоль/л
• Высокий уровень –
более 6,2 ммоль/л
188.
ХОЛЕСТЕРИН ЛПНП• Формула Friedwald:
• ХС ЛПНП, ммоль/л=Общий ХС – ХС ЛПВП – (0,45 хТАГ)
• ХС ЛПНП, мг/дл=Общий ХС – ХС ЛПВП – (0,2 хТАГ)
• Рекомендуемый уровень –
менее 3,37 ммоль/л
• Средний риск ИБС –
3,37-4,12 ммоль/л
• Высокий риск ИБС –
более 4,14 ммоль/л
189.
ХОЛЕСТЕРИН ЛПВП• Нормальная
концентрация:
• Мужчины –
0,9-1,4 mmol/L;
• Женщины –
1,2-1,7 mmol/L.
190.
Концентрация триглицеридовНормальная
Допустимая
Умеренно повышенная
Высокая
<1,6 mmol/L
1,6- 2,2 mmol/L
2,2-2,8 mmol/L
>2,8 mmol/L
191.
Дислипопротеинемии• Нарушения образования, транспорта и
утилизации ЛП, сопровождаемые
изменением плазменного уровня липидов.
Делятся на гипер- и гиполипопортеидемии.
• И гипер- и гиполипопортеидемии делятся
на первичные (наследственные, семейные)
и вторичные (приобретенные).
192.
Первичные гиперлипопортеидемииГЛП I типа. Семейная гиперхиломикронемия.
ГЛП II а типа. Семейная гипер-беталипопротеинемия. Семейная гиперхолестеролемия.
ГЛП II в типа. Семейная гипер-бета и гипер-пре-беталипопротеинемия.
ГЛП III типа. Семейная дис-бета-липопротеинемия.
Болезнь широкой полосы.
ГЛП IV типа. Семейная гипер-пре-беталипопротеинемия.
ГЛП V типа. Семейная гиперхиломикронемия и
гипер-пре-бета-липопротеинемия
193.
ГЛП I типа.Семейная гиперхиломикронемия
• Генетический дефект липопротеидлипазы
или апобелка СII.
• Нарушение катаболизма хиломикронов.
• Повышение содержания хиломикронов в
плазме крови, взятой натощак.
• Содержание триглицеридов в крови резко
увеличено.
• Боли в животе, эруптивные ксантомы,
панкреатит, но риск ИБС не увеличивается.
194.
ГЛП II типа.Семейная гиперхолестеролемия.
• Мутация гена ЛПНП-рецептора или апо
В100.
• Частота гетерозиготных форм – 1 на 500.
• Умеренное повышение уровня холестерина.
• Ксантомы сухожилий.
• Липоидная дуга роговицы.
• Преждевременно развивается ИБС.
195.
ГЛП II а типа.Семейная гиперхолестеролемия.
• Гомозиготные формы (1 на 1 000 000)
• Уровень ХС ˃15,5 ммоль/л
• Плоские и эруптивные ксантомы
сухожилий.
• Выраженный и ранний атеросклероз.
• Ранняя форма коронарной недостаточности,
инфаркты, инсульты, ранняя смерть.
196.
Первичные гиполипопортеидемии• Абеталипопротеинемия
• Гипобеталипопротеинемия
• Анальфалипопротеинемия
• Семейная наследственная недостаточность
ЛХАТ
197.
Aн-альфа-липопротеинемия(болезнь Тангера)
Мутация гена транспортного белка ABCA-1
(ATP-binding cassette transporter) – участвует в
переносе холестерола из клеток на поверхность
ЛПВП.
Уменьшение концентрации ЛПВП.
Накопление эфиров холестерола в ретикулоэндотелиальных клетках.
• Клиническая картина:
Гипертрофия миндалин.
Гепатоспленомегалия.
Увеличение лимфатических узлов.
Полинейропатия.
Атеросклероз.
198.
Дислипидемия при сахарном диабете• “липидная триада”:
• гипертриглицеридемия;
• низкий уровнем ХС ЛПВП;
• увеличение количества мелких частиц ЛПНП
(они больше подвержены окислению и
гликолизированию и способствуют развитию
дисфункции эндотелия, что является одной из
причин повышенного риска ИБС у больных
диабетом).
199.
АтеросклерозХроническое прогрессирующее заболевание
крупных и средних эластических и мышечноэластических артерий, характеризующееся
формированием в интиме атером (фибрознолипидных бляшек). Прогрессирование атером
приводит к осложнениям (изъязвление,
кальциноз, тромбоз и эмболия, аневризмы,
кровотечения).
200.
Главные факторыриска развития атеросклероза
• Дислипопротеинемии
(как наследственные, так и приобретенные).
• Гипертензия
(особенно у лиц старше 50 лет).
• Курение.
• Сахарный диабет
(особенно инсулиннезависимый тип).
• Принадлежность к мужскому полу
(кроме возрастных групп после 75 лет).
201.
«Мягкие» факторыриска развития атеросклероза
• Ожирение (особенно абдоминального типа).
• Гиподинамия.
• Хронический стресс.
• Соревновательно-стрессорный тип
жизнедеятельности.
• Гиперурикемия.
• Гипергомоцистеинеми.я
• Фолациновый гиповитаминоз.
• Гипервитаминоз Д.
• Использование пероральных противозачаточных
средств.
202.
Атерогенная дислипидемия• Увеличение концентрации общего
холестерина.
• Повышение содержания ХС ЛПНП
(особенно мелких частиц ЛПНП и
химически модифицированных).
• Низкий уровень ХС ЛПВП.
• Гипертриглицеридемия.
• Повышение концентрации ЛП(а).
203.
Роль ЛПНП в атерогенезе• Перекисно-модифицированные ЛПНП
распознаются и захватываются скэвенджеррецепторами макрофагов (в переводе с англ. –
мусорщик).
• Этот путь катаболизма ЛПНП не регулируется,
что приводит к превращению макрофагов в
переполненные эфирами ХС пенистые клетки
– компоненты жировых пятен.
• Последние являются предшественниками
атеросклеротической бляшки.
204.
OжирениеИМТ
18,5-24,9
25,0-29,9
30,0-34,9
35,0-39,9
>40,0
Норма
Избыточный вес
Ожирение I ст.
Ожирение II ст.
ОжирениеIII ст.
ИМТ (индекс массы тела)
ИМТ = вес(kg)/квадрат роста(m2)
205.
Факторы риска ожиренияГенетические дефекты (лептин, рецептор
лептина, 3-адренергический рецептор,
IRS-1).
Алиментарные факторы (гиперкалорийность,
высокое содержание углеводов, липидов).
Употребление алкоголя.
Малоподвижный образ жизни.
Стресс.
206.
Факторы риска ожиренияФизиологические факторы
(беременность, лактация).
Эндокринные заболевания (гипотиреоз,
болезнь Кушинга).
Лекарства (кортикостероиды,
пероральные противозачаточные
средства, инсулин).


































































































































 chemistry
chemistry