Similar presentations:
Электролитическая диссоциация. 9 класс
1.
Электролитическаядиссоциация
25.01.2023
1
2.
Проверка электропроводности раствора:Электропроводность
раствора
хлорида
натрия (NaCl)
NaCl
Начать
Закончить
- электролит
Электропроводность
раствора сахара
сахар
Начать
Закончить
- неэлектролит
2
3. Вещества (составить схему стр. 26)
• Название группывеществ
• примеры
• Название группы
веществ
• примеры
3
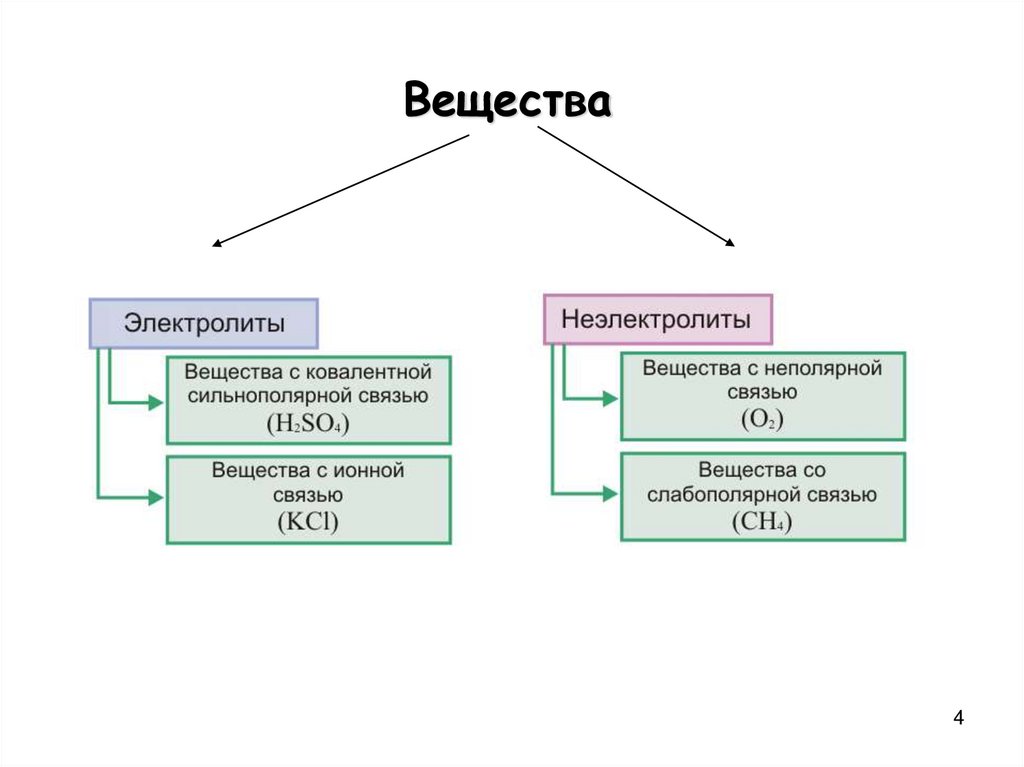
4.
Вещества4
5.
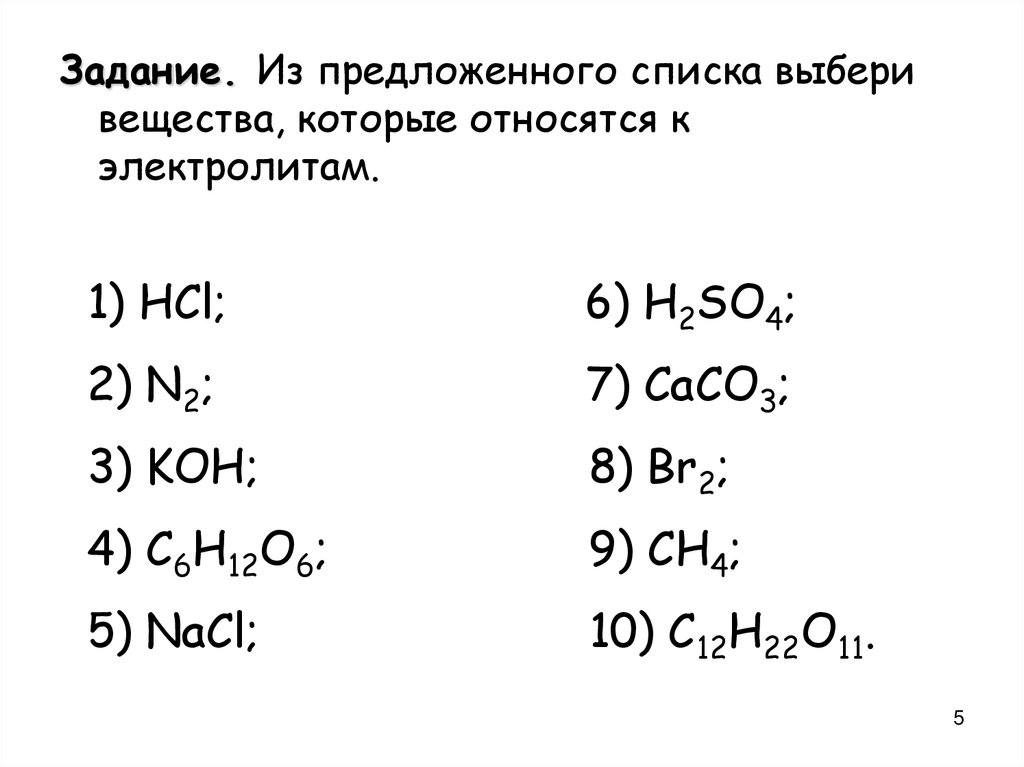
Задание. Из предложенного списка выберивещества, которые относятся к
электролитам.
1) HCl;
6) H2SO4;
2) N2;
7) CaCO3;
3) KOH;
8) Br2;
4) C6H12O6;
9) CH4;
5) NaCl;
10) C12H22O11.
5
6.
Электролитическая диссоциация (написать определение - низ стр. 26, вверх стр.27)Свант е Август
Аррениус
1859-1927гг.
Шведский физико-химик,
создатель теории
электролитической
диссоциации.
6
7.
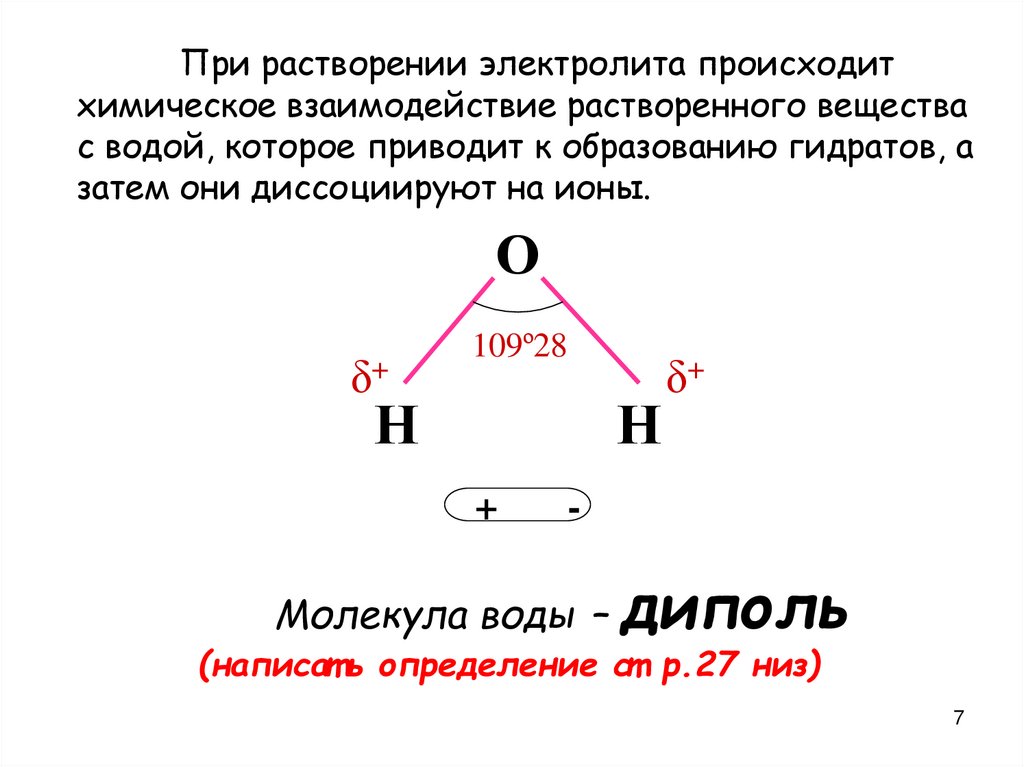
При растворении электролита происходитхимическое взаимодействие растворенного вещества
с водой, которое приводит к образованию гидратов, а
затем они диссоциируют на ионы.
О
δ+
109º28
Н
Н
+
δ+
-
Молекула воды – диполь
(написат ь определение ст р.27 низ)
7
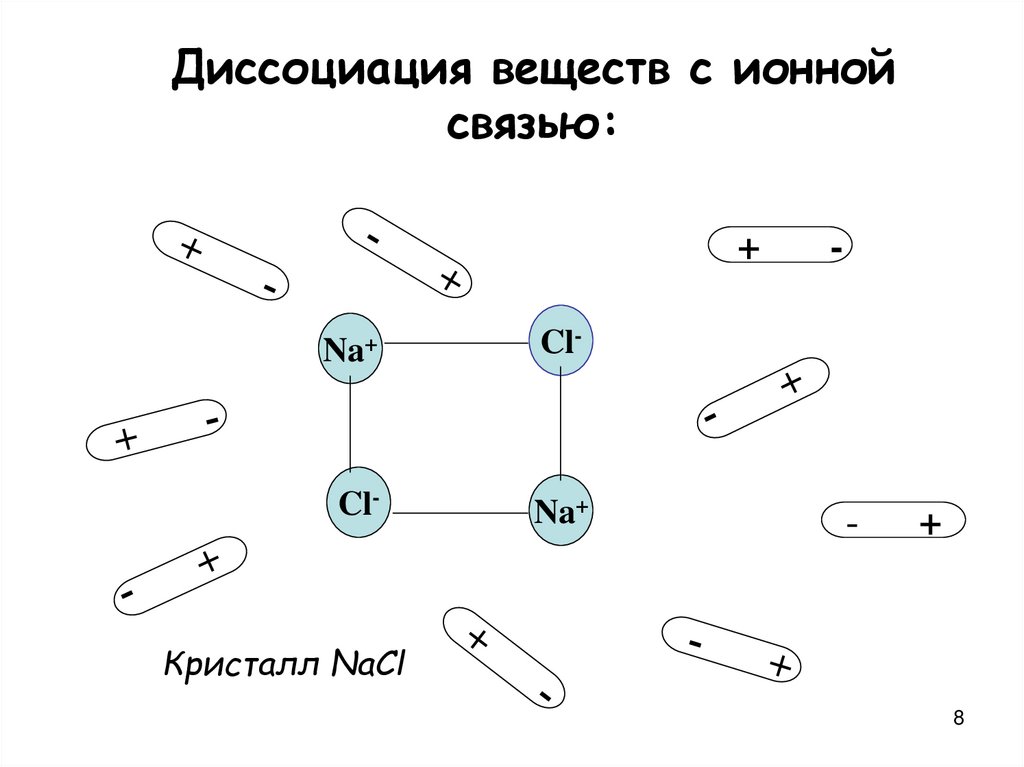
8.
Диссоциация веществ с ионнойсвязью:
+
Na+
Cl-
Cl-
Na+
-
-
+
Кристалл NaCl
8
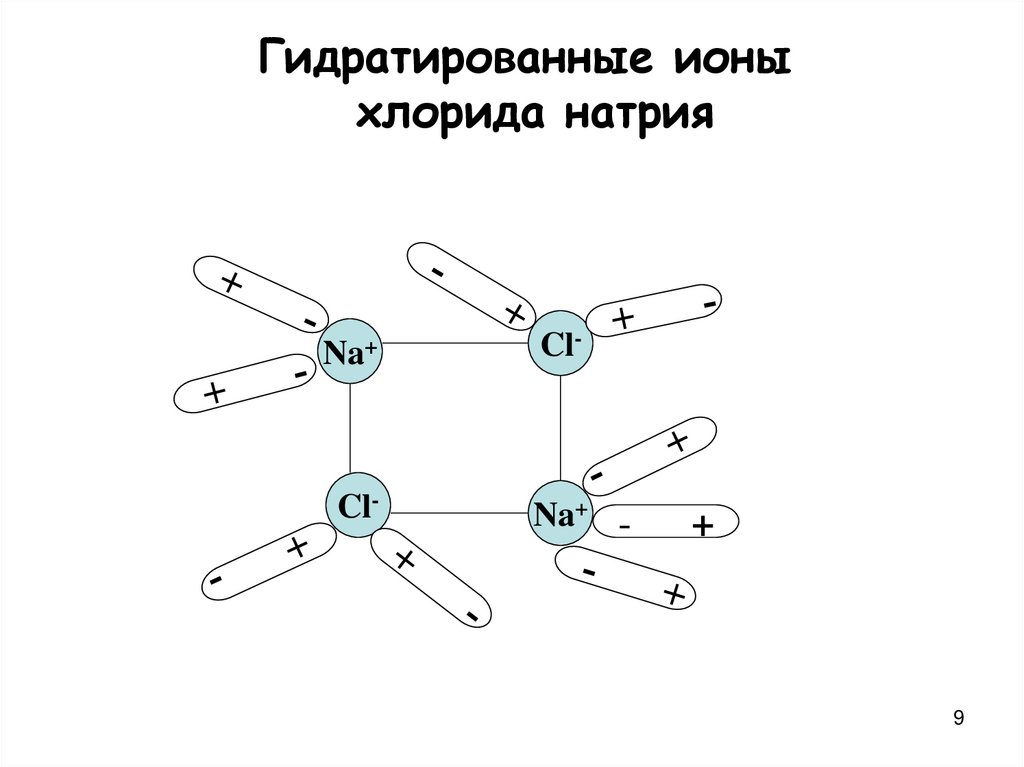
9. Гидратированные ионы хлорида натрия
Na+Cl-
Cl-
Na+ -
+
9
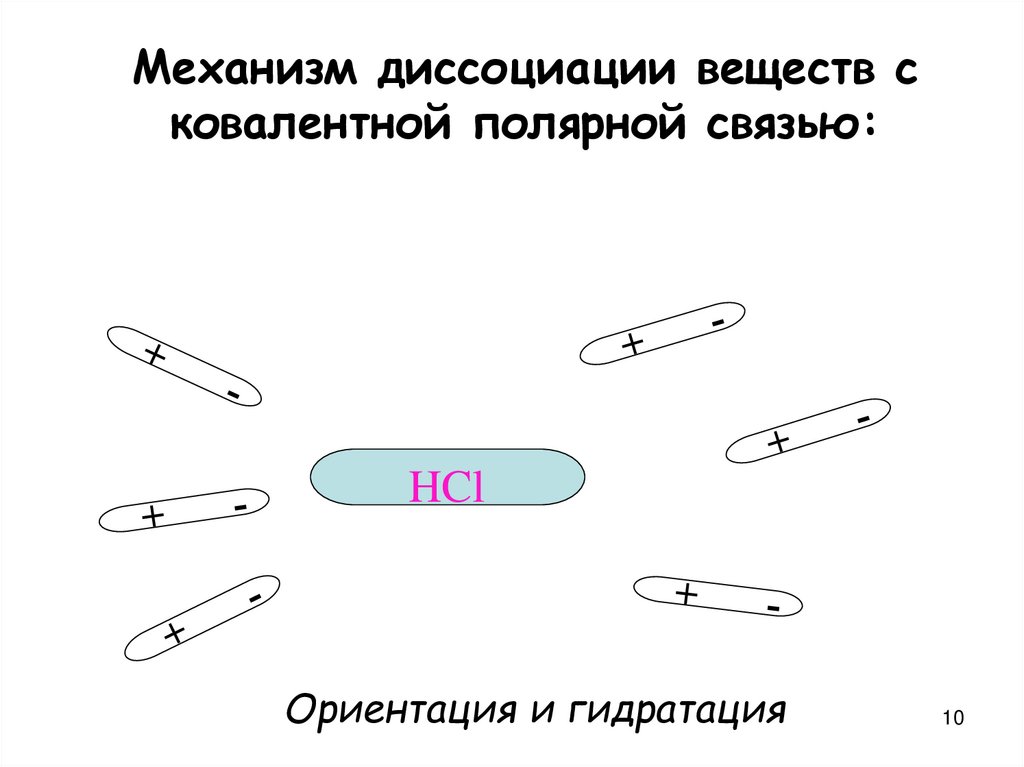
10. Механизм диссоциации веществ с ковалентной полярной связью:
HClОриентация и гидратация
10
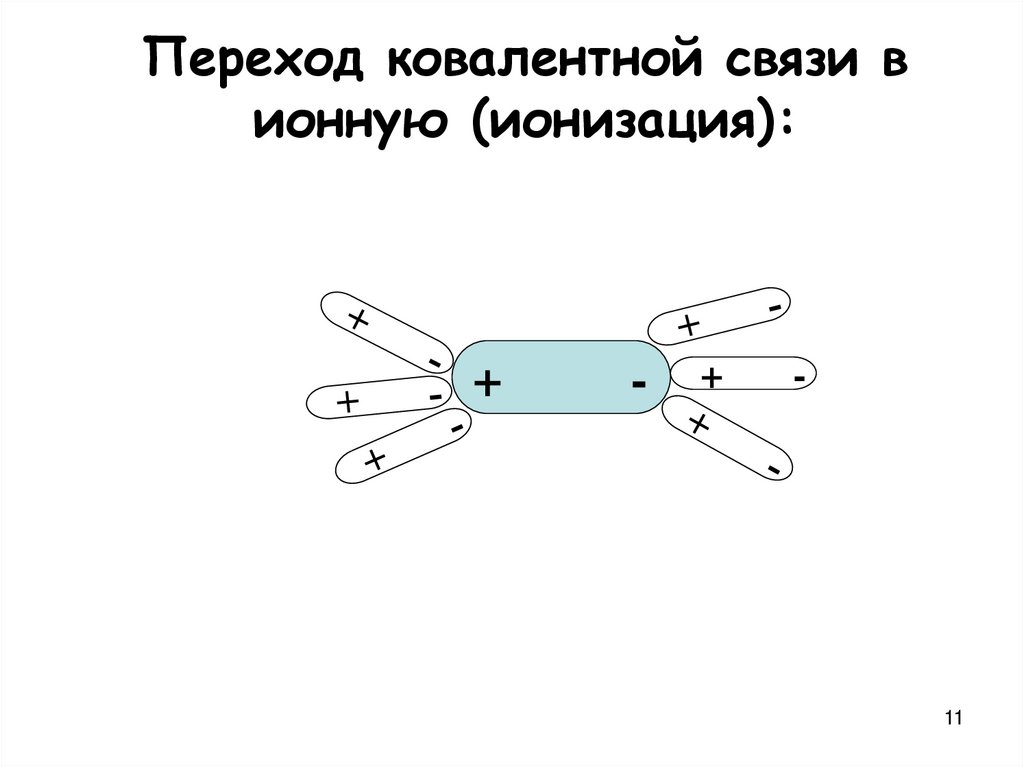
11.
Переход ковалентной связи вионную (ионизация):
+
-
+
-
11
12.
Диссоциация веществ сковалентной полярной связью:
H+ ClГидратированные
ионы
25.01.2023
12
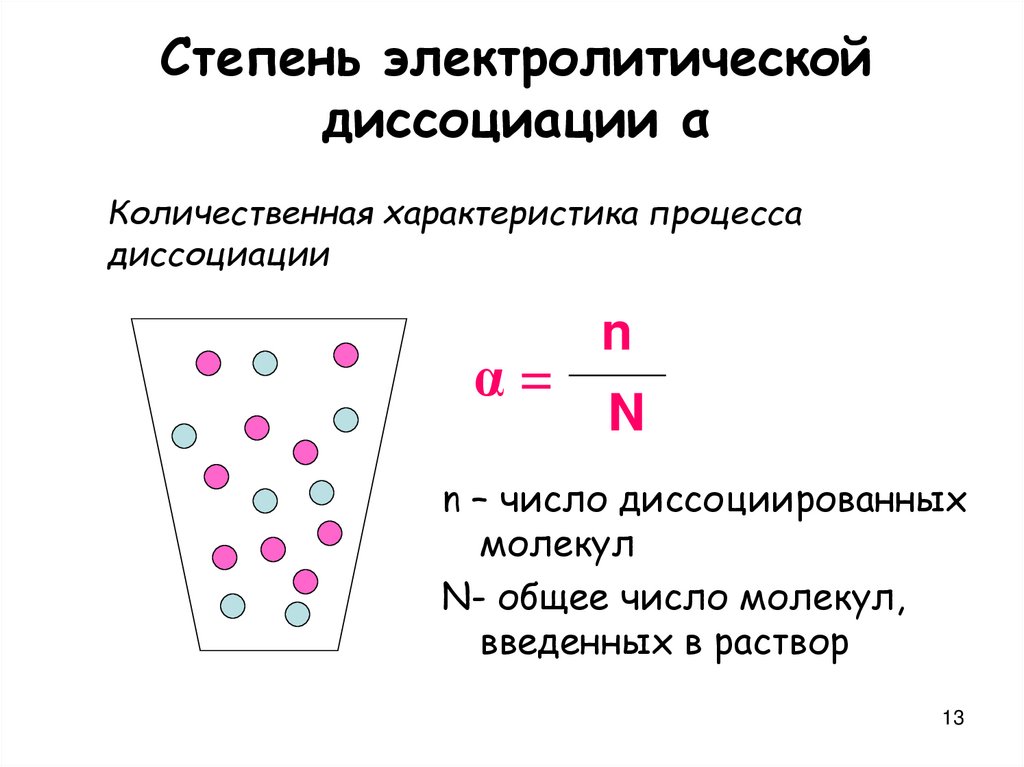
13.
Степень электролитическойдиссоциации α
Количественная характеристика процесса
диссоциации
α=
n
N
n – число диссоциированных
молекул
N- общее число молекул,
введенных в раствор
13
14.
ЭлектролитыСильные
α>30%
Выписать
примеры
стр. 29
Средние
30%>α>3%
Mg(OH)2,
H2SO3, HNO2,
H3PO4
Слабые
α<3%
Выписать
примеры
стр. 29
14
15.
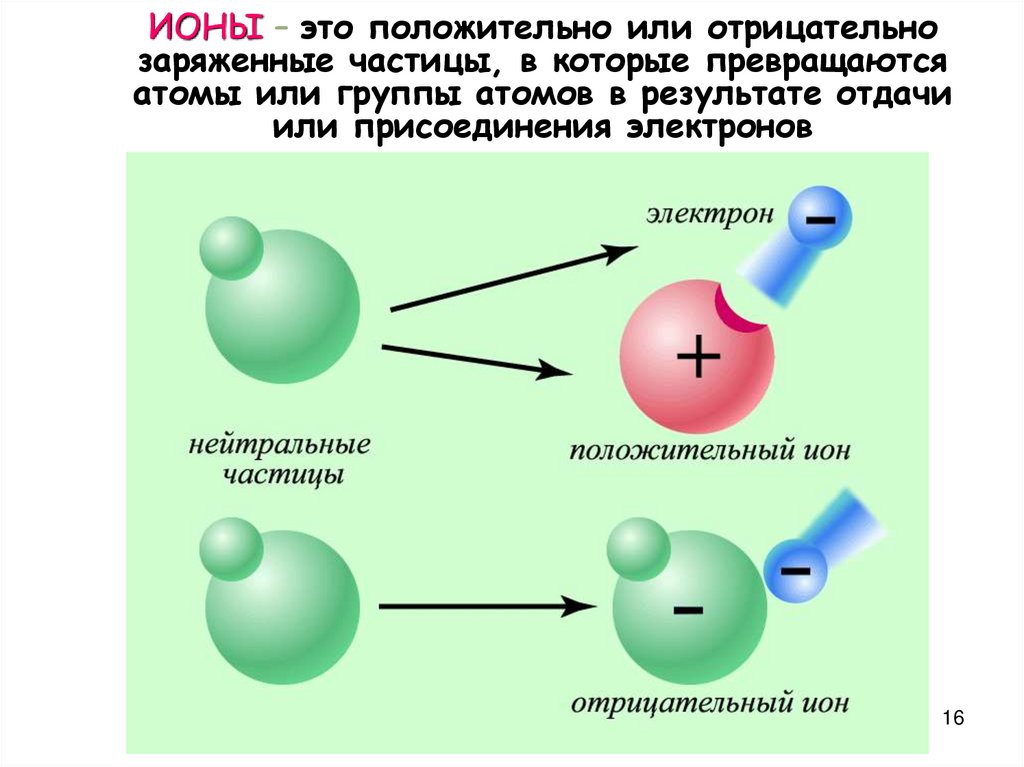
1516. ИОНЫ – это положительно или отрицательно заряженные частицы, в которые превращаются атомы или группы атомов в результате отдачи
или присоединения электронов16
17. Кислоты - это сложные вещества, при диссоциации которых в водных растворах в качестве катионов отщепляются только ионы
Диссоциация кислотКислоты - это сложные вещества, при
диссоциации которых в водных растворах в
качестве катионов отщепляются только ионы
водорода.
+
Н
НCl → …. + Cl –
Н2SO4 → 2 … + SO4 2Н2 CO3
2 … + CO3 2-
17
18. Основания - это сложные вещества, при диссоциации которых в водных растворах в качестве анионов отщепляются только
Диссоциация основанийОснования - это сложные вещества, при
диссоциации которых в водных растворах в
качестве анионов отщепляются только
гидроксид-ионы.
-
+
ОН
KOH → K + …
2+
Ca(OH)2
Ca + 2 …
3+
Al(OH)3
Al + 3 …
18
19. Диссоциация солей Соли -это сложные вещества, которые в водных растворах диссоциируют на катионы металла и анионы кислотного
остатка.NaCl → Na + + СlK2SO4 → 2 K + + SO4 23+
Al(NO3)3 → Al
+ 3NO3 -
n+
Me
25.01.2023
+ (кислотный остаток)
в19
20.
Задание.Напишите уравнение диссоциации веществ.
1. KNO3
2. Mg(NO3)2
3. Ba(OH)2
4. HCl
5. Na2SO4
6. NaOH
7. Fe2(SO4)3
Для слабых электролитов диссоциация обратима!20
21. Характерные симптомы дефицита химических элементов в организме человека
2122.
• Что называют электролитическойдиссоциацией?
• Какие вещества называют электролитами?
Какие вещества к ним относятся? Какой тип
химической связи для них характерен?
• Какие вещества называют
неэлектролитами? Какие вещества к ним
относятся? Какой тип химической связи для
них характерен?
• Каков механизм ЭД при растворении в воде
веществ с ионной и ковалентной полярной
связями?
25.01.2023
22
23.
Задание. Пользуясь таблицейрастворимости, определите, водные
растворы каких веществ будут
диссоциировать на ионы:
КСl, CuO, CuSO4,Cu(OН)2,
NaNO3, K2SO4, BaCl2, BaSO4,
AgNO3, AlCl3, FeCl3, NaOH,
О2.
25.01.2023
23
24.
Домашнее задание:§ 4,5; письменное задание
25.01.2023
24





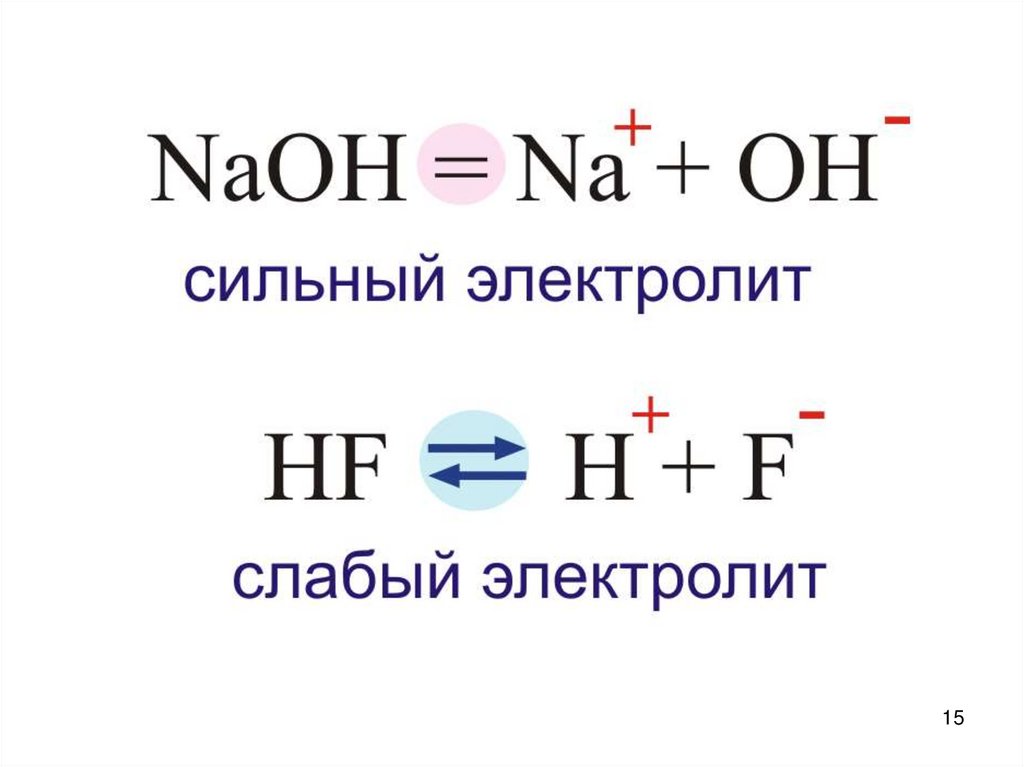








 chemistry
chemistry








