Similar presentations:
Karbonskābes. Kas ir karbonskābes?
1. Karbonskābes
12.klase2. 1.Kas ir karbonskābes?
• Karbonskābes ir ogļūdeņražu atvasinājumi,kuru molekulās ogļūdeņraža atlikums saistīts
ar karboksilgrupu.
3. 2. Funkcionālā grupa
4. 3.Karbonskābju iedalījums un nomenklatūra
1. tabulaPēc ogļūdeņraža atlikuma
Piesātinātās
Pēc karboksilgrupu skaita
Nepiesātinātās Aromātiskās Vienvērtīgās
Vairākvērtīgās
5. 4. Karbonskābju nosaukumi
Pēc IUPAC nomenklatūras karbonskābes oglekļa atomu skaitam atbilstošajamogļūdeņraža nosaukumam pievieno vārdu skābe. Taču ļoti daudzu karbonskābju
nosaukumi veidojušies vēsturiski.
6.
FormulaIUPAC nosaukums
Triviālais nosaukums
HCOOH
metānskābe
skudrskābe
CH3COOH
etānskābe
etiķskābe
CH3CH2COOH
propānskābe
propionskābe
CH3CH2CH2COOH
butānskābe
sviestskābe
CH3(CH2)3COOH
pentānskābe
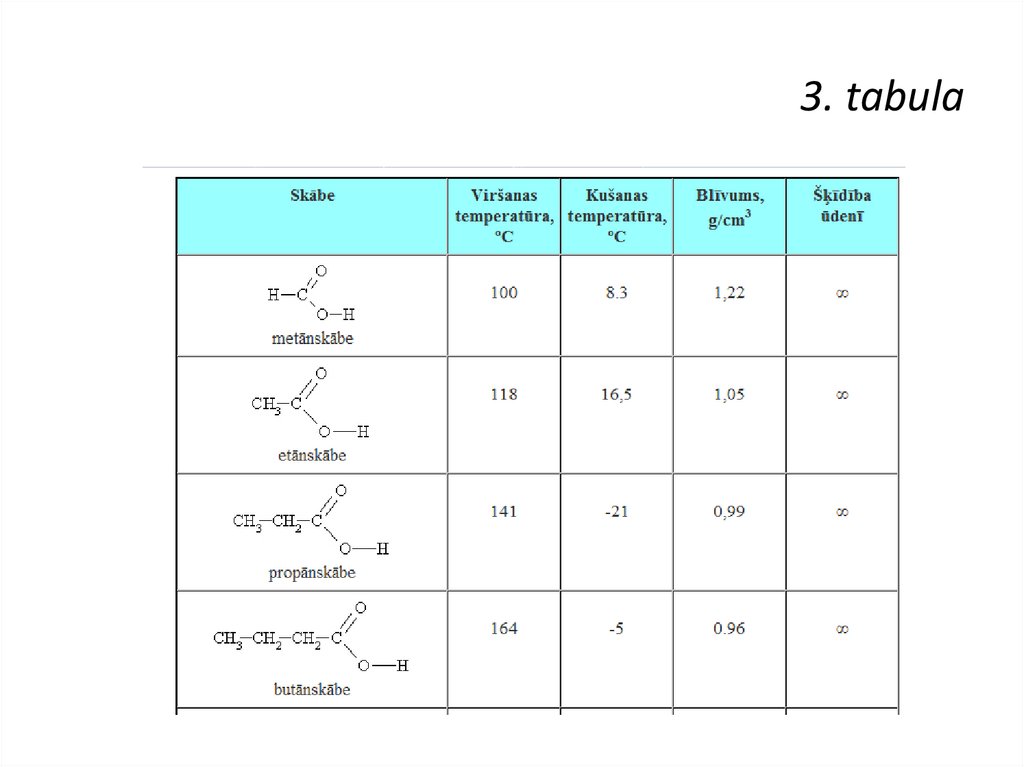
Skābes apraksts
Skudrskābe pirmo reizi iegūta jau 17. gs.,
destilējot sarkanās skudras ar ūdens tvaiku.
(dzērvenēs, brūklenēs)
Etiķskābe jeb „vīna etiķis” – šis vārds
atvasināts no sena franču vārda „vin aigre”,
kas nozīmē „skābais vīns”. 100% etiķskābi
sauc arī par ledus etiķskābi. 60–70%
etiķskābes šķīdumu sauc par etiķa esenci,
5–9% – par galda etiķi, 3–6% pārtikas
etiķi sauc arī par vīna etiķi.
Uz cilvēka ādas un -sviedru dziedzeros var
dzīvot baktērijās (izsitumus, pinnes).
Atrodas esteru veidā vecā sviestā, sieros
CH3(CH2)14COOH heksadekānskābe
baldriānskābe Baldriānskābe dabā sastopama baldriāna
saknēs.
palmitīnskābe
Palmitīnskābe dabā sastopama glicerīna
esteru veidā taukos. Ļoti daudz
palmitīnskābes ir cūku un liellopu tauku
sastāvā esošajos esteros.
7.
CH3(CH2)16COOHoktadekānskābe
CH3(CH2)7CH=CH(CH2)7COOH
stearīnskābe
Mīkstina ādu, taukveida viela
oleīnskābe
Oleīnskābe dabā sastopama glicerīna esteru
veidā augu eļļās, piemēram, olīveļļa satur 70–
85% glicerīna trioleāta.
9-oktadecēnskābe
C6H5COOH
HOOC-COOH
benzolkarbonskābe benzoskābe
etāndiskābe
Benzoskābe pirmoreiz iegūta no dabas
produktiem – benzosveķiem.
Skābeņskābe dabā sastopama daudzos
skābeņskābe augos (skābenēs, rabarberos,
zaķkāpostos) skābo sāļu veidā (K, Ca
sāļi). Dažu vielmaiņas procesu
traucējumu gadījumos tā sastopama arī
cilvēka urīnā.
8. 5. Karbonskābju fizikālās īpašības
Karbonskābju fizikālās īpašības atkarīgas nooglekļa atomu skaita molekulā:
• C1–C3 – šķidrumi ar kodīgu smaržu;
• C4– C8 – smarža kļūst arvien nepatīkamāka;
• C9 – C18 – kristāliskas vielas ar vāju smaržu.
9.
3. tabula10. Uzdevumi
11.
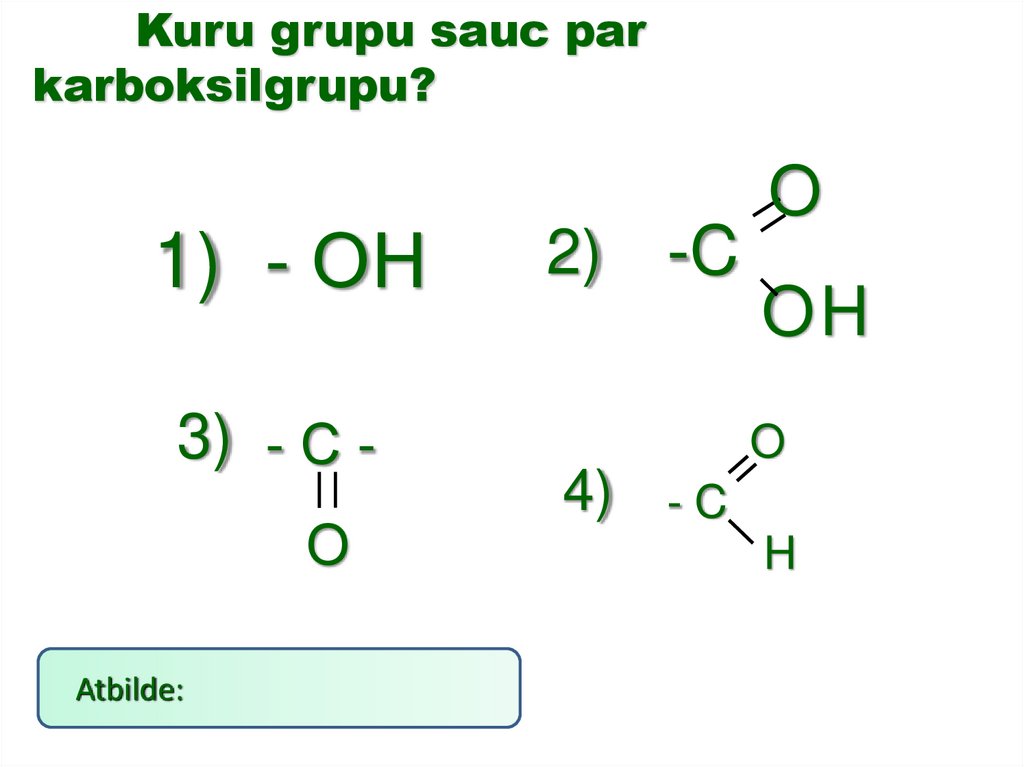
Kuru grupu sauc parkarboksilgrupu?
1) - ОН
3) - С О
Atbilde:
2)
-C
O
OH
O
4) - C
H
12.
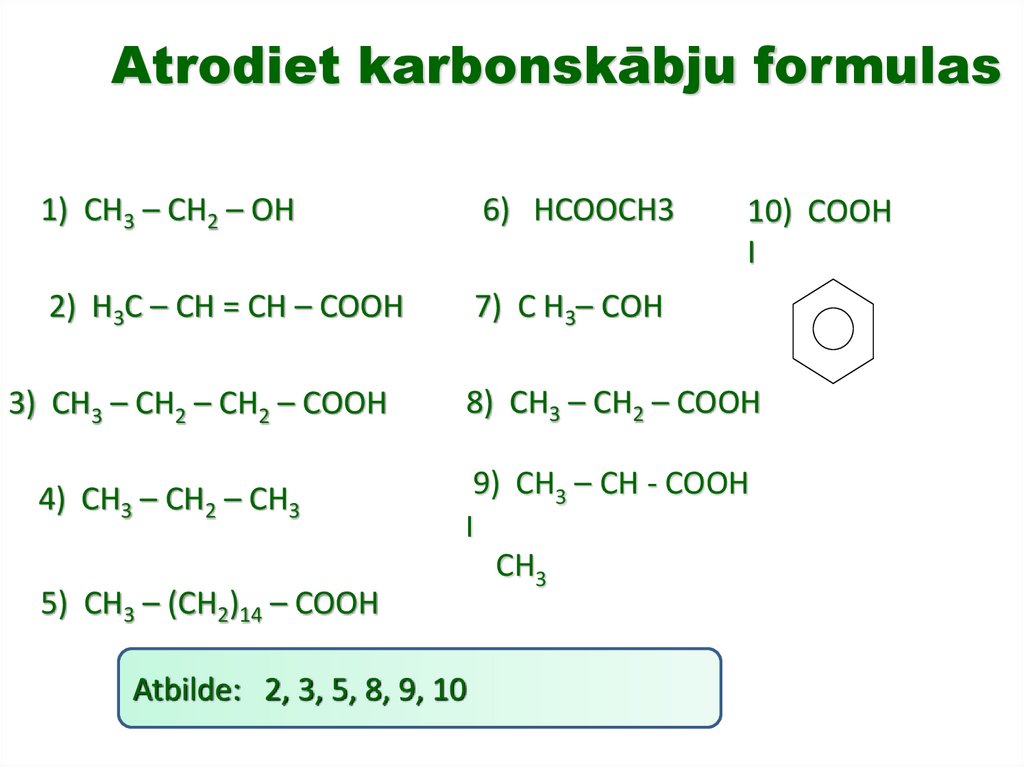
Atrodiet karbonskābju formulas1) CH3 – CH2 – OH
6) HCOOСH3
2) H3C – CH = CH – COOH
7) С Н3– СОН
3) CH3 – CH2 – CH2 – COOH
4) CH3 – CH2 – CH3
5) CH3 – (CH2)14 – COOH
10) COOH
I
8) CH3 – CH2 – COOH
9) CH3 – CH - COOH
׀
CH3
Atbilde: 2, 3, 5, 8, 9, 10
13.
Triviālie nosaukumi1) HCOOH
Skudrskābe
2) CH3 – CH2 – COOH
Propionskābe
3) C17H35 – COOH
Stearīnskābe
4) С Н3– СООН
Etiķskābe
5) CH3 – CH2 – CH2 – CH2 – COOH
Baldriānskābe
6) CH3 – CH2– CH2 – COOH
Sviestskābe
14.
https://padlet.com/laura_uzlovska/zj8yph2uwt02soao15.
6. Karbonskābjuķīmiskās īpašības
16.
• https://www.siic.lu.lv/kim/IT/K_12/default.aspx@tabid=21&id=210.htmlNoskaties video un pieraksti ķīmiskās īpašības!!!!
Atsūtīt līdz 19.01.2021 Mykoob atbildes
17. Neorganisko skābju ķīmiskās īpašības
1.Disociācija:HCl → H+ + Cl2.Reakcija ar metāliem:
2 HCl + Mg → MgCl2 + H2
3. Reakcija ar oksīdiem:
2 HCl + CaO → CaCl2 + H2O
4. Reakcija ar sārmiem:
HCl + NaOH → NaCl + H2O
5. Reakcija ar sāļiem:
2 HCl + Na2CO3 → 2 NaCl + H2O + CO2
6. Reakcija ar amonjaku:
HCl + NH3 → NH4Cl
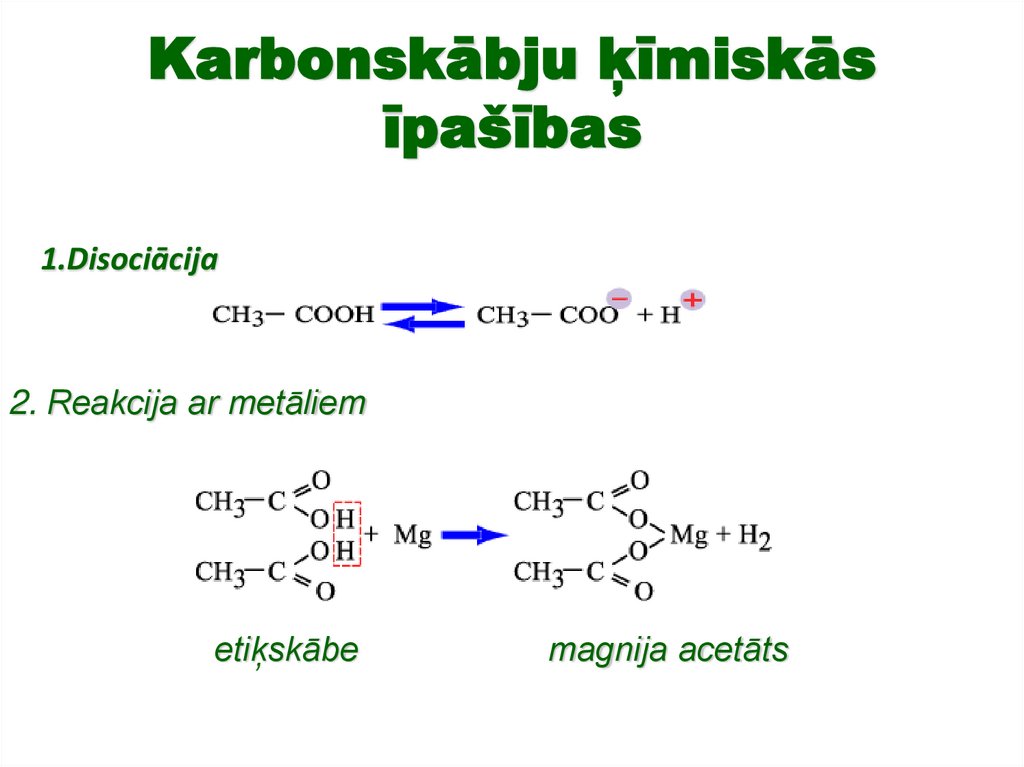
18. Karbonskābju ķīmiskās īpašības
1.Disociācija2. Reakcija ar metāliem
etiķskābe
magnija acetāts
19.
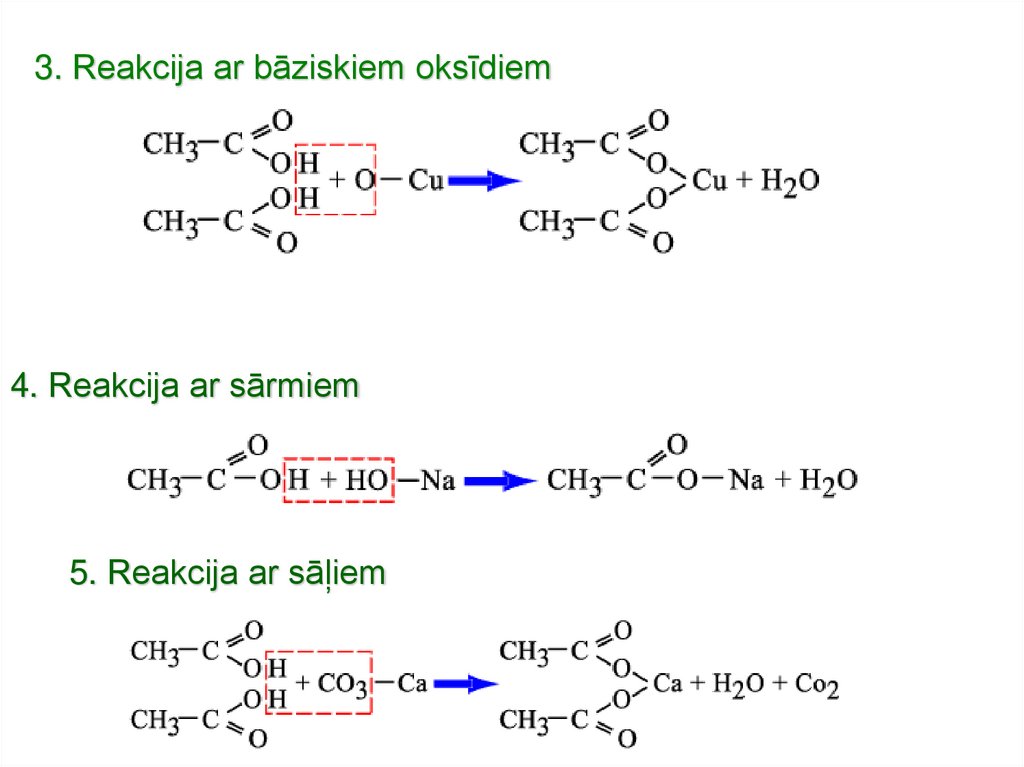
3. Reakcija ar bāziskiem oksīdiem4. Reakcija ar sārmiem
5. Reakcija ar sāļiem
20.
6. Reakcija ar amonjakuCH3COOH + NH3 → CH3COONH4
7. Esterificēšanas reakcija
СН3СООН + С2Н5ОН → СН3СООС2Н5 + Н2О
Etiķskābes metilesteris
















 chemistry
chemistry








