Similar presentations:
Узагальнення й систематизація знань з теми "Початкові хімічні поняття" (1 частина)
1.
2.
1.Що таке тіло?Фізичне тіло – будь який предмет, який має розмір і
форму.
2.Що таке речовина?
Речовина ― це те, з чого складаються фізичні тіла,
тобто навколишні предмети.
3.
Із наведеного переліку визначитиназви речовин і тіл:
А. Скло.
Б.Колба.
В.Пробірка.
Г.Цвях.
Д.Стіл.
Е.Алюміній.
4.
Перевіряємо відповідьРечовини:
А. Скло
Е. Алюміній
Тіла:
Б. Колба
В. Пробірка
Г. Цвях
Д. Стіл
5.
Речовини буваютьчистими, але найчастіше
вони утворюють суміш.
Чим вони відмінні?
6. Перевіряємо відповідь
• Чиста речовина — це речовина індивідуальна, якане містить домішок інших речовин. Вона
складається з частинок певного виду (з однакових
атомів чи молекул) і тому має сталі властивості.
• Суміш — це сукупність різних речовин, тобто
система, що складаються з двох і більше
компонентів. Компоненти можуть змінювати
властивості сумішей.
7.
Із наведеного переліку визначитиназви чистих речовин і сумішей:
А. Кисень.
Б. Повітря.
В. Молоко.
Г. Залізо.
Д. Грунт.
8.
Перевіряємо відповідьЧисті речовини
Суміші
А. Кисень.
Б. Повітря.
Г. Залізо.
В. Молоко.
Д. Грунт
9.
З яких частинокскладаються речовини?
Речовини складаються з атомів,
молекул,
йонів.
10.
Встановіть відповідність міжпозначенням частинки та її назвою:
1. Н2
А. Атом
2. К
Б. Катіон
3. К+
В. Аніон
4. Cl─
Г. Молекула 1
2
5. Н2О
3
6. S
4
5
6
11.
Перевіряємо відповідь1. Н2
2. К
3. К+
4. Cl─
5. Н2О
6. S
А. Атом
Б. Катіон
В. Аніон
Г. Молекула
1
2
3
4
5
6
Г
А
Б
В
Г
А
12.
Для кожної матеріальної частинки можнавизначити масу. В хімії замість абсолютних мас,
виміряних в г чи кг, застосовують відносні.
1.
Що таке відносна атомна маса?
Відносна атомна маса — це відношення маси атома
до 1/12 частини маси атома Карбону.
Відносна атомна маса елемента – це число, що показує, у скільки разів
маса одного атома даного елемента більше 1/12 частини маси атома
Карбону .
2. Як позначається відносна атомна маса?
Відносна атомна маса позначається символом Ar
13.
Запишіть відносні атомні маси такихелементів:
Карбон, Фосфор, Ферум, Нітроген.
Перевіряємо відповідь
Ar (С) = 12
Ar (Р) = 31
Ar (Fe) = 56
Ar (N) = 14
14.
ЗадачаУ скільки разів атом Магнію
важчий за атом Карбону?
15.
Перевіряємо відповідьЗадача
У скільки разів атом Магнію важчий за атом
Карбону?
Ar (Mg) = 24
Ar (С) = 12
Ar (Mg)
Ar (С)
24
12
2
Атом Магнію важчий за атом Карбону у 2 рази
16.
Періодична система – таблиця, якоюкористуються в будь-якій хімічній лабораторії.
Пригадайте будову ПС.
Періодична система складається із періодів і груп.
Кожна група сдладається із підгруп головної та побічної.
17.
18.
Елементи, розташовані в періодичній системі утворюють 7 періодів.Період – це горизонтальний ряд хімічних елементів
Періоди
Малі
1,2,3 періоди
Великі
4,5,6,7 періоди
19.
Елементи, розташовані в періодичній системі, утворюють 8 груп.Група – це вертикальний стовпчик, в якому один під одним розміщені
елементи подібні за властивостями.
Підгрупи
20.
• Де в ПС знаходяться Mg, K, Mn?Перевіряємо відповідь
• Mg знаходиться в
3 періоді, ІІ групі, головній підгрупі.
• K знаходиться в
4 періоді, І групі, головній підгрупі.
• Mn знаходиться в
4 періоді,VІІ групі, побічній підгрупі.
21.
Атоми хімічних елементів сполучаються міжсобою, утворюючи сполуки.
На які 2 групи можна поділити речовини за
складом?
Речовини за складом поділяються
на прості ( складаються з атомів одного
хімічного елемента: О2, Н2, N2)
і складні ( складаються з атомів різних
хімічних елементів: H2O, H2S, CO2 )
22. Як поділяються прості речовини?
Прості речовини поділяютьсяна метали (K, Na, Fe, Cu)
і неметали (S, О2, Н2, N2)
23.
24.
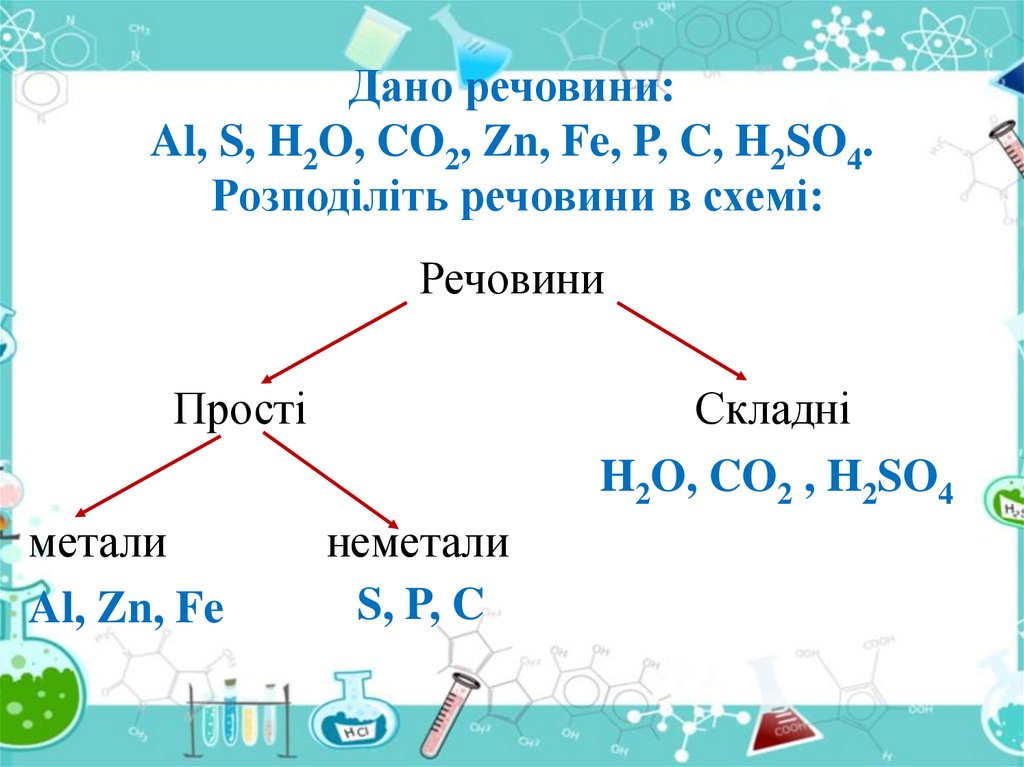
Дано речовини:Al, S, H2O, CO2, Zn, Fe, P, C, H2SO4.
Розподіліть речовини в схемі:
Речовини
Прості
метали
Al, Zn, Fe
Складні
H2O, CO2 , H2SO4
неметали
S, P, C
25.
Що таке формула?Хімічна формула — умовний запис, що відображає
якісний і кількісний склад речовини.
Якісний склад показують за допомогою
символів хімічних елементів,
а кількісний — за допомогою індексів.
H2O, CO2,
H2SO4
26.
Порівняти якісний і кількіснийсклад речовин, формула яких
СO2 та СO
СO2 та СO подібні якісним складом, вони складаються із
атомів Карбону і Оксигену.
Речовини мають однакову кількість атомів Карбону
( по одному), але різну кількість атомів Оксигену
( в СO2 два атома Оксигену, а в СO один атом Оксигену).
27.
Що означають записи:О - один атом Оксигену
2О - два атома Оксигену
О2 - одна молекула кисню
2О2 - дві молекули кисню
СО2 - одна молекула вуглекислого газу
2СО2 - дві молекули вуглекислого газу
28.
Встановити відповідність:1. Один атом Гідрогену
2. Одна молекула водню
3. Два атома Гідрогену
4. Дві молекули водню
А. 2Н
Б. Н
В. 2Н2
Г. Н2
Д. Н2О
1
2
3
4
29.
Перевіряємо відповідьВстановити відповідність:
1. Один атом Гідрогену
2. Одна молекула водню
3. Два атома Гідрогену
4. Дві молекули водню
А. 2Н
Б. Н
В. 2Н2
Г. Н2
Д. Н2О
1 Б
2 Г
3 А
4 В
30. Що називається валентністю?
Вале́нтність — це властивість атомів одногохімічного елемента з'єднуватися з певним
числом атомів інших хімічних елементів.
31. Визначити валентність елементів в сполуках:
• Ca3N2,H2S, CO2, Cr2O3.
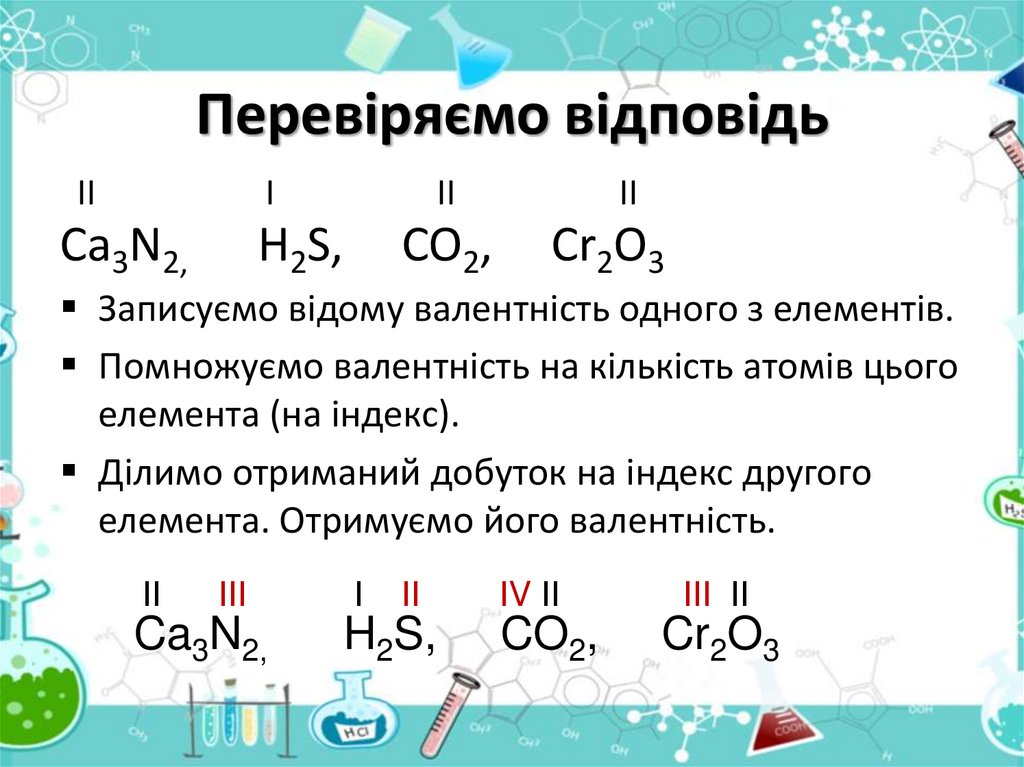
32. Перевіряємо відповідь
ІІІ
Ca3N2,
H2S,
ІІ
ІІ
CO2,
Cr2O3
Записуємо відому валентність одного з елементів.
Помножуємо валентність на кількість атомів цього
елемента (на індекс).
Ділимо отриманий добуток на індекс другого
елемента. Отримуємо його валентність.
ІІ
ІІІ
Ca3N2,
І
ІІ
ІV ІІ
ІІІ ІІ
H2S,
CO2,
Cr2O3
33. Скласти формули: II ІІ ІІІ V VІ Al S, Cu N, Cl O, S O
34. Перевіряємо відповідь
IIІІ ІІІ
V
VІ
Al S, Cu N, Cl O, S O
Над символами елементів записуємо значення валентності.
Якщо елемент може мати різні валентності, то валентність
вказується , а якщо стала, то потрібно записати ії самому.
IIІ ІІ
ІІ
ІІІ
V ІІ
VІ ІІ
Al S, Cu N, Cl O, S O
Знаходимо найменше спільне кратне на обидва значення
валентності.
Ділимо спільне кратне на значення валентності кожного
елемента і отримуємо відповідні індекси.
IIІ ІІ
ІІ
ІІІ
V ІІ
VІ ІІ
Al2 S3, Cu3N2, Cl2O5, S O3
35. Домашнє завдання:
Повторити § 5 -16 у підручнику (Хімія 7 кл.автор: П. Попель, 2020р.)
Підготуватися до контрольної роботи.

































 chemistry
chemistry








